 |
 |
| Korean J Med > Volume 92(6); 2017 > Article |
|
ņÜöņĢĮ
MYH9-RDļŖö ļ¦īņä▒ ļ®┤ņŚŁĒśłņåīĒīÉĻ░Éņåīņ×Éņāēļ░śļ│æņ£╝ļĪ£ ņśżņ¦äļÉśļŖö Ļ▓ĮņÜ░Ļ░Ć Ļ░Ćņן ļ¦ÄĻ│Ā ĒŖ╣Ē׳ ļ│Ė ĒÖśņ×ÉņÖĆ Ļ░ÖņØ┤ Ļ░ĆņĪ▒ļĀźņØ┤ ņŚåļŖö Ļ▓ĮņÜ░ņŚÉ ļŹöņÜ▒ ĻĘĖļĀćļŗż[4]. ļ¦īņØ╝ ĒśłņåīĒīÉņØś ņłśĻ░Ć Ļ░ÉņåīļÉśņ¢┤ ņ׳ņ£╝ļ®░ ĻĘĖ Ēü¼ĻĖ░Ļ░Ć Ēü¼Ļ│Ā Ļ│©ņłś Ļ▓Ćņé¼ņŚÉņä£ Ļ▒░ļīĆĒĢĄņäĖĒżņØś ņłśĻ░Ć ņĀĢņāüņØ┤Ļ▒░ļéś ņĢĮĻ░ä ņ”ØĻ░ĆļÉśņ¢┤ ņ׳Ļ│Ā, ņŗĀĻĖ░ļŖź ņĀĆĒĢś, Ļ░ÉĻ░üņŗĀĻ▓Į ļé£ņ▓ŁņØ┤ ļÅÖļ░śļÉśņ¢┤ ņ׳ļŖö Ļ▓ĮņÜ░ Ēś╣ņØĆ ļ®┤ņŚŁĒśłņåīĒīÉĻ░Éņåīņ×Éņāēļ░śļ│æ ņ╣śļŻīņŚÉ ļ░śņØæņØ┤ ņŚåņØä ļĢīļŖö Ļ░ĆņĪ▒ļĀźņØ┤ ņŚåļŹöļØ╝ļÅä MYH9-RDļź╝ ņØśņŗ¼ĒĢ┤ ļ│┤ņĢäņĢ╝ ĒĢ£ļŗż. MYH9-RDļĪ£ ņ¦äļŗ©ļÉ£ Ļ▓ĮņÜ░ ĒśłņåīĒīÉ ņłśĻ░Ć ļé«ņØäņ¦ĆļØ╝ļÅä ņāØļ¬ģņØä ņ£äĒśæĒĢśļŖö ņČ£ĒśłņØĆ ņĀüļŗżļŖö Ļ▓āņØä ņĢīĻ│Ā ĒśłņåīĒīÉĻ░Éņåīņ”Øļ¦īņ£╝ļĪ£ ņŗ£Ē¢ēĒĢśļŖö ĒśłņåīĒīÉ ņłśĒśłņØĆ Ēö╝ĒĢśĻ│Ā, ņ▓ĀĻ▓░ĒĢŹ ļ╣łĒśłņØś ņśłļ░®, ļ╣äņŖżĒģīļĪ£ņØ┤ļō£ĒĢŁņŚ╝ņĀ£ ņé¼ņÜ® ņĀ£ĒĢ£, Ļ│ĀņØīņØś Ēü░ ņåīļ”¼ ņĀ£ĒĢ£, ļŗ©ļ░▒ļć© ļ░£ņāØņŗ£ ļĀłļŗī-ņĢłņ¦ĆņśżĒģÉņŗĀ ņ¢ĄņĀ£ņĀ£ ņé¼ņÜ®, ļ¦ÉĻĖ░ņŗĀņן ņ¦łĒÖśņ£╝ļĪ£ ņ¦äĒ¢ē ĒĢśņśĆņØä ļĢī ņŗĀņן ņØ┤ņŗØ, ņ▓ŁļĀź ņĀĆĒĢś ņŗ£ ņØĖĻ│ĄņÖĆņÜ░ ņØ┤ņŗØņØä Ļ│ĀļĀżĒĢ£ļŗż. ņłśņłĀņØ┤ļéś ņŗ£ņłĀņØĆ ĒśłņåīĒīÉ ņłśļź╝ ņ”ØĻ░Ćņŗ£Ēé© Ēøä ņŗ£Ē¢ēĒĢĀ ņłś ņ׳Ļ│Ā ņĄ£ĻĘ╝ņØś ļ│┤Ļ│ĀņŚÉ ļö░ļź┤ļ®┤ ĒśłņåīĒīÉ ņłśĒśł ņØ┤ņÖĖņŚÉ ņłĀ ņĀä 20ņØ╝ ņĀĢļÅä ņŚśĒŖĖļĪ¼ļ│┤ĒīŹ ņś¼ļØ╝ļ»╝ņØä ņé¼ņÜ®ĒĢśļŖö Ļ▓āļÅä Ļ│ĀļĀż Ļ░ĆļŖźĒĢśļŗż.
Abstract
A 37-year-old female presented to our hospital with a history of bleeding episodes (excessive bleeding after tooth extraction, gum bleeding, easy bruising, and excessive menstruation) and severe thrombocytopenia (2,000/╬╝L). She had no family history of bleeding tendency or thrombocytopenia. No peripheral lymphadenopathy or splenomegaly was noted. The patientŌĆÖs white blood cell count was normal; hemoglobin was 9.7 g/dL. A peripheral blood smear showed markedly decreased platelets, with occasional giant or large platelets. Bone marrow examination found increased megakaryocytes. The patient also complained of hearing difficulty; a hearing test indicated sensory-neural hearing impairment. Her thrombocytopenia was refractory to treatment with glucocorticosteroids, intravenous gamma-globulin, and danazol. In the 13 years following her initial presentation, the patient required anti- hypertensive treatment, a hearing-aid for progressive hearing loss, and started maintenance kidney dialysis. Her clinical history of refractory thrombocytopenia, progressive hearing impairment, and renal failure suggested myosin heavy chain 9 gene-related congenital syndrome (Epstein syndrome), which was confirmed by the presence of a heterozygous deletion mutation, c.221_223del, (p.Lys74del) in peripheral leukocyte deoxyribonucleic acid.
ņČ£Ēśł Ļ▓ĮĒ¢źĻ│╝ ĒśłņåīĒīÉĻ░Éņåīņ”Øņ£╝ļĪ£ ĒÖśņ×ÉĻ░Ć ļé┤ņøÉĒĢśņśĆņØä ļĢī ļ¦Éņ┤łĒśłņĢĪļÅäļ¦É Ļ▓Ćņé¼ļź╝ ĒåĄĒĢ┤ ļČäņŚ┤ņĀüĒśłĻĄ¼ ņ£Āļ¼┤ļź╝ ĒÖĢņØĖĒĢśņŚ¼ ļ»ĖņäĖĒśłĻ┤Ćļ│æ ņ¦łĒÖśņØä Ļ░Éļ│äĒĢśĻ│Ā, Ļ░äļ╣äļīĆ, ļ╣äņןļ╣äļīĆ, ļ”╝ĒöäņĀł ļ│æļ│Ć, ļ╣äņĀĢĒśĢļ”╝ĒöäĻĄ¼ļź╝ ļÅÖļ░śĒĢśļŖö Ļ▓ĮņÜ░ņŚÉļŖö Ļ▒░ļīĆņäĖĒżļ░öņØ┤ļ¤¼ņŖż, ņŚĪņŖżĒāĆņØĖ-ļ░öļ░öņØ┤ļ¤¼ņŖż, ņØĖĻ░äļ®┤ņŚŁĻ▓░ĒĢŹļ░öņØ┤ļ¤¼ņŖż, ĒåĪņåīĒöīļØ╝ņ”łļ¦łņÖĆ ņäĖĻĘĀņØś Ļ░ÉņŚ╝ņØä ĒÖĢņØĖĒĢśĻ│Ā ņ┤łĻĖ░ ņĀäņŗĀĒÖŹļ░śļŻ©ĒæĖņŖż Ļ░Éļ│äņØä ņ£äĒĢ┤ ĒĢŁĒĢĄĒĢŁņ▓┤ Ļ▓Ćņé¼ļź╝ ĒĢśĻ│Ā, ņøÉļ░£ ĒśłņĢĪ ņ¦łĒÖśņØä ĒÖĢņØĖĒĢśĻĖ░ ņ£äĒĢ┤ Ļ│©ņłś Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢ£ļŗż. ņżæļō▒ļÅä ņØ┤ņāüņØś ļ╣äņןļ╣äļīĆĻ░Ć ļÅÖļ░śļÉśļŖö Ļ▓ĮņÜ░ņŚÉļŖö Ļ░ä ņ¦łĒÖśņØä Ļ░Éļ│äĒĢ£ļŗż. ņØ┤ļ¤░ ņ¦łĒÖśļōżņØ┤ ļ░░ņĀ£ļÉśļ®┤ ļ®┤ņŚŁĒśłņåīĒīÉĻ░Éņåīņ×Éņāēļ░śļ│æ(immune thrombocytopenia purpura)ņØä ņ¦äļŗ©ĒĢ£ļŗż[1]. ĒĢśņ¦Ćļ¦ī ĒśłņåīĒīÉĻ░Éņåīņ”ØņØä ņØ╝ņ£╝ĒéżļŖö ņ£ĀņĀäņ¦łĒÖśļōżļÅä ņ׳ļŗż. ļŗ╣ļŗ©ļ░▒ņ¦ł Ļ▓░ĒĢŹņŚÉ ņØśĒĢ£ ļ▓Āļź┤ļéśļź┤-ņŖÉļ”¼ņŚÉņ”ØĒøäĻĄ░(Bernard-Soulier syndrome), ĻĄ¼Ļ░£ņŗ¼ņןņĢłļ®┤ņ”ØĒøäĻĄ░(Velo-cardio-facial syndrome), ņ╣╝ĒÄśņØĖ(calpain) Ļ▓░ĒĢŹņŚÉ ņØśĒĢ┤ ļ░£ņāØĒĢśļŖö Montreal platelet syndrome, ņé╝ņŚ╝ņāēņ▓┤ņ”ØĒøäĻĄ░ņØĖ ļŗżņÜ┤ņ”ØĒøäĻĄ░(trisomy21), ĒīīĒāĆņÜ░ņ”ØĒøäĻĄ░(trisomy 13), ņŚÉļō£ņøīļō£ņ”ØĒøäĻĄ░(trisomy18), X ņŚ╝ņāēņ▓┤ ļČĆņĪ▒ņŚÉ ņØśĒĢ£ Ēä░ļäłņ”ØĒøäĻĄ░, X ņŚ╝ņāēņ▓┤ņŚÉ ņ£äņ╣śĒĢśļŖö ņ£ĀņĀäņ×É ņØ┤ņāüņŚÉ ņØśĒĢ£ ļ╣äņŖżņĮöĒŖĖ-ņś¼ļō£ļ”¼ņ╣śņ”ØĒøäĻĄ░(Wiskott-Aldrich syndrome), ņŚ¼ļ¤¼ ņ£ĀņĀäņ×É ņØ┤ņāüņŚÉ ņØśĒĢ┤ ļ░£ņāØĒĢśļŖö ļłäļé£ņ”ØĒøäĻĄ░(Noonan syndrome), ņĮöļä¼ļ”¼ņĢäļööļ×Ćņ¦Ćņ”ØĒøäĻĄ░(Cornelia de Lange syndrome), 11ļ▓ł ņŚ╝ņāēņ▓┤ ņØ┤ņāüņŚÉ ņØśĒĢ£ ņĢ╝ņĮźņŖ©ņ”ØĒøäĻĄ░(Jacobsen syndrome), ņäĖĒż Ļ│©Ļ▓® ļŗ©ļ░▒ņ¦łņØä ņĢöĒśĖĒÖöĒĢśļŖö Myosin heavy chain 9 (MYH9) ņ£ĀņĀäņ×É ņØ┤ņāüņ£╝ļĪ£ ļ░£ņāØĒĢśļŖö ļ®öņØ┤ĒŚżĻĖĆļ”░ ņØ┤ņāü(May-Hegglin anomaly), ņŚĪņŖżĒāĆņØĖņ”ØĒøäĻĄ░(Epstein syndrome), ĒÄÖĒŖĖļäłņ”ØĒøäĻĄ░(Fechtner syndrome)Ļ│╝ ņäĖļ░öņŖżĒŗ░ņĢłņ”ØĒøäĻĄ░(Sebastian syndrome), ņĢäņ¦ü ņøÉņØĖ ņ£ĀņĀäņ×ÉĻ░Ć ļ¬ģĒÖĢĒĢśņ¦Ć ņĢŖņØĆ ņĀĆĒśłņåīĒīÉņÜöĻ│©ļ¼┤ĒśĢņä▒ņ”ØĒøäĻĄ░(thrombocytopenia abscent radii syndrome)ļō▒ņØ┤ļŗż[2]. ļ│Ė ņ”ØļĪĆņŚÉņä£ļŖö ļČłņØæņä▒ ĒśłņåīĒīÉ Ļ░ÉņåīņØś ļō£ļ¼Ė ņøÉņØĖ ņżæ ĒĢśļéśņØĖ ņŚĪņŖżĒāĆņØĖņ”ØĒøäĻĄ░ņŚÉ ļīĆĒĢ┤ ļ│┤Ļ│ĀĒĢśĻ│Āņ×É ĒĢ£ļŗż.
20ļģä ņĀä(1998ļģä 7ņøö) 37ņäĖ ņŚ¼ņ×ÉĻ░Ć ņČ£Ēśłņä▒ Ļ▓ĮĒ¢źņŚÉ ļīĆĒĢ┤ ņØ╝ņ░© ņ¦äļŻīĻĖ░Ļ┤ĆņŚÉņä£ ĒśłņĢĪ Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢ£ Ēøä ĒśłņåīĒīÉ Ļ░Éņåī ņåīĻ▓¼ņ£╝ļĪ£ ļé┤ņøÉĒĢśņśĆļŗż. ĒÖśņ×ÉļŖö 12ņäĖņŚÉ ļ░£ņ╣ś Ēøä Ļ│╝ļŗżņČ£ĒśłņØä Ļ▓ĮĒŚśĒĢśņśĆĻ│Ā 14ņäĖņŚÉ ņ┤łĻ▓Į Ēøä ļČłĻĘ£ņ╣ÖņĀü Ļ│╝ļŗżņøöĻ▓ĮņØä Ļ▓ĮĒŚśĒĢśņśĆņ£╝ļ®░ 17ņäĖĻ▓ĮļČĆĒä░ ņåÉĻ│╝ ļ░£ņŚÉ ņēĮĻ▓ī ļ®ŹņØ┤ ļō£ļŖö ņ”ØņāüĻ│╝ ņ×ćļ¬Ė ņČ£Ēśł, ņĮöĒö╝ļō▒ņØä Ļ▓ĮĒŚśĒĢśņśĆļŗż. 27ņäĖĻ▓ĮņŚÉ ņ¦üņן Ļ▒┤Ļ░ĢĻ▓Ćņ¦äņŚÉņä£ ĒśłņåīĒīÉ Ļ░Éņåī ņåīĻ▓¼ņØ┤ ņ׳ņŚłņ£╝ļéś ņČöĻ░Ć Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņ¦Ć ņĢŖņĢśļŗż. ļé┤ņøÉ ļŗ╣ņŗ£ ņÖĖļלņŚÉņä£ ņŗ£Ē¢ēĒĢ£ ļ¦Éņ┤łĒśłņĢĪ Ļ▓Ćņé¼ņŚÉņä£ ļ░▒ĒśłĻĄ¼ 5,600/uL, Ēśłņāēņåī 9.7 g/dL, ĒÅēĻĘĀ ņĀüĒśłĻĄ¼ Ēśłņāēņåī ļåŹļÅä 31.4%, ĒśłņåīĒīÉ 2,000/uLņśĆļŗż. ļ¦Éņ┤łĒśłņĢĪļÅäļ¦É Ļ▓Ćņé¼ņŚÉņä£ ņĀĢņāüņāēņåī ņĀĢņāüņĀüĒśłĻĄ¼ ļ╣łĒśł, Ļ▓ĮļÅäņØś ļ│ĆĒśĢņĀüĒśłĻĄ¼ ņ”ØĻ░Ć, ņĀĆļ¬ģĒĢ£ ĒśłņåīĒīÉ Ļ░Éņåī, Ļ▒░ļīĆĒśłņåīĒīÉņØ┤ ĒÖĢņØĖļÉśņ¢┤ ņ×ģņøÉĒĢśņśĆļŗż. Ļ│╝Ļ▒░ļĀźņ£╝ļĪ£ 20ļīĆņŚÉ ļ¦╣ņן ņĀłņĀ£ņłĀņØä ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░ ļŗ╣ņŗ£ ĒŖ╣ļ│äĒĢ£ ļČĆņ×æņÜ®ņØĆ ņŚåņŚłļŗż. Ļ│äĒåĄļ¼Ėņ¦äņŚÉņä£ ņ▓ŁļĀźņĀĆĒĢśļź╝ ĒśĖņåīĒĢśņśĆļŗż. ĒśłņåīĒīÉ Ļ░Éņåīļéś ņČ£Ēśł Ļ▓ĮĒ¢ź(ņĮöĒö╝, ņ×ćļ¬Ė ņČ£Ēśł, ņēĮĻ▓ī ļ®Źļō” ļō▒)ņØś Ļ░ĆņĪ▒ļĀźņØĆ ņŚåņŚłļŗż. ĒśłņĢĢ 130/80 mmHgļĪ£ Ļ│ĀĒśłņĢĢņØĆ ļÅÖļ░śļÉśņ¦Ć ņĢŖņĢśĻ│Ā ļ¦źļ░Ģ 70/min, ĒśĖĒØĪ ņłś 18/min, ņ▓┤ņś© 36.0ŌäāļĪ£ ļ░£ņŚ┤ņØĆ ņŚåņŚłļŗż. ņ¦äņ░░ņŚÉņä£ ļ¦īņĀĖņ¦ĆļŖö ņ×äĒīīņäĀņØĆ ņŚåņŚłĻ│Ā ļ╣äņןļ╣äļīĆ ņåīĻ▓¼ļÅä ņŚåņŚłļŗż. ņ¦äļŗ©ņØä ņ£äĒĢ┤ ĒĢŁĒśłņåīĒīÉ ĒĢŁņ▓┤, ĒĢŁĒĢĄĒĢŁņ▓┤ļź╝ Ļ▓Ćņé¼ĒĢśņśĆĻ│Ā Ļ▒░ļīĆņäĖĒż ļ░öņØ┤ļ¤¼ņŖż, ņŚĪņŖżĒāĆņØĖ-ļ░öļ░öņØ┤ļ¤¼ņŖż, ņØĖĻ░äļ®┤ņŚŁĻ▓░ĒĢŹļ░öņØ┤ļ¤¼ņŖżņÖĆ Ļ░äņŚ╝ņŚÉ ļīĆĒĢ£ Ēśłņ▓ŁĒĢÖņĀü Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░ ļ¬©ļæÉ ņØīņä▒ņØ┤ņŚłļŗż. Ļ│©ņłś Ļ▓Ćņé¼ņŚÉņä£ Ļ▒░ļīĆĒĢĄņäĖĒż(megakaryocyte)ļŖö 4.5/HPFļĪ£ ņżæļō▒ļÅäņØś ņ”ØĻ░Ćļź╝ ļ│┤ņśĆĻ│Ā ņĀĢņāü ļČäĒżļź╝ ļ│┤ņśĆņ£╝ļ®░ ĒĢĄĒśĢņØĆ ņĀĢņāü ņŚ¼ņä▒ ĒĢĄĒśĢņØ┤ņŚłļŗż. ĒśłņåīĒīÉ ņłśĒśł Ēøä ĒśłņåīĒīÉņØĆ 76,000/uLļĪ£ ņ”ØĻ░ĆĒĢśņśĆļŗż. ļ®┤ņŚŁĒśłņåīĒīÉĻ░Éņåīņ×Éņāēļ░śļ│æņØä ņØśņŗ¼ĒĢśņŚ¼ ĒöäļĀłļō£ļŗłņåöļĪĀ(Solondo, Yuhan Corp., Seoul, Korea) 60 mgņØä 16ņØ╝ Ēł¼ņŚ¼ĒĢśņśĆņ£╝ļéś ĒśłņåīĒīÉņØĆ 8,000/uLļĪ£ Ļ░ÉņåīĒĢśņśĆļŗż. ļ®┤ņŚŁĻĖĆļĪ£ļČłļ”░ 500 mg/kgņØä 5ņØ╝ Ēł¼ņŚ¼ Ēøä ņĖĪņĀĢĒĢ£ ĒśłņåīĒīÉņØĆ 8,000/uLņśĆļŗż. ļ®┤ņŚŁĒśłņåīĒīÉĻ░Éņåīņ×Éņāēļ░śļ│æņØ┤ ņĢäļŗÉ Ļ░ĆļŖźņä▒ņØä Ļ│ĀļĀżĒĢśņśĆĻ│Ā, ļ▓Āļź┤ļéśļź┤-ņłĀļ”¼ņŚÉņ”ØĒøäĻĄ░ņØä ņØśņŗ¼ĒĢśņŚ¼ ņŗ£Ē¢ēĒĢ£ ņ£ĀņäĖĒż ļČäņäØņŚÉņä£ ĒśłņåīĒīÉņØś ļŗ╣ļŗ©ļ░▒ņ¦ł Ib, IIb/IIIa Ļ▓░ĒĢŹņØĆ ĒÖĢņØĖļÉśņ¦Ć ņĢŖņĢśļŗż. ļŗżļéśņĪĖ(Danazol, Young Poong Pharmaceutical, Incheon, Korea) 400 mgņØä 1ņØ╝ 1ĒÜīļĪ£ 6ņØ╝ ņé¼ņÜ® Ēøä ĒśłņåīĒīÉņØ┤ 26,000/uLļĪ£ ņ”ØĻ░ĆĒĢśņŚ¼ Ēć┤ņøÉĒĢśņśĆļŗż. ņØ┤Ēøä ņÖĖļלņŚÉņä£ ĒśłņåīĒīÉņØĆ 30,000-40,000/uLļĪ£ ņ£Āņ¦ĆļÉśņŚłļŗż. ņ▓ŁļĀź ņĀĆĒĢśņŚÉ ļīĆĒĢ┤ ņŗ£Ē¢ēĒĢ£ ņ▓ŁļĀź Ļ▓Ćņé¼ņŚÉņä£ Ļ│ĀņØīņŚŁņØś ņ▓ŁļĀź Ļ░ÉņåīĻ░Ć ļæÉļō£ļ¤¼ņĪīĻ│Ā Ļ░ÉĻ░üņŗĀĻ▓Įļé£ņ▓Ł ņåīĻ▓¼ņØ┤ņŚłļŗż. 1ļģä ļÆż(1999ļģä 11ņøö) 1ņØ╝ 2ĒÜīņØś ĒØæņāēļ│ĆņØä 3ņØ╝ ļÅÖņĢł ļ│Ė Ēøä ņŗżņŗĀĒĢśņśĆĻ│Ā ņāüļČĆņ▓┤ļČĆ ņ£äĻČżņ¢æ ņČ£ĒśłņØ┤ ĒÖĢņØĖļÉśņ¢┤ ĻĄŁņåī ņŚÉĒö╝ļäżĒöäļ”░ņØä ņŻ╝ņé¼ĒĢśņśĆĻ│Ā ņŗØņØ┤ ņ¦äĒ¢ē Ēøä Ēć┤ņøÉĒĢśņśĆļŗż. Ēć┤ņøÉ 6ņØ╝ ļÆż Ēśłļć©Ļ░Ć ļ░£ņāØĒĢśņŚ¼ ņ×¼ņ×ģņøÉĒĢśņśĆĻ│Ā ĒśłņåīĒīÉ 4,000/uLļĪ£ ĒÖĢņØĖļÉśņ¢┤ ĒśłņåīĒīÉ ņłśĒśł Ēøä 28,000/uLļĪ£ ņāüņŖ╣ĒĢśņśĆļŗż. ņŗĀņןņ┤łņØīĒīīļź╝ ņŗ£Ē¢ēĒĢśņśĆĻ│Ā ņÖ╝ņ¬Į ņŗĀņן ņĢäļלņ¬ĮņØś ļŗ©ņł£ ļéŁņóģ ņÖĖņŚÉ ĒŖ╣ņØ┤ ņåīĻ▓¼ņØĆ ņŚåņŚłļŗż. ņĀĢļ¦źņŗĀņÜ░ņĪ░ņśüņłĀļÅä ņĀĢņāü ņåīĻ▓¼ņØ┤ņŚłĻ│Ā Ēśłļć©ļÅä ņŚåņ¢┤ Ēć┤ņøÉĒĢśņśĆņ£╝ļ®░ Ēć┤ņøÉ ļŗ╣ņŗ£ ĒśłņåīĒīÉņØĆ 20,000/uLņśĆļŗż. 2ļģä ļÆż(2000ļģä 12ņøö) Ļ▒┤Ļ░ĢĻ▓Ćņ¦ä ņåīļ│Ć Ļ▓Ćņé¼ņŚÉņä£ ļ░▒ĒśłĻĄ¼ņÖĆ ņĀüĒśłĻĄ¼Ļ░Ć ĒÖĢņØĖļÉśņ¢┤ ņŗ£Ē¢ēĒĢ£ 24ņŗ£Ļ░ä ņåīļ│Ć Ļ▓Ćņé¼ņŚÉņä£ ņ┤Ø ļŗ©ļ░▒ņØĆ 214.9mg/dLņśĆĻ│Ā, ņĀäĻĖ░ņśüļÅÖ Ļ▓Ćņé¼ņŚÉņä£ ņĢīļČĆļ»╝, ņĢīĒīī-1Ļ│╝ ļ▓ĀĒāĆ ļČäĒÜŹņØ┤ĒÖĢņØĖļÉśņ¢┤ ņäĀĒāØņĀü ņé¼ĻĄ¼ņ▓┤ņä▒ ļŗ©ļ░▒ļć© ņåīĻ▓¼ņØ┤ņŚłļŗż. 1ļģä ļÆż(2001ļģä 12ņøö) ĒśłņĢĢņØ┤ ļåÆņĢä ĒāĆ ņøÉņŚÉņä£ ĒĢŁĻ│ĀĒśłņĢĢ ņĢĮļ¼╝ ļ│ĄņÜ®ņØä ņŗ£ņ×æĒĢśņśĆļŗż. ņØ┤Ēøä ĒśłņåīĒīÉ ņłśĒśłņØĆ ĒĢśņ¦Ć ņĢŖĻ│Ā ņÖĖļלņŚÉņä£ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ĒĢśņśĆĻ│Ā ĒśłņåīĒīÉņØĆ 1,000-8,000/uLļĪ£ ņĖĪņĀĢļÉśņŚłļŗż. 5ļģä ļÆż(2006ļģäĻ▓Į) ņ▓ŁļĀź ņĀĆĒĢśņŚÉ ļīĆĒĢ┤ ļ│┤ņ▓ŁĻĖ░ļź╝ ņ░®ņÜ®ĒĢśņśĆļŗż. 1ļģä ļÆż(2007ļģä 11ņøö) ņŗĀĻĖ░ļŖźņØ┤ ņĀĆĒĢśļÉśĻĖ░ ņŗ£ņ×æĒĢśņśĆļŗż. 24ņŗ£Ļ░ä ņåīļ│Ć ļŗ©ļ░▒ņØĆ 3372.8 mg/dLļĪ£ 7ļģä ņĀä 214.9 mg/dLļ│┤ļŗż ņ”ØĻ░ĆĒĢśņśĆļŗż. Ļ│ĀĒśłņĢĢņ£╝ļĪ£ ņØĖĒĢ£ ņŗĀĻĖ░ļŖź ņĀĆĒĢś Ļ░ĆļŖźņä▒ņØä ņØśņŗ¼ĒĢśņśĆĻ│Ā ĒśłņåīĒīÉ Ļ░ÉņåīļĪ£ ņØĖĒĢ£ ņČ£ĒśłņØś ņ£äĒŚśņä▒ņ£╝ļĪ£ ņŗĀņן ņĪ░ņ¦üĻ▓Ćņé¼ļŖö ņŗ£Ē¢ēĒĢśņ¦Ć ņĢŖņĢśļŗż.
4ļģä ļÆż(2011ļģä 6ņøö) ĒśłņĢĢ 170 mmHgļĪ£ ņāüņŖ╣, ĻĄ¼ņŚŁ, ĻĄ¼ĒåĀĻ░Ć ļ░£ņāØĒĢśņśĆĻ│Ā ĒśłņĢĪņÜöņåīņ¦łņåī 117 mg/dL Ēü¼ļĀłņĢäĒŗ░ļŗī 9.7 mg/dLļĪ£ ĒÖĢņØĖļÉśņ¢┤ ņŻ╝ 3ĒÜī ĒśłņĢĪ Ēł¼ņäØņØä ņŗ£ņ×æĒĢśņśĆļŗż. 3ļģä ļÆż(2014ļģä 1ņøö)ņ▓ŁļĀź ņĀĆĒĢśĻ░Ć ĻĖēĻ▓®Ē׳ ņ¦äĒ¢ēĒĢśņśĆĻ│Ā ļ│┤ņ▓ŁĻĖ░ļź╝ ņ░®ņÜ®ĒĢśņŚ¼ļÅä ņל ļōżļ”¼ņ¦Ć ņĢŖņĢśņ£╝ļ®░ ņĖĪļæÉĻ│© ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāüņŚÉņä£ ņÜ░ņĖĪ ļ»ĖļĪ£ņŚ╝ ņåīĻ▓¼ņØ┤ņŚłĻ│Ā ņØ┤ļ╣äņØĖĒøäĻ│╝ņŚÉņä£ ņØĖĻ│ĄņÖĆņÜ░ ņØ┤ņŗØ ņłśņłĀņØä ĻČīņ£Āļ░øņĢśļŗż.
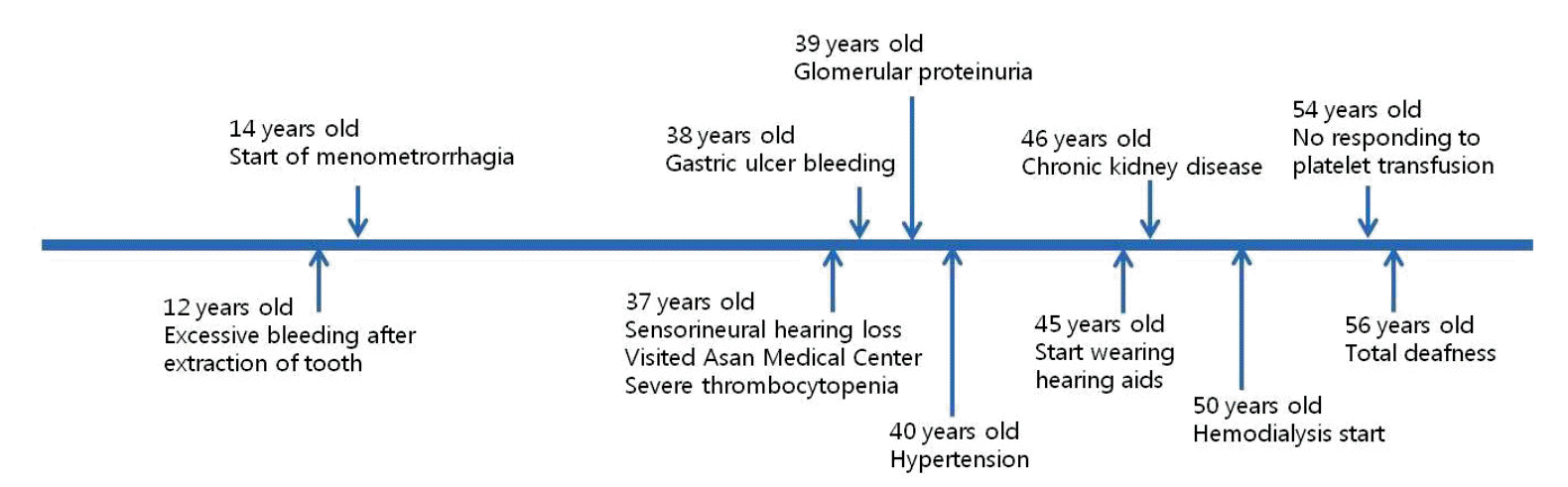
1ļģä ļÆż(2015ļģä 4ņøö) ņ¢æņ¬Į ņĮöĒö╝Ļ░Ć ļ░£ņāØĒĢśņŚ¼ ņØæĻĖēņŗżņŚÉ ļé┤ņøÉĒĢśņśĆĻ│Ā ĒśłņåīĒīÉ 23,000/uLļĪ£ ĒÖĢņØĖļÉśņ¢┤ ļåŹņČĢ ĒśłņåīĒīÉ 8ļŗ©ņ£äļź╝ ņłśĒśłĒĢśņśĆņ£╝ļéś ņłśĒśł Ēøä ĒśłņåīĒīÉ 26,000/uLļĪ£ ņłśĒśł ņĀäĻ│╝ ĒøäņØśĒśłņåīĒīÉ ņłśļŖö ļ╣äņŖĘĒĢśņśĆĻ│Ā ņØ┤ļ╣äņØĖĒøäĻ│╝ņŚÉņä£ ņČ£Ēśł ņĪ░ņĀł Ēøä Ēć┤ņŗżĒĢśņśĆļŗż. 2ļģä ļÆż(2017ļģä 3ņøö) ņ×ćļ¬Ė ņČ£ĒśłĻ│╝ ņĮöĒö╝Ļ░Ć ļ░śļ│ĄļÉśņ¢┤ ņØæĻĖēņŗżņŚÉ ļé┤ņøÉĒĢśņśĆĻ│Ā ĒśłņåīĒīÉ 2,000/uLļĪ£ ĒÖĢņØĖļÉśņ¢┤ ĒśłņåīĒīÉņØä ņłśĒśłĒĢśņśĆņ£╝ļéś ĒśłņåīĒīÉ ņłśņŚÉ ļ│ĆĒÖöĻ░Ć ņŚåņŚłņ£╝ļ®░ ļ®┤ņŚŁĻĖĆļĪ£ļČłļ”░ 500 mg/kgļĪ£ 5ņØ╝ Ēł¼ņŚ¼ Ēøä ĒśłņåīĒīÉņØĆ 15,000/uLļĪ£ ĒÖĢņØĖļÉśņŚłļŗż. ņ×ģņøÉĒĢśņŚ¼ ņŗ£Ē¢ēĒĢ£ ļ¦Éņ┤łĒśłņĢĪļÅäļ¦É Ļ▓Ćņé¼ņŚÉņä£ ņŚŁņŗ£ ĒśłņåīĒīÉņØś Ēü¼ĻĖ░Ļ░Ć ņĀüĒśłĻĄ¼ņØś Ēü¼ĻĖ░ņÖĆ ļ╣äņŖĘĒĢ£ ņĀĢļÅäļĪ£ ņ╗żņĀĖ ņ׳ņŚłĻ│Ā(Fig. 1), Ļ│©ņłś Ļ▓Ćņé¼ņŚÉņä£ ņäĖĒżņČ®ņŗżļÅäļŖö 35% (Fig. 2A), Ļ▒░ļīĆĒĢĄņäĖĒżļŖö 2.8/HPFļĪ£ ņĀüņĀłĒĢśņśĆļŗż(Fig. 2B). ņØ┤ņŚÉ ļīĆĒĢ┤ ņŖżĒģīļĪ£ņØ┤ļō£ ļČłņØæņä▒ ļ®┤ņŚŁĒśłņåīĒīÉĻ░Éņåīņ×Éņāēļ░śļ│æņ£╝ļĪ£ ņŚśĒŖĖļĪ¼ļ│┤ĒīŹ ņś¼ļØ╝ļ»╝(eltrombopagolamine, GlaxoSmithkline Plc., Bradford, UK; ĒŖĖļĪ¼ļ│┤ĒżņØ┤ņŚÉĒŗ┤[thrombopoietin] ņłśņÜ®ņ▓┤ ņ×æņÜ®ņĀ£) 25 mgņØä 1ņØ╝ 1ĒÜīļĪ£ 4ņØ╝ Ēł¼ņŚ¼ Ēøä ĒśłņåīĒīÉņØ┤ 22,000/uLļĪ£ ņāüņŖ╣ĒĢśņŚ¼ ņŚśĒŖĖļĪ¼ļ│┤ĒīŹ ņś¼ļØ╝ļ»╝ņØä ņ£Āņ¦ĆĒĢśļ®░ ņÖĖļלņŚÉņä£ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ĒĢśĻĖ░ļĪ£ ĒĢśĻ│Ā Ēć┤ņøÉĒĢśņśĆļŗż. ļśÉĒĢ£, ņ×ģņøÉ ĻĖ░Ļ░ä ļÅÖņĢł Ļ▒░ļīĆĒśłņåīĒīÉ, ĒśłņåīĒīÉ Ļ░Éņåī, ļ¦ÉĻĖ░ņŗĀņןņ¦łĒÖś, ņ▓ŁļĀź ņĀĆĒĢśļź╝ ņØ╝ņ£╝Ēé¼ ņłś ņ׳ļŖö ņ¦łĒÖśņŚÉ ļīĆĒĢ£ ļ¼ĖĒŚī Ļ▓ĆņāēņØä ĒĢśņśĆĻ│Ā ņĢīĒżĒŖĖņ”ØĒøäĻĄ░, ņŚĪņŖżĒāĆņØĖņ”ØĒøäĻĄ░ņØä ņ¦äļŗ©ĒĢśĻĖ░ ņ£äĒĢ┤ ņĢłĻ│╝ Ļ▓Ćņ¦äņØä ĒĢśņśĆņ£╝ļ®░ ņłśņĀĢņ▓┤ņØś ņĢ×ņøÉņČö ņłśņĀĢņ▓┤ļéś ļ░▒ļé┤ņן ņåīĻ▓¼ņØĆ ņŚåņŚłĻ│Ā ņ▓ŁļĀź Ļ▓Ćņé¼ņŚÉņä£ ņĀäļåŹ ņåīĻ▓¼ņØ┤ņŚłļŗż. ļ¦Éņ┤łĒśłņĢĪ ļ░▒ĒśłĻĄ¼ņŚÉņä£ ņżæĒĢ®ĒÜ©ņåīņŚ░ņćäļ░śņØæņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņŚ╝ĻĖ░ņä£ņŚ┤ ļČäņäØņØä ĒĢ£ Ļ▓░Ļ│╝ MYH9 ņ£ĀņĀäņ×ÉņŚÉņä£ ņØ┤ņĀäņŚÉ ļ│┤Ļ│ĀļÉ£ ļ░öĻ░Ć ņŚåļŹś ļÅīņŚ░ļ│ĆņØ┤Ļ░Ć ļ░£Ļ▓¼ļÉśņŚłļŗż. ņØ┤ļŖö c.221_223del (p.Lys74del)ļĪ£ 74ļ▓łņ¦Ė ņĢäļ»ĖļģĖņé░ņØĖ ļ”¼ņŗĀņØ┤ Ļ▓░ņŗżļÉśļŖö ļ│ĆņØ┤ļĪ£ ņĀĢņāüņØĖņŚÉņä£ļŖö ļ░£Ļ▓¼ļÉśņ¦Ć ņĢŖļŖö ļ│ĆņØ┤ņØ┤ļŗż(Fig. 3). ņØ┤ņāüņØś ļ│æļĀźņØä ņĀĢļ”¼ĒĢśņŚ¼ Fig. 4ņŚÉ ļéśĒāĆļé┤ņŚłļŗż. ņČ£Ēśłņä▒ Ļ▓ĮĒ¢ź, ņŗĀĻĖ░ļŖź ņĀĆĒĢś(ņåīļ│Ćļ¤ē Ļ░Éņåī, ļČĆņóģ, Ēł¼ņäØ), ņ▓ŁļĀźņĀĆĒĢś, ņŗ£ļĀź ņĀĆĒĢśņØś Ļ░ĆņĪ▒ļĀźņŚÉ ļīĆĒĢ┤ ļŗżņŗ£ ĒÖĢņØĖĒĢśņśĆņ£╝ļéś Ļ░ĆņĪ▒ļĀźņØĆ ņŚåņŚłļŗż.
ļ®┤ņŚŁĒśłņåīĒīÉĻ░Éņåīņ×Éņāēļ░śļ│æņ£╝ļĪ£ ņ¦äļŗ©ļÉśļ®┤ ņāØļ¬ģņŚÉ ņ£äĒŚśņØä ņżä ņłś ņ׳ļŖö ņČ£ĒśłņØ┤ ņ׳ņØä ļĢī ņØæĻĖēņ£╝ļĪ£ ĒśłņåīĒīÉ ņłśĒśłņØä ĒĢśļ®░ ļ¦īņä▒ļ®┤ņŚŁĒśłņåīĒīÉĻ░Éņåīņ×Éņāēļ░śļ│æņŚÉņä£ ĒśłņåīĒīÉ ņłśĻ░Ć 20,000/uL ņØ┤ĒĢśņØ┤Ļ▒░ļéś ņČ£ĒśłņØ┤ ņ׳ņ£╝ļ®┤ņä£ ĒśłņåīĒīÉ ņłśĻ░Ć 50,000/uL ņØ┤ĒĢśņØĖ Ļ▓ĮņÜ░ ņŖżĒģīļĪ£ņØ┤ļō£ Ēł¼ņŚ¼, ļ╣äņןņĀłņĀ£, ļ®┤ņŚŁĻĖĆļĪ£ļČłļ”░ Ēł¼ņŚ¼, ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£Ēł¼ņŚ¼ ļō▒ņØś ņ╣śļŻīļź╝ ĒĢ£ļŗż. 20ļģä ņĀä ĒśłņåīĒīÉĻ░Éņåīņ”Øņ£╝ļĪ£ ļé┤ņøÉĒĢśņŚ¼ ļ¦Éņ┤łĒśłņĢĪļÅäļ¦É Ļ▓Ćņé¼, Ļ▒░ļīĆņäĖĒżļ░öņØ┤ļ¤¼ņŖż, ņŚĪņŖżĒāĆņØĖ-ļ░öļ░öņØ┤ļ¤¼ņŖż, ņØĖĻ░ä ļ®┤ņŚŁĻ▓░ĒĢŹ ļ░öņØ┤ļ¤¼ņŖż, Ļ░äņŚ╝ Ēśłņ▓Ł Ļ▓Ćņé¼, ĒĢŁĒĢĄĒĢŁņ▓┤ Ļ▓Ćņé¼ņŚÉņä£ ļ¬©ļæÉ ņØīņä▒ņ£╝ļĪ£ ĒÖĢņØĖļÉśņŚłņ£╝ļ®░ Ļ│©ņłś Ļ▓Ćņé¼ņŚÉņä£ Ļ▒░ļīĆĒĢĄņäĖĒż ņłśĻ░Ć ņĢĮĻ░ä ņ”ØĻ░ĆļÉ£ Ļ▓āņØä ĒżĒĢ©ĒĢśņŚ¼ ĒŖ╣ņØ┤ ņåīĻ▓¼ņØ┤ ņŚåņŚłĻ│Ā ņłśņ░©ļĪĆ ĒÖĢņØĖĒĢśņśĆņ£╝ļéś Ļ░ĆņĪ▒ļĀźļÅä ņŚåņ¢┤ ļ®┤ņŚŁĒśłņåīĒīÉĻ░Éņåīņ×Éņāēļ░śļ│æņ£╝ļĪ£ ņ¦äļŗ©ĒĢśņśĆĻ│Ā ņČ£Ēśł ņåīĻ▓¼ņØ┤ ņ׳ņ£╝ļ®░ ĒśłņåīĒīÉ ņłśĻ░Ć 20,000/uLļ»Ėļ¦īņØ┤ņŚłĻĖ░ ļĢīļ¼ĖņŚÉ ņŖżĒģīļĪ£ņØ┤ļō£, ļ®┤ņŚŁĻĖĆļĪ£ļČłļ”░, ļŗżļéśņĪĖņØä Ēł¼ņŚ¼ĒĢśņśĆņ£╝ļéś ļ¬©ļōĀ ņ╣śļŻīņŚÉ ļ░śņØæņØä ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśļŹś ĒÖśņ×ÉĻ░Ć 20ļģäņØ┤ ņ¦Ćļé£ ļÆżņŚÉ ņŗĀļČĆņĀäņ£╝ļĪ£ ĒśłņĢĪ Ēł¼ņäØņØä ĒĢśĻ│Ā ļ│┤ņ▓ŁĻĖ░ ņ░®ņÜ®ņŚÉļÅä ņåīļ”¼Ļ░Ć Ļ▒░ņØś ļōżļ”¼ņ¦Ć ņĢŖļŖö ņ▓ŁļĀź ņןņĢĀĻ░Ć ļ░£ņāØĒĢ£ Ēøä ņŚĪņŖżĒāĆņØĖņ”ØĒøäĻĄ░ņ£╝ļĪ£ ņ¦äļŗ©ļÉśņŚłļŗż.
1972ļģä Epstein ļō▒[3]ņØĆ Ļ▒░ļīĆĒśłņåīĒīÉ, ĒśłņåīĒīÉĻ░Éņåīņ”Ø, ņŗĀņןņŚ╝(nephritis)Ļ│╝ Ļ░ÉĻ░üņŗĀĻ▓Į ļé£ņ▓ŁņØä ļ¬©ļæÉ ļ│┤ņØ┤ļŖö ĒÖśņ×ÉņŚÉ ļīĆĒĢ┤ ļ│┤Ļ│ĀĒĢśņśĆļŗż. ņŚĪņŖżĒāĆņØĖņ”ØĒøäĻĄ░ņØĆ 2010ļģäņŚÉ ļ░£Ēæ£ļÉ£ ļģ╝ļ¼ĖņŚÉ ļö░ļź┤ļ®┤ 113Ļ░ĆĻ│äļ¦īņØ┤ ļ│┤Ļ│ĀļÉśņŚłņØä ņĀĢļÅäļĪ£ ĒØöĒĢśņ¦Ć ņĢŖņØĆ ņ¦łĒÖśņØ┤ļŗż[4]. ņØ┤ļŖö MYH9 ņŚ░Ļ┤Ć ņ¦łĒÖś(MYH9-related disease [MYH9-RD]) ņżæ ĒĢśļéśļĪ£, ņāüņŚ╝ņāēņ▓┤ ņÜ░ņä▒ ņ¢æņāüņ£╝ļĪ£ ņ£ĀņĀäļÉ£ļŗż. MYH9 ņ£ĀņĀäņ×ÉļŖö ņäĖĒżĻ│©Ļ▓® ņłśņČĢ ļŗ©ļ░▒ņ¦łņØĖ non-muscle myosin IIA (NMM-IIA)ņØś ņżæņćä(heavy chain)ļź╝ ņĢöĒśĖĒÖöĒĢ£ļŗż. NMM-IIAļŖö ņäĖĒżņ¦ł ļČäņŚ┤, ĒżņŗØ ņ×æņÜ®, ņäĖĒż ņÜ┤ļÅÖĻ│╝ ņäĖĒż ļ¬©ņ¢æ ņ£Āņ¦ĆņÖĆ Ļ┤ĆļĀ©ļÉ£ ĻĖ░ļŖźņØä ĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ Ļ▒░ļīĆĒśłņåīĒīÉņØ┤ ļ░£ņāØĒĢśĻ│Ā, ļé┤ņØ┤, ņłśņĀĢņ▓┤, ņŗĀņןņØś ņĪ▒ņäĖĒżņŚÉļÅä ņśüĒ¢źņØä ņżīņ£╝ļĪ£ņŹ© Ļ░ÉĻ░üņŗĀĻ▓Į ļé£ņ▓Ł, ļ░▒ļé┤ņן, ņŗĀņןņŚ╝ļÅä ļ░£ņāØĒĢ£ļŗż. MYH9-RDņŚÉļŖö Ļ░ÉĻ░üņŗĀĻ▓Į ļé£ņ▓Ł, ļ░▒ļé┤ņן, ņŗĀņןņŚ╝Ļ│╝ ĒśĖņżæĻĄ¼ ļ┤ēņ×ģņ▓┤(neutrophil inclusion body)ļØ╝ļŖö 4Ļ░Ćņ¦Ć ĒŖ╣ņ¦ĢņØ┤ ņ׳Ļ│Ā, ņØ┤ 4Ļ░Ćņ¦Ć ĒŖ╣ņ¦ĢņØś ņĪ░ĒĢ®ņŚÉ ļö░ļØ╝ ļ®öņØ┤ĒŚżĻĖĆļ”░ ņØ┤ņāü, ņŚĪņŖżĒāĆņØĖņ”ØĒøäĻĄ░, ĒÄÖĒŖĖļäłņ”ØĒøäĻĄ░Ļ│╝ ņäĖļ░öņŖżĒŗ░ņĢłņ”ØĒøäĻĄ░ņ£╝ļĪ£ ĻĄ¼ļČäļÉ£ļŗż. ļ®öņØ┤ĒŚżĻĖĆļ”░ ņØ┤ņāüĻ│╝ ņäĖļ░öņŖżĒŗ░ņĢłņ”ØĒøäĻĄ░ņØĆ ĒśĖņżæĻĄ¼ ļ┤ēņ×ģņ▓┤Ļ░Ć ņ׳Ļ│Ā ĒÄÖĒŖĖļäłņ”ØĒøäĻĄ░ņØĆ ļ░▒ļé┤ņןņØä ļÅÖļ░śĒĢ£ļŗż. ļ│Ė ĒÖśņ×ÉļŖö ĒśĖņżæĻĄ¼ ļ┤ēņ×ģņ▓┤Ļ░Ć ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśĻ│Ā ļ░▒ļé┤ņןņØ┤ ļÅÖļ░śļÉśņ¦Ć ņĢŖņĢśĻĖ░ ļĢīļ¼ĖņŚÉ MYH9-RD ņżæ ņŚĪņŖżĒāĆņØĖņ”ØĒøäĻĄ░ņŚÉ ĒĢ®ļŗ╣ĒĢśļŗż. MYH9-RD ņżæ ņĢĮ 20-30%ļŖö ņāłļĪ£ ļ░£ņāØĒĢ£ ļÅīņŚ░ļ│ĆņØ┤(de novo mutation)ļĪ£ Ļ░ĆņĪ▒ļĀźņØ┤ ņŚåņØä ņłś ņ׳ļŗż[4].
MYH9-RDņŚÉņä£ ļ¦Éņ┤łĒśłņĢĪņØś ĒśłņåīĒīÉņØĆ Ļ░ÉņåīļÉśņ¢┤ ņ׳ņ¦Ćļ¦ī Ļ│©ņłś Ļ▓Ćņé¼ņŚÉņä£ Ļ▒░ļīĆĒĢĄņäĖĒżņØś ņłśļŖö ņĀĢņāüņØ┤Ļ▒░ļéś ņĢĮĻ░ä ņ”ØĻ░ĆļÉśņ¢┤ ņ׳ļŗż. ĒśłņåīĒīÉņØś Ēü¼ĻĖ░Ļ░Ć Ēü¼ĻĖ░ ļĢīļ¼ĖņŚÉ ĻĖ░Ļ│äļĪ£ ņłśļź╝ ņĖĪņĀĢĒĢĀ Ļ▓ĮņÜ░ ņŗżņĀ£ ĒśłņåīĒīÉ ņłśļ│┤ļŗż ļŹö ņĀüĻ▓ī ņĖĪņĀĢņØ┤ ļÉśļ»ĆļĪ£ ņĀĢĒÖĢĒĢ£ ĒśłņåīĒīÉ ņłśļź╝ ņĖĪņĀĢĒĢśĻĖ░ ņ£äĒĢ┤ņä£ļŖö ņ¦üņĀæ Ļ│äņłśļź╝ ĒĢ┤ņĢ╝ ĒĢ£ļŗż. ņŚĪņŖżĒāĆņØĖņ”ØĒøäĻĄ░ņØä ļ╣äļĪ»ĒĢ£ MYH9-RDņŚÉņä£ ĒśłņåīĒīÉņØś Ēü¼ĻĖ░Ļ░Ć Ēü¼ņ¦Ćļ¦ī ĻĘĖ ĻĖ░ļŖźņŚÉļŖö ņØ┤ņāüņØ┤ ņŚåņ£╝ļ®░ ĒśłņåīĒīÉ ņłśĻ░Ć ļé«ļŹöļØ╝ļÅä ļīĆĻ░£ ņāØļ¬ģņØä ņ£äĒśæĒĢśļŖö ņČ£ĒśłņØĆ ņŚåĻĖ░ ļĢīļ¼ĖņŚÉ ĒśłņåīĒīÉ ņłśĻ░Ć ņĀüņØäņ¦ĆļØ╝ļÅä ņĀĢĻĖ░ņĀüņ£╝ļĪ£ ĒśłņåīĒīÉņØä ņłśĒśłĒĢśņ¦ĆļŖö ņĢŖĻ│Ā, ņČ£ĒśłņØ┤ ļ░£ņāØĒĢśņśĆņØä ļĢī Ēś╣ņØĆ ņČ£ĒśłņØ┤ ņśłņāüļÉśļŖö ņŗ£ņłĀņØ┤ļéś ņłśņłĀ ņĀäņŚÉ ņśłļ░®ņĀüņ£╝ļĪ£ ĒśłņåīĒīÉņØä ņłśĒśłĒĢ£ļŗż. ņŖżĒģīļĪ£ņØ┤ļō£, ļ®┤ņŚŁĻĖĆļĪ£ļČłļ”░, ļ╣äņןņĀłņĀ£ļŖö ĒśłņåīĒīÉ ņłśļź╝ ļŖśļ”¼Ļ▒░ļéś ņČ£Ēśł ņ£äĒŚśņØä ļé«ņČöļŖöļŹ░ ĒÜ©Ļ│╝Ļ░Ć ņŚåļŗż[4]. MYH9-RDņØś ņ╣śļŻīņŚÉņä£ ņżæņÜöĒĢ£ Ļ▓āņØĆ ĒŖ╣Ē׳ Ļ░Ćņ×äĻĖ░ ņŚ¼ņä▒ņŚÉņä£ ņ▓ĀĻ▓░ĒĢŹņä▒ ļ╣łĒśłņØś ļ░£ņāØņØä ņśłļ░®ĒĢśļŖö Ļ▓āņØ┤ļŗż. Ļ▒░ļīĆĒśłņåīĒīÉņØĆ ĒśłĻ┤Ćļ▓Įņ£╝ļĪ£ ņØ┤ļÅÖĒĢśļŖöļŹ░ ņĀüĒśłĻĄ¼ļź╝ ĒĢäņÜöļĪ£ ĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ņĀüĒśłĻĄ¼ņÜ®ņĀüļźĀņØ┤ ļé«ņ£╝ļ®┤ ĒśłņåīĒīÉ-ļé┤Ēö╝ĒĢś ņāüĒśĖņ×æņÜ®(ņØ╝ņ░©ņ¦ĆĒśł)ņØś ļČĆņĀäņØ┤ ņĢģĒÖöļÉśĻĖ░ ļĢīļ¼ĖņØ┤ļŗż. ļśÉĒĢ£, ĒśłņåīĒīÉ ĻĖ░ļŖźņŚÉ ņśüĒ¢źņØä ņŻ╝ļŖö ņĢĮļ¼╝(ņĢäņŖżĒö╝ļ”░ņØ┤ļéś ļŗżļźĖ ļ╣äņŖżĒģīļĪ£ņØ┤ļō£ ĒĢŁņŚ╝ņ”ØņĀ£)ņØś ņé¼ņÜ®ņØä Ēö╝ĒĢ┤ņĢ╝ ĒĢśĻ│Ā ĒĢŁĒśłņåīĒīÉņĀ£ ņé¼ņÜ®ņØä ņĄ£ļīĆĒĢ£ ņĀüĻ▓ī ĒĢ┤ņĢ╝ ĒĢśļ»ĆļĪ£ ļ¦īņĢĮ Ļ┤ĆņāüļÅÖļ¦źņŚÉ ņŖżĒģÉĒŖĖļź╝ ļäŻņ¢┤ņĢ╝ ĒĢ£ļŗżļ®┤ ņĢĮļ¼╝ ņÜ®ņČ£ ņŖżĒģÉĒŖĖļ│┤ļŗż ņØ╝ļ░ś ĻĖłņåŹ ņŖżĒģÉĒŖĖļź╝ ļäŻļŖö Ļ▓āņØ┤ ļæÉ Ļ░Ćņ¦Ć ĒĢŁĒśłņåīĒīÉņĀ£ņĀ£ ļ│ĄņÜ®ĻĖ░Ļ░äņØ┤ ņ¦¦ņ£╝ļ»ĆļĪ£ ļŹö ļéśņØä Ļ▓āņØ┤ļŗż. ĻĘĖļ”¼Ļ│Ā ņ×ćļ¬Ė ņŚ╝ņ”ØņØĆ ņ×ćļ¬ĖņČ£ĒśłņØś ņ£äĒŚśņØä ļåÆņØ┤ļ»ĆļĪ£ ņĀĢĻĖ░ņĀüņØĖ ņ╣śĻ│╝ ņ¦äļŻīļź╝ ļ░øļŖö Ļ▓āņØ┤ ņČöņ▓£ļÉ£ļŗż.
NMM-IIA ļÅīņŚ░ļ│ĆņØ┤ņØś ļ╣äņĪ░ĒśłĻ│ä ņ×äņāü ņ¢æņāüņØä ņśłļ░®ĒĢĀ ņłś ņ׳ļŖö ņ╣śļŻīļ▓ĢņØĆ ņŚåļŗż. ļŹö ņ¢┤ļ”┤ ļĢī ņĢäņŻ╝ Ēü░ ņåīļ”¼ļź╝ Ēö╝ĒĢśļŖö Ļ▓āņØ┤ ņ▓ŁļĀź ņĀĆĒĢśņØś ņåŹļÅäļź╝ ļŖ”ņČ£ ņłś ņ׳ļŗżĻ│Ā ņĢīļĀżņĀĖ ņ׳Ļ│Ā ļ│Ė ĒÖśņ×ÉĻ░Ć ņØ┤ļ╣äņØĖĒøäĻ│╝ņŚÉņä£ ĻČīņ£Āļ░øņĢśļŹś Ļ▓āĻ│╝ Ļ░ÖņØ┤ ņØĖĻ│ĄņÖĆņÜ░ ņØ┤ņŗØ ļśÉĒĢ£ ņ▓ŁļĀź Ē¢źņāüņŚÉ ļÅäņøĆņØä ņżä ņłś ņ׳ļŗż[5]. ņŚĪņŖżĒāĆņØĖņ”ØĒøäĻĄ░ ĒÖśņ×ÉņŚÉņä£ ļĀłļŗī-ņĢłņ¦ĆņśżĒģÉņŗĀ ņ¢ĄņĀ£ņĀ£ļŖö ĒÜ©Ļ│╝ņĀüņ£╝ļĪ£ ļŗ©ļ░▒ļć©ļź╝ Ļ░Éņåīņŗ£Ēéżļ»ĆļĪ£ ņŗĀņן Ļ┤ĆļĀ© ņ”ØņāüņØ┤ ļéśĒāĆļé¼ņØä ļĢī ņé¼ņÜ®ĒĢśļŖö Ļ▓āņØ┤ ņóŗĻ▓Āņ£╝ļéś ņØ┤ ņĢĮļ¼╝ņØś ņé¼ņÜ®ņØ┤ ņŗĀļČĆņĀäņØä ļŖ”ņČöĻ▒░ļéś ņśłļ░®ĒĢĀ ņłś ņ׳ļŖöņ¦ĆļŖö ļ¬ģĒÖĢĒĢśņ¦Ć ņĢŖļŗż. ņŗĀņן ņØ┤ņŗØ ļśÉĒĢ£ ņŗ£Ē¢ēĒĢĀ ņłś ņ׳ņ£╝ļ®░ ņŗĀņן ņØ┤ņŗØņØä ņŗ£Ē¢ēĒĢĀ Ļ▓ĮņÜ░ ĒśłņåīĒīÉņØĆ 100,000/uL ņØ┤ņāüņ£╝ļĪ£ ņ£Āņ¦ĆĒĢśļŖö Ļ▓āņØ┤ ņĢłņĀäĒĢśĻ▓ĀļŗżļŖö ļ│┤Ļ│ĀĻ░Ć ņ׳ļŗż[6].
ņ×äņŗĀņØ┤ļéś ņČ£ņé░Ļ│╝ Ļ┤ĆļĀ©ĒĢ£ ņŻ╝ļÉ£ ņČ£Ēśł ĒĢ®ļ│æņ”ØņØĆ ņ”ØĻ░ĆĒĢśņ¦Ć ņĢŖņ£╝ļ®░ MYH9-RD ĒÖśņ×ÉļØ╝ļŖö Ļ▓āļ¦īņ£╝ļĪ£ ņĀ£ņÖĢņĀłĻ░£ņØś ņĀüņØæņ”ØņØ┤ ļÉśņ¦Ć ņĢŖļŖöļŗż. ļ¦īņĢĮ ļČĆļ¬© ņżæ ĒĢ£ ļ¬ģņØ┤ MYH9-RDļØ╝ļ®┤ ņČ£ņāØ ņ¦üĒøä ņŗĀņāØņĢäņØś ĒśłņåīĒīÉ ņłśĻ░Ć ļé«ņØĆ Ļ▓ĮņÜ░ ļæÉĻ░£Ļ│© ņ┤łņØīĒīīļź╝ ņŗ£Ē¢ēĒĢśņŚ¼ ļæÉĻ░£ ļé┤ ņČ£ĒśłņØ┤ ņ׳ļŖöņ¦Ć ĒÖĢņØĖĒĢśņŚ¼, ļæÉĻ░£ ļé┤ ņČ£ĒśłņØ┤ ņ׳ņØä Ļ▓ĮņÜ░ ĒśłņåīĒīÉ ņłśĒśłņØ┤ ņČöņ▓£ļÉ£ļŗż[4].
ĒśłņåīĒīÉ ņłśĒśłņØä ĒåĄĒĢ┤ ņØ╝ņŗ£ņĀüņ£╝ļĪ£ ĒśłņåīĒīÉ ņłśļź╝ ņś¼ļ”┤ ņłś ņ׳ņ£╝ļéś ļ░śļ│ĄņĀüņØĖ ĒśłņåīĒīÉ ņłśĒśł Ēøä ļÅÖņóģļ®┤ņŚŁņŚÉ ņØśĒĢ┤ ĒśłņåīĒīÉ ņłśĒśłņŚÉ ņĀĆĒĢŁņØ┤ ļ░£ņāØĒĢĀ ņłś ņ׳ļŗż. ņĪ░Ēśłļ¬©ņäĖĒż ņØ┤ņŗØņØä ĒåĄĒĢśņŚ¼ ņ£ĀņĀäņä▒ ĒśłņåīĒīÉĻ░Éņåīņ”ØņØä ņÖäņ╣śĒĢĀ ņłś ņ׳ņ¦Ćļ¦ī ņĪ░Ēśłļ¬©ņäĖĒż ņØ┤ņŗØ ņ×Éņ▓┤ņØś ņ£äĒŚśņØ┤ ņ׳ņ¢┤ņä£ ļ▓Āļź┤ļéśļź┤-ņŖÉļ”¼ņŚÉņ”ØĒøäĻĄ░Ļ│╝ Ļ░ÖņØĆ ņŗ¼Ļ░üĒĢ£ ņśłĒøäļź╝ ļ│┤ņØ┤ļŖö ļ¬ćļ¬ć Ļ▓ĮņÜ░ņŚÉļ¦ī Ļ│ĀļĀżĒĢśļ®░ ļīĆĻ░£ Ļ░Ćļ▓╝ņÜ┤ ņČ£ĒśłņØä ļ│┤ņØ┤ļŖö MYH9-RDļŖö ņĪ░Ēśłļ¬©ņäĖĒż ņØ┤ņŗØņØś Ļ│ĀļĀżļīĆņāüņØ┤ ļÉśņ¦Ć ņĢŖļŖöļŗż. ņŚśĒŖĖļĪ¼ļ│┤ĒīŹ ņś¼ļØ╝ļ»╝ņØĆ Ļ▓ĮĻĄ¼ Ēł¼ņŚ¼ Ļ░ĆļŖźĒĢ£ ļ╣äĒÄ®ĒāĆņØ┤ļō£ ĒŖĖļĪ¼ļ│┤ĒżņØ┤ņŚÉĒŗ┤ ņłśņÜ®ņ▓┤ ĻĖĖĒĢŁņĀ£ļĪ£ ļ¦īņä▒ ļ®┤ņŚŁĒśłņåīĒīÉĻ░Éņåīņ×Éņāēļ░śļ│æĒÖśņ×ÉņÖĆ CĒśĢ Ļ░äņŚ╝ņŚÉ ņØśĒĢ£ Ļ░äĻ▓ĮĒÖö ĒÖśņ×ÉņŚÉņä£ ĒśłņåīĒīÉ Ļ░Éņåīļź╝ Ļ░£ņäĀĒĢĀ ņłś ņ׳ļŗż. 2010ļģä Pecci ļō▒[7]ņØĆ 12ļ¬ģņØś MYH9-RD ĒÖśņ×ÉņŚÉĻ▓ī ņŚśĒŖĖļĪ¼ļ│┤ĒīŹ ņś¼ļØ╝ļ»╝ņØä ņé¼ņÜ®ĒĢśņśĆĻ│Ā 12ļ¬ģ ņżæ 7ļ¬ģņŚÉņä£ ĒśłņåīĒīÉ ņłśĻ░Ć 100 ├Ś 109/L ņØ┤ņāüņ£╝ļĪ£ ņāüņŖ╣ĒĢśņśĆĻ│Ā ņČ£Ēśł ņ”ØņāüļÅä ņÖäņĀäĒ׳ ņåīņŗżļÉśņŚłļŗż. ņØ┤ 7ļ¬ģ ņżæ 5ļ¬ģņØĆ ņŚśĒŖĖļĪ¼ļ│┤ĒīŹ ņś¼ļØ╝ļ»╝ņØä ļ¦żņØ╝ 50 mgņ£╝ļĪ£ 3ņŻ╝Ļ░ä ņé¼ņÜ®ĒĢ£ Ēøä ĒśłņåīĒīÉ ņłśĻ░Ć 100 ├Ś 109/L ņØ┤ņāüņ£╝ļĪ£ ņāüņŖ╣ĒĢśņśĆĻ│Ā ļéśļ©Ėņ¦Ć 2ļ¬ģņØĆ ļ¦żņØ╝ 75 mgņ£╝ļĪ£ 3ņŻ╝ļź╝ ļŹö ņé¼ņÜ®ĒĢ£ ĒøäņŚÉ ĒśłņåīĒīÉ ņłśĻ░Ć 100 ├Ś 109/L ņØ┤ņāüņ£╝ļĪ£ ņāüņŖ╣ĒĢśņśĆļŗż. ĒŖ╣Ē׳ ņØ┤ņĀäņŚÉ ļ╣äņן ņĀłņĀ£ļź╝ ņŗ£Ē¢ēĒĢśņśĆļŹś Ļ▓ĮņÜ░ņŚÉ ĒÜ©Ļ│╝Ļ░Ć ļŹö ņóŗņĢśņ£╝ļ®░ ļ¬©ļōĀ ĒÖśņ×ÉņŚÉņä£ ņČ£Ēśłņä▒ Ļ▓ĮĒ¢źņØĆ ĒśĖņĀäļÉśņŚłĻ│Ā ņĢĮņØä ņżæļŗ©ĒĢ£ Ēøä ļŗżņŗ£ ņČ£Ēśłņä▒ Ļ▓ĮĒ¢źņØ┤ ļ░£ņāØĒĢśņ¦Ć ņĢŖņĢśļŗż. Pecci ļō▒[8]ņØĆ 2012ļģäņŚÉ MYH9-RD ĒÖśņ×ÉņŚÉņä£ ņ¢æņ¬Į ņŚäņ¦Ć ļ░£Ļ░ĆļØĮņŚÉ ļ░£ņāØĒĢ£ Ļ▒┤ļ¦ēļźśņÖĆ ņĀ£2 ņżæņĪ▒Ļ│©ņØś ĻĖ░ĒśĢņŚÉ ļīĆĒĢ┤ Ļ▓ĮĒö╝ņĀü ņĀ£1, ņĀ£2 ņżæņĪ▒Ļ│©ņØś ļ¦Éļŗ© Ļ│©ņĀłņłĀ ņĀäņŚÉ ĒśłņåīĒīÉ ņłśĒśł ļīĆņŗĀ ņŚśĒŖĖļĪ¼ļ│┤ĒīŹ ņś¼ļØ╝ļ»╝ņØä 50mg/dayļĪ£ 20ņØ╝Ļ░ä ņé¼ņÜ®ĒĢśņśĆļŗż. ņŚśĒŖĖļĪ¼ļ│┤ĒīŹ ņś¼ļØ╝ļ»╝ ņé¼ņÜ® 7-8ņØ╝ ļÆż ņ×Éļ░£ ņČ£ĒśłņØĆ ņé¼ļØ╝ņĪīĻ│Ā ņ╣śļŻī 10-12ņØ╝ ļÆż ĒśłņåīĒīÉ ņłśĻ░Ć ĻĖēņ”ØĒĢśņŚ¼ 17ņØ╝ņ¦ĖņŚÉ ĒśłņåīĒīÉņØĆ 195 ├Ś 109/LņŚÉ ļÅäļŗ¼ĒĢśņśĆļŗż. ņØ┤ļ│┤Ļ│Āļź╝ ĒåĄĒĢ┤ MYH9-RD ĒÖśņ×ÉņŚÉņä£ ņłśņłĀ ņĀä ĒśłņåīĒīÉ ņłśĒśł ņÖĖņŚÉ ņŚśĒŖĖļĪ¼ļ│┤ĒīŹ ņś¼ļØ╝ļ»╝ņØä ļŗ©ĻĖ░Ļ░ä ņé¼ņÜ®ĒĢśļŖö Ļ▓āļÅä Ļ│ĀļĀżĒĢ┤ ļ│╝ ņłś ņ׳ļŖö ļ░®ļ▓Ģņ×äņØä ņĢī ņłś ņ׳ļŗż.
ļ│Ė ĒÖśņ×ÉļŖö Ļ░ĆņĪ▒ļĀźņØ┤ ņŚåņŚłĻĖ░ ļĢīļ¼ĖņŚÉ ņ¦äļŗ©ņŚÉ ļŹöņÜ▒ ņ¢┤ļĀżņøĆņØä Ļ▓¬ņŚłļŗż. ņĢ×ņä£ ĻĖ░ņłĀĒĢ£ Ļ▓āņ▓śļ¤╝ ņŚĪņŖżĒāĆņØĖņ”ØĒøäĻĄ░ņØĆ ņāüņŚ╝ņāēņ▓┤ ņÜ░ņä▒ ņ¢æņāüņ£╝ļĪ£ ņ£ĀņĀäļÉśņ¦Ćļ¦ī 20-30%ļŖö Ļ░ĆņĪ▒ļĀźņØ┤ ņŚåņØ┤ ļ░£ņāØĒĢ£ļŗż. 2011ļģäņŚÉ Han ļō▒[9]ņØ┤ ļ│┤Ļ│ĀĒĢ£ ļ░▒ļé┤ņןņØ┤ ņŚåĻ│Ā D├Čhle-like bodiesĻ░Ć ņŚåļŖö 3ļ▓ł ņŚ¼ĒÖśņØ┤ ņŚĪņŖżĒāĆņØĖņ”ØĒøäĻĄ░ņ£╝ļĪ£ ņČöņĀĢļÉśļ®░ Ļ░ĆņĪ▒ļĀźņŚåņØ┤ ļ░£ņāØĒĢ£ ĻĄŁļé┤ ņé¼ļĪĆņØ┤ļŗż. ņØ┤ ļģ╝ļ¼ĖņŚÉņä£ NMM-IIAņØś ņÜ┤ļÅÖ ļÅäļ®öņØĖņŚÉ ļÅīņŚ░ļ│ĆņØ┤Ļ░Ć ņ׳Ļ│Ā Ļ░ĆņĪ▒ļĀźņØ┤ ņŚåļŖö Ļ▓ĮņÜ░Ļ░Ć ņŗ¼ĒĢ£ ņŗĀņןņ╣©ļ▓öĻ│╝ Ļ┤ĆļĀ©ņØ┤ ņ׳ņŚłļŗż[9]. 2015ļģä Makino ļō▒[10]ņØ┤ ļ│┤Ļ│ĀĒĢ£ 3ņé┤ņŚÉ ļ│æņøÉņŚÉ ļé┤ņøÉĒĢśņŚ¼ 20ņäĖņŚÉ ņ”ē, 17ļģä ļ¦īņŚÉ ņ¦äļŗ©ļÉ£ ļé©ņ×É ĒÖśņ×ÉļÅä ļ╣äĻ░ĆņĪ▒ņä▒ ņŚĪņŖżĒāĆņØĖņ”ØĒøäĻĄ░ņØ┤ņŚłļŗż.
REFERENCES
1. Neunert C, Lim W, Crowther M, et al. The American Society of Hematology 2011 evidence-based practice guideline for immune thrombocytopenia. Blood 2011;117:4190ŌĆō4207.


2. Sarangi SN, Acharya SS. Bleeding disorders in congenital syndromes. Pediatrics 2017;139:e20154360.


3. Epstein CJ, Sahud MA, Piel CF, et al. Hereditary macrothrombocytopathia, nephritis and deafness. Am J Med 1972;52:299ŌĆō310.


4. Althaus K, Greinacher A. MYH-9 related platelet disorders: strategies for management and diagnosis. Transfus Med Hemother 2010;37:260ŌĆō267.



5. Singh N, Nainani N, Arora P, Venuto RC. CKD in MYH9-related disorders. Am J Kidney Dis 2009;54:732ŌĆō740.


6. Hashimoto J, Hamasaki Y, Yanagisawa T, Sekine T, Aikawa A, Shishido S. Successful kidney transplantation in Epstein syndrome with atiplatelet antibodies and donor-specific antibodies: a case report. Transplant Proc 2015;47:2541ŌĆō2543.


7. Pecci A, Gresele P, Klersy C, et al. Eltrombopag for the treatment of the inherited thrombocytopenia deriving from MYH9 mutations. Blood 2010;116:5832ŌĆō5837.


8. Pecci A, Barozzi S, d'Amico S, Balduini CL. Short-term eltrombopag for surgical preparation of a patient with inherited thrombocytopenia deriving from MYH9 mutation. Thromb Haemost 2012;107:1188ŌĆō1189.


Peripheral blood smear (├Ś200). Giant platelets, thrombocytopenia, and normochromic normocytic anemia are shown in the peripheral blood smear. Platelet sizes are similar to those of red blood cells (arrows).
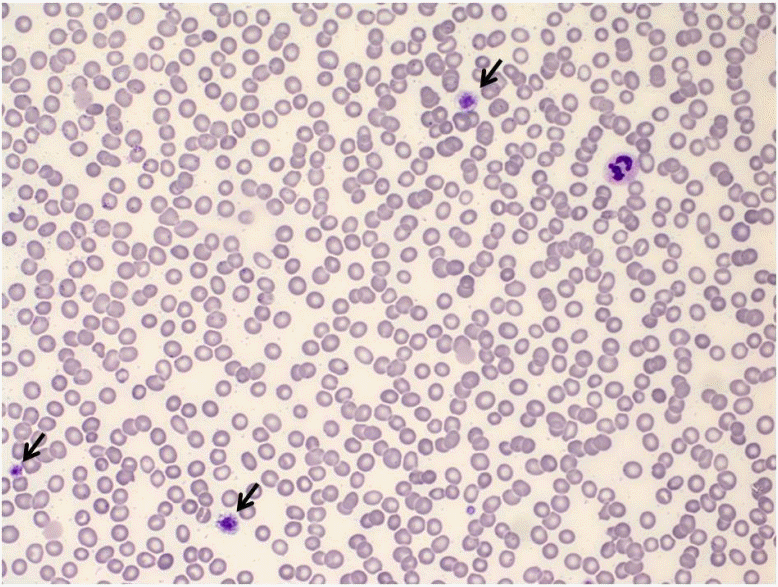
Figure┬Ā1.
Bone marrow study. (A) Bone marrow biopsy. The cellularity is 35%. (B) Bone marrow aspiration (├Ś200). The number of megakaryocytes (arrows) in the bone marrow is adequate.
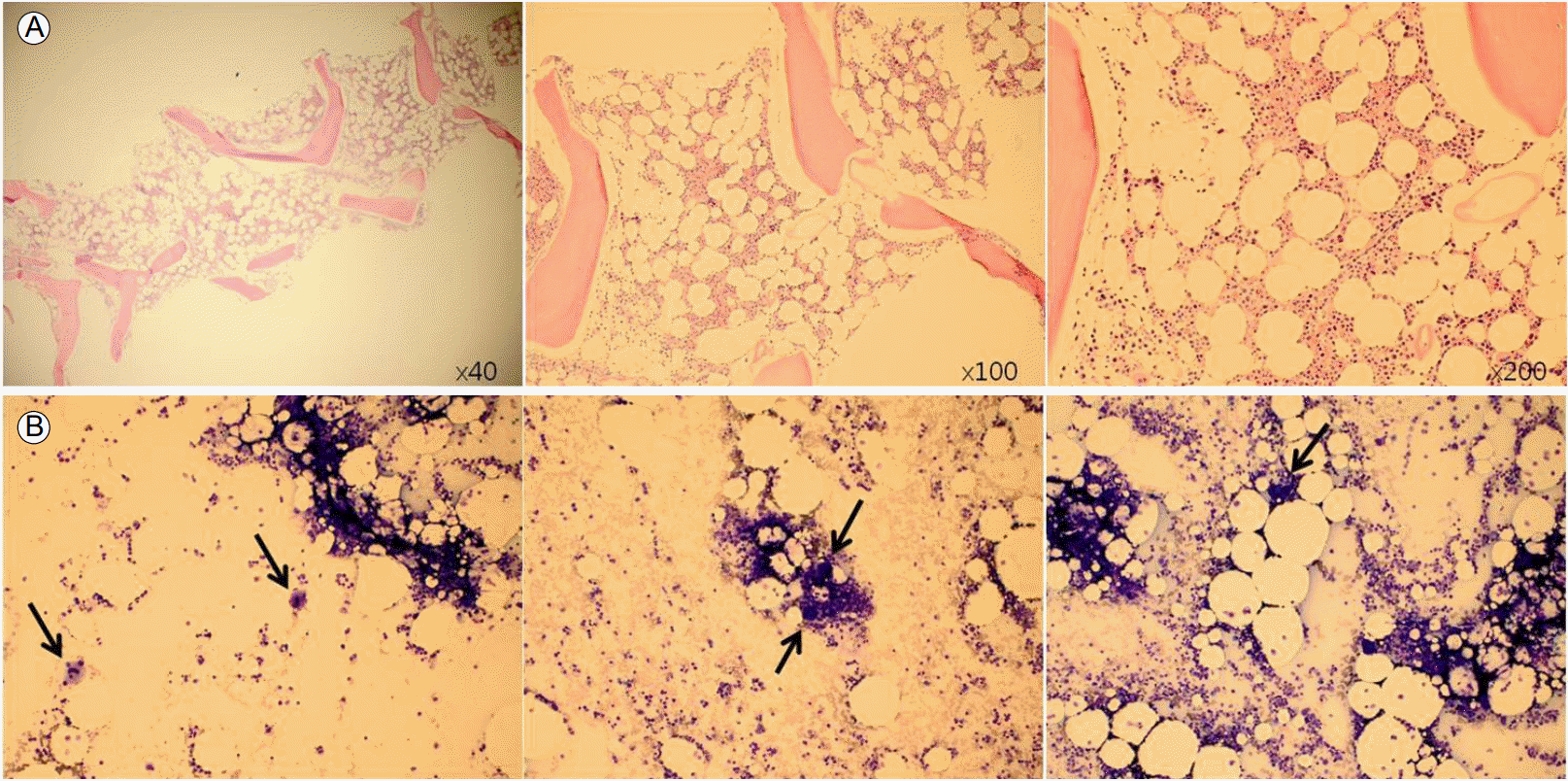
Figure┬Ā2.
Exon 2 of MYH9 was amplified by polymerase chain reaction from genomic deoxyribonucleic acid isolated from peripheral leukocytes. Sequence analyses were performed using BigDye termination kit v.3.0 and an ABI3130xl Genetic analyzer (Applied Biosystems, Foster city, CA, USA). NM_002473.4 in GenBank was used as a reference sequence. The electropherogram identified a novel heterozygous variant, c.221_223del (p.Lys74del). MYH9, myosin heavy chain 9 gene.
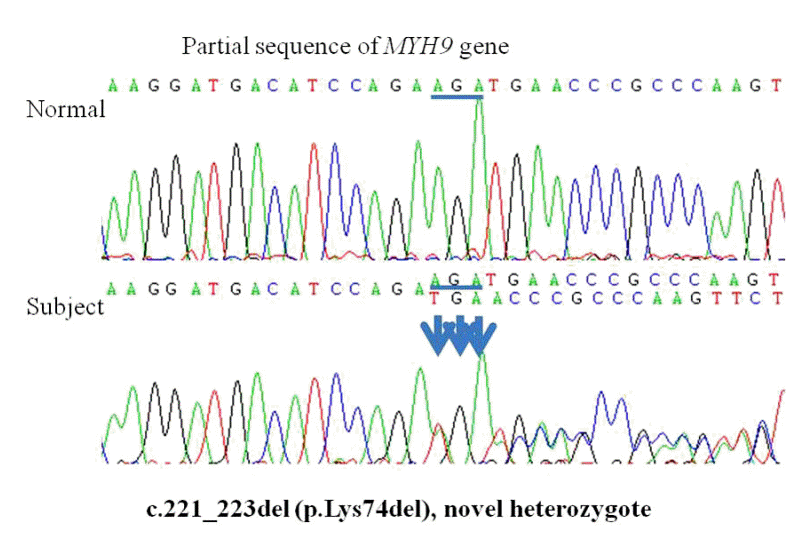



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




