거대 관상동맥류를 동반한 우관상동맥-좌심실 누공
Right Coronary Artery to Left Ventricular Fistula with Giant Right Coronary Artery Aneurysm
Article information
Abstract
35세 남자가 피로감 및 호흡곤란으로 병원에 왔다. 청진상 확장기 심장잡음이 들리고 심전도 및 흉부 X선 검사에서 좌심실비대 소견이 보였다. 가슴 경유 심초음파 검사에서 좌심실 기저부의 하벽에 지름 11 mm 크기의 심근 결손 부위가 보였고 우관상동맥으로 보이는 확장된 혈관구조물로부터 심근 결손 부위를 통해 좌심실 내로 유입되는 확장기 혈류가 보였다. 식도 경유 심초음파 검사에서 최대 지름 17 mm의 확장된 우관상동맥이 보였다. 관상동맥 컴퓨터단층촬영 조영 검사에서 거대 관상동맥류를 동반한 우관상동맥이 좌심실 기저부의 좌심실 벽 결손부를 통해 좌심실과 연결되어 있음을 확인한 후 거대 관상동맥류를 동반한 우관상동맥-좌심실 누공으로 진단하였다. 관상동맥류를 동반한 우관상동맥-좌심실 누공은 드물게 보고되는데, 좌심실의 용적 과부하로 인한 울혈성 심부전 발생의 위험성과 거대 관상동맥류의 자연적 파열 위험성을 고려하여 수술적으로 우관상동맥을 폐쇄 하기로 하였다. 개흉술을 시행하여 우관상동맥의 입구와 우 관상동맥-좌심실 누공 부위를 소심장막패치를 덧대어 봉합 하고 우관상동맥을 결찰하였다. 우관상동맥에서 갈라져 나오는 지름이 큰 동맥가지들이 없어 심근경색을 예방하기 위한 관상동맥 우회로조성술을 시행하지 않기로 하였다. 환자는 수술 관련 합병증 없이 퇴원하였고 증상의 재발 없이 추적 관찰 중이다. 저자들은 임상에서 접하기 힘든 증상을 동반한 우관상동맥-좌심실 누공의 영상 진단 및 수술적 치료 과정을 문헌고찰과 함께 보고하는 바이다.
Trans Abstract
A 35-year-old male with exertional dyspnea was transferred to our hospital for evaluation of a diastolic murmur and cardiomegaly discovered by chest X-ray. Two-dimensional and Doppler echocardiographic studies revealed an aneurysmal dilation of the right coronary artery (RCA) and diastolic inflow from the RCA to the left ventricle (LV) through a myocardial defect 11 mm in diameter in the basal inferior LV wall. Coronary computed tomography angiography (CCTA) confirmed the presence of a giant RCA to LV fistula. Due to the risks for developing overt left heart failure and spontaneous rupture of the giant RCA, the RCA was obliterated surgically. Coronary-cameral fistulas are a rare congenital coronary artery anomaly. A fistula between the coronary artery and LV, especially when combined with coronary artery aneurysm, is a rare occurrence in the literature. Here, we report a case of a giant RCA to LV fistula detected by echocardiography and CCTA.
서 론
선천성 관상동맥 누공(coronary artery fistula)은 관상동맥이 심방 또는 심실, 다른 혈관과 직접 연결되는 단락(shunt)을 형성하는 질병이다. 선천성 관상동맥 누공 중 관상동맥과 심방 또는 심실 사이에 단락이 있는 경우(coronary-cameral fistula)는 드물게 보고되었는데 증상이 있거나 거대 관상동맥류를 동반하는 경우에는 수술적 치료가 필요한 것으로 알려져 있다[1,2]. 저자들은 호흡곤란과 확장기 심장잡음으로 외래를 방문한 젊은 남자를 대상으로 심초음파 및 관상동맥 컴퓨터단층촬영 조영 검사를 시행하여 거대 관상동맥류를 동반한 우관상동맥-좌심실 누공을 진단하였다. 우관상동맥-좌심실 누공의 크기가 커서 좌심실의 용적 과부하에 의해 심부전증이 발생하거나 거대 관상동맥류가 자연적으로 파열될 가능성이 있어 우관상동맥-좌심실 누공을 수술적으로 폐쇄하였다. 이에 증상을 동반한 우관상동맥-좌심실 누공의 진단 및 치료 과정을 문헌고찰과 함께 보고하는 바이다.
증 례
환 자: 35세 남자
주 소: 피로, 운동할 때 발생하는 호흡곤란(New York Heart Association functional class II)
현병력: 환자는 3개월 전부터 피로를 느꼈고 2-3주 전부터는 운동할 때 숨이 차서 동네 의원을 방문하였다. 청진상 확장기 심장잡음이 들리고 단순 흉부 X선 검사에서 심장비대 소견이 보여 정밀 검사를 위해 본원으로 전원되었다.
과거력: 선천성 또는 후천성 심장 질환으로 치료받은 병력은 없었다.
사회력 및 가족력: 흡연은 하지 않았고 심장 질환의 가족력도 없었다.
신체 검사: 병원에 왔을 당시 혈압은 120/80 mmHg, 심장박동수 70회/분, 호흡수 20회/분, 체온 36.4°C였다. 심음 청진상 복장뼈 왼쪽 가장자리 아랫부분에서 확장기 심장잡음이 들렸다. 속목정맥의 확장이나 사지의 오목부종은 관찰되지 않았다.
검사실 소견: 말초 혈액 검사, 간 기능 검사, 콩팥 기능 검사, 전해질 검사, 소변 검사 결과는 정상이었다. 심근 트로포닌 I 검사 결과는 0 ng/mL였다.
흉부 X선 소견: 흉부 X선 검사에서 심장 가슴 비는 0.58이었으며 상행 대동맥의 실루엣이 커져 보였다.
심전도 소견: 정상 동리듬이었으나 심장전유도에서 좌심실비대를 의심할 수 있는 QRS파의 진폭 증가 소견이 보였다.
심장초음파 소견: 좌심실비대 및 확장기 심장잡음에 대한 평가를 위해 가슴 경유 심초음파 검사를 시행하였다. 좌심실 박출률은 62%였으나 좌심실 확장기말 지름은 60 mm로 좌심실이 확장되어 있었다. 도플러 영상에서 좌심실의 확장기에 우관상정맥동(coronary sinus)에서 우관상동맥으로 유출되는 혈류가 보였다(Fig. 1A). 좌심실 기저부의 하벽에 지름 11 mm 크기의 심근 결손 부위가 있었고 하벽의 바깥쪽에서 확장된 우관상동맥으로 보이는 혈관구조물을 볼 수 있었다(Fig. 1B and 1C). 도플러 영상에서 좌심실 하벽의 심근 결손 부위를 통해 좌심실 내로 유입되는 확장기 혈류가 보였다. 거대 관상동맥류를 동반한 우관상동맥-좌심실 누공으로 추정 진단하였다. 경도관 관상동맥 누공 폐색술(transcatheter closure of coronary artery fistula) 시행을 고려하여 우관상동맥류의 유입부를 관찰하고 직경을 정확히 평가하기 위해 식도 경유 심초음파 검사를 시행하였으며 우관상정맥동에서 기원하는 최대 지름 17 mm의 확장된 우관상동맥을 관찰할 수 있었다. 도플러 영상에서 우관상정맥동에서 우관상동맥으로 유출되는 확장기 혈류가 보였다(Fig. 1D).

Echocardiographic findings. (A) Two-dimensional and color Doppler echocardiographic studies from the parasternal short-axis view show the enlarged RCA ostium (empty arrow) and diastolic flows from the right coronary sinus to the RCA. (B) Two-dimensional images from the modified parasternal short-axis view at the level of papillary muscle showed an LV inferior wall defect (arrow) of 11 mm diameter. An enlarged vascular structure (asterisk) was observed below the LV inferior wall. Color Doppler imaging showed diastolic flow running from the enlarged vascular structure to the LV through the LV inferior wall defect, which suggested the presence of a coronary cameral fistula between the giant RCA and the LV. (C) The inferior LV wall defect (arrow) and diastolic inflows through the fistula were shown at the LV base level from a modified apical two-chamber view in color Doppler studies. (D) A transesophageal echocardiogram at 0° showed the enlarged RCA (asterisk), which originated from the right coronary sinus and received diastolic flows. The maximum end-diastolic diameter of the giant RCA was 17 mm. RCA, right coronary artery; LV, left ventricle.
다중검출 컴퓨터단층촬영을 이용한 관상동맥 조영 검사: 다중검출 컴퓨터단층촬영(multidetector computed tomography)을 이용한 관상동맥 조영 검사에서 최대 지름 17 mm의 거대한 우관상동맥이 좌심실의 기저부에서 하벽의 심근 결손 부위를 통해 좌심실로 이어지는 누공을 형성하고 있음을 확인할 수 있었다(Fig. 2). 우관상동맥 근위부의 주행은 정상이었으나 우관상동맥의 원위부에서 후하행관상동맥(posterior descending coronary artery)이나 후측방관상동맥(posterolateral coronary artery)이 갈라져 나오지 않았고 우관상동맥의 원위부가 바로 좌심실로 연결되어 있었다. 상행 대동맥, 좌심실, 좌관상동맥 또한 전반적으로 확장되어 있었다. 우관상동맥에서 갈라져 나오는 지름이 큰 동맥가지들은 보이지 않았다.

Radiographic findings. (A, B) Three-dimensional volume rendering imaging via coronary CT angiography showed an enlarged RCA draining directly into the basal and inferior aspect of the left ventricle. The maximum diameter of the giant RCA measured 17 mm. The posterior descending coronary artery (arrows) originated from the left anterior descending coronary artery. There were no large branches originating from the giant RCA. (C) Multiplanar reconstruction imaging of the RCA revealed a fistula connected to the left ventricle. CT, computed tomography; RCA, right coronary artery.
치료 및 경과: 증상을 동반한 우관상동맥-좌심실 누공을 가진 젊은 환자로 우관상동맥-좌심실 누공의 크기가 커서 좌심실의 용적 과부하에 의해 심부전증이 발생하거나 거대 관상동맥류가 자연적으로 파열될 가능성이 있어 우관상동맥-좌심실 누공을 수술적으로 폐쇄하기로 하였다. 가운데 복장뼈 절개술을 시행한 후 거대 관상동맥류를 동반한 우관상동맥을 육안으로 확인하였다(Fig. 3A). 우관상동맥에서 지름 1.5 mm 미만의 작은 동맥가지들이 갈라져 나왔지만 관상동맥 우회로를 연결할만한 지름이 큰 동맥가지들이 갈라져 나오지는 않았다. 우관상정맥동의 변형에 의한 대동맥 판막의 뒤틀림을 억제하기 위해 소심장막패치(bovine pericardium patch)를 덧대어 우관상동맥의 입구를 폐쇄하였다(Fig. 3B). 우관상동맥을 심실 및 방실 사이고랑(interventricular groove)이 교차하는 부위(crux cordis)에서 가로로 절개한 후 좌심실 벽의 결손 부위를 강화하기 위해 소심장막패치를 덧대어 누공을 폐쇄하였다(Fig. 3C). 좌전하행관상동맥(left anterior descending coronary artery)에서 후하행동맥이 갈라져 나와 좌심실 하벽에 대한 혈액공급이 원활하게 이루어질 수 있었기 때문에 관상동맥 우회로조성술은 시행하지 않기로 하였다(Fig. 3D). 우관상동맥에서 갈라져 나온 지름 1.5 mm 미만의 작은 동맥가지들을 모두 결찰하고 동맥류는 외부에서 연속 봉합술로 결찰하였다. 수술 후 5일째 시행한 추적 가슴 경유 심초음파 검사 결과 우관상동맥에서 좌심실로 유입되는 혈류의 흐름이 보이지 않았고 좌심실 확장기말 지름도 50 mm로 줄어들었으며 우심실 수축 기능의 저하도 없음을 확인하였다. 수술 후 8일째에 시행한 관상동맥 조영 검사에서 관상동맥 누공이 성공적으로 폐쇄되었음을 확인하였다(Fig. 4). 좌전하행관상동맥과 좌선행관상동맥(left circumflex coronary artery)에서 갈라져 나온 잘 발달된 동맥가지들을 통해 좌심실 하벽 및 외벽에 대한 혈액공급이 원활하게 이루어지고 있음을 확인하였다. 환자는 수술 10일째에 합병증 없이 퇴원하였으며 수술 후 1년간 증상의 재발 없이 추적 관찰 중이다.
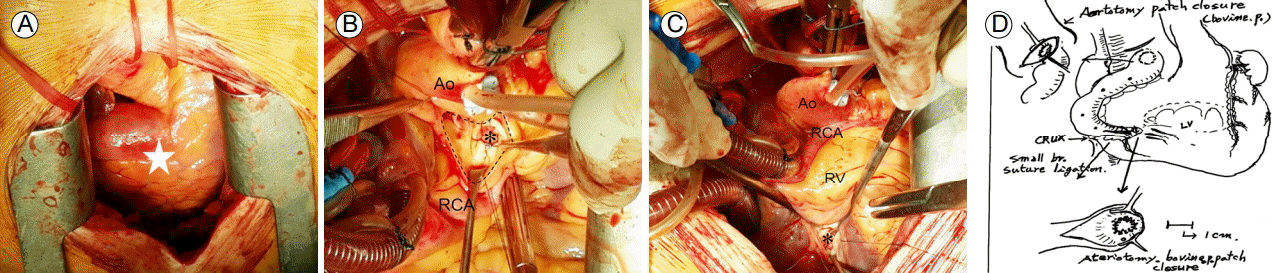
Intraoperative photographic findings. (A) The RCA (star), which originated from the right coronary sinus with aneurysmal dilatation, was revealed after median sternotomy. (B) After aortotomy (dotted line), the 7 mm giant RCA was closed by bovine pericardial patch (asterisk) to minimize deformations of the right coronary sinus and aortic valve. (C) After transverse resection of the giant RCA at the crux cordis level, the RCA to left ventricular fistula opening was closed by bovine pericardia patch (asterisk) to strengthen the defective left ventricular wall. (D) Schematic demonstration of the coronary artery anatomy and surgical procedures. Proximal and distal ends of the RCA were closed by bovine pericardia patches, and small branches originating from the giant RCA were closed directly. Ao, aorta; RCA, right coronary artery; RV, right ventricle.
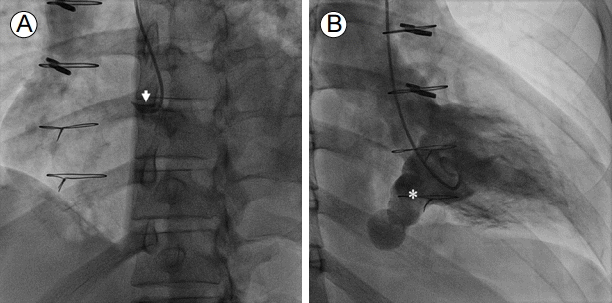
Coronary angiographic findings after surgical closure of the giant RCA. (A) Right coronary angiography showed the stump (arrow) of the closed RCA. (B) Left ventriculography showed a coronary-cameral fistula opening (asterisk) and retrograde filling of the distal end of the closed RCA. However, there was no anterograde or retrograde coronary blood flow through the closed RCA. RCA, right coronary artery.
고 찰
선천성 관상동맥 누공은 선천성 심장 질환의 0.4-0.5%를 차지하는데 이 중 관상동맥과 심방 또는 심실 사이에 직접 단락이 형성되어 있는 경우는 진단적 관상동맥조영술을 시행한 경우의 0.1-0.3%에서 발견되는 것으로 알려져 있다[1,2]. 증상이 없는 경우가 많지만, 여러 개의 누공이 있거나 누공의 크기가 큰 경우에는 심부전증이나 협심증의 증상이 나타날 수 있다[1,3,4]. 저자들의 증례와 같이 관상동맥과 좌심실 사이에 누공이 있는 경우는 전체 선천성 관상동맥 누공 환자의 2-3% 정도에 불과할 정도로 드물게 보고되었다[1,3]. 관상동맥과 좌심실 사이에 누공이 있는 경우 수축기에는 우관상동맥과 좌심실 사이의 압력 차이가 없어 혈류의 흐름이 없지만, 확장기에는 좌심실 내부 압력이 감소하면서 우관상동맥을 통해 좌심실로 혈류의 흐름이 만들어지게 되어 좌심실의 용적 과부하와 대동맥 판막 기능 부전이 발생할 수 있다[5]. 선천적 관상동맥 누공의 자연적 폐쇄는 드물고 20% 정도에서 울혈성 심부전증, 허혈성 심근병증, 감염성 심내막염, 혈전증 등의 합병증이 나타날 수 있는데, 선천성 관상동맥 누공의 치명률은 5% 내외인 것으로 알려져 있다. 시간이 지나면서 합병증이 발생할 위험이 커지므로 증상이 있는 경우 대개 빠른 시일 내에 수술적 치료를 할 것을 권고한다[1,5]. 저자들의 증례와 같이 관상동맥의 지름이 주변에 있는 정상 혈관의 4배 이상이거나 8 mm 이상으로 커진 거대 관상동맥류가 동반되는 경우가 있는데[6], 이 경우 관상동맥의 벽이 점진적으로 약해지면서 관상동맥류가 자연적으로 파열될 수 있으므로 예방적으로 수술적 치료를 할 것을 권고하고 있다[1,5].
선천성 관상동맥 누공의 경우 대개 진단적 관상동맥 조영 검사를 시행하는 도중에 우연히 발견되는 경우가 많지만, 심초음파나 다중검출 컴퓨터단층촬영 등의 비침습적 검사법으로도 진단이 가능하다. 가슴 경유 심초음파를 시행할 경우 이면성 심초음파로 확장된 관상동맥을 관찰하고 도플러 영상에서 심장으로 유입되는 혈류를 확인함으로써 관상동맥 누공의 연결 상태를 파악할 수 있다[5,7]. 식도 경유 심초음파의 경우 가슴 경유 심초음파에 비하여 해상력이 우수하며 관상동맥 누공의 유입부를 더 정확히 관찰할 수 있는 장점이 있어 관상동맥 누공의 평가에는 양자를 모두 시행하는 것이 도움이 된다[7]. 최근에는 관상동맥 기형을 진단하는데 있어 다중열검출기 컴퓨터단층촬영이 많이 이용되고 있다. 일반적인 관상동맥조영술은 관상동맥 누공과 동반된 복잡하고 비정상적인 혈관의 연결 관계를 입체적으로 보여주지 못하는 단점이 있다. 반면에 다중열검출기 컴퓨터단층촬영은 관상동맥의 유입 및 유출 부위를 보여줄 뿐만 아니라 관상동맥의 주행경로 및 주변에 위치한 대혈관들의 위치 관계를 입체적으로 보여주는 장점이 있어 관상동맥 누공 환자의 수술 계획 수립에 도움을 줄 수 있다[8].
관상동맥 누공의 일반적인 치료는 수술적 결찰술이지만 최근에는 코일이나 각종 폐쇄기구 등을 이용한 경도관 관상동맥 누공 폐색술이 활발하게 시도되고 있다. 적절한 환자를 대상으로 경도관 관상동맥 누공 폐색술을 선택적으로 시행할 경우 수술적 치료에 근접하는 좋은 성적을 기대할 수 있고 개흉수술 및 체외순환에 따른 합병증을 피할 수 있는 장점도 있다. 그러나 누공의 크기가 크거나 접근이 어려운 경우에는 시술을 통해 누공을 완전히 폐쇄하는 것이 기술적으로 어려울 수 있다[5,9,10]. 관상동맥 누공의 수술적 결찰은 성공률이 높지만 심근경색을 포함하는 수술 관련 합병증의 발생 빈도가 3-7%에 이르는 것으로 알려져 있다[3,5]. 저자들의 사례에서는 우관상동맥의 주행경로가 굴곡져 있고 동맥류성 확장이 동반되었으며 누공 부위 좌심실 벽의 결손이 11 mm였기 때문에 경도관 관상동맥 누공 폐색술을 시행하더라도 누공을 완전히 폐쇄하지 못할 가능성을 배제할 수 없었다. 누공을 완전히 폐쇄하지 못할 경우 향후 심부전증으로 진행할 가능성이 있고 누공의 연결 부위가 좌심실이어서 경도관 관상동맥 누공 폐색술 중 전신 혈전색전증의 합병증이 발생할 가능성도 있어 수술적 결찰술을 시행하기로 하였다. 선천성 관상동맥 누공의 수술 결과는 좋은 것으로 알려져 있으며 수술 후 심근경색증의 발생률은 3% 정도인 것으로 알려져 있다[3]. 수술을 시행할 때는 심장의 정상적인 혈액공급에 영향을 주지 않도록 관상동맥 누공만 선택적으로 폐쇄해야 한다. 관상동맥-심실 누공 및 관상동맥류 폐쇄술을 시행할 때 해당 관상동맥에서 갈라져 나오는 혈관가지들이 손상되어 심근 기능이 악화될 가능성이 큰 경우 관상동맥 우회로조성술을 동시에 시행해 주어야 한다[3,5]. 저자들의 증례에서는 수술 전 시행한 다중열검출기 컴퓨터단층촬영 검사를 통해 우관상동맥으로부터 갈라져 나오는 직경이 큰 분지들이 없음을 확인하였고 수술 중 집도의가 관상동맥 우회로를 연결할 만한 직경이 큰 분지들이 없음을 육안으로 다시 한 번 확인한 후 관상동맥 우회로조성술 없이 결찰술만 진행하였다.
저자들은 피로감과 가벼운 호흡곤란을 호소하는 젊은 환자에서 심초음파와 관상동맥 컴퓨터단층촬영 조영 검사로 거대 관상동맥류를 동반한 우관상동맥-좌심실 누공을 진단하였으며, 거대 관상동맥류의 자연적 파열 및 울혈성 심부전증의 발생을 예방하기 위해 우관상동맥-좌심실 누공 폐쇄수술을 시행하였다. 임상에서 자주 접하기 어려운 거대 관상동맥류를 동반한 우관상동맥-좌심실 누공의 특징적인 영상 소견과 치료 과정을 문헌고찰과 함께 보고하는 바이다.