 |
 |
| Korean J Med > Volume 90(4); 2016 > Article |
|
žöĒžēĹ
Ūē≠Ž¨łÍ≥ľ žĚłž†ĎŪēú žßĀžě•žēĒžóź ŽĆÄŪēīžĄúŽäĒ ž£ľŽ°ú Ž≥ĶŪöĆžĚĆž†ąž†úžą†Í≥ľ Ūē≠žēĒ ŽįŹ Žį©žā¨žĄ† žĻėŽ£ĆŽ•ľ žčúŪĖČŪēėÍ≥† žěąŽč§. ŪēėžßÄŽßĆ žĚłÍ≥ĶŪē≠Ž¨ł ŽėźŽäĒ žě•Ž£®Ž°ú žā∂žĚė žßąžĚī ŪėĄž†ÄŪěą ŽāģžēĄžßą ÍįÄŽä•žĄĪžĚī ŽÜíŽč§. ŽāīžčúÍ≤Ĺž†źŽßČŪēėŽįēŽ¶¨žą†žĚÄ Ūē≠Ž¨łžĚĄ žāīŽ¶ī žąė žěąžßÄŽßĆ žīąÍłį žēĒžóźŽßĆ ž†Āžö©Žź† žąė žěąÍ≥† žĻėžÉĀžĄ† žĚīŪēėžĚė Ūē≠Ž¨łÍīÄžĚÄ žßĀžě•Í≤įžě•Í≥ľŽäĒ ÍĶ¨Ž∂ĄŽźėŽäĒ ŪēīŽ∂ÄŪēôž†Ā ŪäĻžßēžĚī žěąžĖī žĖīŽ†§žõÄžĚī žěąŽč§. Ūē≠Ž¨łÍīÄŽ∂ÄžúĄžĚė ŽāīžčúÍ≤Ĺžčúžą†žĚÄ ŪēīŽ∂ÄŪēôž†Ā ÍĶ¨ž°įŽ°ú žĚłŪēú ž∂úŪėą, ŪÜĶž¶Ě, žčúžēľŪôēŽ≥īžĚė žĖīŽ†§žõÄ ŽďĪžĚī žěąžĚĄ žąė žěąžúľŽĮÄŽ°ú žĚīŽ•ľ žěė žąôžßÄŪēėÍ≥† žčúžą†žĚĄ žčúŪĖČŪēīžēľ ŪēúŽč§. ž†ÄžěźŽď§žĚÄ žĻėžÉĀžĄ†žĚĄ ŽĄėžĖī Ūē≠Ž¨łÍīÄÍĻĆžßÄ žĻ®Ž≤ĒŪēú žßĀžě•Ūē≠Ž¨łžĘÖžĖϞ̥ ŽāīžčúÍ≤Ĺž†źŽßČŪēėŽįēŽ¶¨žą†Ž°ú ž†úÍĪįŪēú ž¶ĚŽ°ÄŽ•ľ Í≤ĹŪóėŪēėžėÄÍ≥† žēĄžßĀ ÍĶ≠ŽāīžóźŽäĒ Ž≥īÍ≥†Žźú žėąÍįÄ žóÜžĖī Ž¨łŪóĆÍ≥†žįįÍ≥ľ Ūē®ÍĽė Ž≥īÍ≥†ŪēėŽäĒ ŽįĒžĚīŽč§.
Abstract
Anorectal cancer is traditionally treated via abdominoperineal resection and/or chemoradiation. Currently, endoscopic submucosal dissection (ESD) is widely used to treat early gastrointestinal epithelial neoplasias. However, the use of ESD to treat lesions of the anal canal raises concerns that do not arise when treating lesions of the stomach and colorectum. Therefore, particular care is needed when treating lesions in the anal area. We recently treated a 75-year-old woman who was scheduled for surgical resection to treat anorectal cancer. The lesion was successfully removed using ESD. This is the first report of the use of ESD to treat anorectal cancer in Korea. Here, we present our case report and review the relevant literature.
ŽāīžčúÍ≤Ĺž†źŽßČŪēėŽįēŽ¶¨žą†žĚÄ ŪėĄžě¨ žúĄžĄ†žĘÖÍ≥ľ žĚľŽ∂Ä ž°įÍłį žúĄžēĒžĚė ŪĎúž§Ä žĻėŽ£ĆŽ°ú ŽĄźŽ¶¨ žčúŪĖČŽźėÍ≥† žěąžúľŽ©į, žßĀžě•Í≤įžě•žĘÖžĖϞ󟞥úŽŹĄ žú†žö©žĄĪžĚī žěÖž¶ĚŽźėÍ≥† žěąŽč§[1,2]. ŪēėžßÄŽßĆ ŽĆĞ앞󟞥úžĚė žčúžą†žĚÄ ŽāúžĚīŽŹĄÍįÄ ŽÜíÍ≥† žě•ÍłįŽ≥īž°ī(organ saving)žĚė žě•ž†źžĚī ž†ĀžĖī žčúžą† ŽĻąŽŹĄÍįÄ žÉĀŽĆÄž†ĀžúľŽ°ú ž†ĀŽč§. ŪēėžßÄŽßĆ žĻėžÉĀžĄ†žóź Í∑ľž†ĎŪēú ŽĆÄžě•žĘÖžĖĎžĚė Í≤Ĺžöį žôłÍ≥ľž†Ā žąėžą† ŪõĄ ŽßƎ吏ĖīžßÄÍ≤Ć ŽźėŽäĒ žĚłÍ≥ĶŪē≠Ž¨łžúľŽ°ú žĚłŪēī žā∂žĚė žßąžĚī ŪėĄž†ÄŪěą ž†ÄŪēėŽź† žąė žěąŽč§. ŽĒįŽĚľžĄú žĻėžÉĀžĄ†žóź Í∑ľž†ĎŪēú ž°įÍłį žßĀžě•žēĒžĚė Í≤Ĺžöį ŽāīžčúÍ≤Ĺž†Ā ž†ąž†úŽ•ľ Ž®ľž†Ä Í≥†Ž†§Ūēī Ž≥ľ žąė žěąŽč§. ŪēėžßÄŽßĆ žĻėžÉĀžĄ† žĚīŪēėžĚė Ūē≠Ž¨łÍīÄžõźžúĄŽ∂ÄŽäĒ ŪäĻžßēž†ĀžĚł ŪēīŽ∂ÄŪēôž†Ā ÍĶ¨ž°įŽ°ú žĚīŽ£®žĖīž†ł žßĀžě• ŽįŹ ŽĆÄžě•Ž∂ÄžúĄžóźžĄú žĚīŽ£®žĖīžßÄŽäĒ žčúžą†žóź ŽĻĄŪēī ž£ľžĚėÍįÄ ŪēĄžöĒŪēėŽč§. ž†ÄžěźŽď§žĚÄ žĻėžÉĀžĄ†žĚĄ ŽĄėžĖī Ūē≠Ž¨łÍīĞ̥ žĻ®Ž≤ĒŪēú ž°įÍłį ŽĆÄžě•žēĒžĚĄ ŽāīžčúÍ≤Ĺž†źŽßČŪēėŽįēŽ¶¨žą†Ž°ú ž†ąž†úŪēú 1žėąŽ•ľ Í≤ĹŪóėŪēėžėÄÍłįžóź Ž¨łŪóĆÍ≥†žįįÍ≥ľ Ūē®ÍĽė Ž≥īÍ≥†ŪēėÍ≥†žěź ŪēúŽč§.
76žĄł žó¨žěźÍįÄ Ūēú Žč¨ ž†ĄŽ∂ÄŪĄį ÍįĄŪ󟞆ĀžĚł Ž≥ĶŪÜĶžĚī žěąžĖī ŽāīžõźŪēėžėÄŽč§. Žāīžõź ž†Ą žôłŽ∂Ä Ž≥ĎžõźžóźžĄú žčúŪĖČŪēú ŽĆÄžě•ŽāīžčúÍ≤Ĺ Í≤Äžā¨žóźžĄú žßĀžě•žēĒžúľŽ°ú žßĄŽč®ŽźėžóąÍ≥†, Ž≥ĶŽ∂Ä ž†ĄžāįŪôĒŽč®žłĶžī¨žėĀžóźžĄú žēĹ 2-3 cm ŪĀ¨ÍłįžĚė žĘÖÍīīÍįÄ ÍīÄžįįŽźėžóąžúľŽāė ž£ľŽ≥Äž°įžßĀ žĻ®Ž≤ĒžĚīŽāė Ž¶ľŪĒĄž†ą ž†ĄžĚī žÜĆÍ≤¨žĚÄ žóÜžóąŽč§(Fig. 1A). ž°įžßĀÍ≤Äžā¨ Í≤įÍ≥ľ ž§ĎŽďĪŽŹĄ Ž∂ĄŪôĒžĄ†žēĒžĘÖ(moderated differenciated adenocarcinoma)žúľŽ°ú žßĄŽč®ŽźėžóąžúľŽ©į ž∂ĒÍįÄ Í≤Äžā¨ ŽįŹ žĻėŽ£ĆŽ•ľ žúĄŪēī žěÖžõźŪēėžėÄŽč§. Í≥†Ūėąžēē, ŽčĻŽá®, žöįžöłž¶Ě, ÍīÄž†ąžóľžúľŽ°ú žēĹŽ¨ľ žĻėŽ£Ć ž§ĎžĚīžóąÍ≥† ŽįĪŽāīžě• ŽįŹ žöĒž∂ĒžēēŽįēÍ≥®ž†ąŽ°ú žĻėŽ£ĆŽįõžĚÄ Ž≥ĎŽ†•žĚī žěąžóąŽč§. žā¨ŪöĆŽ†•Í≥ľ ÍįÄž°ĪŽ†•žóźžĄú ŪäĻžĚīžā¨Ūē≠žĚÄ žóÜžóąŽč§. žßĀžě• ž∂úŪėą, ŽįįŽ≥ÄžäĶÍīÄ Ž≥ÄŪôĒ, ŪõĄž§ĎÍįź, ž≤īž§ĎÍįźžÜĆ ŽďĪžĚė žÜĆÍ≤¨žĚÄ žóÜžóąŽč§. žč†ž≤īÍ≤Äžā¨žóźžĄú Ž≥ĎžÉČžĚÄ žóÜžóąÍ≥† žĚėžčĚžĚÄ Ž™ÖŽ£ĆŪēėžėÄŽč§. Ž≥ĶŽ∂Ä žßĄžįįžóźžĄú ŪäĻžĚīžÜĆÍ≤¨žĚÄ žóÜžóąÍ≥† žßĀžě•žąėžßÄ Í≤Äžā¨žóźžĄú Ūē≠Ž¨łžóį žÉĀŽį© žēĹ 3 cmžóź ŽßĆž†łžßÄŽäĒ žĘÖÍīīÍįÄ žěąžóąŽč§. žěÖžõź ŽčĻžčú ŪôúŽ†• žßēŪõĄŽäĒ Ūėąžēē 157/88 mmHg, Žß•Žįē 96ŪöĆ/Ž∂Ą, ŪėłŪĚ°žąė 20ŪöĆ/Ž∂ĄžĚīžóąžúľŽ©į, ž≤īžė®žĚÄ 36.1¬įCžėÄŽč§. Ūėąžē° Í≤Äžā¨žóźžĄú ŽįĪŪėąÍĶ¨ 9,900/mm3, ŪėąžÉČžÜĆ 15.1 g/dL, ŪėąžÜĆŪĆź 331,000/mm3žėÄÍ≥† C-ŽįėžĚώ讎įĪžßą 2.49 mg/dL (ž†ēžÉĀ: < 0.3 mg/dL)Ž°ú žēĹÍįĄ žÉĀžäĻŽźėžĖī žěąžóąžúľŽ©į carcinoembryonic antigenžĚÄ 2.3 mg/dL (ž†ēžÉĀ: 0-6 mg/dL)žėÄŽč§. žĖĎž†ĄžěźŽį©ž∂úŽč®žłĶžī¨žėĀžóźžĄú Ūö°ŪĖČÍ≤įžě•Ž∂ÄžúĄžóź hot uptakeÍįÄ ÍīÄžįįŽźėžĖī(Fig. 1B) ŽĆÄžě•ŽāīžčúÍ≤Ş̥ žčúŪĖČŪēėžėÄŽč§. ŽĆÄžě•ŽāīžčúÍ≤Ĺ Í≤Äžā¨žóźžĄú Ūö°ŪĖČÍ≤įžě•žóź ŽįėŪĚĒžĚī ÍīÄžįįŽźėžóąÍ≥†(Fig. 2A), žßĀžě•žóź žēĹ 45 mm ŪĀ¨ÍłįžĚė ŪėľŪē©Í≥ľŽ¶ĹŪėē(mixed granular) žł°Žį©Žįúžú°Ūėē žĘÖžĖĎžĚī ÍīÄžįįŽźėžóąÍ≥†, žĘÖžĖĎŪĎúŽ©īžóź Í∂§žĖĎžĚÄ žóÜžóąŽč§. žĘÖžĖĎžĚė žĚľŽ∂ÄŽäĒ žĻėžÉĀžĄ†žĚĄ ŽĄėžĖī Ūē≠Ž¨łÍīĞ̥ žĻ®Ž≤ĒŪēėžėÄŽč§(Fig. 2B and 2C). žôłÍ≥ľžĚėžā¨žôÄ ŪėϞߥ ŪõĄ, ŪôėžěźžĚė ŽāėžĚīžôÄ Íłįž†ÄžßąŪôė, žąėžą† ŪõĄ žā∂žĚė žßąžĚĄ Í≥†Ž†§ŪēėÍ≥†, ŽāīžčúÍ≤Ĺž†Ā ž†úÍĪį ŪõĄ ž∂ĒÍįÄ žôłÍ≥ľž†Ā žąėžą†žĚė ÍįÄŽä•žĄĪžĚĄ žěźžĄłŪěą žĄ§Ž™ÖŪēú ŪõĄ ŪôėžěźžôÄ Ž≥īŪėłžěź ŽŹôžĚė Ūēėžóź žĚėžčĚŪēė žßĄž†ēžÉĀŪÉúžóźžĄú ŽāīžčúÍ≤Ĺž†źŽßČŪēėŽįēŽ¶¨žą†žĚĄ žčúŪĖČŪēėžėÄŽč§. Ūē≠Ž¨łÍīÄŽ∂ÄžúĄž†ąÍįú ŽŹôžēą ŽįúžÉĚŪē† žąė žěąŽäĒ ŪÜĶž¶ĚžĚĄ žėąŽį©ŪēėÍłį žúĄŪēī Ūē≠Ž¨łÍīÄžóź Ų̄žĄĚŽźú 2% Ž¶¨ŽŹĄžĻīžĚł(lidocaine) žēĹ 3 mLŽ•ľ ž£ľžěÖŪēėžėÄÍ≥† žĚīŪõĄ glycerol, indigocarmine ŽįŹ epinephrinežĚĄ ŪėľŪē©Ūēú žö©žē° ŽėźŽäĒ žó¨Íłįžóź ŪěąžēĆŽ£®Ž°†žāį(hyaluronic acid)žĚĄ ž∂ĒÍįÄŪēú žö©žē°žĚĄ ž†źŽßČŪēėžóź ž£ľžěÖŪēú ŪõĄ Ūē≠Ž¨łŽį©ŪĖ•žóźžĄúŽ∂ÄŪĄį ž†ąÍįú ŽįŹ ŽįēŽ¶¨Ž•ľ žčúžěĎŪēėžėÄŽč§(Fig. 3A and 3B). ž†ąÍįú(precutting)ŽäĒ ž£ľŽ°ú Kachu flex knife (Kachu, Seoul, Korea)Ž•ľ žā¨žö©ŪēėžėÄÍ≥†, ŽįēŽ¶¨ŽäĒ Kachu flexžôÄ IT-nano knife (Olympus, Tokyo, Japan)Ž•ľ žĚīžö©ŪēėžėÄŽč§. ž†ĄÍłįžÜĆžěĎÍłį(VIO 200D, ERBE Co, Tubingen, Germany) žĄ§ž†ēžĚÄ endocut I (effect 3, duration 3, interval 3)Í≥ľ Swift coagulation (Effect3, 30 watt)žĚĄ ž£ľŽ°ú žā¨žö©ŪēėžėÄžúľŽ©į žßÄŪėąÍ≤łžěź(Coagrasper, Olympus, Tokyo, Japan) žā¨žö© žčúžóźŽäĒ soft coagulation (effect 4, 25-35 watt)žĚĄ žĚīžö©ŪēėžėÄŽč§. 120Ž∂Ą ŽŹôžēą žčúžą†žĚĄ žčúŪĖČŪēėžėÄÍ≥†, Ž≥ĎŽ≥ÄžĚÄ žĚľÍīĄž†ąž†ú ŽźėžóąŽč§(Fig. 3C). ž≤úÍ≥Ķ ŽďĪžĚė Ūē©Ž≥Ďž¶ĚžĚÄ žóÜžóąÍ≥†, žčúžą† ŽŹôžēą ŪÜĶž¶ĚžĚÄ ŪėłžÜĆŪēėžßÄ žēäžēėŽč§. Ž≥ĎŽ¶¨ž°įžßĀŪēôž†Ā žÜĆÍ≤¨žóźžĄú Í≤Äž≤ī ŪĀ¨ÍłįŽäĒ 50 √ó 32 mmžĚīÍ≥† Ž≥ĎŽ≥ÄžĚÄ 40 √ó 31 mmžėÄŽč§. ž†źŽßČžóź ÍĶ≠ŪēúŽźú Í≥†Ž∂ĄŪôĒ žĄ†žēĒžĚīžóąÍ≥† Ž¶ľŪĒĄ ŽįŹ ŪėąÍīÄ žĻ®Ž≤ĒžĚÄ žóÜžóąŽč§(Fig. 4A and 4B). žčúžą† ž§Ď žú°žēąž†ĀžúľŽ°ú Ž≥ĎŽ≥ÄžĚÄ Ž™®ŽĎź ž†úÍĪįŪēėžėÄžúľŽāė Ūē≠Ž¨ł ž™Ĺ ž†ąž†úŽ©īžĚÄ Í≥†ŽŹĄžĚīŪėēžĄĪ žÜĆÍ≤¨žúľŽ°ú Ž≥ĎŽ¶¨Ūēôž†ĀžúľŽ°ú Ž∂ąžôĄž†Ąž†ąž†úŽ•ľ Ž≥īžėÄÍ≥†, žĚľŽ∂ÄŽäĒ Ūē≠Ž¨ł ž™Ĺ ŪéłŪŹČžÉĀŪĒľžôÄ ŽčŅžēĄ Ūē≠Ž¨łÍīĞ̥ žĻ®Ž≤ĒŪēėÍ≥† žěąžóąŽč§(Fig. 4C). ŪôėžěźŽäĒ 2žĚľÍįĄ Ūē≠Ž¨łžóź ŪĒľÍįÄ Ž¨ĽŽäĒ ž†ēŽŹĄžĚė ž∂úŪėąžĚī žěąžóąžúľŽāė žěźžóį Ūėłž†ĄŽźėžóąÍ≥† ŪÜĶž¶ĚžĚÄ ŪėłžÜĆŪēėžßÄ žēäžēėŽč§. ŪôėžěźŽäĒ Ūē©Ž≥Ďž¶Ě žóÜžĚī žčúžą† 5žĚľžßł ŪáīžõźŪēėžėÄÍ≥† 6ÍįúžõĒ ŪõĄ žčúŪĖČŪēú ÍĶ¨Ž∂ąÍ≤įžě•ŽāīžčúÍ≤Ĺ ž∂Ēž†Ā Í≤Äžā¨žóźžĄú žě¨ŽįúžĚīŽāė ŪėĎžį© ŽďĪžĚė žĚīžÉĀžÜĆÍ≤¨žĚÄ žóÜžóąŽč§(Fig. 5).
Ž≥ł ž¶ĚŽ°ÄŽäĒ žĻėžÉĀžĄ†žĚĄ ŽĄėžĖī Ūē≠Ž¨łÍīÄÍĻĆžßÄ žĻ®Ž≤ĒŪēú žßĀžě•Ūē≠Ž¨łžĘÖžĖϞ̥ ŽāīžčúÍ≤Ĺž†źŽßČŪēėŽįēŽ¶¨žą†Ž°ú ž†ąž†úŪēú žėąŽ°ú, žĚī Ž∂ÄžúĄŽ•ľ žčúžą†ŪēėÍłį ž†ĄžóźŽäĒ Ūē≠Ž¨łž£ľŽ≥ÄžĚė ŪäĻžßēž†ĀžĚł ŪēīŽ∂ÄŪēôž†Ā ÍĶ¨ž°įŽ•ľ žĚīŪēīŪē† ŪēĄžöĒÍįÄ žěąŽč§. Ūē≠Ž¨łÍīÄžóźŽäĒ žÉĀ‚ħž§Ď‚ħŪēė žßĀžě•ž†ēŽß•(superior, middle, and inferior rectal vein)žĚī žěąžĖī ž≤īžąúŪôė(systemic system)Í≥ľ ÍįĄŽ¨łŽß•Í≥Ą(portal system)žĚė ŪÜĶŽ°úÍįÄ ŽźėžĖī ŪíćŽ∂ÄŪēú ŪėąÍīÄžĖľÍłį(plexus)Ž•ľ ŪėēžĄĪŪēėŽ©į žĻėŪēĶžĚī ŽįúŽč¨Ūē† žąė žěąŽč§. Ūē≠Ž¨łÍīÄžĚÄ žßĀžě•Í≥ľ Žč¨Ž¶¨, ŪéłŪŹČžÉĀŪĒľŽ•ľ ÍįÄžßÄŽ©į ÍįźÍįĀžč†Í≤ĹžĚī Ž∂ĄŪŹ¨Ūēėžó¨ ŪÜĶž¶Ěžóź ŽĮľÍįźŪēėÍ≥†[3], Žāī‚ħžôłŪē≠Ž¨łž°įžěĄÍ∑ľžĚī žěąžĖī Ūē≠žÉĀ ž°įžĚīŽäĒ ŪěėžĚī žěĎžö©ŪēėÍ≥† žěąŽč§. ŽĒįŽĚľžĄú Ūē≠Ž¨łÍīÄ ŽėźŽäĒ žĻėžÉĀžĄ†Í≥ľ Í∑ľž†ĎŪēú Ž≥ĎŽ≥Ğ̥ ž†ąž†úŪē† ŽēĆŽäĒ žĚīŽü¨Ūēú ŪäĻžßēžĚĄ Í≥†Ž†§Ūēīžēľ ŪēúŽč§. Ž≥ł ž¶ĚŽ°ÄžóźžĄúŽŹĄ žĚīŽü¨Ūēú ž†źžĚĄ Í≥†Ž†§Ūēėžó¨ žĄ†Žč®Ž∂Äžóź Ūą¨Ž™Öžļ°žĚĄ žě•žį©Ūēú ŽĆÄžě•ŽāīžčúÍ≤Ş̥ žĚīžö©ŪēėžėÄžúľŽ©į, Ūē≠Ž¨ł ž™ĹžĚÄ ÍĶ≠žÜĆŽßąž∑®ž†úŽ•ľ žĚīžö©Ūēėžó¨ ž†źŽßČŪēėž£ľžě̥֞ žčúŪĖČŪēėžėÄÍ≥†, Ūē≠Ž¨łÍīÄŽ∂ÄžúĄŽ•ľ ž†ąž†úŪēėŽäĒ ŽŹôžēąžóźŽäĒ žÉĀŪĒľŪēė ŪėąÍīÄžĚė žÜźžÉĀžĚĄ žĶúžÜĆŪôĒŪēėÍłį žúĄŪēī ŽÖłŽ†•ŪēėžėÄŽč§. ÍĶ≠ŽāīžóźžĄúŽäĒ Kim ŽďĪ[4]žĚī Ūē≠Ž¨łÍīÄ ŪéłŪŹČžĄłŪŹ¨žēĒžĚĄ ž†źŽßČž†ąž†úžą†Ž°ú žßĄŽč® ŽįŹ žĻėŽ£ĆŪēú ž¶ĚŽ°ÄŽ≥īÍ≥†ÍįÄ žěąžóąžúľŽāė, ŽāīžčúÍ≤Ĺž†źŽßČŪēėŽįēŽ¶¨žą†žĚĄ žĚīžö©Ūēėžó¨ žĻėŽ£ĆŪēú ž¶ĚŽ°ÄŽäĒ žóÜŽč§. 2012ŽÖĄ Nakadoi ŽďĪ[5]žĚÄ žĻėžÉĀžĄ†žĚĄ ŪŹ¨Ūē®Ūēú Ž≥ĎŽ≥ÄžĚė ŽāīžčúÍ≤Ĺž†źŽßČŪēėŽįēŽ¶¨žą† ž¶ĚŽ°Ä 14žėąŽ•ľ Ž™®žēĄžĄú Ž≥īÍ≥†ŪēėžėÄÍ≥†, 2014ŽÖĄ Holt ŽďĪ[6]žĚī žĻėžÉĀžĄ†žóź 2 cm žĚīŽāīŽ°ú Í∑ľž†ĎŪēú Ž≥ĎŽ≥Äžóź ŽĆÄŪēú ŽāīžčúÍ≤Ĺž†źŽßČž†ąž†úžą†žóź ŽĆÄŪēú Ž≥īÍ≥†Ž•ľ ŪēėžėÄŽäĒŽćį, žĚīžÉĀžĚė Ž¨łŪóĆÍ≥†žįįÍ≥ľ ž†ÄžěźžĚė Í≤ĹŪóėžĚĄ ŽįĒŪÉēžúľŽ°ú ŽāīžčúÍ≤Ĺžčúžą†žčú Í≥†Ž†§Ūēīžēľ Ūē† Ūē≠Ž¨łÍīÄžĚė ŪēīŽ∂ÄŪēôž†Ā ŪäĻžßēÍ≥ľ Í∑ĻŽ≥ĶŽį©žēąžĚĄ ž†ēŽ¶¨ŪēėžėÄŽč§.
Ūē≠Ž¨łÍīĞ̥ ŪŹ¨Ūē®Ūēú ŽāīžčúÍ≤Ĺ žčúžą† ŽŹôžēąžóźŽäĒ 1) ŪíćŽ∂ÄŪēú ŪėąÍīÄžĖľÍłįžôÄ žĻėŪēĶžóź žĚėŪēú ž∂úŪėą ŽįŹ Íįźžóľ žúĄŪóėžĄĪ, 2) ÍįźÍįĀžč†Í≤Ĺžóź žĚėŪēú žčúžą† ž§ĎÍ≥ľ žčúžą† ŪõĄžĚė ŪÜĶž¶Ě, 3) ž°įžěĄÍ∑ľžóź žĚėŪēú žčúžēľŪôēŽ≥īžĚė žĖīŽ†§žõÄ, 4) žčúžą† ŪõĄ žĄ¨žú†ŪôĒžôÄ ŪėĎžį©žĚė ŽįúžÉĚ ÍįÄŽä•žĄĪ ŽďĪžĚĄ Í≥†Ž†§Ūēīžēľ ŪēúŽč§. žĚīŽü¨Ūēú ž†źžĚĄ Í∑ĻŽ≥ĶŪēėÍłį žúĄŪēīžĄúŽäĒ ž≤ęžßł, Ūē≠Ž¨łÍīÄ ž£ľžā¨ŽäĒ ŽĻĄžä§Žď¨Ūēú Žį©ŪĖ•žúľŽ°ú ŪēėŽ©į ž†ąÍįúŽ•ľ žĖēÍ≤Ć Ūēėžó¨ ž†źŽßČŪēė ŪėąÍīÄžĚė žÜźžÉĀžĚĄ žĶúžÜĆŪôĒŪēėÍ≥† ŽÖłž∂úŽźú ŪėąÍīÄžĚÄ žßÄŪėąÍ≤łžěźŽ°ú žĚĎÍ≥†žčúžľú žĶúŽĆÄŪēú ž∂úŪėąžĚĄ žėąŽį©ŪēúŽč§. ŽėźŪēú žßĀÍ≤ĹžĚī ŪĀį Ūą¨Ž™Öžļ°žĚĄ žě•žį©Ūēėžó¨ žēēŽįēŪēėŽ©ī žĚľŽ∂Ä žßÄŪėąŪö®Í≥ľŽ•ľ ÍłįŽĆÄŪē† žąė žěąŽč§. ŽĎėžßł, ÍĶ≠žÜĆ Žßąž∑®ž†úŽ•ľ žĚīžö©Ūēėžó¨ ŪÜĶž¶ĚžĚĄ ž°įž†ąŪēėÍ≥† ŽįėÍįźÍłįÍįÄ Íłī žēĹŽ¨ľžĚĄ žā¨žö©ŪēėŽ©ī žąėžą† ŪõĄ ŪÜĶž¶ĚžĚė Í≤ĹÍįźŽŹĄ žĚľŽ∂Ä ÍłįŽĆÄŪē† žąė žěąŽč§. žēĹŽ¨ľ Ž∂ÄžěĎžö©žúľŽ°ú Ž∂Äž†ēŽß•žĚė ÍįÄŽä•žĄĪžĚī žěąžúľŽĮÄŽ°ú žēĹŽ¨ľ Ūą¨žó¨ ŽŹôžēą žč¨ž†ĄŽŹĄ ŽďĪžĚĄ ŪÜĶŪēī Ūôėžěź ÍįźžčúŽ•ľ Ūēīžēľ ŪēúŽč§. žÖčžßł, žĄ†Žč®Ž∂Ä žļ°žĚĄ žĚīžö©Ūēėžó¨ žčúžēľŽ•ľ ŪôēŽ≥īŪēúŽč§. ŽĄ∑žßł, žėąŽį©ž†Ā Ūē≠žÉĚž†ú žā¨žö©žóź ŽĆÄŪēīžĄúŽäĒ žēĄžßĀ Í∑ľÍĪįÍįÄ Ž∂Äž°ĪŪēėžó¨ ž∂ĒÍįÄ žóįÍĶ¨ÍįÄ ŪēĄžöĒŪēėŽč§. Žč§žĄĮžßł, žčúžą† ŪõĄ ŽįúžÉĚŪē† žąė žěąŽäĒ ŪėĎžį©Í≥ľ ŪÜĶž¶Ěžóź ŽĆÄŪēīžĄúŽäĒ žä§ŪÖĆŽ°úžĚīŽďú žĘĆžēĹ, žÜźÍįÄŽĚĹŪôēžě•žą†, žßĄŪÜĶž†ú ŽďĪžĚĄ žĚīžö©Ūē† žąė žěąŽč§[5,6].
žēÖžĄĪžĘÖžĖϞ̥ ŽāīžčúÍ≤Ĺžčúžą†Ž°ú žĻėŽ£ĆŪēėÍłį ž†Ą Ž≥ĎŽ≥ÄžĚė žĻ®žäĶ ž†ēŽŹĄŽ•ľ ŪĆĆžēÖŪēėŽäĒ Í≤ÉžĚÄ Žß§žöį ž§ĎžöĒŪēėŽč§. žĚīŽ•ľ ŪÜĶŪēī žôłÍ≥ľž†Ā žąėžą† ŽėźŽäĒ ŽāīžčúÍ≤Ĺž†ąž†úžą† ŽďĪ ž†Āž†ąŪēú žĻėŽ£Ć Í≥ĄŪöćžĚĄ žąėŽ¶ĹŪē† žąė žěąžúľŽ©į, ŽāīžčúÍ≤Ĺž†ąž†úžą†žĚĄ žčúŪĖČŪē† Í≤Ĺžöį ÍįÄžě• ž†ĀŪē©Ūēú ž†ąž†ú Žį©Ž≤ē ŽėźŪēú Í≤įž†ēŪē† žąė žěąÍłį ŽēĆŽ¨łžĚīŽč§. žčúžą† ž†Ą Ž≥ĎŽ≥ÄžĚė žĻ®Ž≤Ē ž†ēŽŹĄ ŽįŹ Ž≥ĎŽ¶¨Ž•ľ ž∂Ēž†ēŪē† žąė žěąŽäĒ Žį©Ž≤ēžúľŽ°ú ŽāīžčúÍ≤ĹžīąžĚĆŪĆĆ, pit-pattern, non-lifting sign ŽďĪžĚĄ žĚīžö©Ūē† žąė žěąŽč§. Ž≥ł ž¶ĚŽ°ÄžóźžĄúŽäĒ žúĄžôÄ ÍįôžĚÄ Í≤Äžā¨Ž•ľ žčúŪĖČŪēėžßÄ žēäžĚÄ ž†úŪēúž†źžĚī žěąžúľŽāė, Ž≥ĶŽ∂Ä ž†ĄžāįŪôĒŽč®žłĶžī¨žėĀ Í≤Äžā¨žóźžĄú ž£ľŽ≥Äž°įžßĀ žĻ®Ž≤ĒžĚīŽāė Ž¶ľŪĒĄž†ą ž†ĄžĚīžÜĆÍ≤¨žĚī žóÜžóąÍ≥† ŽāīžčúÍ≤Ĺ žÜĆÍ≤¨žóźžĄú žł°Žį©Žįúžú°Ūėē žĘÖžĖĎ ž§ĎžóźžĄúŽŹĄ Í∂§žĖĎžĚīŽāė Ūē®Ž™įžĚī žóÜŽäĒ ŪėľŪē©Í≥ľŽ¶ĹŪėēžĚīžóąÍ≥† žčúžą† ŽŹôžēą non-lifting signžĚī žóÜžĖī ŽāīžčúÍ≤Ĺž†Ā žĻėŽ£ĆŽ•ľ žßĄŪĖČŪēėžėÄŽč§. Í∑łŽü¨Žāė Ž∂ąŪēĄžöĒŪēėÍĪįŽāė Ž¨īŽ¶¨Ūēú žąėžą† ŽėźŽäĒ žčúžą†žĚĄ ŪĒľŪēėÍłį žúĄŪēīžĄúŽäĒ žčúžą† ž†Ą ž†Āž†ąŪēú Í≤Äžā¨Ž•ľ ŪÜĶŪēī žč¨Žč¨ŽŹĄŽ•ľ ŪŹ¨Ūē®Ūēėžó¨ ÍįĚÍīÄž†ĀžĚīÍ≥† ž†ēŪôēŪēėÍ≤Ć Ž≥ĎŽ≥Ğ̥ ŪĆĆžēÖŪēėÍ≥†, ž†Āž†ąŪēú žĻėŽ£ĆÍ≥ĄŪöćžĚĄ žąėŽ¶ĹŪēėŽäĒ Í≤ÉžĚī ŽįĒŽěĆžßĀŪēėŽč§. žĚīŽ•ľ ŪÜĶŪēī žĶúžĄ†žĚė žĻėŽ£Ć Žį©Ž≤ēžĚĄ žĄ†ŪÉĚŪē† žąė žěąÍ≥†, Ž≥ł ž¶ĚŽ°ÄžôÄ ÍįôžĚī ŪôėžěźžĚė žėąŪõĄžôÄ žā∂žĚė žßąžĚĄ ŪĖ•žÉĀžčúŪā¨ žąė žěąžĚĄ Í≤ÉžĚīŽč§.
ž†ÄžěźŽď§žĚÄ žĻėžÉĀžĄ†žĚĄ ŽĄėžĖī Ūē≠Ž¨łÍīÄÍĻĆžßÄ ÍĪłž≥źžěąŽäĒ žßĀžě•Ūē≠Ž¨łžĘÖžĖϞ̥ ŽāīžčúÍ≤Ĺž†źŽßČŪēėŽįēŽ¶¨žą†Ž°ú ž†úÍĪįŪēėžėÄÍłįžóź Ž¨łŪóĆÍ≥†žįįÍ≥ľ Ūē®ÍĽė Ž≥īÍ≥†ŪēėŽäĒ ŽįĒžĚīŽč§.
REFERENCES
1. Saito Y, Uraoka T, Matsuda T, et al. Endoscopic treatment of large superficial colorectal tumors: a case series of 200 endoscopic submucosal dissections (with video). Gastrointest Endosc 2007;66:966‚Äď973.


2. Tamegai Y, Saito Y, Masaki N, et al. Endoscopic submucosal dissection: a safe technique for colorectal tumors. Endoscopy 2007;39:418‚Äď422.


3. Moore KL. Clinically oriented anatomy. 3rd. Baltimore: Williams & Wilkins, 1992.
4. Kim SW, Cha JM, Lee JI, et al. A case of early-stage squamous cell carcinoma of the anal canal diagnosed by endoscopic mucosal resection. Korean J Gastrointest Endosc 2010;40:329‚Äď333.
(A) Abdominal computed tomography reveals a mass about 2-3 cm in diameter in the distal rectum, suggestive of rectal cancer (arrow). No significant infiltration of the perirectal tissue or the regional lymph nodes is evident. (B) Positron emission tomographic finding shows hot uptake lesions on the transverse colon (arrow) and the distal rectum (arrowhead).
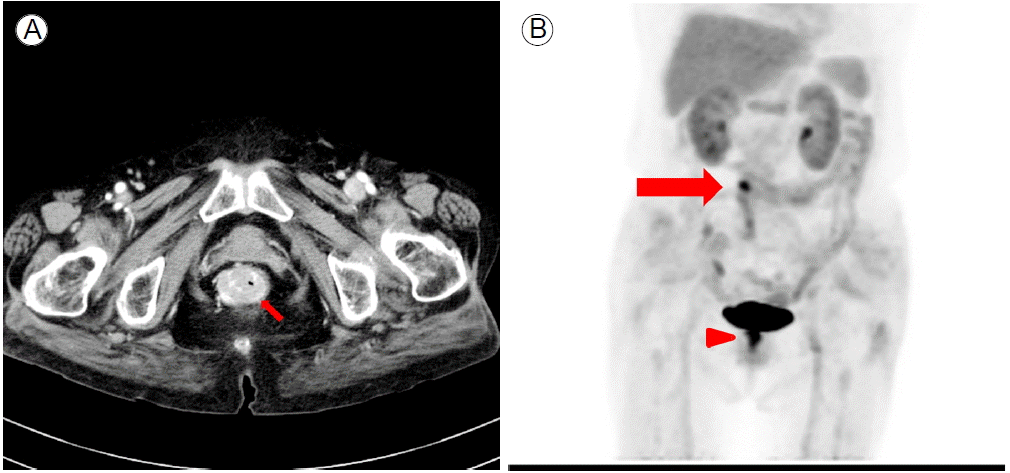
Figure 1.
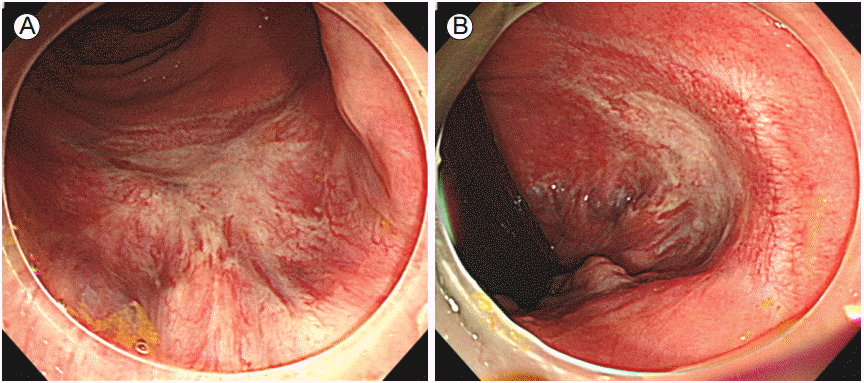
Colonoscopic findings. (A) An EMR scar is evident on the transverse colon. (B, C) A retroflexed and forward view of a 45-mm-diameter, mixed nodular type laterally spreading tumor involving the dentate line of the anorectal area. EMR, endoscopic mucosal
resection.
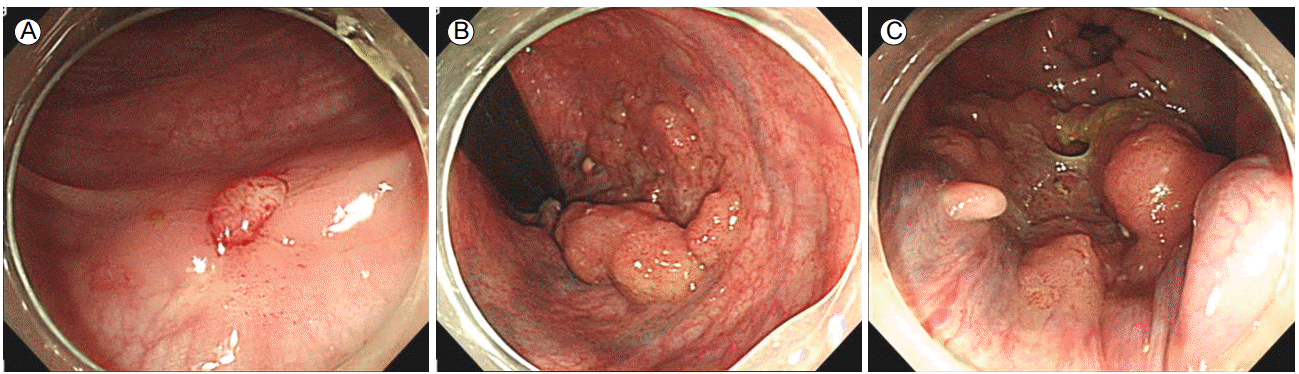
Figure 2.
Endoscopic submucosal dissection (ESD) to treat the anorectal tumor. (A) An incision was commenced on the anal side. (B) A large vessel was apparent after shallow incision. (C) An anorectal ulcer evident after ESD.
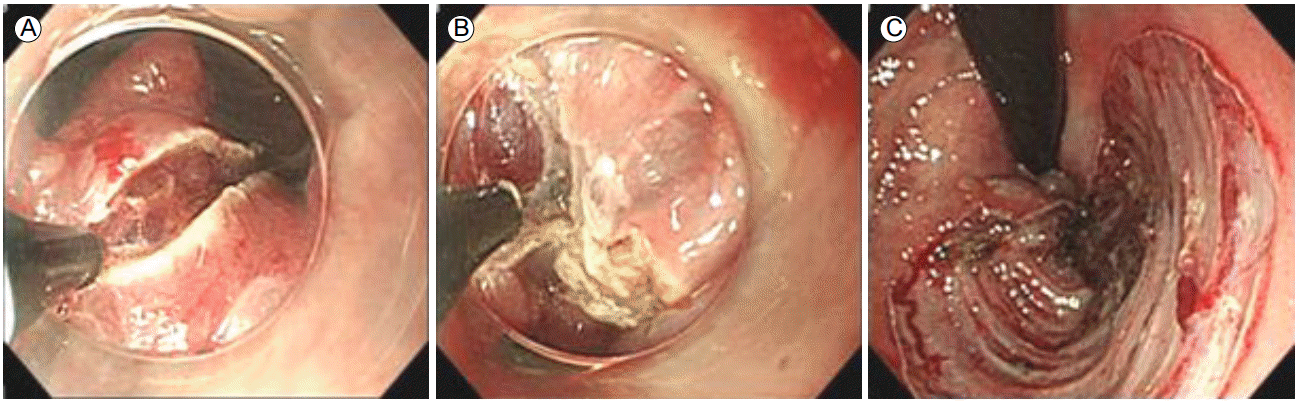
Figure 3.
Pathological findings. (A) The tumor is an intramucosal adenocarcinoma against a background of high-grade dysplasia (H&E, √ó20). Two foci of the invasion (of the lamina propria) are evident (circles). (B) A high-power view of an invasion of the lamina propria (the left-side circle of A above). A desmoplastic stromal reaction (arrow) is apparent (H&E, √ó200). (C) The squamous epithelium of the anal mucosa (arrow) is involved in the adenoma; high-grade dysplasia is evident (H&E, √ó100).




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




