м„ң лЎ
лӮҙмӢңкІҪ м җл§үн•ҳ л°•лҰ¬мҲ (endoscopic submucosal dissection)мқҖ лҰјн”„м Ҳ м „мқҙк°Җ м—ҶлҠ” мЎ°кё° мң„мһҘкҙҖм•”мқҳ кё°ліё м№ҳлЈҢлЎң л„җлҰ¬ л°ӣм•„л“Өм—¬м§Җкі мһҲлӢӨ[1]. л°ңмғқн• мҲҳ мһҲлҠ” н•©лі‘мҰқмңјлЎңлҠ” м¶ңнҳҲ, мІңкіө, нҳ‘м°©, нқЎмқём„ұ нҸҗл ҙ, м •л§ҘнҳҲм „мғүм „мҰқ, кіөкё°мғүм „мҰқ л“ұмқҙ ліҙкі лҗҳкі мһҲмңјлӮҳ лҢҖк°ң лӮҙмӢңкІҪм Ғ м№ҳлЈҢлӮҳ ліҙмЎҙм Ғ м№ҳлЈҢлЎң нҳём „мқ„ ліҙмқёлӢӨ[1].
кёүм„ұ лҙүмҶҢм—јм„ұ мң„м—јмқҖ мң„ лІҪмқҳ м„ёк· м„ұ к°җм—јмңјлЎң л°ңмғқн•ҳлҠ” м№ҳлӘ…м Ғмқҙкі , л§Өмҡ° л“ңл¬ё мң„м—јмңјлЎң кіјлҸ„н•ң мқҢмЈј, л©ҙм—ӯм Җн•ҳмғҒнғң, мң„мқҳ м җл§ү мҶҗмғҒмқҙ мң„н—ҳмқёмһҗлЎң м•Ңл Өм ё мһҲмңјл©° лҢҖл¶Җ분 мң„м Ҳм ңлҘј мӢңн–үн•ң кІғмңјлЎң ліҙкі лҗҳм—ҲлӢӨ[2]. мөңк·ј лӮҙмӢңкІҪ м җл§үн•ҳ л°•лҰ¬мҲ мқҳ мӢңн–ү мҰқк°ҖмҷҖ лҚ”л¶Ҳм–ҙ мқҙм—җ л”°лҘё н•©лі‘мҰқмңјлЎңлҸ„ ліҙкі лҗҳкі мһҲм–ҙ мқҙм—җ лҢҖн•ң кҙҖмӢ¬кіј н•Ёк»ҳ м Ғк·№м Ғмқё м№ҳлЈҢк°Җ н•„мҡ”н•ҳлӢӨ[2].
м Җмһҗл“ӨмқҖ лӮҙмӢңкІҪ м җл§үн•ҳ л°•лҰ¬мҲ мӢңн–ү нӣ„ л°ңмғқн•ң лҙүмҶҢм—јм„ұ мң„м—јм—җ лҢҖн•ҙ н•ӯмғқм ң мЎ°кё° нҲ¬м—¬л§ҢмңјлЎң нҳём „мқ„ кІҪн—ҳн•ҳмҳҖкё°м—җ ліҙкі н•ңлӢӨ.
мҰқ лЎҖ
нҷҳ мһҗ: 46м„ё лӮЁмһҗ
мЈј мҶҢ: мң„мқҳ м ҖлҸ„м„ мў…м—җ лҢҖн•ң лӮҙмӢңкІҪм Ҳм ңмҲ
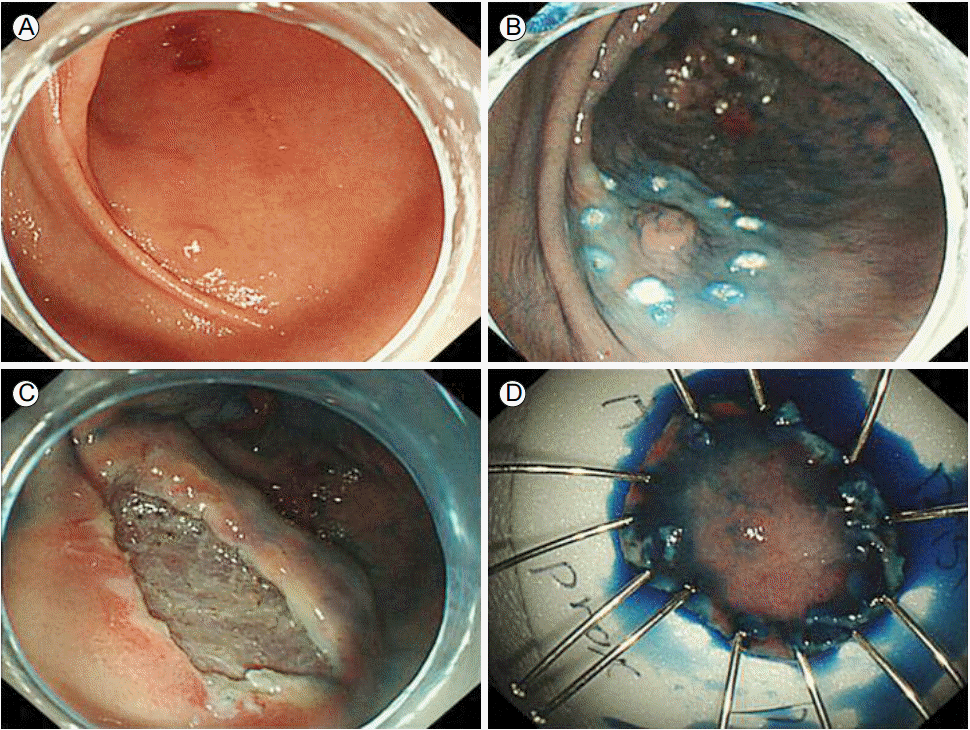
нҳ„лі‘л Ҙ: нҷҳмһҗлҠ” мң„лӮҙмӢңкІҪм—җм„ң м ҖлҸ„м„ мў…мқҙ л°ңкІ¬лҗҳм–ҙ лӮҙмӢңкІҪ м җл§үн•ҳ л°•лҰ¬мҲ мқ„ мӢңн–үл°ӣкё° мң„н•ҙ мһ…мӣҗн•ҳмҳҖлӢӨ. мһ…мӣҗ лӢ№мқј лӘёмӘҪ лӮ л¬ёл°© лҢҖл§ҢкіЎл¶Җмң„м—җ мң„м№ҳн•ң 2 cm нҒ¬кё°мқҳ м ҖлҸ„м„ мў…м—җ лҢҖн•ҙ лӮҙмӢңкІҪ м җл§үн•ҳ л°•лҰ¬мҲ мқ„ мӢңн–үн•ҳмҳҖлӢӨ(Fig. 1). мӢңмҲ мқҖ н‘ңмӢң(marking), мЈјмӮ¬(injection), м Ҳк°ң(incision), л°•лҰ¬(dissection)мқҳ мҲңм„ңлЎң мӢңн–үн•ҳмҳҖмңјл©°, мӢңмҲ нӣ„ м¶ңнҳҲмқҙлӮҳ мІңкіөмқҳ 징нӣ„лҠ” кҙҖм°°лҗҳм§Җ м•Ҡм•ҳлӢӨ. мӢңмҲ нӣ„ н•ҳлЈЁк°Җ кІҪкіјн•ҳм—¬ нҷҳмһҗлҠ” м„ӯм”Ё 39в„ғмқҳ л°ңм—ҙ л°Ҹ мғҒліөл¶Җ нҶөмҰқмқ„ нҳёмҶҢн•ҳмҳҖлӢӨ.
кіјкұ°л Ҙ: 40к°‘л…„мқҳ нқЎм—°л Ҙ мҷём—җ нҠ№мқҙлі‘л ҘмқҖ м—Ҷм—ҲлӢӨ.
к°ҖмЎұл Ҙ: л¶Җм№ңмқҙ 진нҸҗмҰқ, лӘЁм№ңмқҙ лҢҖмһҘм•”мқҳ лі‘л Ҙмқ„ к°Җм§Җкі мһҲм—ҲлӢӨ.
м§Ғм—…л Ҙ: кұҙм„Өм—…
진찰 мҶҢкІ¬: мһ…мӣҗ лӢ№мӢңм—җ нҠ№мқҙмҶҢкІ¬мқҖ кҙҖм°°лҗҳм§Җ м•Ҡм•ҳлӢӨ. л°ңм—ҙмқҙ мӢңмһ‘лҗң мқҙнӣ„м—җлҠ” кёүм„ұ лі‘мғүмқҙм—Ҳкі мқҳмӢқмқҖ лӘ…лЈҢн•ҳмҳҖлӢӨ. нҳҲм••мқҖ 130/70 mmHg, л§Ҙл°•мҲҳлҠ” 100нҡҢ/분, нҳёнқЎмҲҳ 20нҡҢ/분, мІҙмҳЁ 39в„ғмҳҖлӢӨ. ліөл¶Җ нҢҪл§Ңкіј н•Ёк»ҳ мһҘмқҢмқҖ м Җн•ҳлҗҳм–ҙ мһҲм—Ҳмңјл©° мғҒліөл¶Җ мҙү진мӢңм—җ м••нҶөмҷҖ л°ҳл°ң м••нҶөмқҙ мһҲм—ҲлӢӨ.
кІҖмӮ¬мӢӨ мҶҢкІ¬: лӮҙмӣҗ лӢ№мӢң мҳЁнҳҲкө¬кі„мӮ°м—җм„ң нҳҲмғүмҶҢ 15.9 g/dL, л°ұнҳҲкө¬ 10,350/mm3 (мӨ‘м„ұкө¬ 68.1%, лҰјн”„кө¬ 22.9%, лӢЁн•өкө¬ 5.4%, нҳёмӮ°кө¬ 1.5%), нҳҲмҶҢнҢҗ 353,000/mm3 мҳҖмңјлӮҳ л°ңм—ҙ мқҙнӣ„ л°ұнҳҲкө¬ 16,140/mm3 (мӨ‘м„ұкө¬ 88.1%, лҰјн”„кө¬ 5.4%, лӢЁн•өкө¬ 5.1%, нҳёмӮ°кө¬ 0.6%)мңјлЎң мҰқк°Җн•ҳмҳҖлӢӨ. нҳҲм•Ўнҷ”н•ҷ кІҖмӮ¬м—җм„ң C-л°ҳмқ‘лӢЁл°ұм§ҲмқҖ 3.5 mg/dLм—җм„ң мӢңмҲ нӣ„ 5.9 mg/dLлЎң мҰқк°Җн•ҳмҳҖкі мқҙнӢҖ л’Ө 36.20 mg/dLк№Ңм§Җ мҰқк°Җн•ҳмҳҖлӢӨ.
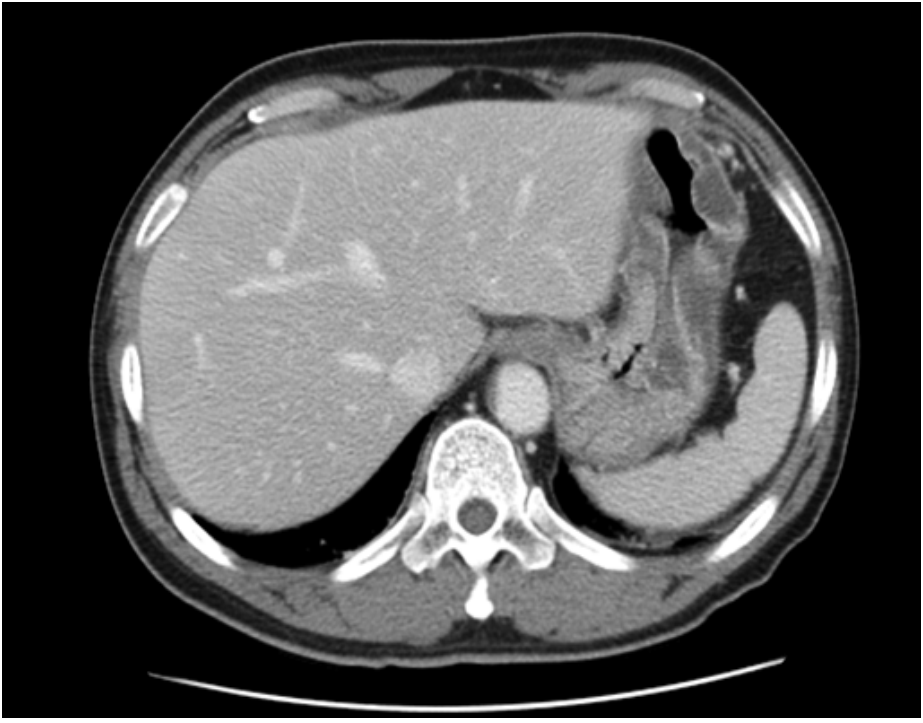
л°©мӮ¬м„ кІҖмӮ¬: к°ҖмҠҙ X-м„ м—җм„ң мІңкіө л°Ҹ нҸҗл ҙ мҶҢкІ¬мқҖ кҙҖм°°лҗҳм§Җ м•Ҡм•ҳлӢӨ. м ң2лі‘мқјм—җ ліөл¶Җ м»ҙн“Ён„°лӢЁмёөмҙ¬мҳҒмқ„ мӢңн–үн•ҳмҳҖмңјл©° мӨ‘к°„ мң„лӘёнҶөл¶Җн„° лӮ л¬ёл¶Җм—җ кұёміҗ лҜёл§Ңм„ұ м җл§үн•ҳ м Җк°җмҮ лі‘ліҖкіј м „мІҙ мң„лІҪмқҳ лҜёл§Ңм„ұ л¶Җмў…мқҙ кҙҖм°°лҗҳм—ҲлӢӨ(Fig. 2).
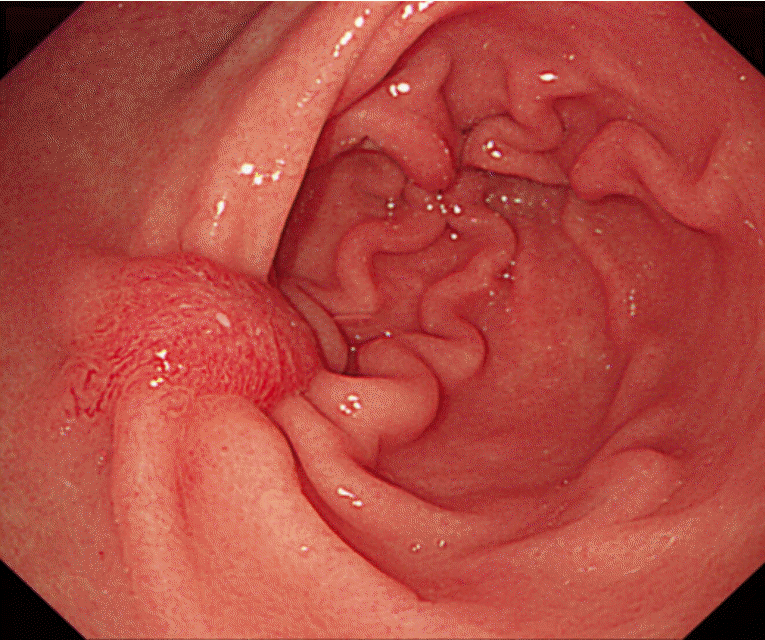
진лӢЁ л°Ҹ мһ„мғҒкІҪкіј: 진лӢЁмқ„ мң„н•ҙ м ң2лі‘мқјм—җ мң„ лӮҙмӢңкІҪкІҖмӮ¬лҘј мӢңн–үн•ҳмҳҖкі лӮҙмӢңкІҪ м җл§үн•ҳ л°•лҰ¬мҲ мқ„ мӢңн–үн•ң лӮ л¬ёл°© лҢҖл§ҢкіЎ л¶Җмң„лҘј нҸ¬н•Ён•ҳм—¬ мң„лІҪ м „мІҙм—җ м „л°ҳм Ғмқё л¶Җмў…кіј л°ңм Ғмқҙ мһҲм—ҲлӢӨ(Fig. 3). мң„ м җл§үм—җм„ң кі лҰ„мқҙлӮҳ м—јмҰқм„ұ мӮјм¶ңл¬јмқҙ кҙҖм°°лҗҳм§ҖлҠ” м•Ҡм•ҳмңјлӮҳ лӮҙмӢңкІҪмңјлЎң кіөкё°лҘј 집м–ҙл„Јкұ°лӮҳ нқЎмқёмӢң м җл§үм—җм„ң мүҪкІҢ м¶ңнҳҲн•ҳмҳҖлӢӨ. мЎ°м§Ғ л°°м–‘мқ„ мң„н•ҙ мң„м җл§ү мЎ°м§ҒкІҖмӮ¬лҘј мӢңн–үн•ҳмҳҖкі мқҙнӣ„ мң„м•Ў л°°м–‘мқ„ мң„н•ң кІҖмІҙ мұ„м·ЁлҘј мӢңлҸ„н•ҳмҳҖмңјлӮҳ нқЎмқёмӢң лӢӨлҹүмқҳ м¶ңнҳҲмқҙ мһҲм–ҙ мң„м•Ў л°°м–‘мқҖ мӢңн–үн•ҳм§Җ лӘ»н•ҳмҳҖлӢӨ.
м ң2лі‘мқј л°ңм—ҙ л°ңмғқ мӢңм җм—җ нҳҲм•Ўл°°м–‘ кІҖмӮ¬лҘј мӢңн–үн•ҳкі ліөк°•лӮҙ к°җм—јм—җ мӨҖн•ҳм—¬ кІҪн—ҳм ҒмңјлЎң 3м„ёлҢҖ м„ёнҢ”лЎңмҠӨнҸ¬лҰ°(Ceftriaxone 2 g q 24 hrs)кіј л©”нҠёлЎңлӢҲлӢӨмЎё(metronidazole 500 mg q 8 hrs)мқ„ нҲ¬м—¬н•ҳмҳҖлӢӨ. к·ёлҹ¬лӮҳ н•ӯмғқм ңлҘј мӮ¬мҡ©н•ҳкі мһҲмқҢм—җлҸ„ л¶Ҳкө¬н•ҳкі мғҒліөл¶Җ лҸҷнҶө л°Ҹ л°ҳл°ңнҶөкіј м••нҶөмқҙ м§ҖмҶҚлҗҳм—Ҳкі , м„ӯм”Ё 39в„ғ мқҙмғҒмқҳ л°ңм—ҙмқҙ кі„мҶҚлҗҳм—ҲлӢӨ.
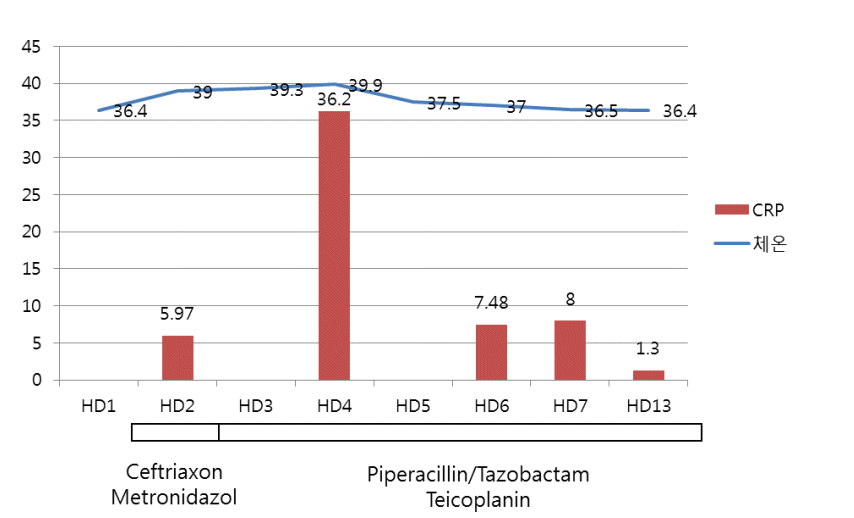
мөңмў… мң„м җл§ү мЎ°м§ҒкІҖмӮ¬ лі‘лҰ¬ кІ°кіјлҠ” кёүм„ұ м—јмҰқмқҙм—Ҳмңјл©° ліөл¶Җ м»ҙн“Ён„°лӢЁмёөмҙ¬мҳҒ кІ°кіјмҷҖ мң„ лӮҙмӢңкІҪ мҶҢкІ¬мқ„ мў…н•©н•ҳм—¬ лҙүмҶҢм—јм„ұ мң„м—јмқҙ к°ҖлҠҘм„ұмқҙ к°ҖмһҘ лҶ’лӢӨкі мғқк°Ғн•ҳмҳҖлӢӨ. мқҳлЈҢ кҙҖл Ё ліөмһЎм„ұ ліөк°•лӮҙ к°җм—јмӢң кҙ‘лІ”мң„ н•ӯмғқм ңмқҳ мӮ¬мҡ©мқҙ к¶Ңкі лҗҳлҠ” м җмқ„ кі л Өн•ҳм—¬[3] м ң3лі‘мқјл¶Җн„° н”јнҺҳлқјмӢӨлҰ°/нғҖмЎ°л°•нғҗ(piperacillin/tazobactam 4/0.5 g q 8 hrs)кіј н…ҢмқҙмҪ”н”ҢлқјлӢҢ(teicoplanin 400 mg q 24 hrs)мңјлЎң ліҖкІҪн•ҳм—¬ нҲ¬м•Ҫн•ҳмҳҖлӢӨ. мҲҳмҲ м Ғ м№ҳлЈҢлҘј кі л Өн•ҳмҳҖмңјлӮҳ нҷҳмһҗмҷҖ ліҙнҳёмһҗк°Җ н•ӯмғқм ң м№ҳлЈҢлҘј мң м§Җн•ҳл©ҙм„ң кІҪкіјкҙҖм°°мқ„ мӣҗн•ҳмҳҖкі н•ӯмғқм ң мӮ¬мҡ© 6мқјм§ёл¶Җн„° н•ҙм—ҙлҗҳм—Ҳмңјл©° л°ұнҳҲкө¬мҰқк°ҖмҰқмқҳ нҳём „ л°Ҹ C-л°ҳмқ‘лӢЁл°ұм§Ҳ мҲҳм№ҳк°Җ к°җмҶҢн•ҳм—¬ мҲҳмҲ мқ„ мӢңн–үн•ҳм§Җ м•Ҡм•ҳлӢӨ(Fig. 4).
лӮҙмӢңкІҪ м җл§үн•ҳ л°•лҰ¬мҲ лЎң м Ҳм ңн•ң мЎ°м§Ғмқҳ мөңмў… лі‘лҰ¬ кІ°кіјлҠ” мң„ м ҖлҸ„м„ мў…мқҙм—Ҳмңјл©° лҙүмҶҢм—јм„ұ мң„м—јмқҳ мҶҢкІ¬мқҖ м—Ҷм—ҲлӢӨ. нҷҳмһҗлҠ” мһ„мғҒкІҪкіјк°Җ нҳём „лҗҳм–ҙ кІҪкө¬ н•ӯмғқм ңмқё лӘ©мӢңн”ҢлЎқмӮ¬мӢ (moxifloxacin 400 mg)мңјлЎң ліҖкІҪн•ҳм—¬ нҮҙмӣҗн•ҳмҳҖмңјл©° 2мЈјк°„ ліөмҡ© нӣ„ мӨ‘лӢЁн•ҳмҳҖлӢӨ. нҮҙмӣҗ л‘җ лӢ¬ нӣ„ мҷёлһҳм—җм„ң 추м Ғ мң„ лӮҙмӢңкІҪмқ„ мӢңн–үн•ҳмҳҖкі лӮҙмӢңкІҪ м җл§үн•ҳ л°•лҰ¬мҲ мқ„ мӢңн–үн–ҲлҚҳ л¶Җмң„ к¶Өм–‘ нқүн„° мҷё мқҙм „ лӮҙмӢңкІҪм—җм„ң кҙҖм°°лҗҳм—ҲлҚҳ мң„ лӮҙлІҪмқҳ л°ңм Ғкіј л¶Җмў…мқҖ кҙҖм°°лҗҳм§Җ м•Ҡм•ҳлӢӨ(Fig. 5).
кі м°°
кёүм„ұ лҙүмҶҢм„ұ мң„м—јмқҖ мң„м җл§үн•ҳмёө л°Ҹ к·јмңЎмқҳ м„ёк· м„ұ к°җм—јмңјлЎң мқён•ҙ л°ңмғқн•ҳкі мң„м „лІҪмқҳ л¶Җмў…кіј кҙҙмӮ¬лҘј лҸҷл°ҳн•ҳлҠ” л§Өмҡ° л“ңл¬јкі м№ҳлӘ…м Ғмқё м§ҲнҷҳмңјлЎң мғҒліөл¶Җ нҶөмҰқ, мҳӨмӢ¬, кө¬нҶ мҷҖ кі м—ҙмқҙ лҸҷл°ҳлҗңлӢӨ[2]. Streptococci, Staphylococci, Haemophilus influenzae, Escherichia coli л“ұмқҙ нқ”н•ң мӣҗмқёк· мңјлЎң м•Ңл Өм ё мһҲмңјл©° мЈјлЎң мң„ мғқкІҖ мЎ°м§Ғ, ліөмҲҳ, л°Ҹ мң„м•Ў л°°м–‘мӢң лҸҷм •лҗңлӢӨ[2].
1862л…„ мІҳмқҢ кё°мҲ лҗң мқҙлһҳ кіјлҸ„н•ң мқҢмЈј, л©ҙм—ӯм Җн•ҳ мғҒнғң(мӮ¬лһҢл©ҙм—ӯкІ°н•Қл°”мқҙлҹ¬мҠӨ к°җм—ј, мҳҒм–‘кІ°н•Қ, лӢ№лҮЁ, лҘҳл§ҲнӢ°мҠӨм„ұ кҙҖм Ҳм—ј, л§Ңм„ұ мӢ л¶Җм „, м№ҙнҸ¬мӢң мңЎмў…, лӢӨл°ңм„ұ кіЁмҲҳмў…, л°ұнҳҲлі‘, л§Ңм„ұл¶ҖмӢ н”јм§Ҳ нҳёлҘҙлӘ¬м ң мӮ¬мҡ©) л“ұ лҢҖмғҒмһҗмқҳ м „мӢ мғҒнғңмҷҖ кҙҖл Ёлҗң мң„н—ҳ мқёмһҗл“Өмқҙ м ңмӢңлҗҳм—ҲлӢӨ[2]. лҳҗн•ң м№ҳлЈҢ лӮҙмӢңкІҪмқҳ л°ңлӢ¬лЎң к·ё мӢңн–үмқҙ мҰқк°Җн•Ём—җ л”°лқј мң„ м җл§ү лі‘ліҖм—җ лҢҖн•ң лӮҙмӢңкІҪ м№ҳлЈҢ мһҗмІҙлҸ„ лҙүмҶҢм„ұ мң„м—јмқҳ мң„н—ҳмқёмһҗлЎң м ңмӢңлҗҳм—ҲлӢӨ[4]. мқҙм „мқҳ л¬ён—Ңл“Өм—җм„ңлҠ” лӮҙмӢңкІҪм Ғ мЎ°м§ҒкІҖмӮ¬ мқҙнӣ„ л°ңмғқн•ң мҳҲ[5], лӮҙмӢңкІҪмҙҲмқҢнҢҢлҘј мқҙмҡ©н•ң нқЎмқёкІҖмӮ¬ нӣ„ л°ңмғқн•ң мҳҲ[6], лӮҙмӢңкІҪ м җл§үм Ҳм ңмҲ л°Ҹ лӮҙмӢңкІҪ м җл§үн•ҳ л°•лҰ¬мҲ мӢңн–ү нӣ„ л°ңмғқн•ң мҳҲк°Җ ліҙкі лҗҳм—ҲлӢӨ[7].
ліё мҰқлЎҖм—җм„ңлҠ” м ҖлҸ„м„ мў…мқ„ лӮҙмӢңкІҪ м җл§үн•ҳ л°•лҰ¬мҲ лЎң м ңкұ°н•ҳмҳҖкі , нҷҳмһҗк°Җ лӢӨмқҢ лӮ л¶Җн„° м„ӯм”Ё 39в„ғ мқҙмғҒмқҳ кі м—ҙ л°Ҹ visual analogue scale 10м җмқҳ ліөнҶөмқ„ нҳёмҶҢн•ҳмҳҖлӢӨ. лӮҙмӢңкІҪ м җл§үн•ҳ л°•лҰ¬мҲ мқҙнӣ„ л°ңмғқн•ң л°ңм—ҙмқҳ кІҪмҡ° нқЎмқём„ұ нҸҗл ҙмңјлЎң мқён•ң кІҪмҡ°к°Җ 2.2-6.6%лЎң ліҙкі лҗҳм—ҲмңјлӮҳ[8] ліё мҰқлЎҖмқҳ к°ҖмҠҙ X-м„ кІҖмӮ¬м—җм„ңлҠ” нҸҗл ҙмқ„ мқҳмӢ¬н• мҲҳ мһҲлҠ” лі‘ліҖмқҙ кҙҖм°°лҗҳм§Җ м•Ҡм•ҳкі , мІңкіө лҳҗн•ң кҙҖм°°лҗҳм§Җ м•Ҡм•ҳлӢӨ.
лӮҙмӢңкІҪ мӢңмҲ мӢң мӮ¬мҡ©н•ҳлҠ” м „кё°мҶҢмһ‘м—җ мқҳн•ҙ мЎ°м§Ғмқҙ м—ҙмҶҗмғҒмқ„ л°ӣм•„ л°ңм—ҙкіј н•Ёк»ҳ C-л°ҳмқ‘лӢЁл°ұм§Ҳкіј к°ҷмқҖ м—јмҰқ м§Җн‘ңк°Җ мқјмӢңм ҒмңјлЎң мғҒмҠ№н•ҳлҠ” нҳ„мғҒмқ„ мқ‘кі мҰқнӣ„кө°мқҙлқјкі н•ҳлҠ”лҚ°[9] л°ҳліөм Ғ м „кё°мҶҢмһ‘мқ„ к°Җн•ҳм—¬ лі‘ліҖмқ„ м Ҳм ңн•ҳлҠ” лӮҙмӢңкІҪ м җл§үн•ҳ л°•лҰ¬мҲ мқҳ мӢңмҲ нҠ№м„ұмқ„ кі л Өн• л•Ң мқ‘кі мҰқнӣ„кө° лҳҗн•ң л°ңм—ҙмқҳ мӣҗмқёмңјлЎң кі л Өн•ҙм•ј н•ңлӢӨ[8]. к·ёлҹ¬лӮҳ лӮҙмӢңкІҪ м җл§үн•ҳ л°•лҰ¬мҲ мӢңн–ү нӣ„ мқ‘кі мҰқнӣ„кө°мқҙ л°ңмғқн•ң нҷҳмһҗмҷҖ м •мғҒмқҳ кІҪкіјлҘј к°Җм§ҖлҠ” нҷҳмһҗлҘј 비көҗн•ң көӯлӮҙ ліҙкі м—җм„ң мқ‘кі мҰқнӣ„кө°мқҳ кІҪмҡ° л°ңм—ҙмқҳ м§ҖмҶҚ кё°к°„мқҖ нҸүк· 23.7мӢңк°„мңјлЎң ліҙкі лҗҳм—ҲлӢӨ[8]. мқҙм—җ 비н•ҙ ліё мҰқлЎҖлҠ” кҙ‘лІ”мң„ н•ӯмғқм ңлҘј мӮ¬мҡ©н•ҳкі мһҲмқҢм—җлҸ„ кі м—ҙмқҙ 3мқј лҸҷм•Ҳ м§ҖмҶҚлҗҳм—ҲлӢӨ. C-л°ҳмқ‘лӢЁл°ұм§Ҳ лҳҗн•ң мқ‘кі мҰқнӣ„кө°м—җм„ң нҸүк· 14 mg/dLк№Ңм§Җ мҰқк°Җн•ңлӢӨкі ліҙкі лҗң кІғм—җ 비н•ҙ[8] 35 mg/dLлЎң нҒ¬кІҢ мҰқк°Җн•ҳм—¬ мқ‘кі мҰқнӣ„кө°мқҳ мһҗм—° кІҪкіјмҷҖлҠ” м°ЁмқҙлҘј ліҙмҳҖлӢӨ. мқ‘кі мҰқнӣ„кө°мқҳ кІҪмҡ° н•ӯмғқм ңмқҳ мӮ¬мҡ© мң л¬ҙк°Җ мһ„мғҒкІҪкіјмқҳ нҳём „м—җ мҳҒн–Ҙмқ„ мЈјм§Җ м•Ҡм•ҳлӢӨкі ліҙкі лҗң л°” мһҲлҠ”лҚ°[8], ліё мҰқлЎҖм—җм„ңлҠ” ліөл¶Җ м»ҙн“Ён„°лӢЁмёөмҙ¬мҳҒ кІҖмӮ¬мҷҖ лӮҙмӢңкІҪ мҶҢкІ¬мқҙ кёүм„ұ лҙүмҶҢм„ұ мң„м—јмқҳ м „нҳ•м Ғмқё мҶҢкІ¬мқ„ ліҙмҳҖмңјл©° кҙ‘лІ”мң„ н•ӯмғқм ң м№ҳлЈҢлҘј мғҒлӢ№кё°к°„ мң м§Җн•ң мқҙнӣ„м—җм•ј нҳём „лҗҳм—ҲмқҢмқ„ кі л Өн•ҳм—¬ мқ‘кі мҰқнӣ„кө°ліҙлӢӨлҠ” кёүм„ұ лҙүмҶҢм„ұ мң„м—јмқҙ н•©лі‘лҗҳм—ҲлӢӨкі м§„лӢЁн•ҳмҳҖлӢӨ.
лӮҙмӢңкІҪ м җл§үн•ҳ л°•лҰ¬мҲ мӢң мӮ¬мҡ©лҗң лӮҙмӢңкІҪ л°Ҹ л¶ҖмҶҚ кё°кө¬л“ӨмқҖ лҢҖн•ңмҶҢнҷ”кё°лӮҙмӢңкІҪн•ҷнҡҢмқҳ мҶҢлҸ… м§Җм№Ё[9]м—җ л”°лқј мҶҢлҸ…н•ҳм—¬ мӮ¬мҡ©н•ҳкұ°лӮҳ мқјнҡҢмҡ© кё°кө¬лҘј мӮ¬мҡ©н•ҳмҳҖмңјл©°, мӢңмҲ мһҗмҷҖ мӢңмҲ ліҙмЎ°мһҗ лӘЁл‘җ лӮҙкіјм Ғ л¬ҙк· лІ•м—җ мһ…к°Ғн•ҳм—¬ мӢңмҲ м—җ мһ„н•ҳмҳҖлӢӨ. к·ёлҹ¬лӮҳ м„ёк· мқҙ м җл§үмқ„ нҶөн•ҙ м§Ғм ‘ нҢҢкёүлҗЁмңјлЎңмҚЁ л°ңмғқн•ҳлҠ” лҙүмҶҢм„ұ мң„м—јмқҳ лі‘нғң мғқлҰ¬лҘј кі л Өн• л•Ң мӢңмҲ кіјм •м—җм„ң мң„ м җл§үм—җ м§Ғм ‘ лӢҝм•ҳлҚҳ мЈјмӮ¬м№ЁмқҙлӮҳ м Ҳк°ңлҸ„мқҳ мҳӨм—јмқҙ мӣҗмқёмқј мҲҳ мһҲмқҢмқ„ л°°м ңн• мҲҳ м—ҶлӢӨ. л”°лқјм„ң лӮҙмӢңкІҪ мӢңмҲ кіј кҙҖл Ён•ң лҙүмҶҢм„ұ мң„м—јмқҳ н•©лі‘мқ„ мҳҲл°©н•ҳкё° мң„н•ҙм„ңлҠ” лӮҙмӢңкІҪ мӢңмҲ мӢң мӮ¬мҡ©н•ҳлҠ” кё°кө¬мқҳ ліҙлӢӨ мІ м Җн•ң мҶҢлҸ… л°Ҹ мІӯкІ° кҙҖлҰ¬к°Җ мӨ‘мҡ”н•ҳкІ лӢӨ.
кёүм„ұ лҙүмҶҢм„ұ мң„м—јмқҖ м№ҳлЈҢлҘј мӢңн–үн•ҳм§Җ м•Ҡм•ҳмқ„ л•Ң к·ё м№ҳлӘ…лҘ мқҙ 100%м—җ лӢ¬н•ҳлҠ” м§ҲнҷҳмңјлЎң мҲҳмҲ м Ғ м№ҳлЈҢ л°Ҹ н•ӯмғқм ң м№ҳлЈҢк°Җ мӣҗм№ҷмңјлЎң лҗҳм–ҙ мһҲкі мөңк·ј мҶҢмҲҳм—җм„ң н•ӯмғқм ң м№ҳлЈҢл§ҢмңјлЎң нҡҢліөлҗң мҳҲл“Өмқҙ ліҙкі лҗҳм—ҲлӢӨ[10]. ліё мҰқлЎҖм—җм„ңлҠ” нҷҳмһҗмҷҖ ліҙнҳёмһҗмқҳ мҡ”мІӯм—җ мқҳн•ҙ мҲҳмҲ м№ҳлЈҢлҘј м—°кё°н•ҳкі н•ӯмғқм ң м№ҳлЈҢл§Ң мң м§Җн•ҳмҳҖмңјлӮҳ мӢңмҲ мқҙнӣ„ нҷҳмһҗк°Җ кёүкІ©нһҲ м•…нҷ”лҗҳлҠ” м–‘мғҒмқҳ ліөнҶө л°Ҹ кі м—ҙмқ„ ліҙмқј л•ҢлҠ” лҙүмҶҢм„ұ мң„м—јмқ„ мҡ°м„ м ҒмңјлЎң мқҳмӢ¬н•ҳкі мҲҳмҲ м Ғ к°ңмһ…мқ„ м Ғк·№м ҒмңјлЎң кі л Өн•ҳлҠ” кІғмқҙ н•„мҡ”н•ҳкІ лӢӨ.
ліё мҰқлЎҖлҠ” лӮҙмӢңкІҪ м җл§үн•ҳ л°•лҰ¬мҲ мӢңн–ү нӣ„ л°ңмғқн•ң кёүм„ұ лҙүмҶҢм„ұ мң„м—јмқҙ н•ӯмғқм ң м№ҳлЈҢл§ҢмңјлЎң нҳём „лҗҳм—ҲлӢӨлҠ” м җм—җм„ң к·ё мқҳмқҳк°Җ мһҲмңјлӮҳ мЎ°м§Ғ л°°м–‘мқ„ нҶөн•ҙ мӣҗмқё к· мЈј нҷ•мқёмқ„ н•ҳм§Җ лӘ»н–ҲлӢӨлҠ” н•ңкі„лҘј м§ҖлӢҢлӢӨ. лҳҗн•ң лӮҙмӢңкІҪм Ғ м№ҳлЈҢ мқҙнӣ„ л°ңмғқн•ң кёүм„ұ лҙүмҶҢм„ұ мң„м—јмқҳ л°ңмғқ л№ҲлҸ„лҠ” м •нҷ•нһҲ м •лҰ¬н•ҳм—¬ ліҙкі лҗң л°”к°Җ м—ҶмңјлӮҳ л°ңмғқн•ҳкІҢ лҗҳл©ҙ м№ҳлӘ…м Ғмқё кІ°кіјлҘј к°Җм ёмҳ¬ мҲҳ мһҲлӢӨлҠ” м җ л°Ҹ лӮҙмӢңкІҪ м№ҳлЈҢмқҳ мӢңн–ү кұҙмҲҳк°Җ мҰқк°Җн•ҳлҠ” 추세мһ„мқ„ кі л Өн• л•Ң мӢңмҲ мқҙнӣ„ л°ңм—ҙмқҙ мһҲмңјл©° нҶөмғҒм Ғмқё мқ‘кі мҰқнӣ„кө°кіј 비көҗн•ҳм—¬ кёүкІ©н•ң мһ„мғҒм–‘мғҒмқҳ м•…нҷ”лҘј ліҙмқҙлҠ” кІҪмҡ°м—җлҠ” ліё м§ҲнҷҳмңјлЎң мқҳмӢ¬мқ„ н•ҳкі м Ғк·№м Ғмқё м№ҳлЈҢлҘј мӢңн–үн•ҳлҠ” кІғмқҙ нҷҳмһҗмқҳ мҳҲнӣ„м—җ лҸ„мӣҖмқҙ лҗ кІғмңјлЎң мғқк°Ғн•ңлӢӨ.




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






