요도암에서 구획증후군으로 나타난 염증성 근염 1예
Compartment Syndrome followed by Inflammatory Myositis in a Patient with Urethral Cancer
Article information
Abstract
염증성 근염은 부종양증후군의 하나이나, 국내에서 요도암과 연관되거나 또한 염증성 근염이 구획증후군으로 나타난 보고는 없었다. 저자는 요도암 환자에서 CCRT 시행 중 염증성 근염에 의한 구획증후군이 발생하여 근막 절개, 고용량 스테로이드(250 mg/일) 및 면역글로불린(1 g/Kg)을 투여하고 호전을 보인 예를 경험하였기에 이에 대한 문헌고찰과 함께 증례를 보고하는 바이다.
Trans Abstract
Inflammatory myositis is a heterogeneous group of rare diseases characterized by inflammation of the skeletal muscle. The association between cancer and inflammatory myositis is well established, with most cancer-associated myopathies diagnosed within 2 years of initial diagnosis. However, despite this strong association, inflammatory myositis as a paraneoplastic syndrome of urethral cancer has not been reported in Korea. Furthermore, compartment syndrome in the context of inflammatory myositis is extremely rare. A 69 year-old woman presented with paresthesia and painful swelling of the right lower extremity 2 months after diagnosis with urethral cancer, which was treated by chemoradiotherapy. Painful numbness was particularly severe when extending the knee, leading to a preliminary diagnosis of myositis with compartment syndrome, which was confirmed by magnetic resonance imaging. After fascia resection, the patient was treated with high dose steroid and immunoglobulin therapy. Here, we report a case of compartment syndrome followed by inflammatory myositis in a patient with urethral cancer.
서 론
염증성근염(Inflammatorymyositis)은 부종양 증후군(Paraneoplastic syndrome)의 하나로, 염증성 근염이 요도암과 연관되어 발생하는 경우는 드물다[1]. 구획증후군(Compartment syndrome)은 주로 외상성 혹은 비외상성으로 근막에 둘러 쌓인 폐쇄된 구획 내의 조직압이 높아져서 모세혈관에서의 관류가 저하되어 구획 내의 근육과 신경 등 연부조직이 괴사되면서 나타나는 임상증상을 통칭하며 염증성 근염이 구획증후군으로 나타나는 경우는 더욱 드물다[2].
저자들은 요도암 환자에서 항암요법 시행 중 양측 허벅지의 통증성 부종 및 우측 하지 말단의 감각저하가 발생하였고 내원 당일 급격히 악화되어 염증성 근염에 의한 구획증후군으로 진단 후 근막 절개 및 감압술 시행, 고용량 스테로이드(250 mg/일)와 면역글로불린(1 g/Kg)을 투여하고 호전을 보여 이에 대한 문헌고찰과 함께 증례를 보고하는 바이다.
증 례
환 자: 69세 여자
주 소: 양측 허벅지의 통증성 부종 및 우측 하지 말단의 감각저하
현병력: 내원 6개월 전부터 시작된 육안적 혈뇨 및 배뇨통을 주소로 내원하여 요도 악성종양(cT3N2M0) 진단 후, 내원 5개월 전부터 3개월 전까지 cisplatin을 기본으로 하는 동시 항암화학 방사선요법(concurrent chemoradiation therapy, CCRT)을 시행하였고 내원 2개월 전 제 1차 gemcitabin (1,000 mg/m3)과 cisplatin (70 mg/m3) 항암요법을 시행하였다. 이후 호흡곤란 및 크레아티닌 상승소견을 보여 gemcitabin (1,000 mg/m3)과 carboplatin (6 mg/ml/min × [glomerular filtration rate (ml/min) + 25])으로 변경하여 제 2차 항암요법을 시행하였다. 경과관찰 중 내원 1주일 전부터 발생한 양측 허벅지의 통증성 부종 및 우측 하지 말단의 감각저하가 발생하였고 내원 당일 급격히 악화되었다.
과거력 및 약물력: 내원 20년 전 고혈압 진단 후 felodipine 5 mg/일, 내원 10년 전 당뇨 진단 후 nateglinide 90 mg/일 복용 중이며 갑상선 기능저하증 진단 하에 levothyroixine sodium 125 mcg/일 복용 중이다.
사회력: 40년 전 3갑년의 흡연력이 있었고 30년 전부터 금연 중이다.
가족력: 아버지가 고혈압 진단을 받은 것 이외에 자가면역질환 및 악성종양의 가족력은 없다.
이학적 소견: 내원 당시 활력 징후는 혈압 110/60 mmHg, 맥박 96회/분, 호흡수 20회/분, 체온 36.5℃였다. 신장 154.5 cm, 체중 46.2 kg, 체질량지수 19.4 kg/m2였고 양쪽 대퇴부는 숫자통증등급(numeric rating scale) 8점의 통증 및 부종 소견을 보였다. 부종과 통증은 우측이 더욱 심하였다. 전상 장골극에서 15 cm 하방 기준으로 측정했을 때 왼쪽 허벅지 둘레 39 cm, 오른쪽 허벅지 둘레 47 cm였고 함요 부종 및 전반적 부종이 보였다. 우측 하지 말단의 감각저하를 호소하였고 무릎의 신전시 대퇴부의 통증 및 저림이 더 심해지는 소견을 보였으나 말단부 청색증은 뚜렷하지 않았다(Fig. 1A).

(A) Upon admission, the patient presented with a painful pitting edema in the right thigh 47 cm in circumference at a depth 15 cm below the anterior superior iliac spine. (B) After treatment including fasciotomy, painful edema and paresthesia were resolved. Following treatment, circumference of the right thigh decreased to 38.5 cm, similar to that of the left side.
검사실 소견: 내원시 시행한 말초혈액 검사에서 백혈구 4700/mm3 (호중구 69.6%, 림프구 8.5%, 단핵구 19.7%, 호산구 2.1%), 혈색소 8.9 g/dL, 혈소판 48,000/mm3였다. 혈액생화학 검사에서 AST/ALT 57/20 U/L, 총 단백 7.1 g/dL, 알부민 4.1 g/dL, 혈액요소질소 22.4 mg/dL, 크레아티닌 1.32 mg/dL (정상: 0.60-1.30 mg/dL), 나트륨 134 mEq/L, 칼륨 4.7 mEq/L, 마그네슘 2.3 mEq/L, 칼슘 8.2 mg/dL, 인 3.6 mg/dL, 혈당 79 mg/dL였으며 적혈구 침강속도(erythrocyte sedementation rate, ESR) 84 mm/hr (정상: 0-30), C 반응성 단백 (c-reactive protein, CRP) 5.38 mg/dL (정상: 0-0.5)로 증가되었고 D-dimer 815.0 ng/mL, 섬유소 분해산물(fibrin degradation product) 6.2 mcg/mL로 증가되었다. 크레아틴 인산효소(creatine phosphokinase, CPK) 3576 U/L, 젖산탈수소효소(lactate dehydrogenase, LDH) 326 U/L (정상: 106-211), 알돌라아제(Aldolase) 14.5 U/L (정상: 0-7.6)로 근효소 수치가 증가되었다. 항핵항체 음성, 항 Jo-1 항체, C-항 호중구 세포질 항체, P-항 호중구 세포질 항체, 항-ds DNA 항체 음성 소견을 보였고 보체 C3 54 mg/dL (정상: 65-135), 보체 C4 22mg/dL (정상: 13-35)로 정상 범위 이내였다. 요화학 검사상 혈뇨(4+) 및 단백뇨(1+) 양성소견을 보였으나 이는 내원 한 달 전과 차이가 없었다.
방사선 소견: 폐색전증 전산화 단층촬영(computed tomography, CT) 및 하지 정맥 조영(lower extremity venogram)에서 폐색전증 또는 심부정맥 혈전증은 보이지 않았다. 양측 하지 자기공명영상(magnetic resonance imaging)에서 오른쪽 대퇴부의 근위부에서 원위부까지 피하 지방층의 광범위한 종창과 침윤소견이 보였고 오른쪽 대퇴부 근육의 전면부에서 후면부까지 확산된 종창과 T2 영상에서 비균질적인 고음영(heterogeneous high signal intensity change)이 혼합되어 있었다. 또한 넙다리곧은근(rectus femoris), 큰모음근(adductor magnus), 가쪽넒은근(vastus lateralis)에 부분적으로 조영되지 않는 부분이 있었고 오른쪽 대퇴부의 다른 근육 구조와 안쪽 근육 사이 근막(intermuscular fascia)의 약한 조영 증강소견이 보였다. 이는 몇몇 근육의 괴사성 변화를 동반한 확장성 근괴사 소견으로 보여 오른쪽 대퇴부의 구획증후군에 합당한 소견이었다(Fig. 2A).

(A) Magnetic resonance imaging revealed diffuse heterogeneous high signal intensity, suggesting extensive muscle necrosis in the anterior to posterior right thigh muscle (arrows). (B) Fascia resection was performed to decompress the area.
치료 및 경과: 오른쪽 대퇴부의 구획증후군에 대한 응급 치료로 감압을 위한 근막 절개술을 시행하였다(Fig. 2B). 수술시 육안 관찰 소견으로 연부 조직의 부종 및 발적이 보이나 화농이 보이는 감염소견은 보이지 않았고, 육안적으로 발등 동맥(dorsalis pedis artery) 순환은 보존되어 괴사나 청색 소견은 없었다. 근막 절개 후, 감염 예방을 위해 광범위 항생제를 근염 치료를 위해 고용량 스테로이드(methylprednisolone, 250 mg/day)와 면역글로불린(1 g/kg)을 투여하였다. 근막절개를 응급으로 시행하여 충분한 양의 근육 조직을 확보하지는 못하였으나 오른쪽 대퇴부의 근육 조직검사 결과 급성의 비특이적 염증과 섬유소 침착을 동반한 골격근 염증소견을 확인하였고 수술부위의 균주검사 및 배양검사에서 감염은 배제되었다(Fig. 3).
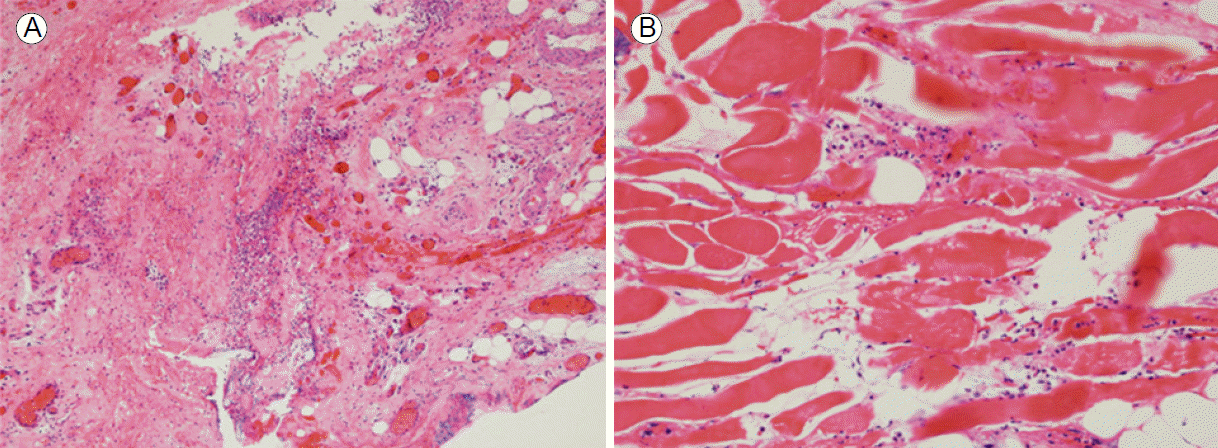
(A) Infiltration of neutrophils in the soft tissue was accompanied by interstitial hemorrhage (HE stain, ×100). (B) Mild endomysial expansion with significant inflammatory cell infiltrate and fibrin are seen (HE stain, ×200).
수술 17일 후 왼쪽 허벅지 둘레 38 cm, 오른쪽 허벅지 둘레 38.5 cm으로 부종이 호전되었고 통증 및 우측 하지 말단의 감각 이상도 호전되었다(Fig. 1B). 말초혈액 검사상 AST 23 U/L (정상: 0-31), ALT 19 U/L (정상: 0-31), CPK 105 U/L (정상: 30-165), LDH 214 U/L (정상: 106-211), ESR 2 mm/hr (정상: 0-30), CRP 0.25 mg/dL (정상: 0-0.5)으로 염증성 근염 및 구획증후군으로 인한 이상소견이 모두 정상범위로 호전되었다. 수술 11일 후부터 능동적 재활 치료를 시행하여 보조기를 사용하여 보행이 가능하였고 무릎이 신전 시에도 통증 및 감각 이상이 발생하지 않았다. CCRT 및 항암요법 중에 발생하였으나 완전관해 상태가 아니므로 요도암에 의한 부종양증후군으로 염증성 근염이 발생했다고 생각되어 수술 부위 회복 후 바로 예정된 항암요법을 추가적으로 실시하였고 외래에서 경과관찰 중이다.
고 찰
염증성 근염 환자의 초기 진단이나 임상적 경과가 악화되고 치료에 반응이 없을 시에는 내재된 악성종양을 의심하여야 할 정도로 이에 대한 상관 관계는 잘 알려져 있다[3]. 여러 보고들에서 염증성 근염 환자에서 악성종양의 발생빈도는 같은 성별, 나이를 가진 정상 인구보다 높다고 하였다. 근염에서 악성종양은 선행해서 발생할 수도, 동시에 발견되기도 하며, 근염 진단 후 2년 이내 악성종양의 진단이 높게 된다[4]. 근염에서 악성종양이 호발되는 장기는 피부 근염 환자에서 난소, 폐, 췌장, 위, 대장암, 비-호지킨림프종 등의 순서로 발생빈도가 높았고, 다발성 근염 환자에서는 비-호지킨림프종, 폐암, 방광암 순서로 높았다. 우리나라에서는 위암의 빈도가 가장 높았으며 그 외에 비인두암, 대장암, 림프종, 간암, 폐암 등의 보고가 있었다[4,5]. 악성종양은 직접 근골격계를 침범하지 않고서도 류마티스질환과 유사한 증상을 유발시킬 수 있고 악성종양과 연관된 부종양증후군으로 류마티스질환이 발생하는 경우는 종종 있으나, 염증성 근염이 요도암과 연관되어 발생하는 경우는 드물다. 악성종양은 많은 수의 근골격 증상과 연관될 수 있으며 이는 직접 침범하는 경우와 면역감시체계의 변화에 의해 부종양증후군으로 나타나는 경우가 있다[4,5]. 면역체계의 조절 장애가 류마티스질환의 전환을 유발하는 보고된 예로는 류마티스관절염, 쇼그렌증후군(Sjogren’s syndrome), 전신경화증(Systemic sclerosis), 전신홍반루푸스(Systemic lupus erythematous) 그리고 근염이 있다[5,6]. 부종양증후군으로 나타난 류마티스질환의 경과는 일반적인 경우보다 예후가 불량하며 원 종양과 임상경과를 같이 한다[7].
구획증후군은 사지의 한정된 공간이나 구획에 종창이나 압력이 증가하는 것으로 강한 근막 조직에 둘러싸인 근육에서 발생한다. 구획은 비탄력적인 조직에 둘러싸인 근육, 신경, 혈관들로 이루어져 있으므로 각 구획 안의 근막은 늘어나지 못하기 때문에 내부의 출혈이나 부종은 그 구획 내부의 조직, 즉 근육, 신경, 혈관을 압박한다. 제한된 구역의 조직압 상승으로 인해 혈액 순환이 잘 되지 않고 조직의 기능이 떨어져 그 결과로 신경근의 허혈 및 기능의 이상이 발생한다[8]. 구획증후군은 상지 및 하지 모두에서 발생할 수 있으며, 원인은 외상성이 가장 많고 비외상성 원인 중 근염은 매우 드물다. 하지에 발생한 구획증후군은 외상, 혈전, 허헐성 변화, 감염, 근육내 혈종, 그리고 근막염 및 근육에서 기인한 종양 등의 원인 감별이 필요하다[8]. 구획증후군의 증상은 극심한 통증이며 특히 신전 시에 심하고 진행되면 마비, 무감각, 맥박의 저하나 감소, 피부의 긴장 등이 발생할 수 있다[8]. 본 증례에서는 양측 허벅지의 통증성 부종 및 우측 하지 말단의 감각저하가 발생하였고 내원 당일 급격히 악화되었으며 무릎의 신전시 대퇴부의 통증 및 저림이 더 심해지는 소견을 보였다. 입원 당시 이전 CCRT 시행 부위의 발적과 열감이 관찰되어 상 대퇴부의 다발성 농양 같은 감염과의 감별이 필요했으며 입원 당시 시행한 생화학적 검사에서 백혈구 증가 및 호중구 증가소견이 관찰되지 않았고 경험적 항생제 투여 후에도 증상이 호전되지 않았던 점과 이후 혈액배양소견에서도 모두 음성이어서 감염을 배제할 수 있었다. 또한 폐색전증 CT 및 하지정맥조영으로 폐색전증과 심부정맥 혈전증을 배제하였다. 임상적으로 구획증후군을 의심할 수 있는 여섯 가지 임상증상이 있는데, 통증, 창백, 지각 이상, 무맥, 마비 그리고 변온이다. 객관적 진단 방법으로는 stryker 바늘을 이용한 방법으로 의심되는 구획 부위에 바늘을 직접 삽입하여 압력을 측정하는 것으로 압력이 30 mmHg을 초과하는 경우 응급 근막 절개술이 필요하다[8]. 본 환자의 경우 극심한 통증 및 급격한 부종, 감각이상이 빠르게 진행하여 압력 측정을 하지 못하였지만 근막절개술 이후 상기 증상들이 빠르게 개선되었고, 광범위 항생제만으로 호전이 없다가 고용량 스테로이드(methylprednisolone, 250 mg/일)와 면역글로불린(1 g/Kg)을 투여한 후 말초혈액 검사상 CRP, ESR 및 근육 효소 수치가 모두 정상범위로 회복되었다.
악성종양에 동반된 근염의 임상적 경과를 보면 종양 자체의 치료시 근염의 현저한 호전이 있다고 하였으나 완전관해는 되지 않는 경우가 많으며, 스테로이드 및 면역억제제의 투여시 부가적인 효과가 있는 것으로 미루어 종양과 숙주의 횡문근의 공통항원에 대한 자가면역이 관여할 것이라는 가정을 뒷받침해준다[9,10]. 종양에 의한 급성 염증성 근염이 구획증후근을 일으키는 것은 매우 드물다. 일반적인 구획증후군은 사지의 통증, 근력약화, 부종 등의 증상이 심하고 근막내 압력이 증가하면 즉시 감압을 위한 근막절개가 필요하나 근염과 동반되는 경우는 스테로이드를 포함한 면역억제제의 투여를 고려하여 가능한 수술을 피하는 것이 좋다. 그러므로 종양과 동반된 근염이 의심되면 이에 대한 치료를 신속히 결정하여 질병의 진행을 예방하고 구획증후군까지 진행이 안되게 예방하는 것이 중요하다. 또한 수술 전 스테로이드의 초기 투여에 반응이 없을 경우에만 근막절개술을 고려하는 것이 이차 감염을 줄일 수 있다.
해외의 류마티스관절염 환자에서 급성 근염 발생으로 인한 구획증후군이 발생하여 스테로이드 투여 및 근막절개술 후 호전된 예가 있으나[6], 국내에서는 요도암에서 급성 근염이 생겨 스테로이드, 면역글로불린, 근막절개술 후 호전된 예는 없었다. 이에 문헌고찰과 함께 증례를 보고하는 바이다.