Вёю вАа
вЊцВ░йВъљ ВдЮьЏёЖх░(afferent loop syndrome)ВЮђ ВюёВЋёВаёВаѕВаюВѕа в░Ј Billroth II Вюё-Ж│хВъЦ вгИьЋЕВѕа ВЮ┤ьЏёВЌљ ВЋй 0.5-2%ВЌљВёю в░юВЃЮьЋўвіћ вДцВџ░ вЊювгИ ьЋЕв│ЉВдЮВЮ┤вІц. Виї-ВІГВЮ┤ВДђВъЦ ВаѕВаюВѕа(pancreaticoduodenectomy) ВЮ┤ьЏёВЌљвЈё ВЌГВІю в░юВЃЮьЋа Вѕў ВъѕвІц[1,2]. ВЏљВЮИВЮђ вѓ┤вХђ ьЃѕВъЦ, ВъЦ ВюаВ░Е, ВъЦ Ж╝гВъё в░Ј в╣ёьІђвд╝, ВѕўВѕа вХђВюё ьўЉВ░Е, ВиїВъЦВЌ╝Ж│╝ Ж░ЎВЮђ ВќЉВё▒ ВџћВЮИВЌљВёювХђьё░ ВЋЁВё▒ ВбЁВќЉВЮў Въгв░ю в░Ј ВаёВЮ┤ВЌљ ВЮ┤вЦ┤ЖИ░Ж╣їВДђ вІцВќЉьЋўвІц[3]. вЊцВ░йВъљ(afferent loop)ВЮў ВЎёВаё ьў╣ВЮђ вХђвХё ьЈљВЄёЖ░ђ в░юВЃЮьЋювІцвЕ┤ вІ┤ВдЎЖ│╝ ВиїВЋАВЮў ВаЋВ▓┤вАю вІ┤Ж┤ђВЌ╝, ВиїВъЦВЌ╝ВЮ┤ в░юВЃЮьЋа Вѕў ВъѕВю╝вЕ░ вѓ┤Ж░ЋВЮў ВЋЋваЦВЮ┤ вєњВЋёВДђЖ▓ї вљўВќ┤ ВъЦВЮў Ж┤┤ВѓгВЎђ В▓юЖ│хВЮ┤ в░юВЃЮьЋа Вѕў ВъѕвІц[4]. ВќЉВё▒ ВџћВЮИВЌљ ВЮўьЋю вЊцВ░йВъљ ВдЮьЏёЖх░ВЮў Жи╝в│ИВаЂВЮИ ьЋ┤Ж▓░ в░ЕВЋѕВЮђ ВѕўВѕаВаЂ В╣ўвБїВЮ┤вѓў ВЋЁВё▒ ВџћВЮИВЮИ Ж▓йВџ░ВЌљвіћ в╣ёВѕўВѕаВаЂ в░Ев▓ЋвЊцВЮ┤ ВІюьќЅвља Вѕў ВъѕвІц. ВађВъљвЊцВЮђ ВиїВъЦВЋћ ьЎўВъљВЌљВёю Whipple ВѕўВѕа ьЏё Въгв░юВё▒ ВбЁВќЉВю╝вАю ВЮИьЋ┤ в░юВЃЮьЋю вЊцВ░йВъљ ВдЮьЏёЖх░ВЮё 2Ж░юВЮў вѓ┤ВІюЖ▓йВЮё ВЮ┤ВџЕьЋю ЖИѕВєЇ ВіцьЁљьіИ ВѓйВъЁВЮё ьєхьЋўВЌг Вё▒Ж│хВаЂВю╝вАю В╣ўвБїьЋю ВўѕвЦ╝ Ж▓йьЌўьЋўВўђЖИ░ВЌљ в│┤Ж│аьЋўЖ│аВъљ ьЋювІц.
ВдЮ вАђ
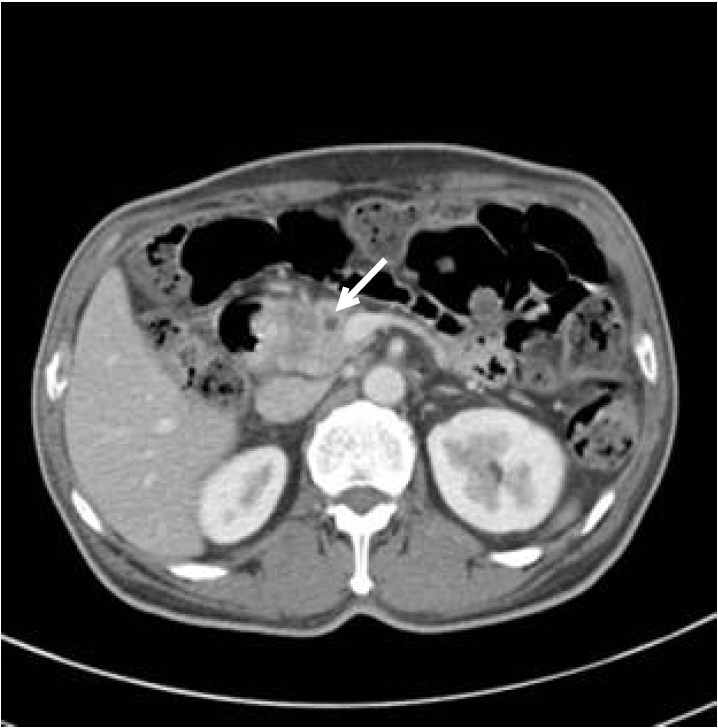
57ВёИ вѓеВъљЖ░ђ ВєїьЎћвХѕвЪЅЖ│╝ ВєЇ ВЊ░вд╝ВЮё ВБ╝ВєївАю ВЎИвъўвЦ╝ в░ЕвгИьЋўВўђвІц. ьЎўВъљвіћ 10вЁё ВаёвХђьё░ вІ╣вЄев│ЉВю╝вАю ВЋйвг╝ В╣ўвБїьЋўвЇў ВцЉВЮ┤ВЌѕВю╝вЕ░ ВѕаЖ│╝ вІ┤в░░віћ ьЋўВДђ ВЋіВЋўвІц. ВІюьќЅьЋю в│хвХђ ВаёВѓ░ьЎћ вІеВИх В┤гВўЂВЌљВёю ВиїВъЦвЉљвХђВЋћВЮ┤ Ж┤ђВ░░вљўВЌѕВю╝вЕ░ ВІГВЮ┤ВДђВъЦВю╝вАюВЮў В╣еВюцВЮ┤ ВЮўВІгвљўВЌѕвІц(Fig. 1). ьЃђ ВъЦЖИ░вАюВЮў ВаёВЮ┤ ВєїЖ▓гВЮђ Ж┤ђВ░░вљўВДђ ВЋіВЋўвІц. Whipple ВѕўВѕаВЮё ВІюьќЅьЋўВўђВю╝вЕ░ ВА░ВДЂ Ж▓ђВѓг Ж▓░Ж│╝ 3.5 cm ьЂгЖИ░ВЮў ВІГВЮ┤ВДђВъЦЖ│╝ В┤ЮвІ┤Ж┤ђВЮё В╣ев▓ћьЋўвіћ ВиїЖ┤ђ ВёаВЋћВбЁ в░Ј ВиїВъЦ ВБ╝в│ђ вд╝ьћёВаѕ ВаёВЮ┤Ж░ђ Ж┤ђВ░░вљўВЌѕвІц(stage IIB, Ameriacn Joint Committee on Cancer, 2010) [5]. ВѕўВѕа ьЏё в│┤ВА░ьЎћьЋЎВџћв▓ЋВЮё Ж│авацьЋўВўђВю╝вѓў ьЎўВъљВЮў Ж░юВЮИ ВѓгВаЋВю╝вАю ВІюьќЅьЋўВДђ вф╗ьЋўВўђвІц.
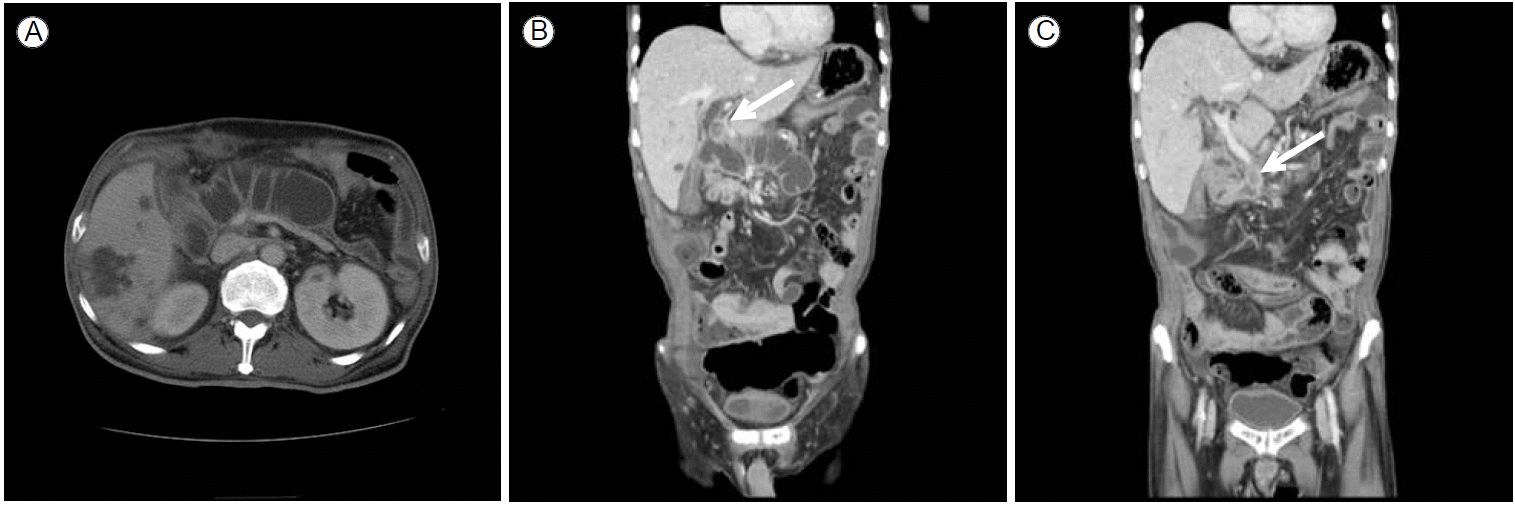
7Ж░юВЏћ вњц ьЎўВъљвіћ в│хьєхЖ│╝ в░юВЌ┤, ьЎЕвІг ЖиИвдгЖ│а в░ўв│хвљўвіћ Жхгьєа ВдЮВЃЂВЮё ВБ╝ВєївАю ВЮЉЖИЅВІцВЮё в░ЕвгИьЋўВўђвІц. вѓ┤ВЏљ вІ╣ВІю ьўѕВЋЋ 135/92 mmHg, вДЦв░ЋВѕў вХёвІ╣ 116ьџї, ьўИьЮАВѕў вХёвІ╣ 20ьџї, В▓┤Вўе 39.9┬░CВўђВю╝вЕ░ ВІюьќЅьЋю ВІаВ▓┤Ж▓ђВѓгВЌљВёю Вџ░ВЃЂв│хвХђВЮў ВЋЋьєх в░Ј Ж░ђВіцьїйвДї ВєїЖ▓гВЮ┤ Ж┤ђВ░░вљўВЌѕвІц. вДљВ┤ѕ ьўѕВЋА Ж▓ђВѓгВЌљВёю в░▒ьўѕЖхг 24,730/uL, ьўѕВЃЅВєї 9.6 g/dL, ьўѕВєїьїљ 90,000/uLВЮ┤ВЌѕВю╝вЕ░ ВЋёВіцьїївЦ┤ьЁїВЮ┤ьіИВЋёв»ИвЁИВаёвІгьџеВєї 443 IU/L, ВЋївЮ╝вІїВЋёв»ИвЁИВаёвІгьџеВєї 130 IU/L, В┤Ю в╣ївдгвБев╣ѕ 6.5 mg/dL, ВЋїВ╣╝вдгВЮИВѓ░вХёьЋ┤ьџеВєї 898 IU/L, Ж│аЖ░љвЈё C-в░ўВЮЉВё▒ вІев░▒(high-sensitive C-reactive protein) 15.57 mg/dLвАю Ж┤ђВ░░вљўВЌѕвІц. ьЈљВЄёВё▒ ьЎЕвІг в░Ј вІ┤Ж┤ђВЌ╝ ВЮўВІгьЋўВЌљ в│хвХђ ВаёВѓ░ьЎћ вІеВИх В┤гВўЂВЮё ВІюьќЅьЋўВўђвІц. В┤гВўЂ Ж▓░Ж│╝ Ж░ё-Ж│хВъЦ вгИьЋЕвХђВЌљ ВЋй 3.6 cm ьЂгЖИ░ВЮў ВбЁЖ┤┤Ж░ђ Ж┤ђВ░░вљўВЌѕВю╝вЕ░ ВЮ┤в│┤вІц Жи╝ВюёвХђ Ж│хВъЦВЌљвЈё ВЋй 3.6 cm ьЂгЖИ░ВЮў ВбЁЖ┤┤Ж░ђ Ж┤ђВ░░вљўВЌѕвІц. Жи╝ВюёвХђ Ж│хВъЦВЮў ВбЁЖ┤┤вАю ВЮИьЋ┤ ВъЦ ьЈљВЄёЖ░ђ в░юВЃЮьЋўВЌг ВЏљВюёвХђ Ж│хВъЦВЮў ьЎЋВъЦЖ│╝ Ж░ёвѓ┤вІ┤Ж┤ђВЮў ьЎЋВъЦВЮ┤ Ж┤ђВ░░вљўВЌѕвІц. Ж░ёВЌљвіћ вІцв░юВё▒ ВаёВЮ┤ВЎђ вЇћвХѕВќ┤ Ж░ёвєЇВќЉВЮ┤ Ж┤ђВ░░вљўЖ│а ВъѕВЌѕвІц(Fig. 2). Въгв░юьЋю ВаёВЮ┤Вё▒ ВиїВъЦВЋћВЌљ ВЮўьЋю вЊцВ░йВъљ ьЈљВЄёвАю ьїљвІевљўВЌѕвІц.
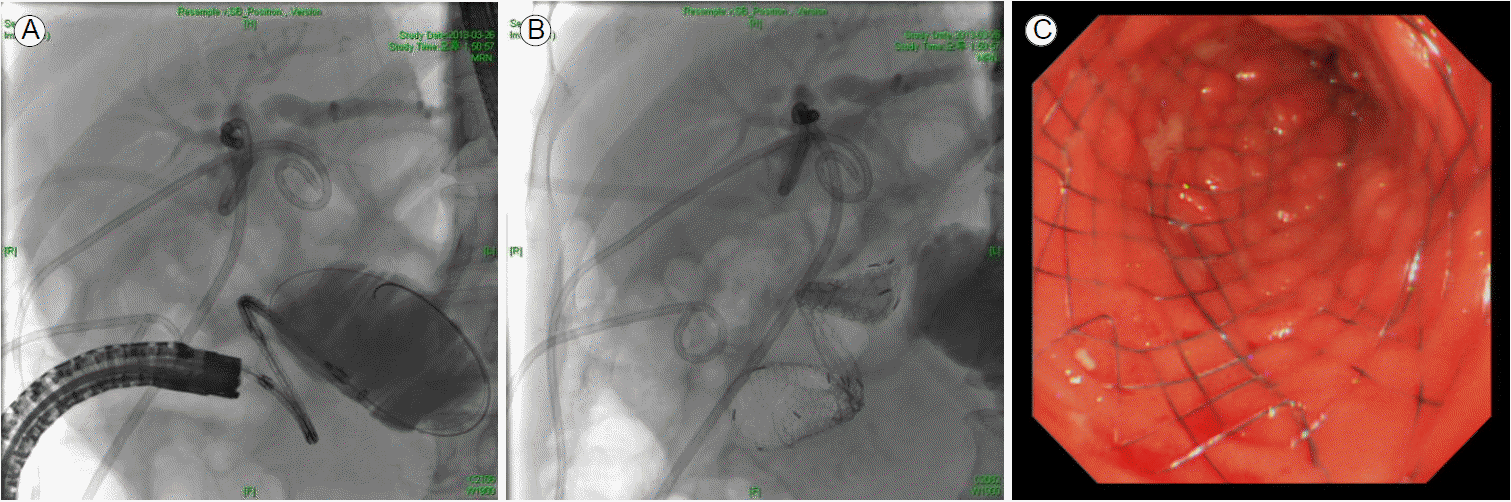
ВЮ╝вІе вІ┤вЈёВЮў Ж░љВЋЋВЮё ВюёьЋ┤ Ж▓йьћ╝ВаЂ вІ┤Ж┤ђ в░░ВЋАВѕаВЮё ВІюьќЅьЋўВўђВю╝вЕ░ ВХћЖ░ђвАю Ж░ёвєЇВќЉВЌљ вїђьЋ┤ Ж▓йьћ╝ВаЂ вЈёЖ┤ђ в░░ВЋАВѕаВЮё ВІюьќЅьЋўВўђвІц. ВЮ┤ьЏё вІ┤ВдЎ в░░ВЋАвАювЦ╝ ьєхьЋўВЌг вДЅьъї ВєїВъЦВЮў ВіцьЁљьіИ ВѓйВъЁВЮё ВІювЈёьЋўВўђвІц. ьЋўВДђвДї ВъЦВЮў ВўѕЖ░ЂьЎћВЎђ ьЈљВЄё ВаЋвЈёЖ░ђ ВІгьЋўВЌг ВюавЈё В▓аВѓгВЮў ВДёВъЁВЌљ ВІцьїеьЋўВўђвІц. 4ВЮ╝ вњц ьЎўВъљвіћ вѓ┤ВІюЖ▓йВаЂ ВаЉЖи╝ВЮё ВІювЈёьЋўВўђвІц. ве╝Вађ в╣ёЖхљВаЂ Ж░ђвіўВќ┤ ВбЂВЮђ ЖИИВЮё ьєхЖ│╝ьЋўвіћ вЇ░ ВюаВџЕьЋю вѓ┤ВІюЖ▓й(GIF-H260, Olympus, Tokyo, Japan)ВЮё ВЮ┤ВџЕьЋўВЌг ВДёВъЁВЮё ВІювЈёьЋўВўђВю╝вЕ░ ВъЦВЮў вБеьћёЖ░ђ ВЃЮЖИ░віћ Ж▓ЃВЮё ВхювїђьЋю в░ЕВДђьЋўЖИ░ ВюёьЋўВЌг Вюё вѓ┤ВЮў Ж│хЖИ░вЦ╝ ВхювїђьЋю ьЮАВЮИьЋўЖ│а ВъЦВЮё вІеВХЋьЎћьЋўВЌг ВхювІеЖ▒░вдгвАю ВаЉЖи╝ьЋўВўђвІц. Whipple ВѕўВѕа в░Ј Ж│хВъЦ-Ж│хВъЦ вгИьЋЕВЮё ВІюьќЅьЋўВЌг ВёИ Ж░ѕвъўВЮў ВДёВъЁвАюЖ░ђ Ж┤ђВ░░вљўВЌѕВю╝вЕ░ ВаЂВаѕьЋю в░ЕьќЦВю╝вАю ВДёВъЁьЋўВЌг ьЈљВЄёвХђВюёВЌљ вЈёвІгьЋа Вѕў ВъѕВЌѕвІц. ВбЁЖ┤┤вАю ВЮИьЋю ВъЦ ьЈљВЄёЖ░ђ ВІгьЋўВЌг Вќ┤вацВЏђВЮ┤ ВъѕВЌѕВю╝вѓў Ж▓░ЖхГ ВюавЈё В▓аВѓгВЎђ В╣┤ьЁїьё░ВЮў ВѓйВъЁВЌљ Вё▒Ж│хьЋа Вѕў ВъѕВЌѕвІц(Fig. 3). ВЮ┤ьЏё ВюавЈё В▓аВѓгвЦ╝ вѓеЖ▓евЉћ В▒ё вѓ┤ВІюЖ▓йВЮё ВаюЖ▒░ьЋю ьЏё ВіцьЁљьіИ ВѓйВъЁВЮ┤ Ж░ђвіЦьЋю вѓ┤ВІюЖ▓й(GIF-2T240, Olympus)ВЮё ВюавЈё В▓аВѓгвЦ╝ вћ░вЮ╝ ьЈљВЄёвХђВюёЖ╣їВДђ ВюёВ╣ўВІюВ╝░вІц. ВЮ┤ьЏё ВъљЖ░ђ ьїйВ░йВё▒ ЖИѕВєЇ ВіцьЁљьіИ(Bonastent┬«, Standard Sci Tech, ВДЂЖ▓й 18 mm ├Ќ ЖИИВЮ┤ 12 cm; Seoul, Korea)вЦ╝ ВѓйВъЁьЋўВўђвІц(Fig. 4). ВЮ┤ьЏё ВІюьќЅвљю вІ┤Ж┤ђ ВА░ВўЂВѕаВЌљВёю ьЎЋВъЦвљю ВіцьЁљьіИВЎђ ВА░ВўЂВаюЖ░ђ Жи╝ВюёвХђ Ж│хВъЦВю╝вАю ВЏљьЎюьъѕ в░░ВХювљўвіћ Ж▓ЃВЮё Ж┤ђВ░░ьЋа Вѕў ВъѕВЌѕвІц. вўљьЋю в░ўв│хВаЂВЮИ Жхгьєа ВдЮВЃЂВЮђ ьўИВаёвљўВЌѕВю╝вЕ░ В┤гВўЂьЋю в│хвХђ X-Вёа Ж▓ђВѓгВЌљВёю вЊцВ░йВъљВЮў Ж░ђВіц ьїйвДї ВєїЖ▓гВЮђ Ж┤ђВ░░вљўВДђ ВЋіВЋўвІц. ьЈљВЄёВё▒ ьЎЕвІгВЮђ ьўИВаёвљўВќ┤ 2ВБ╝ вњц ьўѕВЋА Ж▓ђВѓгВЌљВёю В┤Юв╣ївдгвБев╣ѕВЮђ 2.2 mg/dLвАю Ж░љВєїьЋўВўђвІц. ьЋўВДђвДї ьЎўВъљвіћ ВіцьЁљьіИ ВѓйВъЁ ьЋю вІг ьЏё Ж░ёвєЇВќЉ в░Ј ВЮ┤вАю ВЮИьЋю ьїеьўѕВдЮВю╝вАю ВѓгвДЮьЋўВўђвІц.
Ж│а В░░
вЊцВ░йВъљ ВдЮьЏёЖх░ВЮў В╣ўвБївіћ ьЂгЖ▓ї ВѕўВѕаВаЂ в░Ев▓ЋЖ│╝ в╣ёВѕўВѕаВаЂ в░Ев▓ЋВю╝вАю вѓўвЅўВќ┤ВДђЖ▓ї вљювІц. ВѕўВѕаВаЂ В╣ўвБї в░Ев▓ЋВю╝вАювіћ Ж│хВъЦЖ░ёВЌ░Ж▓░Вѕа(jejunojejunostomy)ВЮ┤вѓў Roux-en-Y Вџ░ьџїВѕаВЮ┤ ВБ╝вАю ВІюьќЅвљўВќ┤ВДђЖ▓ї вљўвЕ░ Жи╝В╣ўВаЂ ВаѕВаюВѕаВЮ┤вѓў Ж│хВъЦВА░вБеВѕа(jejunostomy) ВЌГВІю Ж│авацьЋ┤ в│╝ Вѕў ВъѕвІц. ВѕўВѕаВаЂ В╣ўвБївіћ Жи╝в│ИВаЂВю╝вАю вгИВаювЦ╝ ьЋ┤Ж▓░ьЋа Вѕў Въѕвіћ ВюаВЮ╝ьЋю в░Ев▓ЋВЮ┤вІц[1,2]. ьЋўВДђвДї в│И ВдЮвАђВЎђ Ж░ЎВЮ┤ ВЋЁВё▒ ВбЁВќЉВЮў Въгв░ю в░Ј ВаёВЮ┤ВЌљ ВЮўьЋ┤ в░юВЃЮьЋю Ж▓йВџ░ ьЎўВъљВЮў ВаёВІа ВЃЂьЃювѓў ВЃЂьЎЕВЮ┤ ВѕўВѕаВЮё ВІюьќЅьЋўЖИ░ Вќ┤вацВџ┤ Ж▓йВџ░Ж░ђ вїђвХђвХёВЮ┤вІц. вћ░вЮ╝Вёю ВъёВІюВаЂ в░ЕьјИВю╝вАю Ж▓йЖ░ёВаЂ ьў╣ВЮђ ВДЂВаЉВаЂВЮИ Ж▓йьћ╝ВаЂ Ж▓йвАювЦ╝ ьєхьЋю ВіцьЁљьіИВЮў ВѓйВъЁВЮ┤вѓў вѓ┤ВІюЖ▓йВаЂ В╣ўвБївЦ╝ Ж│авацьЋўЖИ░вЈё ьЋювІц[6-8].
Ж▓йЖ░ёВаЂ Ж▓йвАювЦ╝ ьєхьЋю ВіцьЁљьіИВЮў ВѓйВъЁВЮђ ьЈљВЄёВё▒ ьЎЕвІгВЮ┤ в░юВЃЮьЋю Ж▓йВџ░ВЌљ ВюаВџЕьЋю в░Ев▓ЋВЮ┤вЮ╝ ьЋа Вѕў ВъѕвІц. ьЎЋВъЦвљўВќ┤ Въѕвіћ вІ┤вЈёвЦ╝ ьєхьЋўВЌг Ж▓йьћ╝ Ж▓йЖ░ё вІ┤вЈё в░░ВЋАВѕаВЮё ВІюьќЅьЋю вњц ВЮ┤ьЏё ВЮ┤ Ж▓йвАювЦ╝ ьєхьЋўВЌг ВіцьЁљьіИвЦ╝ ВЮ┤вЈЎВІюьѓцвіћ в░Ев▓ЋВЮ┤вІц. ьЋўВДђвДї ВЮ┤ в░Ев▓ЋВЮђ ьЈљВЄё вХђВюёЖ░ђ вІ┤вЈё-ВъЦ вгИьЋЕ вХђВюёВЎђВЮў Ж▒░вдгЖ░ђ ве╝ Ж▓йВџ░ВЌљ ВаЉЖи╝ВЮ┤ ВЅйВДђ ВЋіВю╝вЕ░ Ж░ёвѓ┤ вІ┤вЈёВЮў ьЎЋВъЦВЮ┤ ВЌєвіћ вЊцВ░йВъљВдЮьЏёЖх░ ьЎўВъљВЮў Ж▓йВџ░ ВаЂВџЕВЌљ Вќ┤вацВЏђВЮ┤ ВъѕвІц[7].
вўљ вІцвЦИ в░Ев▓ЋВЮђ ВДЂВаЉВаЂВю╝вАю вЊцВ░йВъљвЦ╝ В▓юВъљьЋўВЌг Ж▓йьћ╝ВаЂ в░░ВЋАВЮё ВІюьќЅьЋўвіћ в░Ев▓ЋВЮ┤вІц. ЖиИвЪгвѓў вЊцВ░йВъљЖ░ђ в│хв▓йВЌљ Ж│аВаЋвљўВќ┤ ВъѕВДђ ВЋіВЮђ Ж▓йВџ░ ВІюВѕаВЮ┤ Вќ┤вацВџИ Вѕў ВъѕЖ│а вўљьЋю ьїйВ░йвљўВќ┤ ВъѕвЇў вЊцВ░йВъљЖ░ђ ВцёВќ┤вЊцвЕ┤Вёю вІ┤ВдЎВЮў вѕёВХю в░Ј ВЮ┤вАю ВЮИьЋю в│хвДЅВЌ╝ВЮ┤ в░юВЃЮьЋа Вѕў ВъѕвІц. Laasch [6]віћ ВЮ┤вЦ╝ Жи╣в│хьЋўЖИ░ ВюёьЋўВЌг TВъљьўЋ ВА░ВъёВЄёвЦ╝ ВЮ┤ВџЕьЋю в│хв▓й Ж│аВаЋВѕаВЮё ВаюВЋѕьЋўЖИ░вЈё ьЋўВўђВДђвДї ВХћЖ░ђВаЂВЮИ ВЌ░ЖхгЖ░ђ ьЋёВџћьЋ┤ в│┤ВЮИвІц.
в│И ВдЮвАђВЮў Ж▓йВџ░ ве╝Вађ Ж▓йьћ╝ Ж▓йЖ░ё вІ┤вЈё в░░ВЋАВѕаВЮё ВІюьќЅьЋю вњц Ж▓йЖ░ёВаЂ Ж▓йвАювЦ╝ ьєхьЋю ВіцьЁљьіИВЮў ВѓйВъЁВЮё ВІюьќЅьЋўвац ьЋўВўђВю╝вѓў ВъЦВЮў ВўѕЖ░ЂьЎћЖ░ђ ВІгьЋўЖ│а вЊцВ░йВъљВЮў ВЎёВаё ьЈљВЄёвАю ВЮИьЋ┤ ВіцьЁљьіИ ВѓйВъЁВЌљ ВІцьїеьЋўВЌг Ж▓░ЖхГ вѓ┤ВІюЖ▓йВаЂ ВаЉЖи╝ВЮё ВІювЈёьЋўВўђвІц. вЊцВ░йВъљ ВдЮьЏёЖх░ВЮў вѓ┤ВІюЖ▓йВаЂ В╣ўвБїВЮў ВъЦВаљВЮђ в╣ёВ╣еВіхВаЂВЮ┤вЕ░ ВДЂВаЉ ВюАВЋѕВю╝вАю ьЈљВЄёвХђВюёвЦ╝ ьЎЋВЮИьЋа Вѕў ВъѕВю╝в»ђвАю ВДёвІе в░Ј В╣ўвБїЖ░ђ ВџЕВЮ┤ьЋўвІцвіћ Ж▓ЃВЮ┤вІц. ьЋўВДђвДї вїђвХђвХё ВѕўВѕавАю ВЮИьЋю ьЋ┤вХђьЋЎВаЂ в│ђьўЋВю╝вАю ьЈљВЄё вХђВюёЖ╣їВДђ вѓ┤ВІюЖ▓йВЮў ВаЉЖи╝ВЮ┤ ВЅйВДђ ВЋівІц. Burdick вЊ▒[3]ВЮђ вЊцВ░йВъљ ьўЉВ░Е ьЎўВъљВЌљВёю ВєїВЋёВџЕ вїђВъЦвѓ┤ВІюЖ▓йВЮё ВЮ┤ВџЕьЋ┤ ьЈљВЄё вХђВюёВЌљ ВаЉЖи╝ьЋю вњц endoscopic retrograde cholangiopancreatography(ERCP)ВџЕ ВіцьЁљьіИвАю в░░ВЋАВЮё Вё▒Ж│хВаЂВю╝вАю ВІюьќЅьЋю ВўѕвЦ╝ в│┤Ж│аьЋўВўђвІц. вўљьЋю Kim вЊ▒[8]ВЮђ Въгв░юВё▒ ВиїВъЦВЋћВю╝вАю ВЮИьЋ┤ в░юВЃЮьЋю вЊцВ░йВъљ ВдЮьЏёЖх░ВЮё Вё▒ВЮИВџЕ вїђВъЦвѓ┤ВІюЖ▓йВЮё ВЮ┤ВџЕьЋўВЌг ьЈљВЄёвХђВюёВЌљ ВаЉЖи╝ ьЏё ВъљЖ░ђ ьїйВ░йВё▒ ЖИѕВєЇ ВіцьЁљьіИвЦ╝ ВѓйВъЁьЋўВЌг В╣ўвБїьЋю ВѓгвАђвЦ╝ в│┤Ж│аьЋўВўђвІц. ЖиИвЪгвѓў ВєїВЋёВџЕ вїђВъЦвѓ┤ВІюЖ▓йВЮђ working channelВЮў ьЂгЖИ░Ж░ђ ВъЉВЋё ЖИѕВєЇ ВіцьЁљьіИВЮў ВѓйВъЁВЮ┤ вХѕЖ░ђвіЦьЋўвІц. вўљьЋю Вё▒ВЮИВџЕ вїђВъЦ вѓ┤ВІюЖ▓йВЮђ ВДЂЖ▓йВЮ┤ В╗цВёю ьЈљВЄё вХђВюёЖ╣їВДђВЮў ВаЉЖи╝ВЮ┤ ЖиИвІцВДђ ВџЕВЮ┤ьЋю Ж▓ЃВЮђ ВЋёвІѕвІц. ВхюЖи╝ Вўцв▓ё ьіювИї(overtube)ВЎђ ьњЇВёаВЮё ВЮ┤ВџЕьЋю ВєїВъЦвѓ┤ВІюЖ▓й ЖИ░ВѕаВЮё ьєхьЋ┤ ьЋ┤вХђьЋЎВаЂ в│ђьўЋВЮ┤ Въѕвіћ ьЎўВъљвЊцВЌљВёю ERCPвЦ╝ ВІюьќЅьЋю ВѓгвАђЖ░ђ в│┤Ж│ављўЖ│а ВъѕВю╝вѓў вЊцВ░йВъљ ВдЮьЏёЖх░ВЌљВёюВЮў ВаЂВџЕ Вўѕвіћ вЊювг╝вІц[9,10].
в│И ВдЮвАђВЌљВёювіћ в╣ёЖхљВаЂ ВДЂЖ▓йВЮ┤ ВъЉВЮђ вѓ┤ВІюЖ▓йВЮё ВЮ┤ВџЕьЋўВЌг ВюавЈёВ▓аВѓгвЦ╝ вЊцВ░йВъљ вѓ┤вАю ВаёВДёВІюьѓе вњц ВюавЈё В▓аВѓгвЦ╝ вѓеЖ▓евЉћ В▒ё ВъљЖ░ђ ьїйВ░йВё▒ ЖИѕВєЇ ВіцьЁљьіИВЮў ВѓйВъЁВЮ┤ Ж░ђвіЦьЋю вѓ┤ВІюЖ▓йВю╝вАю ЖхљВ▓┤ьЋўВЌг Вё▒Ж│хВаЂВю╝вАю ВіцьЁљьіИвЦ╝ ВѓйВъЁьЋа Вѕў ВъѕВЌѕвІц. ВЮ┤ ВІюВѕаВЮў ВъЦВаљВЮђ ВДЂЖ▓йВЮ┤ ВъЉВЮђ вѓ┤ВІюЖ▓йВЮё ВѓгВџЕьЋеВю╝вАюВЇе Вбђ вЇћ ВЅйЖ│а в╣авЦ┤Ж▓ї в│Љв│ђ вХђВюёВЌљ ВаЉЖи╝ьЋа Вѕў ВъѕВю╝вЕ░ ьЎўВъљВЮў вХѕьјИЖ░љ ВЌГВІю Ж░љВєїьЋа Ж▓ЃВю╝вАю ВўѕВЃЂвљювІц. вўљьЋю вЊцВ░йВъљ ВдЮьЏёЖх░ВЮў ВЏљВЮИ вўљвіћ ВДёвІеВЮ┤ вХѕвХёвфЁьЋю Ж▓йВџ░ ВЮ╝В░еВаЂВю╝вАю ВІювЈёьЋ┤ в│╝ Вѕў ВъѕЖ▓аВю╝вЕ░ ВєїВъЦвѓ┤ВІюЖ▓йВѕаЖ│╝ Ж░ЎВЮђ ьі╣ВѕўьЋю ВъЦв╣ёвѓў ЖИ░ВѕаВЮ┤ ВЌєвіћ ЖИ░Ж┤ђВЌљВёювЈё ВЮ╝В░еВаЂ ВаЉЖи╝ в░Ев▓ЋВЮ┤ ВІцьїеьЋўВўђВЮё Ж▓йВџ░ В░еВёаВ▒ЁВю╝вАю ВІюьќЅьЋ┤ в│╝ Вѕў ВъѕЖ▓авІц. в│И ВдЮвАђВЌљВёювіћ ВЮ╝в░ўВаЂ ВДёвІеВџЕ вѓ┤ВІюЖ▓й(GIF-H260, Olympus)ВЮё ВѓгВџЕьЋўВўђВДђвДї ВЃЂьЎЕВЌљ вћ░вЮ╝ Ж▓йв╣ё вѓ┤ВІюЖ▓й вўљвіћ ВєїВЋёВџЕ вїђВъЦвѓ┤ВІюЖ▓йВЮё ВЮ┤ВџЕьЋю ВаЉЖи╝вЈё Ж░ђвіЦьЋа Ж▓ЃВЮ┤вІц. ьЋўВДђвДї ВБ╝ВЮўьЋа Ж▓ЃВЮђ вѓ┤ВІюЖ▓йВЮё ЖхљВ▓┤ьЋа вЋї в░юВЃЮьЋа Вѕў Въѕвіћ ВюавЈё В▓аВѓгВЮў ВєїВІцВЮ┤вІц. ВЮ┤вЦ╝ в░ЕВДђьЋа Вѕў Въѕвіћ в░Ев▓ЋВю╝вАю ВХЕвХёьЋю ЖИИВЮ┤ВЮў ВюавЈёВ▓аВѓгвЦ╝ вЊцВ░йВъљ вѓ┤вАю ВаёВДёВІюВ╝ю вєЊВЋёВЋ╝ ьЋўвЕ░ вѓ┤ВІюЖ▓й ЖхљВ▓┤ ВІю Ж░ђвіЦьЋю Вюё вѓ┤ВЮў Ж│хЖИ░вЦ╝ ВхювїђьЋю ьЮАВЮИьЋўВЌг ВюавЈё В▓аВѓгЖ░ђ вІ╣Ж▓еВДђвіћ Ж▓ЃВЮё вДЅВЋёВЋ╝ ьЋўЖ▓авІц.
ВѕўВѕавАю ВЮИьЋю ьЋ┤вХђьЋЎВаЂ в│ђьўЋВЮ┤ ВъѕВЮё вЋї вЊцВ░йВъљ вѓ┤ВЮў ьЈљВЄё в│Љв│ђВю╝вАюВЮў вѓ┤ВІюЖ▓й ВѓйВъЁ в░Ев▓ЋВЮђ ВЋёВДЂЖ╣їВДђ ьЉюВцђьЎћвљўВќ┤ ВъѕВДђ ВЋівІц. ВађВъљвЊцВЮ┤ ВаюВІюьЋю ВаЉЖи╝в▓Ћ ВЌГВІю ВЋёВДЂЖ╣їВДђ вІцвЦИ в░Ев▓ЋвЊцЖ│╝ВЮў в╣ёЖхљ ВЌ░Жхгвіћ ВЋївацВаИ ВъѕВДђ ВЋівІц. ьЋўВДђвДї ВЮ┤вЪгьЋю ВІювЈёЖ░ђ вѓ┤ВІюЖ▓й ВѓйВъЁ в░Ј В╣ўвБї ВІцьїеВюеВЮё вѓ«ВХћвіћ вўљ ьЋўвѓўВЮў вїђВЋѕВЮ┤ вља Вѕў ВъѕВЮё Ж▓ЃВю╝вАю ВЃЮЖ░ЂвљювІц.




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






