š ŠÀ
õ¡ŠÈ´š¿Çõ°ÊšÚˋÚ¯Š-1 (glucagon like peptide -1, GLP-1)š šËš L-š¡Ú˜šš ŠÑŠ¿ŠšÇ šñšË Šý Úš¡Ú˜š š¡šŠÎ¯ ŠÑŠ¿ŠË¥ šÇšÏÚõ° šÚš¡Ú˜š õ¡ŠÈ´š¿Çõ°Ê ŠÑŠ¿ŠË¥ šçš Úš˜ š¯ŠÎ˜ Šˆ¡š ÚŠ¿š šÀ¯š ÚŠ ššˋšÇ šŠÊ. ÚšÏŠÏ GLP-1 ššˋšýÇõ¯ šñšË šÇš¡š ŠÑšš¡ ššËõÇ, š˜šË, ÚõÇ, Š, š šË, Ú, Š¥ ŠÝš šÀÇš˜Úõ¡¯ ŠŠ˜¡š GLP-1šÇŠ GLP-1š õñ¥õÝ¯Ú š§Š˜¥š¿ŠÈŠ õ¯ õ¡¯õÇŠÏŠÊ ŠÊšÚ Ú´õ°¥ŠÊš ŠÚŠ¥ š šŠÊ. šÇŠË¥ š ŠÎ˜ÚÇŠ°ÇŠˋÇ Ú 1õ°¥ õ¯šÇ ššË šÇŠ šçš (šŠ¯¯šÑ šÏš¯), ŠÇÚ¥š¡Ú˜ Š°ÇÚ¡, š˜Š¯šÑ šÎõ¯ Š¯ ÚÚš ŠÚ š˜šËš¡Ú˜ Š°ÇÚ¡, šššçš , šýÇšÊõ¯š, Šš õý§ Š°ÇÚ¡, š šË Š°ÇÚ¡, õ°´Š¯Š šÎõ¯ ŠÝš ŠÊšÚ ššˋšÇ šŠÊ. ŠÚ õ°¥õݯšŠ õ¯šÇŠ šÏŠ¯ˋ, õñ¥šÀšŠ GLP-1 ššˋšýÇõ¯ šŠÊõ° šŠ Êš ¡ ššš¥Š, šçõñ¥šŠ ššˋšýÇõ¯ šÀÇš˜ÚŠÊõ° Š Úõ° ššˋšýÇõ¯ šŠ ššˋšýÇš Š˜ÇõÇÚ õý§ŠÀŠÀ ššˋÚŠÊŠ š¯õç˜ õý¯õ°¥ŠÊšÇ Š°Çõ° Šõ° šŠÊ.
Š¯Š¥š šÇ Š
¥Š˜¡ššŠ šÏõ¡õ¿šÏ Š°Çõ° Š ŠÏš š¯õç˜õý¯õ°¥ŠÊš šÂ
ÚˋÚš˜ šñšË šÇš¡š õ¯õ¯š ŠÊšÚ õ¡¯õÇšš ŠÚŠŠ GLP-1š šñšË š¡ Ú´õ°¥š ŠÚÇ š ŠÎ˜ÚÇŠ°Çõ° š ÚŠÊ.
Š°¡ ŠÀ
ššËš ŠÚ ššˋ
GLP-1š ššËš ŠÚ ššˋš š šŠ Êš ¡ šŠÊ. šš¯ŠÑŠ¿ŠË¥ šçš Úõ° ššËš šš Š¯¯šÑš šÏš¯šÚ´ŠÊ. šËššŠ õ¯šÊÚ¡ŠÎ¯ ŠÑŠ¿ŠË¥ šçš Úõ° ššËš šŠÏÚ šÊÚÚÇ ŠÑŠ¿ŠË¥ šÎõ¯šÚÊŠ õýõ°¥ š¯õÇŠšÇ šŠÊõ° ÚŠÊ[1]. ÚšÏŠÏ Š¥šÏŠ š˜ŠššŠ õ¯šÊÚ¡ŠÎ¯šÇŠ šŠÏÚ šÊÚÚÇ ŠÑŠ¿šš õÇŠ ´šÝš š õ° , šÊšÑš õý§õ°š šš¿Ú ššˋšýÇŠ Š₤¡šÈ¥š õý§šÇ õÇš˜Ú õýš¥ŠÀ Š°Çõ° Šõ° šŠÊ[2]. ŠÚ ššËš šš Š¯¯šÑš šÏš¯šÚÊõ° ššËš ššÏšš ŠˋšÑŠ š¥Šˆ
ãileal brakeã ššˋš ÚçÚÇ šÚ ÚŠ¿š šÎõ¯ŠË¥ ŠÛšÑ¯šÈ¥Š ššˋš ÚŠÊ[3].
š˜ÚõÇõ°š ŠÚ ššˋ
GLP-1 ššˋšýÇ õ¡¡ÚÙš Š dipeptidyl peptidase-4 (DPP4) inhibitorŠ ŠÏš ššš¯õ瘚šŠ ÚŠ¿õ°¥ Š˜ÇõÇÚõý š˜ÚõÇõ°š šÂš Ú´õ°¥õ¯ šššÇ Š°Çõ° Šõ° šŠÊ. š˜ÚõÇõ°šš GLP-1š ššˋšýÇ Š¯Úš š˜õñ¥š¡Ú˜, ÚõÇš ŠÇÚ¥š¡Ú˜, ÚõÇÚÚõñ¥š¡Ú˜šš Š¯ÚŠŠÊ.
GLP-1š š˜šËš positive inotropic & chronotropic Ú´õ°¥õ¯ šš¥Šˋ¯, ÚõÇššŠ ŠÇÚ¥š¡Ú˜š õ¡¯ŠËš ÚËššÚÊŠ õýš¥ŠÀ šŠ Êš ¡ šŠÊ[4]. šÇŠ¯ GLP-1š Ú´õ°¥Š GLP-1 ššˋšýÇõ¯ šŠ ššË š¯õ瘚š Š¯ÚšÏõ¡¯ ššÚšŠŠ¯, šÇ ŠŠ˜¥ššŠ šÚ 2Š˜ šÏ¡ šš šš š˜Š¯šõ¯ õ¯šŠšÇ šõ° , šÂš˜šÊš end-diastolic pressureõ¯ šÎõ¯ŠšÇ ššš¥Šˋ¯, šÚ 5Š˜šÏ¡ šÂš˜šÊ Šõ£õ¯ šÎõ¯ŠšÇ šš¥Š šÂš˜šÊ ššÑõ¡¯ŠËõ°¥ šÇšõ¡¯ŠËšÇ ššŠšÇ ššÇ GLP-1šÇ š˜šË õ¡¯ŠËš ŠÏÊš¯ šÊšÚ šÙÚ š ڊΘŠ¥ šõ¯ŠšŠÊ[5]. ŠÚ GLP-1š Ú˜š˜ÚŠˋÇ ÚõÇ Š¯ š˜šËš¡Ú˜šš Š¿šÙšñ´ŠË¥ šÎõ¯šÚÊõ° , cAMP, cGMP ŠÑŠ¿õ¯ šÎõ¯ŠŠˋ¯, šÂš˜šÊšš šÎõ¯ Š¯ õÇšŠŠÏËš ÚŠËõ¯ šÎõ¯ŠŠÊ. õñ¡Š¯Š¯ šÇŠ¯ Ú´õ°¥Š GLP-1 ššˋšýÇõ¯ šŠ Glp1r-/- ššËššŠ õÇš¯¯šÇ Šõ¡¯ ŠŠ˜¡š, GLP-1 ššˋšýÇš Š˜ÇõÇÚ ŠÊŠË¡ õý§ŠÀõ¯ šš õýš¥ŠÀ šõ¯ŠŠˋ¯ šŠÏŠ ÚšÝÚš¡ GLP-1 (7-36)š ŠÑÚšÝÚŠ Šš˜šýÇŠ¥õ° šõ¯ŠšŠ GLP-1 (9-36)õ°¥ õ¯š Šš˜Š˜¥šÏšÇ GLP-1š ššˋšýÇš Š˜ÇõÇÚ õý§ŠÀŠË¥ ÚçÚÇ š¥ŠÑ š˜ÚõÇ Š°ÇÚ¡ššˋš õÇš˜Ú õýš¥ŠÀ šõ¯ŠŠÊ[6].
šçõñ¥šŠ š˜šËš ÚÚšõñ¿š šÊ Ú GLP-1 (9-36)šÇŠ GLP-1 ššˋšýÇ õ¡¡ÚÙš š¡ EX-4ŠË¥ Ú˜š˜ÚŠˋÇ š˜õÇŠËõ¯ šÎõ¯ŠŠˋ¯ š˜õñ¥õý§šš ŠýšŠË¥ šÊš˜ šÊšÇ Úš¡ŠšŠÊ. šÇŠ exendin (9-39)š šÚÇ Ú´õ°¥õ¯ ššŠšš¥Šˋ¯, GLP-1 ššˋšýÇõ¯ šŠ Glp1r-/- ššËššŠ š˜š Ú õÇš¯¯ŠšŠÊ[7]. ÚÚ-š˜õÇŠË ššš ŠŠ˜¥Šˆ´Š¡šš GLP-1š šÚ š˜õ¡¯ŠË Ú¡š š¯õ瘊˥ Š¯Úš¥ŠÀ šçõñ¥šŠ š˜Ššõý ššš¯õç˜õ¯ šÚŠšŠŠ¯, õ¡šÝš˜õñ¥õý§šõ°¥ šÂš˜šÊ š˜Š¯šÑŠË šÇ 40% Š₤¡ŠÏš¡ š˜Ššõý 72šõ¯ GLP-1š šÈ¥š˜Ú õý¯õ°¥ ŠšÀ¯õ篚 Š¿ÚÇ š šÚ šÂš˜šÊ õ¡¯ŠËÚËššÇ õÇš¯¯ŠšŠÊ[8]. ŠÚ õ¯š š¯õ瘚ŠÊš 12Šˆ
š š˜ŠÑš Úššõý 5šÈ¥õ¯ GLP-1š šÈ¥š
Ú õý¯õ°¥ šÂš˜šÊ õ¡¯ŠË Š¯ š˜õñ¥š š¯ššÙšñ´š´, 6ŠÑ õÝñŠ õݯŠÎ˜, Š¯ šÑš šÏ ÚËššÇ Š°Çõ° ŠšŠÊ[9].
ŠÚ GLP-1š ÚõÇš ŠÚ Ú´õ°¥Š ÚõÇŠÇÚ¥š¡Ú˜š õ¡¯ŠË Š¯ ššÀÇš ÚËššÚÊõ° šÊŠÏš ÚõÇÚÚõñ¥ š¡Ú˜š šÎšš šçš ÚŠˋ¯, ÚõÇš šÚÚŠË¥ šŠ¯ˋÚŠ õýš¥ŠÀ šŠ Êš ¡ šŠÊ[10]. š˜Šš ŠŠŠÏË ŠÇÚ¥š¡Ú˜š ÚÚššš š Š¯Ú Ú GLP-1 (9-36)šÇŠ GLP-1 ššˋšýÇ õ¡¡ÚÙš š¡ EX-4ŠË¥ šýŠÎ˜ÚŠˋÇ GLP-1 (9-36)ŠÏ š¡Ú˜š ššÀÇš šÎõ¯šÚÇšÇ Úš¡ŠšŠÊ[11]. šÇ š¯õç˜õý¯õ°¥ šÙš GLP-1š ÚõÇŠ°ÇÚ¡Ú´õ°¥š ššÇš GLP-1 ššˋšýÇ šÇš¡š ŠÊŠË¡ õý§ŠÀõ¯ šÀÇš˜Ú´š šš˜ÚŠÊ. GLP-1š ÚõÇÚÚõñ¥š¡Ú˜š ŠÚ Ú´õ°¥Š ššÏšÊÚ
š IIš šÚÇ šÎõ¯Š šÎš Š¯ šÇšÈ¥ŠË¥ ERK1/2š JNK š Ú¡ŠË¥ ÚçÚÇ šçš ŠŠ šŠ¯ˋÚ´šÇ Š°Çõ° ŠšŠÊ[12]. šÈ§šõý§ÚšÎ Š¯ ÚõÇšÚÚš ŠÚ GLP-1š š¯õ瘊 ŠÏšÇ šÏÚŠõ° šš¥Šˋ¯, GLP-1š ššˋšýÇ ššˋš (agonist)š¡ exenitideŠ ÚõÇÚÚõñ¥š¡Ú˜š šÚÚŠË¥ šçš ÚŠˋ¯, š˜õ¡¯šŠ NF-ö¤B/RANKL š Ú¡šýÇõ°õ¯ õÇŠ ´šÇ šŠÊõ° šŠ Êš ¡ šŠÊ[13].
Š¯Š¥š GLP-1š š˜šË Š¯ ÚõÇš ŠÚ Ú´õ°¥Š ššˋšýÇ ššÀÇš š¡ õý§ŠÀŠ¢ šŠŠ¥ ššˋšýÇ Š¿ššÀÇš š¡ õý§ŠÀ, šÎ GLP-1š õñ¡ Šš˜šýÇŠË¥ ÚçÚÇš š˜šËš ššÑõ¡¯ŠËÚËš Š¯ ÚõÇš ŠŠÏËõý§ÚšŠ¯ˋš ŠÚ ššˋšÇ šŠÊ.
Úš ŠÚ ššˋ
šËš ÚÚ˜ŠÏššŠ GLP-1 ššˋšýÇõ¯ ŠÏÊš¯ Šõý Š¯ÚŠõ° šš¥Šˋ¯, šËš õ¡¯õǚϚ ÚŠŠÏËš GLP-1š šýŠÎ˜ÚŠˋÇ š šÀ ŠÑŠ¿ŠË¥ šÎõ¯šÚÊõ° õ¡¯õǚϚ ÚÚõñ¥š¡Ú˜š šÇšš šõñ¿ÚšŠÊ[14]. ÚÚŠˋÇښݚ ŠË¥ ŠÑŠ¿ÚŠ type II pneumocyteššŠ GLP-1 ššˋšýÇš Š¯ÚšÇ ŠÏÊš¯ Šõý Š°Çõ° Šõ° šš¥Šˋ¯ GLP-1šÇ ÚÚŠˋÇښݚ š ŠÑŠ¿ŠË¥ šõñ¿ÚŠÊŠ Š°Çõ° õ¯ šŠÊ[15]. Úšš GLP-1š ššˋšýÇ Š¯ÚšÇ Šš õýš Š°ÇŠˋÇ, GLP-1šÇ šÊšÚ šÙÚ š Ú õýš¥ŠÀ šõ¯ŠŠ, ššÏ š¯õç˜ õý¯õ°¥ŠÊšÇ ŠÏšÏ ššš Š ŠÏš š¯õç˜ŠÊšÇ šÏÚŠõ¡¯ŠË¥ õ¡¯ŠÚõ° šŠÊ.
Šš ŠÚ ššˋ
GLP-1š Šš ŠÚ ššˋš Š¿õçš šçõñ¥š Š¯ÚšÀŠŠ¯, ššÚŠÑš ššˋÚÇš ššõ°¥ Š˜¥š šÙšñ´ŠË¥ šçš ÚŠÊ. ŠŠ˜¥š¯õ瘚š GLP-1š š 3ŠšÊš Ú˜š˜ÚŠˋÇ šššÇ Úš Ú õ¯šÚšõ° , ššÚŠÑš š õý§š¡Ú˜šš c-fosš Š¯ÚšÇ šÎõ¯Ššš¥Šˋ¯, GLP-1 ššˋšýÇ õ¡¡ÚÙš (antagonist)š¡ exendin 9-39ŠË¥ õ¯šÇ Ú˜š˜ÚŠˋÇ õñ¡ Ú´õ°¥õ¯ ššŠšŠÊ[16]. GLP-1š Š ÚÇšýŠ¥ ššš šçš ÚŠˋ¯, ššš šÇšÏÚŠ CRF, neuropeptide Yš õ¯š Ú¡ŠËÇŠˆ˜š šçš Úš˜ ššš šçš ÚŠ ššˋš ÚŠÊ. ŠŠ˜¥šÊÚš ÚçÚÇ GLP-1 ššˋšýÇõ¯ ššÚŠÑš arcuate Úç, paraventricular Úç, supraoptic Úç, subfornical organ, organum vascularum, laminae terminus, õñ¡ŠÎ˜õ° area postremaš õ¯š sensory circumventricular õ¡¯õÇš ŠÏšÇ šÀÇš˜Ú´š Úš¡ÚšŠÊ[17]. õñ¡Š¯Š¯ GLP-1 ššˋšýÇõ¯ šŠ Glp-1r-/- ššËŠ Š¿ŠÀ ÚŠ¿š Šš Ú¡šÇšÏŠÏ š šš š¡ šÙš šÚŠË¥ Š°ÇšÇŠ₤ŠÀ šÂ Š š¯õç˜õ¯ ÚšÚŠÊ[18]. ŠÚ GLP-1š ššËš L-š¡Ú˜Š¢ šŠŠ¥, ŠššŠ šÏš ÚˋšÝ Š¯ ŠÑŠ¿ŠË¥ Ú š šõ¡¯ ŠŠ˜¡š šÇŠ ŠÑššš ššÝŠ GLP-1š šÚÇ šššÇ šÀ¯š ŠŠšÏš ŠÚÇšŠ Š š¯õ瘊šÇš¥ ÚŠÊ. ÚšÏŠÏ š˜ŠššŠ š šš¡šÇŠ šŠŠˋÇ š 2Ú Š¿Š´Š° ÚššÇŠ šÏ õ¯š GLP-1š Ú˜š˜Úõ° 2, 6, 8, 48šõ¯šÏ¡ Ú˜ŠÏõ¯šÇ šÎõ¯Úõ° šššÇ šçš Š´šÇ Úš¡ŠšŠÊ[19,20]. Š¯Š¥š ššš šÙšñ´ÚŠˋÇ ššËš Lš¡Ú˜šš ŠÑŠ¿Š GLP-1š ÚšÀš ÚçÚÇš ŠŠ Š₤¡šÈ¥š õý§š ÚçÚÇš Šš šššÊšÑš ššˋÚš˜ ššš šçš šÚÊŠ õýš¥ŠÀ šõ¯ŠŠÊ.
šçõñ¥šŠ šŠÏš š šš š¯õ瘊˥ ÚçÚÇš GLP-1šÇ š õý§š¡Ú˜š ŠÚÇ Š°ÇÚ¡Ú´õ°¥õ¯ šššÇ šŠ ÊšÏõ° šŠÊ. ŠÚ Alzheimer Š°õ°¥ õ¯šÇ š õý§ÚÇÚšÝ šÏÚšš š 2Ú Š¿Š´Š°õ°¥ õ¯šÇ š¡šŠÎ¯ š Ú¡š Š˜š šËš õ¯ Š°Çõ° Šõ° ššÇš, GLP-1š Šš õý§š ÚÇÚšÝ šÏÚš ššÇš šŠÀšÇ š¿ŠÈš§š ŠÀ š¯õç˜õ¯ šÏÚŠõ° šŠÊ. ŠšÀ¡šÊ, ÚÚ´š´Š°šÇŠ Alzheimer (šš¡ ښNJ´¡)Š°š ŠŠ˜¥Šˆ´Š¡šš GLP-1šÇ ÚÙ-š¥šÎ, ÚÙ-š¯Ú, ÚÙ-šš¯š¡Ú˜š˜ ššˋšÇ Š°Çõ° Šõ° šš¥Šˋ¯, šŠ¯ŠÀšÇŠ ښݚ šÊšÇõ° õ¡¯šçŠ Ëš ÚËššÚÊŠ ŠÝ šÂš Ú´õ°¥õ¯ Š°Çõ° Šõ° šŠÊ[21,22]. Š¯Š¥š šçõñ¥šŠ šš¡ ښNJ´¡Š°šÇ šŠ Úššõý liraglutide [23,24]Š exenitide [25]ŠË¥ Ú˜š˜Úšš Š Ú´õ°¥ŠË¥ š¯õç˜ÚŠ ššš¯õç˜ŠÊšÇ Úš˜ šÏÚ šÊš šŠÊ. Š¯Š¥š GLP-1š šË-Šš šÑš ššÇ šÊšÚ šÙÚ š ÚŠ Ú¡ŠËÇŠˆ˜š¥ŠÀ šššçš Ú´õ°¥ šÇš¡šŠ š õý§š¡Ú˜ Š°ÇÚ¡Ú´õ°¥õ¯ õ¡¯ŠŠŠ Š¯šÇŠÊ[26].
š šËššš ššˋ
š šËšš GLP-1 ššˋšýÇš Š¯ÚšÇ Úš¡ŠššÏŠÏ ššÏ š ÚÚ šš¿ Š¯ õ¡¯ŠËš ŠÚÇšŠ ŠÏšÇ šŠ ÊšÏšÏ ššŠÊ. ŠŠÑŠÑš š¯õ瘚šŠ GLP-1 ššˋšýÇŠ š šËš ÚõÇšš Š¯õý˜ŠŠÊõ° ÚŠˋ¯, ššš¡Š´õÇššŠ Š¯ÚŠšÏ šõ° , õñ¥šš¡Š´õǚNJ š˜õ瘚ýÇšš Š¯õý˜šÇ ŠŠÊŠ Š°Çõ° Š šŠÊ. ÚšÏŠÏ š˜ŠššŠ šÊõ¯ šÇšš Ú¯ š šË ŠŠÏËšš Š¯õý˜ŠŠˋ¯ š¡Š´õǚNJ š˜õ瘚ýÇššŠ Š¯õý˜ŠšÏ šŠŠÊõ° Š°Çõ° Šõ° šŠÊ[27]. š šËš ŠÚ GLP-1š Ú´õ°¥Š Ú˜õý 3õ¯šÏ š¡ÀŠˋÇšš Š°¥ š šŠŠ¯, ŠÚ¡ŠË´Š´Š¯¯šÊššˋ(natriuresis), š šËš ÚŠËšÎõ¯, š˜õ瘚ýÇš˜õ°¥š´ šÎõ¯šÇŠÊ.
2002Š
š šýšš¥ŠÀ GLP-1š š šËš ŠÚ šÇŠ´ššˋšÇ Š°Çõ° [28]Š šÇÚŠÀ GLP-1, exendin-4, liraglutide, DPP4 šçš š Šˆ´Ššš ŠÚ¡ŠË´Š´Š¯¯šÊ šÇšÏššˋ Š¯ šÇŠ´ššˋšÇ šššÇ Š°Çõ° ŠšŠÊ[29]. õñ¡ õ¡¯š š š šËš õñ¥šš¡Š´õÇšš Na-H ion exchanger isoform 3š šçš ŠË¥ ÚçÚÇ ŠÚ¡ŠË´š š˜ÚÀšŠË¥ šçš Ú´š¥ŠÀš´ natriuresis (ŠÚ¡ŠË´Š´Š¯¯šÊ)ŠË¥ šÎõ¯šÚÇšÇ Úš¡ŠšŠÊ[30]. šÇŠ ŠõñŠˆ´ ššš¯õ瘚š GLP-1 ššˋšýÇ ššˋš Ú˜š˜ Ú õÇš¯¯ŠŠ Úš õ¯ÚÚ´õ°¥ŠË¥ š¥ŠÑ šÊŠˆ
Ú š šŠÊ. GLP-1š ŠÏšñ´Š šËš Ú˜š˜ÚŠˋÇ š šËš ÚŠËŠË¥ 22%õ¯Š šÎõ¯šÚ´ŠÊŠ š¯õç˜[31]õ¯ šš¥Š, õÝÇõ¯Ú šÝš¡ Š´šÝššŠ š šË ÚŠËš š Ú Š°Úõ¯ šŠÊ(95% confidence interval [CI] -3.6~8.8%)Š Š°Çõ° Š šŠÊ[32]. š˜õ瘚ýÇš˜õ°¥š´š ŠÚ GLP-1š Ú´õ°¥Š š š Š¿Šš˜š¡ šËššŠ GFRš šÎõ¯šÚÊŠ õýš¥ŠÀ šŠ Êš ¡ šš¥Š, õÝÇõ¯Ú šÝš¡ššŠ GFRš šÎõ¯šÚÊŠ Ú´õ°¥õ¯ õݯš Š₤¡Š₤¡ÚŠˋ¯, Š¿Š´Š° Šˆ´Š¡ššŠ õñ¥šŠÑš¡Š´õÇš ŠÚ¡ŠË´ Š¯ š ÚÇšÏ š˜ÚÀšŠË¥ šçš šš¥ õñ¥šŠÑ ššš¯´õ¯ šÎõ¯ŠŠ₤ŠÀ GFRšÇ õ¯šŠŠÊŠ Š°Çõ° õ¯ šŠÊ. Š¯Š¥š š˜õ瘚ýÇš˜õ°¥š´š ŠÚ GLP-1š Ú´õ°¥Š ŠŠ˜¥š¡šÏ š˜Šš¡šÏš Š¯Š¥, Š¿Šš˜ šÇš š˜ŠÑš Š¯Š¥, GLP-1š Ú˜š˜ õ¡¯õ¯šÇŠ Ú˜š˜ ÚÚš Š¯Š¥ ŠÊšÚõý ŠÚŠŠÊ.
GLP-1šÇ š šËš ššˋÚŠ Š¯ ššÇšŠ š˜Š¯ˋš ŠÚ¡ŠË´šÇŠ´ÚˋÚ¯Š(atrial natriuretic peptide, ANP)Š Š Š-ššÏšÊÚ
š ššÊÚ
šÇ õÇš˜ÚŠÊõ° šŠ Êš ¡ šŠÊ. ŠŠ˜¥ššŠ GLP-1š šÈ¥š˜ÚŠˋÇ š˜Š¯ˋš ANPõ¯ šÎõ¯ÚŠˋÇš ŠÚ¡ŠË´Š´ Š¯¯šÊššˋšÇ šÎõ¯ÚŠ š˜ŠššŠ Š¿ŠÀ ŠÚ¡ŠË´Š´Š¯¯šÊššˋšÇ šÎõ¯ÚšÏŠÏ ÚšÀš ANPšŠ Š°Úõ¯ ššŠÊ[33]. GLP-1 ššˋšýÇ ššˋš Š ŠŠ˜¥š¯õ瘚š ššÏšÊÚ
š IIš šÚÇ š ŠŠŠ õ° Úš, š¯ÚšÊÚ¡Š šÊŠË¥ š¯´Š´Úšõ° š˜õ瘚ýÇ ŠÇÚ¥š¡Ú˜šš PKAŠË¥ ÚçÚ GLP-1 ššˋšýÇŠË¥ šõñ¿ÚŠˋÇ cRafš ŠÚ ššÏšÊÚ
šÏ II š Ú¡š Š˜šýÇõ°ŠË¥ šçš Ú´šÇ Úš¡ŠšŠÊ[34]. õÝÇõ¯Ú šÝš¡ššŠ GLP-1š šÈ¥š
ÚŠˋÇ ÚšÀš ššÏšÊÚ
š II ŠŠõ¯ õ¯šŠšõ° š šË Š°ÇÚ¡ Ú´õ°¥õ¯ õÇš¯¯ŠšŠÊ[31].
GLP-1š Š¿Š´Š°šÝ š šÎ Šˆ´Š¡šÇŠ õ¡šÝ š ššš ŠŠ˜¥Šˆ´Š¡šš š šË Š°ÇÚ¡Ú´õ°¥õ¯ Úš¡ŠšŠÊ. GLP-1š šÚ š šË Š°ÇÚ¡ Ú´õ°¥Š 2007Š
š šýšš¥ŠÀ Š°Çõ° Ššš¥Šˋ¯, 2Ú Š¿Š´Š° Šˆ´Š¡š¡ db/db ššËš exendin-4ŠË¥ 8šÈ¥õ¯ Ú˜š˜Ú Ú Š´Š¯ÝŠ´š õ¯š, š¯ÚšÊÚ¡Š šÊš õ¯š, Š¿Š´Š°šÝ š šÎš Š°ŠÎ˜šõý˜š Ú¡š šÇ õÇš¯¯ŠšŠÊ[35]. šÇŠ¯ š šË Š°ÇÚ¡Ú´õ°¥Š õñ¡ Ú 2Ú Š¿Š´Š° ÚšŠË¥ Ššš¥ŠÀ Ú ššš¯õ瘚šŠ exendin-4, liraglutide, vildagliptin, linagliptin, alogliptin Ú˜š˜ Ú Š´Š¯ÝŠ´ õ¯š , š¯ÚšÊÚ¡Š šÊ õ¯š, š˜šÇÚ š¿Çš¡š õ¯š, Š¯ šÀ¯šÏŠ°ŠÎ˜Úš šõý˜š Ú¡š šÇ Š°Çõ° ŠšŠÊ[27].
Š¥š ŠÚ ššˋ
š¥ŠÑ Š¿Š´Š° š§š õ¯ õ°´Šš˜š šÂšÏ šš šÚËš Š₤¡š° õ°´š šÚš š˜ŠÎ˜Š õý§š¯õ¯ šŠÊõ° Š šŠ Êš ¡ šŠŠ¯, GLP-1š Š¥š ŠÚ Ú´õ°¥Š šÇŠ Ú õýš¡õ¯?
Úõý§Ú š˜šÝš Ššš¥ŠÀ DPP4 Ú´š ÚšÝõ°¥ õ°´Š¯Ššš š¯õǚݚ šÀ¯š˜Ú š¯õç˜ õý¯õ°¥ŠË¥ Š°ÇŠˋÇ, ÚšÀšš DPP4 Ú´šš ÚšÝšÇ Šš õ篚š ÚšÝÚ GLP-1š ŠŠõ¯ ŠÛõ° õ°´Š¯Šõ¯ ŠÛš õýš¥ŠÀ Š°Çõ° Ššš¥Šˋ¯ homeostatic model-insulin resistance, IL-6, high sensitivity C reactive protein šš¿šŠ š¯õÇšÇ ššŠÊ[36]. Š¯Š¥š š¥ŠÑ š¡šŠÎ¯ š ÚٚݚNJ š¥šÎš DPP4 ښ݊ õÇš˜Ú š šš¥Š, DPP4 ښݚ šÎõ¯õ¯ šÇŠ š Š Š
ŠÎ§š š¥ŠÀ õ°´ŠÊõ°çšÎõ°¥Š š¯õÇšÇ šš õýš šš˜ÚŠ šõý˜šÇŠÊ.
ŠŠ˜¥š¯õ瘚šŠ GLP-1 ššˋšýÇŠË¥ šËõ¡¯õ¯ Ú˜š˜ÚŠˋÇ š˜š šÈ¥ õ°´(trabecular bone)š šÏŠ Š¯ õ瘚À¯ŠË¥ ÚËššÚÊŠ õýš¥ŠÀ Š°Çõ° Šõ° šŠÊ. ŠšŠË¥ š š Ú ššËšš õ°´ššÊš š ŠÚõ° liraglutide 0.3 mg/kg/day, exenatide 10 ö¥g/kg/dayŠË¥ 4šÈ¥õ¯ Ú˜š˜Ú õý¯õ°¥, Ú¥šÏõ°´šŠ š šÚ Š°Úõ¯ ššš¥Š š˜š šÈ¥õ°´š šÏŠšÇ šÎõ¯Úšõ° , ÚšÀš sclerostinš õ¯šÚõ° calcitoninš šÎõ¯ÚšŠÊ[37].
š˜ŠššŠ GLP-1 ššˋšýÇ ššˋš ŠË¥ 52šÈ¥õ¯ Ú˜š˜ Ú õ°´Šš˜ŠË¥ š¯õç˜Ú õý¯õ°¥, GLP-1 ššˋšýÇ ššˋš ŠË¥ Ú˜š˜Ú õ篚š õ°´ÚšÝšÇ 16% šÎõ¯Úšõ° õ°´ššÊš šŠ¯ˋÚ´šÇ Úš¡ŠšŠÊ[38]. Š¯Š¥š GLP-1š Š¥š šÏš š š¥ŠÀ šÂš Ú´õ°¥õ¯ šš õýš¥ŠÀ õ¡¯ŠŠŠÊ. ÚšÏŠÏ Clinical Practice Research Datalink (2007-2012)šŠÈŠË¥ šÇšˋÚš˜ GLP-1 š˜šˋšš Š¿š˜šˋš õ¯š õ°´š šÚš šÀ¯š˜Ú õý¯õ°¥ GLP-1 ššˋšýÇ ššˋš š š˜šˋš õ°´š šÚš õ¯ššÚÊŠ õýš¥ŠÀ Š°ÇšÇšÏ ššõ° (adjusted hazard ratio 0.99, 95 % CI 0.82-1.19), õ°´ŠÊõ°çšÎšÝ õ°´š šÚŠ õ¯ššÚʚϊ šŠ õý¯õ°¥ŠË¥ Š°ÇšŠÊ[39]. Š¯Š¥š õ°´Šš˜š ŠÚ GLP-1š Ú´õ°¥Š šÂ Š ŠÏš š¯õç˜õ¯ ÚšÚ õýš¥ŠÀ šõ¯ŠŠÊ.
õ¯, õñ¥šÀ, šÏŠ¯ˋš ŠÚ ššˋ
GLP-1 ššˋšýÇŠ õ¯, õñ¥šÀ, šÏŠ¯ˋš šÀÇš˜ÚŠõ¯?
GLP-1š šŠÎ˜š š¡ ššˋš ŠŠÑŠÑ GLP-1š ššˋšýÇŠË¥ ÚçÚÇ š¥šÇŠ š šŠŠ¯, GLP-1 ššˋšýÇõ¯ Š¯ÚŠŠ šÀ¯šÏš šš š¡õ¡Ú ŠŠÀ šñŠ, ššË, Ú, Š, š šË, ššÚŠÑ, š˜ÚõÇõ°, õñ¡ŠÎ˜õ° ššËšÇŠÊ[40]. õñ¡Š˜Š õ¯, šÏŠ¯ˋ, õñ¥šÀššŠ GLP-1š ššˋšýÇõ¯ Úš¡šÇ š ŠŠÊõ° Úõ¡¯Š Úõ° š¥ŠÑššŠ Úš¡šÇ ŠŠÊõ° Š Úš˜ ŠÊš Šˆ´Ú¡Ú šÚšÇŠÊ[41]. ÚšÏŠÏ 1ښNJ 2Ú Š¿Š´Š° ŠŠ˜¥ š¯õ瘚š GLP-1š Ú˜š˜ÚŠˋÇ õ¯ššŠ glucose transporter type 2 (GLUT2)š Š¯Úš šÎõ¯šÚÊõ° õñ¥šÀõ°¥ šÏŠ¯ˋššŠ GLUT4š Š¯Úš šÎõ¯šš¥¯ŠÊ[42]. šÇš õ¯šÇ šÚõǚNJ ŠŠ˜¥Šˆ´Š¡šš GLP-1ŠË¥ Ú˜š˜ÚŠˋÇ õ¯, šÏŠ¯ˋ, õñ¥šÀšš š¡šŠÎ¯õ°¥ Š˜ÇõÇÚŠˋÇš š¡šŠÎ¯õ°¥ Š¿šñÚ ššˋš ÚçÚÇ ÚŠ¿š šÀ¯š ÚŠÊŠ Š°Çõ° õ¯ ššÇš ššˋšýÇ šÇš¡š ŠÊŠË¡ õý§ŠÀŠË¥ ÚçÚÇ Š¿Šš˜ õ¯š š ŠÚ Ú´õ°¥õ¯ šŠšÏš š¯õç˜õ¯ šÏÚŠõ° šŠÊ.
GLP-1š õ°¥š¯ õ¯, õñ¥šÀ, šÏŠ¯ˋšš šñšË š¡ Ú´õ°¥õ¯ ššõ¿?
GLP-1šÇ šñšËš š¡šŠÎ¯šÇŠ õ¡ŠÈ´š¿Çõ°Êš ŠÑŠ¿š Š˜ÇõÇÚõý ÚŠ¿š šÀ¯š ÚŠ Ú´õ°¥õ¯ ššõ¿? õ¯šË šýš GLP-1š šñšË š¡ Ú´õ°¥ŠË¥ Š°Çõ° Ú Gutniak ŠÝ[43]š c-peptideõ¯ š Ú ŠÑŠ¿ŠšÏ šŠ š 1Ú Š¿Š´Š° Úššõý GLP-1š š ŠÏË Ú˜š˜ÚŠˋÇš hyperinsulinemic clampŠË¥ šÚÚ õý¯õ°¥, glucose infusion rateõ¯ šÎõ¯Ú´š õÇš¯¯Úšõ° , õñ¡ Ú šÚõÇŠÇ šÊÚš ÚçÚÇ GLP-1šÇ õñ¥šÀ, šÏŠ¯ˋ, õ¯šš Š¿šÙšñ´ŠË¥ šÎõ¯šÚÇš Úš¡ÚšŠÊ[44]. šçõñ¥ Prigeon ŠÝ[45]Š octreotideŠË¥ Ú˜š˜Úš˜ š¡šŠÎ¯šÇŠ õ¡ŠÈ´š¿Çõ°Êš ŠÑŠ¿ŠË¥ šçš Ú šÚšš š š šÝš¡šõý GLP-1š Ú˜š˜ÚŠˋÇš ÚŠ¿š Š°ÚŠË¥ õÇš¯¯Ú õý¯õ°¥, ÚšÀš š¡šŠÎ¯šÇŠ õ¡ŠÈ´š¿Çõ°Êš ŠÑŠ¿õ¯ šçš ŠšÇ Š°Úõ¯ šššŠ ŠÑõç˜Úõ° , ŠÇš¡šÝ Š¿ššÝšÇ šçš ŠšÇ õ°çŠ°çÚŠ¿šÇ Š´šÇšÏŠ õýš õÇš¯¯ÚšŠÊ. Š¯Š¥š GLP-1š šñšËš š¡šŠÎ¯šÇŠ õ¡ŠÈ´š¿Çõ°Êš ŠÑŠ¿š Š˜ÇõÇÚõý šÏš š š¡ ÚŠ¿ õ¯ÚÚ´õ°¥õ¯ ššš šš˜ÚŠÊ.
õ¯š ŠÚ ššˋ
GLP-1 ššˋšýÇ Š¯Úš õ°¥õݯ ŠÏš š¯õ瘚š õݯš Š¯ÚŠšÏ šŠŠÊõ° Š°Çõ° Ššõ° [42], GLP-1šÇ õ¯š cAMP ššÝš šÎõ¯šÚÊšÏ šõ° glycogenolysisš õݯš ššˋÚšÏ šŠŠÊŠ Š°Çõ° Š šš¥Š[46], phosphatidylinositol 3-kinase (PI3K)/PKB, PKCš ښݚ ÚçÚÇ šËš õ¯š¡Ú˜šš glycogen synthase ښݚ šÎõ¯šÚ´ŠÊŠ Š°Çõ° Š šõ° [47], exenitide Ú˜š˜Š Š¿Š´Š° ŠŠ˜¥ Šˆ´Š¡šš õ¯š Š¿š šš šçš ÚŠˋ¯ š¡šŠÎ¯ š Úٚݚ õ¯š šÚÇšÇ Š°Çõ° ŠšŠÊ[48]. ŠÚ õ¯šÇŠ õñ¥šÀššš GLP-1 ššˋš GLP-1 ššˋšýÇõ¯ šŠ inositolphosphoglycanšÇ GLP-1š second messanger šÙÚ š Úš˜ š Ú¡š Š˜šÇ š¥šÇŠŠÊŠ Š°Çõ° Š šŠÊ[49]. Š¯Š¥š GLP-1š Š¿Šš˜š ŠÚ š¯õ瘊 GLP-1š šÏš š š¡ Ú´õ°¥š¡šÏ, ššˋšýÇŠË¥ ÚçÚ õÝÇšÏ šŠŠˋÇ ŠÊŠË¡ õ¡¯š šÇ šŠšÏ ŠÝš ŠÚÇš šÂ Š ŠÏš š¯õç˜õ¯ ÚšÚ šÚšÇŠÊ.
ÚšÏŠÏ šçõñ¥ š¯õ瘚šŠ š˜Šš õ¯š¡Ú˜Š õ¯šš¡Ú˜šÈ¥šš GLP-1š ššˋšýÇ Š¯ÚšÇ Úš¡Ššõ° [50], õ¯ššš šÏŠ¯ˋŠš˜š šÊšÚ šÙÚ š Ú´šÇ Š°Çõ° Šõ° šŠÊ[51,52]. Exendin-4ŠË¥ ob/ob ššËšõý Ú˜š˜Úšš Š š¡šŠÎ¯ š ÚÙšÝ Š¯ šÏŠ¯ˋõ¯šÇ Ú¡š Ššõ° , õ¯š¡Ú˜š Ú˜š˜Ú õý§š¯ CAMPŠË¥ šÎõ¯šš¥¯ŠÊ[53]. ŠÚ šçõñ¥ Š¿šš§šÝšÏŠ¯ˋõ¯šÏÚ(nonalcoholic fatty liver disease, NAFLD) Úšš õ¯šš DPP-4 mRNA Š¯ÚšÇ õÝÇõ¯Ú šÝš¡š Š¿ÚÇ Šõý Š°Çõ° Šõ° ššÇš šŠÏŠ GLP-1š ŠÑÚšÝÚŠ š Ú¡š Š˜šýÇõ°š šÇšõ°¥ š¡šŠÎ¯ š ÚÙšÝ, NAFLD õ¯š šÚ¡š¯õÇšÝšÇ šš õýš šš˜ÚŠÊ[54].
õñ¥šÀš ŠÚ ššˋ
GLP-1š õñ¥šÀš ŠÚ Ú´õ°¥Š š¡šŠÎ¯ š Úٚݚ õ¯š šÚÊõ° , õñ¥šÀš õ瘚À¯ Š¯ Š₤¡Ú š§ŠŠÎ˜šš ššš šÊšÇŠ õýš¥ŠÀ šŠ Êš ¡ šŠÊ. õ° šÏŠ¯ˋššÇš š šˋŠ šÊÚ¡Š Ú šÀ¯Ú š š Ú˜š˜Úš˜ ŠÏŠ 2Ú Š¿Š´Š° ŠŠ˜¥Šˆ´Š¡ššŠ exenitideŠË¥ 8šÈ¥õ¯ Ú˜š˜Ú õý¯õ°¥ ÚŠ¿, šÊšÝšÏŠ¯ˋ, š Š¯ŠšÏŠ´Š¯Ýš§Š šÊÚ
ŠÀÊ(low density lipoprotein-cholesterol), š¡šŠÎ¯š šš¿õ¯ š šÚõý õ¯šÚšõ° õñ¥šÀšš Š¿šÙšñ´õ¯ šÎõ¯Ššš¥Šˋ¯ š¡šŠÎ¯ š ÚÙšÝšÇ õ¯šÚšõ° , õñ¥šÀš¡Ú˜š š¡Ú˜šÏš¡ŠÏ(endoplasmic reticulum)šÇŠ Š₤¡Ú š§ŠŠÎ˜šš šššÇ õ¯šŠ´š Úš¡ÚšŠÊ[55]. ŠÚ Š¿Š´Š° ššËš¡ KKAyš liraglutideŠË¥ Ú˜š˜Ú õý¯õ°¥šš šÙš õñ¥šÀš õ瘚À¯Š Š₤¡Ú š§ŠŠÎ˜šš šššÇ ŠšÀ¯õ篚 Š¿ÚÇ š šÚõý ŠÛšš¥Šˋ¯, õñ¡ õ¡¯š š¥ŠÀ protein tyrosine phosphatase 1B Š¯Úš šçš š PI3K Š¯ GLUT4 Š¯Úš šÎõ¯š õÇŠ ´šÇ šŠÊŠ Š°Çõ° õ¯ šŠÊ[56].
šÏŠ¯ˋšÀ¯šÏš ŠÚ ššˋ
GLP-1 ššˋšýÇŠ šÏŠ¯ˋ šÀ¯šÏšš õݯš Š¯ÚŠšÏ šŠŠÊõ° Š°Çõ° Ššš¥Š[57], šÏŠ¯ˋ š¡Ú˜ŠÏšš GLP-1š õý¯Úˋ ŠÑšõ¯ Úš¡ŠšÇ šÇŠ GLP-1 ššˋšýÇšŠ šÂ ŠÊŠË¡ šÝšÏš¡ õýš¥ŠÀ Š°Çõ° Šõ° šŠÊ[58]. Š¿ŠÀ GLP-1 ššˋšýÇš ښݚ õÇš¯¯ŠšÏ ššŠŠ¥Š exendin-4 Ú˜š˜Š GLP-1 Ú˜š˜ Ú šÏŠ¯ˋš¡Ú˜šš GLUT4š ښݚ ÚçÚÇ Š¿šÙšñ´õ¯ šÎõ¯Š´šÇ Š°Çõ° ŠšŠÊ[59]. ŠÚ Tomas ŠÝ[60]š õ° šÏŠ¯ˋššÇŠÀ š ŠŠ Š¿ŠÏ ššËš GLP-1 (32-36)š Ú˜š˜Ú õý¯õ°¥, õ¯ššÏŠ¯ˋšš UCP-1, UCP-3š Š¯Úš šÎõ¯šÚÊõ° , õñ¥šÀššŠ UCP-3š Š¯Úš šÎõ¯šÚÊŠˋ¯ acetylCoA carboxylaseŠË¥ šçš šš¥ šÏŠ¯ˋš¯ š¯Ú Š¯ Š¯šÇššˋš šÎõ¯šÚÇš Š°Çõ° ÚšŠÊ. šÇŠ GLP-1 ššˋšýÇš Š˜ÇõÇÚõý GLP-1 ššˋšýÇ õ¡¡ÚÙšýÇõ¯ nonapeptideŠ pentapeptideŠË¥ ÚçÚÇ ššˋšýÇš Š˜ÇõÇÚõý ššˋÚ õýš šš˜ÚŠÊ.
GLP-1š šÏšÏŠš˜š ŠÚ Ú´õ°¥Š šÊšÝšÏŠ¯ˋš ÚÀšŠË¥ šçš ÚŠ õýš¥ŠÀ šŠ Êš ¡ šŠÊ. š˜Ššõý GLP-1š Ú˜š˜Ú õý¯õ°¥ šÚ šÊšÝšÏŠ¯ˋ ŠŠ Š¯ š ŠÎ˜šÏŠ¯ˋš¯ ŠŠõ¯ š šÚõý õ¯šÚšŠÊ. šÇŠ¯ Ú´õ°¥Š GLP-1š šÏŠ¯ˋšÀ¯šÏš ŠÚ šÏš š š¡ Ú´õ°¥Š¥õ¡¯ Š°ÇŠÊŠ ššš šš Š¯¯šÑš šÏš¯šÚÊõ° š¡šŠÎ¯š šÚ šÏŠ¯ˋŠÑÚÇŠË¥ šçš ÚŠ ššˋ ŠŠ˜¡š¥ŠÀ ŠÑšŠõ° šŠÊ[61].
õý¯ ŠÀ
GLP-1š šËš L-š¡Ú˜šš ŠÑŠ¿ŠŠ š¡Ú˜Š ÚÇ Ú¡ŠËÇŠˆ˜š š¥šÂ
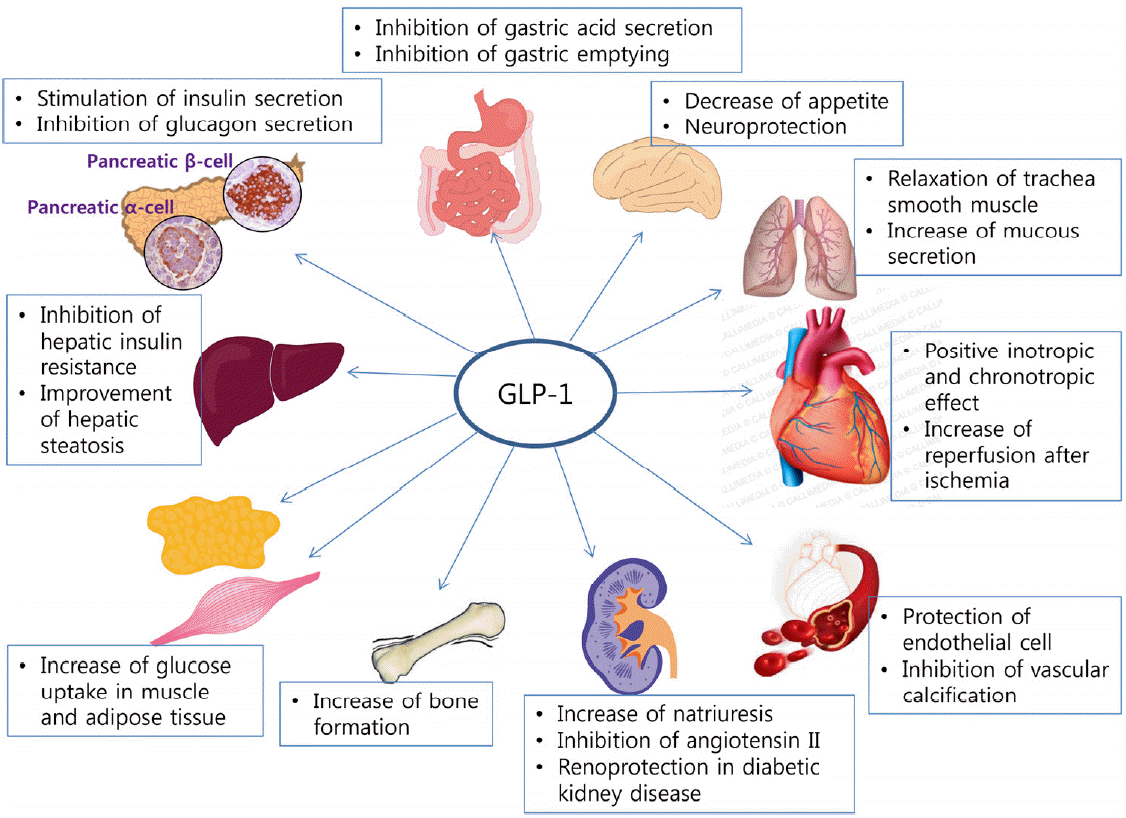
š¥ŠÀ šñšËš Šý Úš¡Ú˜šš š¡šŠÎ¯ ŠÑŠ¿ŠË¥ šÇšÏÚõ° šÚš¡Ú˜šš õ¡ŠÈ´š¿Çõ°Êš ŠÑŠ¿ŠË¥ šçš ÚŠ õýšÇ šÈ¥ššˋšÇŠÊ. ÚšÏŠÏ GLP-1š ššˋšýÇõ¯ šñšËŠ¢ šŠŠ¥ ŠÊŠË¡ š˜Š˜ šÀ¯šÏšš Š¯ÚŠŠ₤ŠÀ GLP-1š õñ¥õÝ¯Ú š§Š˜¥ š¿ŠÈŠ ŠÊšÚ ššˋš ڊΘŠ¥ šõ¯ŠŠÊ. GLP-1š šñšË š¡ Ú´õ°¥ŠË¥ šš§ÚÇŠ°ÇŠˋÇ ššË šÇŠ šçš (šŠ¯¯šÑ šÏš¯), ŠÇÚ¥š¡Ú˜ Š°ÇÚ¡, š˜Š¯šÑ šÎõ¯ Š¯ ÚÚš ŠÚ š˜šËš¡Ú˜ Š°ÇÚ¡, šššçš , šýÇšÊõ¯š, Šš õý§ Š°ÇÚ¡, š šË Š°ÇÚ¡, õ°´Š¯Š šÎõ¯ ŠÝš ŠÊšÚ ššˋšÇ šŠÊ(Fig. 1).
šš¥ŠÀŠ GLP-1š šŠÀšÇ ššˋŠÊšÇ Š Š¯ÚšÏŠÎ˜Š¥ õ¡¯ŠŠŠÊ. ŠÚ õñ¡ õ¡¯š š¥ŠÀš šÇŠ¯ ŠÊšÚ Ú´õ°¥õ¯ GLP-1 ššˋšýÇŠË¥ ÚçÚ šÏš š š¡ Ú´õ°¥š¡šÏ š¡šŠÎ¯šÇŠ õ¡ŠÈ´š¿Çõ°Ê šÀ¯š š ÚçÚ õ¯š š š¡ Ú´õ°¥š¡šÏ, ŠÏš¥ šÏš š š¡ Ú´õ°¥Š¥ŠˋÇ GLP-1 ššˋšýÇ ššÀÇš š¡šÏ šŠŠˋÇ ššˋšýÇš Š˜ÇõÇÚõý Šš˜šýÇŠ ŠÊŠË¡ š Ú¡ š Š˜šýÇõ°õ¯ šÀÇš˜ÚŠšÏ ŠÝš ŠÚ Š šÑõ¯š š¡ š¯õç˜õ¯ ÚšÚŠÊ.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






