서 론
환상췌장은 희귀한 질환으로 대개 유아기 때 발견되는 선천성 이상이다. 환상췌장이 성인에서 발현되는 경우는 주로 원위부 담관이나 췌관의 협착을 통해 황달이나 복통 등의 증상을 통해 발견되고 이는 내시경적 시술 혹은 수술로 치료하게 된다[1].
호산구성 췌장염 또한 전 세계적으로 매우 희귀한 질환으로 대부분 호산구성 위장관염 혹은 말초혈액의 호산구증가증과 연관이 있었다[2-5]. 호산구성 췌장염의 진단은 대부분에서 수술을 통해서 이루어졌는데, 이는 췌장의 국소적인 염증성 병변을 영상의학적으로 암과 구분하기 어렵기 때문이다[6]. 실제로 20건 중에 수술시행 없이 진단된 증례는 단 두 건이었다[7,8].
저자들은 환상췌장과 호산구성 췌장염이 동반된 환자에서 스테로이드를 사용하여 증상이 호전된 증례를 경험하였기에 문헌고찰과 함께 보고하고자 한다.
증 례
환 자: 김〇〇, 여자, 43세
주증상: 식후 구토
현병력: 내원 1주 전부터 발생한 식후 구토를 주소로 내원하였다. 내원 3일 전 타 병원에서 12시간 금식 후 위내시경 검사 시행하였으나 위 속 음식물이 남아있어 검사 중단 후 추가적인 검사 위해 내원하였다.
과거력: 없음
사회력: 5갑년의 흡연력
음주력: 소주 한 병씩 주 3-4회
진찰 소견: 내원 당시 급성병색이었고, 활력징후는 100/60mmHg, 매각 72회/분, 호흡수 20회/분, 체온 36.6℃였다. 의식은 명료하였으며 결막충혈, 공막황달, 피부발진, 혀의 탈수 소견은 없었다. 경부, 액와부 및 서혜부에서 림프절은 촉지되지 않았고 흉부 진찰에서도 이상 소견은 없었다. 복부 진찰에서 간종대와 비장 종대는 없었으며 심와부 압통이 있었지만 반동 압통은 없었고 복부 청진에서 장음은 정상적이었다. 근골격계 진찰에서 이상 소견은 없었다.
검사실 소견: 입원 시의 말초혈액검사에서 혈색소 13.9 g/dL, 백혈구 6,380/μL (호중구 33.6%, 림프구 48.0%, 단핵구 10.7%, 호산구 6.1%, 호염구 1.6%), 혈소판 211,000/μL였고, 혈청화 학검사에서 AST 23 IU/L, ALT 15 IU/L, 아밀라제 26 U/L, 리파제 20 U/L, 알칼리성 포스파타제 174 IU/L, 총 빌리루빈 0.7 mg/dL이었으며 혈청전해질검사, 혈액응고검사는 정상이었다. 혈청면역글로불린검사에서 IgG 1,200 mg/dL, IgA 261 mg/dL, IgM 132 mg/dL, IgG4 57.3 mg/dL로 모두 정상이었다. 형광항핵항체 시험에서 1+, 균일한 양상을 보였으나 항중성구세포질항체와 류마티스인자는 음성이었다.
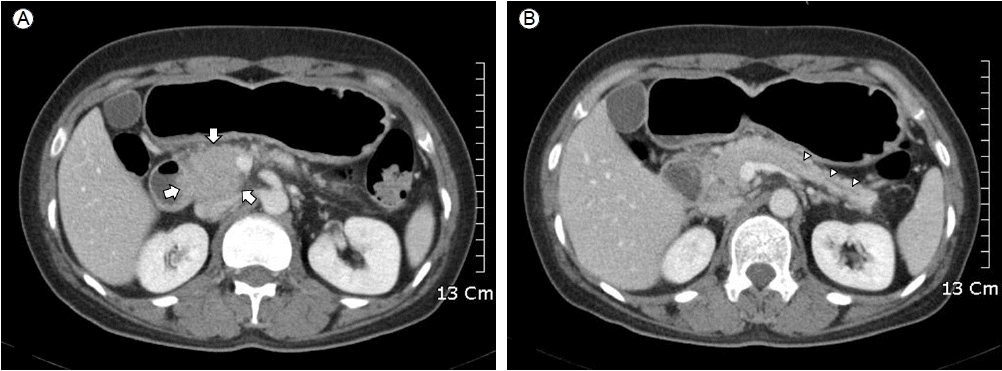
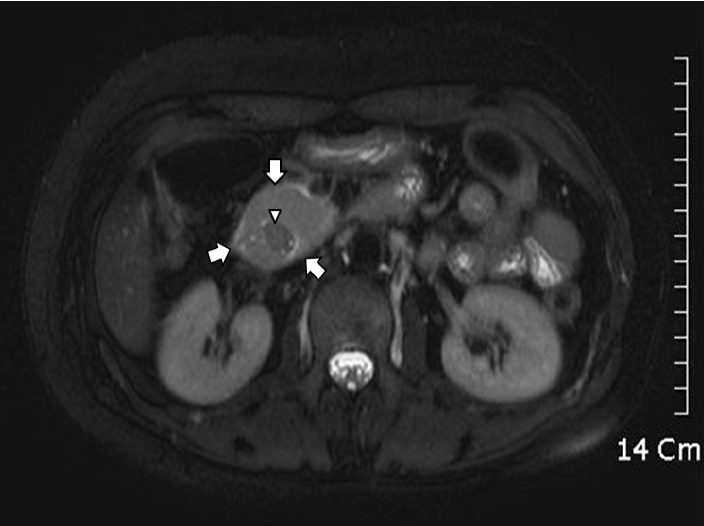
방사선학적 소견: 복부 전산화단층촬영에서 췌장 두부에서 바터씨 팽대부까지 걸쳐서 불균일한 조영을 보이는 종대가 보였으나 췌관이나 담관은 정상이었다(Fig. 1). 췌장 자기공명영상에서는 십이지장 제2부를 둘러싼 환상췌장이 발견되었고(Fig. 2), 양성자 단층촬영에서는 췌두부 주변에서 최대 표준화 섭취계수 7.5의 선상의 과대사 병변이 관찰되었으나 췌장암과 급성 염증성 반응을 구분할 수는 없었다. 췌관의 협착 등은 보이지 않았다.
위 내시경 소견: 위내시경상에서는 장상피화생을 시사하는 위점막의 회백색의 결절성 변화와 발적 등 만성 위염과 십이지장염 소견을 보였으나 십이지장 제2부 근위부에 협착이 있어 내시경을 진행할 수 없었다.
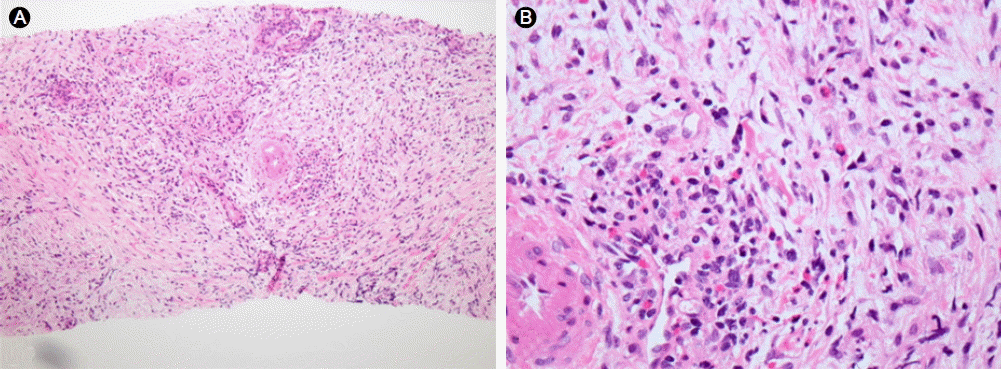
조직 검사 소견: 췌두부의 종괴를 초음파 유도하 침생검을 시행하였고 조직검사에서 췌실질에 미만성 섬유화와 다수의 호산구와 림프구 그리고 약간의 형질세포가 침윤해 있었다. 췌장 꽈리 구조가 파괴 또는 위축되어 있었으며 세정맥염과 세정맥주위염이 동반되어 있었다(Fig. 3). IgG4 양성세포는 다섯 개의 고배율 시야에서 열 개 이하로 관찰되었다.
치료 및 경과: 조직 검사 소견을 통해 호산구성 췌장염을 확인하고 스테로이드 치료를 시작하였다. 장폐색으로 인하여 경구섭취가 불가능하여 하이드로코티손 150 mg을 5일간 정맥주사하였다. 이후 시행한 상부위장관 조영술에서 십이지장의 협착이 호전되고 유동식 배출이 정상화 되어 경구용 스테로이드와 식이를 진행하여 구토 등의 증상이 없어 퇴원 후 외래 추적관찰 중이다.
고 찰
호산구성 췌장염은 매우 희귀한 질환으로 정확한 발생원인은 알려져 있지 않다. 현재까지 문헌보고된 20개의 증례를 분석하여보면(Table 1), 호산구성 위장관염 혹은 말초혈액 호산구증가증이 각각 75% 정도에서 동반되고 2건에서만 뚜렷한 알러지 질환의 과거력이 있었다[9]. 호산구성 췌장염의 약 절반 정도가 췌장의 종괴로 발현하여 임상적으로 췌장암과 감별진단이 어렵다. 췌장에 대한 영상의학 검사로 복부전산화단층촬영, 초음파검사, 자기공명영상 등을 시도해 볼 수 있으나 이러한 검사들로는 췌장암과 확실한 감별이 어렵기 때문에 조직 검사가 필요하다. 지금까지 보고된 20건 중 단 두건에서만 경피적 침생검이 시행되었고[7,8], 나머지 18건에서는 수술과 병행한 조직 검사가 시행되었다. 그러므로 췌장의 종양성 병변이 관찰되고 호산구성 위장관염이나 말초혈액 호산구증가증이 동반되는 경우 양성질환인 호산구성췌장염의 가능성에 대해 주의를 기울일 필요가 있다. 영상의학 검사로 미만성 췌장의 종대가 있거나 역행성 췌담관조영술에서 췌관 전체에 걸쳐 불규칙한 협착이 있는 경우 호산구성 췌장염을 의심하여야 한다[7].
조직학적 소견으로는 소엽 간, 소엽 내의 섬유화, 췌소엽의 미만성 호산구 침윤, 주췌관 상피세포 파괴와 췌관 주위의 호산구 침윤, 세정맥 및 세동맥의 호산구 침윤 등이 보고된 바 있다[7]. 육안소견은 다수의 소결절부터 췌두부의 미만성 경화성 종대 등의 소견을 보이고 괴사 및 농양이 동반된 예도 있었다[9]. 본 증례에서는 췌실질의 미만성 섬유화와 더불어 호산구 및 림프구 침윤이 보였고 췌장 선구조는 파괴되거나 위축되어 있었고 세정맥과 주위의 염증이 동반되어 있었다(Fig. 3). 면역화학 염색상에서는 P53, CEA, MIB-1 음성 소견을 보였고 IgG4에서 또한 음성 소견을 보여 자가면역 췌장염과 구분되는 조직학적 소견을 보였다.
자가면역성 췌장염은 영상의학 검사상에서 췌실질의 비대를 보이고 이는 종종 종양으로 의심되며 스테로이드를 이용한 치료에 극적인 호전을 보인다는 점에서 호산구성 췌장염과 일견 공통되는 특징을 가진다[10]. 그러나 호산구성 췌장염의 경우는 조직 검사에서 호산구의 침범이 우세하다. 최근의 자가면역성 췌장염은 조직학적으로 림프형질세포 경화성 췌장염(lymphoplasmacytic sclerosing pancreatitis)와 특발성 췌관 중심 췌장염(idiopathic duct centric pancreatitis, IDCP)로 분류되고 전자의 경우는 IgG4염색 양성 세포가 고배율에서 최소 20개 이상이 발견된다[10]. IDCP에서는 IgG4염색 양성세포는 거의 발견되지 않고 호산구가 아닌 호중구의 침범(granulocyte epithelial lesion)이 췌관 중심에 나타나는 차이가 있다[10]. 임상적으로는 대부분의 경우 호산구성 위장관염이나 말초혈액 호산구증가증이 동반되는 호산구성 췌장염과 달리 IDCP는 궤양성 대장염 이외의 동반 질환은 알려져 있지 않다[10]. 또한 무통성의 황달이 주증상인 자가면역성 췌장염과는 달리[10] 호산구성 췌장염의 경우는 복통이 주증상이다(Table 1).
호산구성 췌장염의 치료는 호산구성 위장관염과 마찬가지로, 경구 스테로이드를 사용하게 된다. 본 증례의 환자에서는 금식과 동시에 증상이 사라져 정확한 호전시기를 알 수 없었으나 스테로이드 사용 5일 후 시행한 상부위장관 조영술에서 십이지장 협착의 호전을 확인할 수 있었다.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






