ьДЬ ыба
1950ыЕДыМАьЧР ь▓ШьЭМ ьЖМъ░ЬыРЬ ьЭ┤эЫД warfarinьЭА ъ╖╕ ьВмьЪйыЯЙьЭ┤ ьзАьЖНьаБьЬ╝ыбЬ ьжЭъ░АэХШьЧм эШДьЮм ъ░АьЮе ыДРыжм ьВмьЪйыРШыКФ эХньЭСъ│аьаЬыбЬ, ьЧ░ъ░Д ь▓Шы░йыЯЙьЭА ьаДьД╕ъ│ДьЭ╕ъ╡мьЭШ ьХ╜ 0.5ьЧРьДЬ 1.5%ьЧР эХ┤ыЛ╣эХЬыЛд[1]. WarfarinьЭШ ъ░АьЮе эЭФэХЬ ы╢АьЮСьЪйьЭА ь╢ЬэШИьЭ┤ый░ ъ╖╕ ьЬДэЧШыПДыКФ эХньЭСъ│аьЭШ ьаХыПДьЩА эБ░ ъ┤АыаиьЭ┤ ьЮИыКФыН░, ьдСьЪФэХЬ ым╕ьаЬьаРьЭА ьаБьаИэХЬ эХньЭСъ│а ьИШьдАьЧР ыПДыЛмэХШыКФ ыН░ эХДьЪФэХЬ ьЪФъ╡мыЯЙьЧР ьЮИьЦ┤ ъ░Ьъ░ЬьЭ╕ ъ░ДьЭШ ь░иьЭ┤ъ░А эБмыЛдыКФ ьаРьЭ┤ыЛд. ьЭ┤ьЧР ыМАэХЬ ьЭМьЛЭ, ьЧ░ыа╣, ьЭ╕ьвЕ ы░П ыЛдые╕ ьХ╜ым╝ъ│╝ьЭШ ьГБэШ╕ьЮСьЪй ыУ▒ьЧР ьЭШэХЬ ьШБэЦеьЭА ьЮШ ьХМыадьа╕ ьЮИьЬ╝ый░ ъ╖╝ыЮШьЧРыКФ CYP2C9 ы░П VKORC1ъ│╝ ъ░ЩьЭА warfarin ыМАьВмьЩА ъ┤АыаиыРЬ ьЬаьаДьЮРыУдьЭ┤ ы░ЭэШАьа╕ эЩЬы░ЬэХШъ▓М ьЧ░ъ╡мыРШъ│а ьЮИыЛд[2].
ьаАьЮРыУдьЭА ьЛдьаЬ warfarin ьВмьЪй ьдС эХйы│СьжЭьЬ╝ыбЬ ь╢ЬэШИьЭ┤ ы░ЬьГЭэХЬ эЩШьЮРьЧРъ▓МьДЬ ь╡Ьъ╖╝ ьЖМъ░ЬыРЬ POC (point of care) ьЮеы╣Дые╝ ьВмьЪйэХШьЧм CYP2C9, VKORC1 ьЬаьаДьЮРьЭШ ь╢ЬэШИьД▒ ьб░эХйьЭД ъ░ДэО╕эХШъ▓М эЩХьЭ╕эХЬ ьжЭыбАые╝ ъ▓╜эЧШэХШьШАъ╕░ьЧР ьЭ┤ые╝ ъ┤Аыаи ым╕эЧМъ│аь░░ъ│╝ эХиъ╗Ш ы│┤ъ│аэХШыКФ ы░ФьЭ┤ыЛд.
ьжЭ ыбА
эЩШ ьЮР: ьЧмьЮР, 69ьД╕
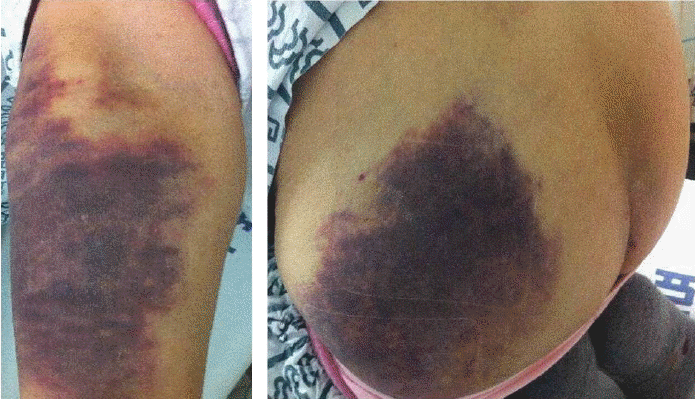
ьг╝ ьЖМ: ьЦСь╕б ьГБьзА ы░П ьЧЙыНйьЭ┤ьЭШ эГАы░ХьГБъ│╝ эШИьвЕ
эШДы│Сыае: эЩШьЮРыКФ 2005ыЕД 9ьЫФъ▓╜ы╢АэД░ atrial fibrillation, rheumatic mitral stenosis ы░П aortic regurgitationьЬ╝ыбЬ ьИЬэЩШъ╕░ыВ┤ъ│╝ ьЩ╕ыЮШьЧРьДЬ digoxin, propafenoneьЭД эПмэХиэХЬ ьХ╜ьаЬые╝ ы│╡ьЪйэХШый░ ыПЩьЬиыПЩ ьГБэГЬыбЬ ъ▓╜ъ│╝ъ┤Аь░░ ьдСьЭ┤ьЧИыЛд. 2012ыЕД 2ьЫФ 16ьЭ╝ ьЩ╕ыЮШьЧРьДЬ ыЛдьЛЬ ы░ЬьГЭэХЬ ьЛмы░йьД╕ыПЩьЭ┤ эЩХьЭ╕ыРШьЦ┤ ъ╕░ьб┤ьХ╜ьаЬ ы│╡ьЪйьЭД ьдСыЛиьЛЬэВи эЫД amiodaroneъ│╝ эХШыги 2 mgьЭШ warfarinьЭД ь▓Шы░йэХШьШАьЬ╝ый░ 2012ыЕД 3ьЫФ 15ьЭ╝ ьЩ╕ыЮШы░йым╕ ьЛЬ prothrombin time (PT) ьЧ░ьЮеьЖМъ▓мьЭД ы│┤ьШАьЬ╝ыВШ ым┤ьжЭьГБьЭ┤ьЦ┤ьДЬ PTьЮмъ▓А ьЭШыв░ эЫД warfarinьЭД эХШыги 1 mgьЬ╝ыбЬ ъ░РыЯЙэХШьЧм ь▓Шы░йэХШьШАыЛд. ьЭ┤эЛА эЫДьЭ╕ 2012ыЕД 3ьЫФ 17ьЭ╝, ыВ┤ьЫР ыЛ╣ьЭ╝ ы░ЬьГЭэХЬ ьГБъ╕░ ьг╝ьЖМыбЬ ы│╕ьЫР ьЭСъ╕ЙьД╝эД░ыбЬ ыВ┤ьЫРэХШьШАъ│а ьЩ╕ьГБэЭФьаБьЭА ьЧЖьЧИыЛд.
ъ░Аьб▒ыае: эК╣ьЭ┤ьВмэХн ьЧЖьЧИыЛд.
ъ│╝ъ▒░ыае: ьЪ░ьЪ╕ьжЭьЬ╝ыбЬ эГА ы│СьЫРьЧРьДЬ эХньЪ░ьЪ╕ьаЬые╝ ы│╡ьЪй ьдСьЭ┤ьЧИыЛд.
ьЭ┤эХЩьаБ ьЖМъ▓м: ыВ┤ьЫР ыЛ╣ьЛЬ эЩЬыаеьзХэЫДыКФ эШИьХХ 100/60 mmHg, ызеы░ХьИШ 110эЪМ/ы╢Д, эШ╕эЭбьИШ 20эЪМ/ы╢Д, ь▓┤ьШи 37.1тДГьШАыЛд. ьЛаь▓┤ ъ▓АьВмьЧРьДЬ ъ│╡ызЙьЭА ьаХьГБьЭ┤ьЧИьЬ╝ыВШ ъ▓░ызЙьЭА ь░╜ы░▒эХШьШАьЬ╝ый░ эЭЙы╢Аь▓ньзДьГБ эШ╕эЭбьЭМьЭА ьаХьГБьЭ┤ьЧИьЬ╝ыВШ ьЛмы░ХыПЩьЭА ы╢Иъ╖Ьь╣ЩэХШьШАъ│а ьаЬ1 ьЛмьЭМьЭШ ьжЭъ░АьЩА ьЛмь▓иы╢АьЧРьДЬ II-IIIыПДьЭШ ьЭ┤ьЩДъ╕░ьД▒ ьЛмьЮбьЭМьЭ┤ ь▓нь╖иыРШьЧИыЛд. ы│╡ы╢АьзДь░░ьЧРьДЬ ъ░Д ы░П ы╣ДьЮеьЭШ ьвЕыМАыКФ ьЧЖьЧИьЬ╝ый░ ыЛдые╕ ы│╡ы╢АьвЕъ┤┤ыПД ь┤ЙьзАыРШьзА ьХКьХШыЛд. ьЦСь╕б ьГБьзА ы░П ьЧЙыНйьЭ┤ьЧР ыЛды░ЬьД▒ эГАы░ХьГБьЭ┤ ъ┤Аь░░ыРШьЧИьЬ╝ый░ ъ▓╜ыПДьЭШ ьХХэЖ╡ьЭД ыПЩы░ШэХЬ эШИьвЕьЭ┤ ь┤ЙьзАыРШьЧИыЛд(Fig. 1).
ъ▓АьВмьЛд ьЖМъ▓м: ызРь┤ИэШИьХбъ▓АьВмьЧРьДЬ ы░▒эШИъ╡м 12.7 ├Ч 103/╬╝L, эШИьГЙьЖМ 6.6 g/dL, эШИьЖМэМР 168 ├Ч 103/╬╝LьШАыЛд. BUN 55 mg/dL, Cr 2.1 mg/dL, AST 47 IU/L, ALT 22 IU/L, ALP 152 IU/LьШАьЬ╝ый░ ь┤Э ы╣Мыжмыгиы╣И 0.9 mg/dL, ьзБьаС ы╣Мыжмыгиы╣И 0.4 mg/dL, CRPыКФ 0.27 mg/dLьШАыЛд. CK, CK-MB, LDH, troponin-IыКФ ъ░Бъ░Б 402 U/L, 10 U/L, 1,018 IU/L, 0.019 ng/dLьШАыЛд. PTыКФ ь╕бьаХъ░АыКеь╣ШьЭШ ьГБэХЬ ьЭ┤ьГБ(> 120 sec), aPTT (activated partial thromboplastin time)ьЭА 79.0ь┤ИыбЬ ьЧ░ьЮеыРШьЦ┤ ьЮИьЧИыЛд.
ы░йьВмьДа ьЖМъ▓м: эЭЙы╢А X-ьДа ъ▓АьВмьЧРьДЬ ьЛмьЮеы╣ДыМАъ░А ъ┤Аь░░ыРШьЧИьЬ╝ыВШ эПРы╢АьвЕ ьЖМъ▓мьЭА ьЧЖьЧИыЛд.
ьЛмьаДыПД: эСЬьдА 12ьЬаыПД ьЛмьаДыПДьГБ ы╢ДыЛ╣ 110эЪМьЭШ ы╣аые╕ ьЛмьЛды░ШьЭСьЭД ы│┤ьЭ┤ыКФ ьЛмы░йьД╕ыПЩьЭШ ьЖМъ▓мьЭД ы│┤ьШАыЛд.
ь╣ШыгМ ы░П ъ▓╜ъ│╝: ыВ┤ьЫР ьаД ызИьзАызЙьЬ╝ыбЬ ьЛЬэЦЙэХЬ ъ▓АьВмьГБьЭШ эШИьГЙьЖМьИШь╣Шъ░А 11.6 g/dLьШАьЬ╝ыВШ ыВ┤ьЫР ьЛЬ 6.6 g/dLъ╣МьзА ъ░РьЖМэХЬ ъ╕ЙьД▒ ьЛдэШИьЖМъ▓мьЭД ы│┤ьЧм ыЖНь╢ХьаБэШИъ╡м(packed red blood cell, packed RBC)ые╝ ьИШэШИэХШьШАьЬ╝ый░ ьГБьзА ьЫРьЬДы╢АьЭШ ызеы░ХьЭА ып╕ьХ╜эХШъ▓М ь┤ЙьзАыРШьЧИьЬ╝ыВШ эШИьвЕы╢АьЬДыКФ ьХХэЖ╡ъ│╝ эХиъ╗Ш эФ╝ы╢Аъ╕┤ьЮеыПДъ░А ьжЭъ░АэХШьЧм ьЮИьЦ┤ ь╢Фъ░А ь╢ЬэШИьЭ┤ ы░ЬьГЭэХа ъ▓╜ьЪ░ ъ╡мэЪНьжЭэЫДъ╡░ьЭШ ы░ЬьГЭ ъ░АыКеьД▒ьЭ┤ ьЪ░ыадыРШьЧИыЛд. ъ╡мэЪНьжЭэЫДъ╡░ьЭШ ы░ЬьГЭьЭД ып╕ьЧ░ьЧР ы░йьзАэХШыКФ ъ▓ГьЭ┤ ьдСьЪФэХа ъ▓ГьЬ╝ыбЬ эМРыЛиыРШьЧИьЬ╝ый░ ыШРэХЬ ы╣ИэШИьЧР ьЭШэХЬ ьЛмэХЬ ьаДьЛа ым┤ыаеъ░РьЬ╝ыбЬ ьЭ╕эХЬ эЭбьЭ╕ьЭШ ьЬДэЧШьЭ┤ ьЮИьЦ┤ ь╢Фъ░АьаБьЭ╕ ь╢ЬэШИьЭД ы░йьзАэХШъ╕░ ьЬДэХ┤ vitamin K ьаХызе ыВ┤ ьг╝ьЮЕъ│╝ ьЛаьДаыПЩъ▓░эШИьЮе ьИШэШИьЭД эЖ╡эХ┤ ьЛаьЖНэЮИ PTые╝ ъ╡РьаХэХШьШАыЛд. эШИы│АьЭ┤ыВШ эЭСьГЙы│АьЭА ьЧЖьЧИьЬ╝ыВШ ьЬДьЮеъ┤Аь╢ЬэШИьЧР ьЭШэХЬ эШИьГЙьЖМьИШь╣Ш ъ░РьЖМые╝ ы░░ьаЬэХШъ╕░ ьЬДэХ┤ ьЬДыВ┤ьЛЬъ▓╜ьЭД ьЛЬэЦЙэХШьШАьЬ╝ый░ ъ▓╜ыПДьЭШ ьЧныеШьД▒ ьЛЭыПДьЧ╝ ы░П ьЬДь╢Х ьЬДьЧ╝ ьЩ╕ьЧР эЩЬыПЩьД▒ ь╢ЬэШИьЭШ ьжЭъ▒░ыКФ ьЧЖьЧИъ│а ъ╖╕ ьЩ╕ ь╢ЬэШИьЭШ ьЫРьЭ╕ьЬ╝ыбЬ эМРыЛиыРШыКФ ьЮДьГБьаБ ьЖМъ▓мьЭА ьЧЖьЧИыЛд. ыВ┤ьЫР ьЭ┤эЛА эЫД эШИьГЙьЖМ, PT, aPTTыКФ ъ░Бъ░Б 10.3 g/dL, 13.4ь┤И, 21.5ь┤ИыбЬ ьаХьГБэЩФыРШьЧИыЛд.
PT ьЧ░ьЮеьЧР ьЭШэХЬ эФ╝эХШь╢ЬэШИ ы░П ъ╖╕ьЧР ыФ░ые╕ ы╣ИэШИыбЬ эМРыЛиэХШъ│а ъ│╝ыПДэХЬ PT ьЧ░ьЮеьЭШ ьЫРьЭ╕ьЧР ыМАэХЬ ьб░ьВмые╝ ьЛЬьЮСэХШьШАыЛд. Warfarinъ│╝ ыЛдые╕ ьХ╜ым╝ ыШРыКФ ьЭМьЛЭъ│╝ьЭШ ьГБэШ╕ьЮСьЪйьЧР ьдСьаРьЭД ыСРъ│а ьб░ьВмые╝ ьЛЬэЦЙэХШьШАьЬ╝ый░ ъ╖╕ ъ▓░ъ│╝ ьЭМьЛЭъ│╝ьЭШ эК╣ы│ДэХЬ ьЧ░ъ┤АьД▒ьЭА ы░Ьъ▓мыРШьзА ьХКьХШьЬ╝ыВШ, эЩШьЮРъ░А 2011ыЕД 3ьЫФы╢АэД░ ьЪ░ьЪ╕ьжЭъ│╝ ызРь┤ИьЛаъ▓╜ы│СьжЭьЬ╝ыбЬ эГАы│СьЫРьЧРьДЬ ыкЗ ъ░АьзАьЭШ эХньЪ░ьЪ╕ьаЬые╝ эПмэХиэХЬ ьХ╜ьаЬьЭ╕ flunitrazepam (ыгиыВШэМЬтУЗ) 1 mg, bromazepam (ы╕МыбЬызИьаЬэМЬтУЗ) 3 mg, trazodone hydrochloride (эК╕ыжмэЛ░ь╜ФтУЗ) 25 mg, pyridoxine(эФ╝ыжмыПЕьЛатУЗ) 50 mgьЭД ь▓Шы░йы░ЫьХД ы│╡ьЪй ьдСьЮДьЭ┤ ы░ЭэШАьбМыЛд. ьаАьЮРыУдьЭА ьХ╜ым╝ ъ░ДьЭШ ьГБэШ╕ьЮСьЪйьЧР ьЭШэХЬ PT ьЧ░ьЮеьЭШ ъ░АыКеьД▒ ьЩ╕ьЧР warfarin ьЪйыЯЙ ьЪФъ╡мыЯЙъ│╝ ъ┤АыаиыРЬ ьЬаьаДьЮР ы│АьЭ┤ьЭШ ъ░АыКеьД▒ьЭД ъ│аыадэХШьЧм ь╡Ьъ╖╝ ьЮДьГБьЧР ыПДьЮЕыРЬ POC ьЮеы╣ДьЭ╕ VerigeneтУЗ system(Nanosphere, Northbrook, IL)ьЭД ьЭ┤ьЪйэХШьЧм CYP2C9 ьЬаьаДьЮРьЩА VKORC1 ьЬаьаДьЮРьЭШ ы│АьЭ┤ьЧР ыМАэХЬ ъ▓АьВмые╝ ьЛЬэЦЙэХШьШАьЬ╝ый░ эЩШьЮРьЭШ ьЬаьаДьЮРьЧРьДЬ CYP2C9 *1/*3 ьЭ┤эШХьаСэХйь▓┤(heterozygote)ьЩА VKORC1 A/A ыЛиьЭ╝ ьЧ╝ъ╕░ ыЛдэШХьД▒(single nucleotide polymorphism)ьЭ┤ ьб┤ьЮмэХиьЭД эЩХьЭ╕эХШьШАыЛд.
ьЭ┤эЫД эЩШьЮРьЭШ ьЦСь╕б ьГБьзА ы░П ьЧЙыНйьЭ┤ьЭШ эГАы░ХьГБъ│╝ эШИьвЕьЭА эШ╕ьаДыРШьЧИъ│а ь╢Фъ░АьаБьЭ╕ ь╢ЬэШИ ьЖМъ▓мыПД ъ┤Аь░░ыРШьзА ьХКьХД WarfarinьЭД эХШыги 0.5 mgьЬ╝ыбЬ ъ░РыЯЙэХШьЧм ыЛдьЛЬ эИмьЧмые╝ ьЛЬьЮСэХШьШАьЬ╝ый░ ьЩ╕ыЮШьЧРьДЬ ъ▓╜ъ│╝ъ┤Аь░░эХШый░ ьЪйыЯЙьЭД ьб░ьаИэХШъ╕░ыбЬ эХШъ│а эЗ┤ьЫРэХШьШАыЛд.
ъ│а ь░░
WarfarinьЭА ы╣ДэГАып╝ KьЭШ ъ╕╕эХньаЬыбЬ ьЛмы░йьД╕ыПЩ ыШРыКФ ьЭ╕ъ│╡эМРызЙьЭД ъ░АьзД эЩШьЮРьЭШ ьаДьЛаьГЙьаДьжЭ ьШИы░йьЧР ьг╝ыбЬ ьВмьЪйыРШъ│а ьЮИыЛд. ьаБьаИэХЬ эХньЭСъ│а ьИШьдАьЭД ьЬаьзАэХШыКФ ыН░ эХДьЪФэХЬ warfarinьЭШ ьЪФъ╡мыЯЙьЭА ъ░Ьъ░ЬьЭ╕ ъ░ДьЭШ ь░иьЭ┤ъ░А эБмъ╕░ ыХМым╕ьЧР ы╣ДэГАып╝ KьЧР ьЭШьб┤эХШыКФ ьЭСъ│аьЭ╕ьЮРьЩА ъ┤АыаиыРЬ PT ь╕бьаХьЭД эЖ╡эХЬ ьХ╜ым╝ыЖНыПДьЭШ ъ░РьЛЬъ░А эХДьЪФэХШыЛд.
ьаБьаИэХЬ PT ы▓ФьЬДьЭШ ьб░ьаИьЧР ьЮИьЦ┤ ьзИьаБьЭ╕ ь░иьЭ┤ыКФ ьЮИьЭД ьИШ ьЮИъ▓аьзАызМ эХЬ ьЧ░ъ╡мьЧР ыФ░ые┤ый┤ warfarin ь╣ШыгМ ьдСьЧР ы░ЬьГЭэХЬ ьг╝ьЪФ ь╢ЬэШИьЭШ ы░ЬьГЭыеаьЭА 3.36%ьШАыЛд[3]. ь╢ЬэШИьЭШ ьЬДэЧШыПДыКФ эХньЭСъ│аьЭШ ьаХыПДьЩА эБ░ ъ┤АыаиьЭ┤ ьЮИыКФыН░ ьЭ┤ыКФ ьЭМьЛЭ, ьЧ░ыа╣, ьЛаьЮе, ь▓┤ьдС, ьЭ╕ьвЕ, эЭбьЧ░ ьЬаым┤ ы░П ы│╡ьЪйэХШыКФ ыЛдые╕ ьХ╜ым╝ъ│╝ьЭШ ьГБэШ╕ьЮСьЪйьЧР ьЭШэХ┤ ьШБэЦеьЭД ы░ЫьЭД ьИШ ьЮИыЛд. ы│╕ ьжЭыбАьЭШ ъ▓╜ьЪ░ amiodarone, benzodiazepineъ│╝ trazodone ъ│ДьЧ┤ьЭШ ьХ╜ым╝ьЭД warfarinъ│╝ эХиъ╗Ш ы│╡ьЪй ьдСьЭ┤ьЧИыЛд. ыи╝ьаА amiodaroneьЭА warfarinьЭШ ыМАьВмьЩА ъ┤АыаиыРЬ CYP2C9ые╝ эПмэХиэХШыКФ ыкЗ ъ░АьзАьЭШ cytochrome P450 ыМАьВмъ▓╜ыбЬые╝ ьЦ╡ьаЬэХШыКФ ъ▓ГьЬ╝ыбЬ ьХМыадьа╕ ьЮИьЬ╝ый░ ьЭ┤ыбЬ ьЭ╕эХ┤ ъ░СьЮСьКдыЯ╜ъ│а эШДьаАэХЬ PT ьЧ░ьЮеьЭ┤ ыВШэГАыВа ьИШ ьЮИыЛд. ы╣Дъ╡РьаБ ьаБьЭА ьЪйыЯЙьЭШ warfarinьЭД ьВмьЪйэЦИьЭМьЧРыПД ы╢Иъ╡мэХШъ│а PT ьЧ░ьЮеъ│╝ ь╢ЬэШИьЭ┤ ьЮИьЧИыНШ ъ▓ГьЭА amiodaroneъ│╝ьЭШ ьХ╜ым╝ ьГБэШ╕ьЮСьЪйьЭ┤ ьЭ╝ьаХы╢Аы╢Д ьЫРьЭ╕ьЬ╝ыбЬ ьЮСьЪйэЦИыНШ ъ▓ГьЬ╝ыбЬ эМРыЛиыРЬыЛд. эХШьзАызМ Kerin ыУ▒[4]ьЭШ ы│┤ъ│аьЧР ыФ░ые┤ый┤ amiodaroneъ│╝ warfarinьЭШ ыПЩьЛЬ ьВмьЪйьЧР ьЭШэХЬ PT ьЧ░ьЮеьЭА эПЙъ╖а 44% (22-108%)ьШАьЬ╝ый░ ы│╕ ьжЭыбАьЭШ ъ▓╜ьЪ░ ыЛиьзА amiodaroneъ│╝ьЭШ ьГБэШ╕ьЮСьЪйызМьЬ╝ыбЬ PTъ░А ьЧ░ьЮеыРШьЧИыЛдъ│а ы│┤ъ╕░ьЧРыКФ ъ╖╕ ьаХыПДъ░А ьЛмэХЬ ъ▓ГьЬ╝ыбЬ эМРыЛиэХШьШАыЛд. Warfarinъ│╝ ъ░ЩьЭА ы╣ДэГАып╝ K ъ╕╕эХньаЬьЭ┤ый░ coumarinьЭШ ьЬаыПДь▓┤ьЭ╕ acenocoumarolые╝ ьВмьЪйэХШыКФ эЩШьЮРыУдьЧРъ▓МьДЬ ы░ЬьГЭэХЬ ь╢ЬэШИьЬДэЧШыПДьЧР ьб░ьВмэХЬ ьЧ░ъ╡мьЧР ьЭШэХШый┤ ьЬаьаДьЮР ы│АьЭ┤ъ░А ыПЩы░ШыРЬ эЩШьЮРыУдьЭ┤ amiodaroneьЭД ы│╡ьЪйэХШыКФ ъ▓╜ьЪ░, ьЬаьаДьЮР ы│АьЭ┤ызМ ьЮИъ▒░ыВШ ьЬаьаДьЮР ы│АьЭ┤ ьЧЖьЭ┤ amiodaroneызМ ы│╡ьЪйэХШыКФ эЩШьЮРъ╡░ьЧР ы╣ДэХ┤ ь╢ЬэШИьЬДэЧШыПДъ░А ыНФ ыЖТьЭА ъ▓ГьЬ╝ыбЬ ы│┤ъ│аэХШъ│а ьЮИыЛд. ыШРэХЬ ьЬаьаДьЮРы│АьЭ┤ъ░А ьЮИыКФ ъ╡░ьЭ┤ ьЬаьаДьЮР ы│АьЭ┤ ьЧЖьЭ┤ amiodaroneызМ ы│╡ьЪйэХЬ ъ╡░ы│┤ыЛд ь╢ЬэШИьЬДэЧШыПДъ░А ыНФ эБ░ ъ▓ГьЬ╝ыбЬ ыВШэГАыВШ ьЮИыЛд. ъ╖╕ ьЩ╕ эЩШьЮРъ░А ы│╡ьЪйэХШыНШ ьХ╜ым╝ ьдС benzodiazepineьЭА warfarinъ│╝ьЭШ ьХ╜ым╝ ьГБэШ╕ьЮСьЪйьЭ┤ ыУЬым╝ый░ trazodoneьЭА ыПДыжмьЦ┤ PTые╝ ыЛиь╢ХьЛЬэВдыКФ ъ▓ГьЬ╝ыбЬ ьХМыадьа╕ ьЮИыЛд[5].
эЩШьЮРьЭШ ьЮЕьЫР ьЛЬ Cr ьИШь╣Шъ░А 2.1 mg/dLыбЬ ьдСыУ▒ыПДьЭШ ьЛаъ╕░ыКе ы╢АьаДьЭД ы│┤ьШАьЬ╝ыВШ ьЭ┤ьаД ъ▓АьВмьЛд ьЖМъ▓мьЧРьДЬ ьаХьГБ Cr ьИШь╣Шые╝ ы│┤ьШАъ│а ьЮЕьЫР ьЛЬ эШИьГЙьЖМ ьИШь╣Шъ░А 6.6 g/dLыбЬ ыВоьХШыЛдыКФ ьаР ы░П эЗ┤ьЫРьЛЬ эЩШьЮРьЭШ ьГБэГЬъ░А эШ╕ьаДыРШый░ Cr ьИШь╣Ш ьЧньЛЬ 1.4 mg/dLыбЬ ьаХьГБэЩФыРЬ ьаР ыУ▒ьЭД ъ│аыадэХ┤ ы┤дьЭД ыХМ ьЛдэШИьЧР ыФ░ые╕ эШИъ┤А ыВ┤ ьЪйьаБьЭШ ъ░РьЖМ ы░П ъ╖╕ьЧР ыФ░ые╕ ъ╕ЙьД▒ьЛаы╢АьаДьЬ╝ыбЬ эМРыЛиыРШьЧИыЛд. WarfarinьЭА ъ░ДьЭШ cytochrome P450ьЭД эЖ╡эХ┤ ыМАы╢Аы╢Д ыМАьВмыРШьЦ┤ ьЛаъ╕░ыКеьЭШ ьШБэЦеьЭД эБмъ▓М ы░ЫьзА ьХКыКФ ъ▓ГьЬ╝ыбЬ ьХМыадьа╕ ьЮИьЬ╝ыВШ ьдСыУ▒ыПД ыШРыКФ ьдСьжЭьЭШ ьЛаы╢АьаДьЭ┤ ьЮИыКФ ъ▓╜ьЪ░ cytochrome P450ьЭШ эХШэЦеьб░ьаИьЭ┤ ьЮИьЭД ьИШ ьЮИьЬ╝ый░ ьЭ┤ыЯмэХЬ ьаРьЭ┤ warfarin ьЪФъ╡мыЯЙьЭШ ъ░РьЖМьЩА ъ┤АыаиьЭ┤ ьЮИыКФ ъ▓ГьЬ╝ыбЬ ьХМыадьа╕ ьЮИыЛд[6]. эХШьзАызМ эХЬ ьЧ░ъ╡мьЧР ыФ░ые┤ый┤ warfarin ьВмьЪй эЩШьЮРьЧРъ▓МьДЬ ьЛаъ╕░ыКе ьаАэХШъ░А PT ьЧ░ьЮеьЭШ ьЫРьЭ╕ьЭ┤ ыРа ьИШ ьЮИьзАызМ, ьЬаьаДьЮР ы│АьЭ┤ъ░А PT ьЧ░ьЮеьЧР ып╕ь╣ШыКФ ьШБэЦеьЭ┤ ыНФ эБ░ ъ▓ГьЬ╝ыбЬ ы│┤ъ│аэХШьЧм ы│╕ ьжЭыбАьЭШ ъ▓╜ьЪ░ьЧРьДЬыПД ьЛаъ╕░ыКеьаАэХШызМьЬ╝ыбЬ PTъ░А ьЧ░ьЮеыРШьЧИьЭД ъ░АыКеьД▒ьЭА ыВоьЭА ъ▓ГьЬ╝ыбЬ эМРыЛиэЦИыЛд[7].
ьаАьЮРыУдьЭА ьХЮьДЬ ьВ┤эО┤ы│╕ ьЭМьЛЭ, ьХ╜ым╝ъ│╝ ьЛаъ╕░ыКе ьаАэХШызМьЬ╝ыбЬыКФ ьДдыкЕыРШьзА ьХКыКФ PT ьЧ░ьЮеьЧР ьШБэЦеьЭД ыБ╝ь│дыНШ ыЛдые╕ ьЫРьЭ╕ьЭ┤ ьЮИьЭД ъ▓ГьЬ╝ыбЬ эМРыЛиэХШьШАьЬ╝ый░ эЩШьЮРьЧРъ▓М ьЬаьаДьЮР ы│АьЭ┤ъ░А ьб┤ьЮмэХа ъ░АыКеьД▒ьЭД ъ│аыадэХШьШАыЛд. 1990ыЕДыМАьЧР ьЬаьаДьЮР ъ▓АьВмые╝ эЖ╡эХ┤ warfarinьЭШ ыСР ъ░АьзА ъ┤СэХЩьЭ┤ьД▒ь▓┤ьдС ьД╕ ы░░-ыЛдьДп ы░░ ъ░ХэХЬ ьЧнъ░Аые╝ ъ░АьзД(S)-ьЭ┤ьД▒ь▓┤ьЭШ ыМАьВмьаЬъ▒░ьЧР ъ┤АьЧмэХШыКФ CYP2C9 ьЬаьаДьЮРьЭШ ы│АьЭ┤ъ░А warfarin ьЪФъ╡мыЯЙьЧР ы│АэЩФые╝ ьдД ьИШ ьЮИыЛдыКФ ъ▓░ъ│╝ъ░А ы│┤ъ│аыРШьЧИьЬ╝ый░ ьИШыЕД ыТд warfarinьЭШ эСЬьаБьЭ╕ vitamin K epoxide reductaseьЩА ъ┤АыаиыРШьЦ┤ warfarin ьЪФъ╡мыЯЙьЧР ы│АэЩФые╝ ьдД ьИШ ьЮИыКФ ыШР ыЛдые╕ ьЬаьаДьЮРьЭ╕ VKORC1 ьЬаьаДьЮР ы│АьЭ┤ьЧР ъ┤АэХЬ ьЧ░ъ╡мыПД ы░ЬэСЬыРШьЧИыЛд[2]. ьаАьЮРыУдьЭА эЩШьЮРьЧРъ▓М ьЭ┤ ъ░ЩьЭА ьЬаьаДьЮРьЭШ ы│АьЭ┤ъ░А ьб┤ьЮмэХа ъ░АыКеьД▒ьЭД ъ│аыадэХШьЧм ъ▓АьВмые╝ ьЛЬэЦЙэХШьШАьЬ╝ый░ ь╡Ьъ╖╝ьЧР ъ╡ныВ┤ьЧР ыПДьЮЕыРЬ POC ьЮеы╣ДьЭ╕ VerigeneтУЗ systemьЭД ьЭ┤ьЪйэХЬ ьЬаьаДьЮР ъ▓АьВмъ▓░ъ│╝ CYP2C9*1/*3 ьЭ┤эШХьаСэХйь▓┤ьЩА VKORC1 A/A ыЛиьЭ╝ ьЧ╝ъ╕░ ыЛдэШХьД▒ ьЦСьД▒ьЬ╝ыбЬ ыВШэГАыВмыЛд. CYP2C9ьЩА VKORC1 ьЬаьаДьЮР ы│АьЭ┤ыКФ ъ│╝ыПДэХЬ эХньЭСъ│аьЭШ ьЬДэЧШыПДьЩА эБ░ ъ┤АыаиьД▒ьЭД ъ░АьзАъ│а ьЮИьЬ╝ый░ ы│╕ ьжЭыбАьЩА ъ░ЩьЭА VKORC1 A/A ьЬаьаДьЮР ы│АьЭ┤ьЭШ ъ▓╜ьЪ░ ьХДьЛЬьХДьЭ╕ьвЕ ьдС ьХ╜ 85-89%ьЭШ ы╢ДэПмьЬиьЭД ъ░АьзАъ│а ьЮИьзАызМ CYP2C9 *1/*3ьЭШ ъ▓╜ьЪ░ ьХ╜ 8-9%ыбЬ ыВоьЭА ы╢ДэПмьЬиьЭД ы│┤ьЭ┤ый░ эХЬъ╡ньЭ╕ьЭД ыМАьГБьЬ╝ыбЬ ьЛЬэЦЙэХЬ эХЬ ьЧ░ъ╡мьЧРьДЬ ы│╕ ьжЭыбАьЩА ъ░ЩьЭА ьЧ╝ъ╕░ ьб░эХйьЭШ ы╣ИыПДыКФ ьХ╜ 13%ыбЬ ы│┤ъ│аэХШъ│а ьЮИыЛд[8]. ъ░Бъ░БьЭШ ьЬаьаДьЮР ы│АьЭ┤ьЭШ ьб░эХйьЧР ыФ░ыЭ╝ warfarin ьЪФъ╡мыЯЙьЭ┤ ыЛдые┤ыЛдыКФ ъ▓ГьЭА ь╡Ьъ╖╝ьЭШ эЩЬы░ЬэХЬ ьЧ░ъ╡мьЧР ьЭШэХ┤ ьЮШ ьХМыадьа╕ ьЮИыЛд. FDA (Food and Drug Administration, ып╕ъ╡ньЛЭэТИьЭШьХ╜ъ╡н)ьЧРьДЬыКФ 2010ыЕД ьХ╜ым╝ ыЭ╝ы▓иьЧР ьЬаьаДьЮР ы│АьЭ┤ьЭШ ьб░эХйьЧР ыФ░ые╕ warfarin эИмьЧмьЪйыЯЙьЭД ъ╢Мъ│аэХШьШАьЬ╝ый░ ьЦ┤ыЦаэХЬ эЩШьЮРыУдьЭД ыМАьГБьЬ╝ыбЬ ьЭ┤ыЯмэХЬ ьХ╜ым╝ ьЬаьаДэХЩ ъ▓АьВмые╝ ьЛЬэЦЙэХа ъ▓ГьЭ╕ъ░АьЧР ыМАэХ┤ьДЬыКФ ыЕ╝ыЮАьЭ┤ ызОьЭА ьГБэГЬьЭ┤ыВШ ыкЗыкЗьЭШ ьаДым╕ъ░АыУдьЭА ьЭ┤ьаДьЧР warfarin ь╣ШыгМые╝ ьЛЬэЦЙэХЬ ьаБьЭ┤ ьЧЖьЦ┤ ьаБьаИэХЬ warfarin ьЪйыЯЙьЭ┤ эЩХыж╜ыРШьЦ┤ьЮИьзА ьХКьЭА эЩШьЮРыУд, INR ыкйэСЬъ░А 2-3ьЭ╕ эЩШьЮРыУд, ь╢ЬэШИьЭШ ьЬДэЧШьД▒ьЭ┤ ыЖТьЭА эЩШьЮРыУдьЧРъ▓М ъ▓АьВмые╝ ъ│аыадэХ┤ы│╝ ъ▓ГьЭД ъ╢МьЬаэХШъ│а ьЮИыЛд[9]. ьЬаьаДьЮР ьаХы│┤ ьЧЖьЭ┤ warfarin ьЪйыЯЙьЭД ьб░ьаИэХа ьЛЬ эПЙъ╖аь┤Иъ╕░ ьЪйыЯЙьЭА ыМАъ░Ь 3-4 mgьЭ┤ьзАызМ ьЭ┤ эЩШьЮРьЭШ ъ▓╜ьЪ░ FDA ъ╢Мъ│а warfarin ьЪйыЯЙьЭА 0.5-2 mgьЭ┤ьЧИъ│а ьЛдьаЬыбЬ ьЭ┤ьЭШ ь╡ЬыМА ьЪйыЯЙьЭ╕ 2 mgьЭД 3ьг╝ъ░Д ьВмьЪйэХШьШАъ│а ьЧмъ╕░ьЧР amiodaroneьЭШ ьХ╜ым╝ ьГБэШ╕ьЮСьЪйьЧР ьЭШэХ┤ ь╢ЬэШИьЭ┤ ы░ЬьГЭэХШьШАыЛд. ьаАьЮРыУдьЭА ъ╢МьЬа ьЪйыЯЙ, эЩШьЮРьЭШ ыВШьЭ┤ ы░П amiodaroneьЭД ыПЩьЛЬ ы│╡ьЪйэХШыКФ ьаРьЭД ъ│аыадэХ┤ ьЮЕьЫР эЫД ьЬаьаДьЮР ьаХы│┤ые╝ ьвЕэХйэХ┤ 0.5 mg ьаХыПДые╝ ьаБьаИэХЬ ьЪйыЯЙьЬ╝ыбЬ ь╢ФьаХэХ┤ эЩШьЮРьЭШ warfarin ьЪйыЯЙьЭД ьб░ьаИэХЬ эЫД эЗ┤ьЫРьЛЬэВм ьИШ ьЮИьЧИыЛд.
ьЛмы░йьД╕ыПЩьЭШ ь╣ШыгМьЧР ьЮИьЦ┤ amiodaroneъ│╝ warfarinьЭА ыПЩьЛЬ ьВмьЪйыРШыКФ ъ▓╜ьЪ░ъ░А ызОьЬ╝ый░ ьХ╜ым╝ ъ░Д ьГБэШ╕ьЮСьЪйьЧР ьЭШэХ┤ ы│╕ ьжЭыбАьЩА ъ░ЩьЭА PT ьЧ░ьЮе ы░П ъ╖╕ьЧР ыФ░ые╕ эХйы│СьжЭьЭШ ы░ЬьГЭьЭ┤ ым╕ьаЬъ░А ыРШъ│а ьЮИыЛд. ьЭ┤ыЯ░ ь╕бый┤ьЧРьДЬ ы┤дьЭД ыХМ warfarinъ│╝ьЭШ ьХ╜ым╝ ьГБэШ╕ьЮСьЪйьЭ┤ ы╣Дъ╡РьаБ ьаБьЭА ъ▓ГьЬ╝ыбЬ ьХМыадьа╕ ьЮИыКФ ьГИыбЬьЪ┤ ы╢АьаХызеь╣ШыгМ ьХ╜ьаЬьЭ╕ dronedaroneьЭШ эИмьЧмые╝ ъ│аыадэХ┤ ы│╝ ьИШ ьЮИыЛд. эХШьзАызМ dronedaroneьЭА ыПЩьЬиыПЩ ьЬаьзАьЭШ эЪиыКе ый┤ьЧРьДЬ ьЭШым╕ьаРьЭ┤ ьЮИьЬ╝ый░ ьХИьаХьаБьЭ╕ warfarin ьЪйыЯЙьЭД ьЬаьзАэХШыНШ эЩШьЮРьЧРьДЬ dronedarone ьВмьЪй эЫД эШДьаАэХЬ PT ьЧ░ьЮеьЭ┤ыВШ ь╢ЬэШИ эХйы│СьжЭьЭ┤ ы░ЬьГЭэХЬ ы│┤ъ│аъ░А ьЮИыЛд[10]. PT ьЧ░ьЮе ы░П ь╢ЬэШИ эХйы│СьжЭьЭШ ы░ЬьГЭьЭА dronedaroneьЭ┤ warfarinьЭШ ьг╝ьЪФ ыМАьВм ъ▓╜ыбЬьЭ╕ CYP2C9ые╝ ьЦ╡ьаЬэХШьзАыКФ ьХКьзАызМ ыЛдые╕ ъ▓╜ыбЬьЭ╕ CYP3Aые╝ ьЦ╡ьаЬэХиьЬ╝ыбЬ ьЭ╕эХ┤ ы░ЬьГЭэЦИьЭД ъ░АыКеьД▒ьЭ┤ ыЖТьЭА ъ▓ГьЬ╝ыбЬ ь╢Фь╕быРШый░ ьХДьзБьЭА amiodaroneъ│╝ ы╣Дъ╡РэХШьЧм ьЮДьГБьЧРьДЬьЭШ ъ▓╜эЧШьЭ┤ ы╢Аьб▒эХШый░ эЦеэЫД ь╢Фъ░АьаБьЭ╕ ьЮДьГБ ы│┤ъ│аъ░А эХДьЪФэХа ъ▓ГьЬ╝ыбЬ эМРыЛиыРЬыЛд.
ь╡Ьъ╖╝ ьГИыбЬьЪ┤ эХньЭСъ│аьаЬыУдьЭШ ь╢ЬэШДьЬ╝ыбЬ warfarinьЭ┤ эЦеэЫД ьГЙьаД ьжЭьЭ┤ыВШ ыЗМьб╕ьдСьЭШ ьШИы░йъ│╝ ь╣ШыгМьЧР ьЮИьЦ┤ ъ╖╕ ьЮЕьзАъ░А ьЦ┤ыЦ╗ъ▓М ы░ФыАФьзАыКФ ьХМ ьИШ ьЧЖьЬ╝ыВШ эШДьЮмъ╣МьзА ъ░АьЮе ызОьЭ┤ ьВмьЪйыРШъ│а ызОьЭА ьЮДьГБъ▓╜эЧШьЭ┤ ь╢ХьаБыРЬ ьХ╜ым╝ьЮДьЭА ьЭШьЛмэХа ы░Ф ьЧЖыЛд. ы╣ДыбЭ ы╣ДьЪйыМАы╣Д эЪиъ│╝ьЩА ьЛдьаЬ ьЮДьГБъ▓░ъ│╝ьЭШ эШ╕ьаДьЭ┤ ьжЭыкЕыРШьзА ьХКьХД ъ░АьЭ┤ыУЬыЭ╝ьЭ╕ьЧРьДЬ ъ╢Мъ│аыРШьзАыКФ ьХКъ│а ьЮИьзАызМ POC ьЮеы╣ДьЭШ ыУ▒ьЮеъ│╝ ъ░ЩьЭА ъ▓АьВмы░йы▓ХьЭШ ы░ЬьаДьЭД эЖ╡эХ┤ ъ│╝ъ▒░ьЩА ы╣Дъ╡РэХШьЧм ъ░ДэО╕эХШъ│а ьаБьЭА ы╣ДьЪйьЭ┤ ыУдый░ ы╣аые╕ ъ▓░ъ│╝ые╝ ьЦ╗ьЭД ьИШ ьЮИъ▓М ыРШьЧИыЛд. эШДьЮм warfarinьЭШ ьХ╜ым╝ьЬаьаДэХЩъ▓АьВмьЭШ ьЬаьЪйьД▒ьЧР ыМАэХ┤ьДЬыКФ ьХДьзБ ъ▓░ыбаыВ┤ыжмъ╕░ эЮШыУдьзАызМ ызМьД▒ьаБьЬ╝ыбЬ ьЮШ ьб░ьаИыРШыКФ эЩШьЮРьЧРьДЬыКФ ыПДьЫАьЭ┤ ыРШьзА ьХКьЬ╝ыВШ ьГИыбЬьЭ┤ эХньЭСъ│аьаЬ ьВмьЪйьЭ┤ эХДьЪФэХЬ ъ▓╜ьЪ░ьЧР ъ░АьЮе ыПДьЫАьЭ┤ ыРШыКФ ъ▓ГьЬ╝ыбЬ ъ░Дьг╝ыРШъ│а ьЮИыЛд[1]. ъ╖╝ыЮШ ьЬаьаДьЮР ъ▓АьВмы▓ХьЭ┤ ъ░ДэО╕эХШъ│а ы╣аые╕ ъ▓░ъ│╝ые╝ ьЦ╗ъ▓М ыРиъ│╝ ыПЩьЛЬьЧР ьЧмыЯм ьЮДьГБьЧ░ъ╡мъ░А ьзДэЦЙ ыШРыКФ ы░ЬэСЬые╝ ьХЮыСРъ│а ьЮИыКФ ьГБэЩйьЭ┤ый░ ьЭ┤эЫД ьзАьЖНьаБьЬ╝ыбЬ ьЬаьаДьЮР ъ▓АьВмые╝ ьЛЬэЦЙэХа ъ▓ГьЭ╕ъ░АьЧР ыМАэХ┤ьДЬыКФ ьЭ┤ыЯмэХЬ ьЧ░ъ╡мыУдьЭШ ъ▓░ъ│╝ые╝ ьзАь╝Ьы│╝ эХДьЪФъ░А ьЮИыЛдъ│а ьГЭъ░БэХЬыЛд[7].
ьаАьЮРыУдьЭА warfarinьЭД ы│╡ьЪйэХШыНШ ьдС ъ│╝ыПДэХЬ PT ьЧ░ьЮеьЬ╝ыбЬ эФ╝ы╢А ы░С ь╢ЬэШИьЭ┤ ы░ЬьГЭэХЬ эЩШьЮРьЧРъ▓МьДЬ CYP2C9ьЩА VKORC1 ьЬаьаДьЮРьЭШ ыПЩьЛЬы│АьЭ┤ые╝ POC ьЮеы╣Дые╝ эЖ╡эХ┤ ъ░ДэО╕эХШъ│а ы╣аые┤ъ▓М ьзДыЛи эЫД ъ╖╕ ъ▓░ъ│╝ые╝ ы░ФэГХьЬ╝ыбЬ ьЬаьаДьЮРэШХьЧР ыФ░ые╕ ъ╢Мъ│аьЪйыЯЙьЧР ыФ░ыЭ╝ ьаБьаХыЯЙьЭШ warfarinьЭД ь▓Шы░йэХШьШАыЛд. ьЭ┤ьЩА ъ░ЩьЭА ьЬаьаДьЮРьЭШ ы│АьЭ┤ъ░А warfarin ьЪФъ╡мыЯЙьЧР ьШБэЦеьЭД ьдД ьИШ ьЮИыЛдыКФ ьВмьЛдьЭА ьЮШ ьХМыадьа╕ ьЮИьЬ╝ыВШ ьЛдьаЬ ьЮДьГБьЧРьДЬ ьЭ┤ыЯ░ ьаРьЭД ъ░Дъ│╝эХШыКФ ъ▓╜ьЪ░ъ░А ызОьЬ╝ый░ ьЭ┤ыКФ ъ│╝эХньЭСъ│аьЩА ь╢ЬэШИ эХйы│СьжЭьЭШ ьЫРьЭ╕ьЭ┤ ыРа ьИШ ьЮИыЛд. ьЭ┤ыЯмэХЬ ьжЭыбАъ░А ъ╡ныВ┤ьЧР ы│┤ъ│аыРЬ ы░Ф ьЧЖъ╕░ьЧР ъ┤Аыаи ым╕эЧМъ│аь░░ъ│╝ эХиъ╗Ш ы│┤ъ│аэХШый░ ъ│╝ыПДэХЬ эХньЭСъ│аые╝ ьШИы░йэХШъ╕░ ьЬДэХЬ ьХ╜ыжмьЬаьаДэХЩьаБ ъ▓АьВмьЭШ ьдСьЪФьД▒ьЭД ъ░Хьб░эХШыКФ ы░ФьЭ┤ыЛд.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






