지역사회에서 획득된 Acinetobacter baumannii에 의한 감염성 심내막염 1예
A Case of Infective Endocarditis Caused by Community-Acquired Acinetobacter baumannii
Article information
Abstract
기저 질환이 없는 젊은 여성이 급성 뇌경색이 발생하여 내원하였으며 A. baumannii 균혈증이 확인되었다. 경흉부 심초음파에서 우식증이 관찰되어 심내막염 진단과 함께 cefoperazon/sulbactam을 총 5주 동안 사용한 결과 추가적인 합병증이 발생하지 않고 심내막염이 완치되었다. 지역사회 획득 A. baumannii에 의하여 발생한 감염성 심내막염의 국내 첫 증례를 경험하였기에 문헌고찰과 함께 보고하는 바이다.
Trans Abstract
Acinetobacter baumannii has become an important pathogen that causes healthcare-associated infections, including pneumonia, bacteremia, and urinary tract infection. Only sporadic cases of infective endocarditis (IE) have been reported worldwide, and in particular, community-acquired IE caused by A. baumannii is very rare. To our knowledge, no case has ever been reported in Korea. We report a 30-year-old woman who recovered from native-valve community-acquired IE caused by A. baumannii. She did not have any underlying diseases and presented with left-sided weakness, dysarthria, and fever. On investigation of acute cerebral infarction, a vegetation on her anterior mitral leaflet was found in echocardiography, and A. baumannii was cultured from the blood. In this case, A. baumannii showed intermediate resistance to cefotaxime and was sensitive to all other antibiotics. She underwent antibiotic therapy with cefoperazone/sulbactam for 5 weeks, without surgery. Consequently, the vegetation was absent in follow-up echocardiography, and no complications related to IE developed. (Korean J Med 2013;84:313-317)
서 론
Acinetobacter banumannii는 그람 음성의 호기성 균주이며, 흙, 물, 음식 혹은 수초와 같은 환경에 널리 분포한다[1]. 사람의 피부, 침, 대변, 질 분비물에서도 동정되며, 의료 환경에서 흔하게 존재하여 인공호흡기 관련 폐렴을 포함한 의료관련 감염의 흔한 원인 균이다[1]. A. baumannii에 의한 의료관련 감염은 알코올 중독, 흡연, 만성 폐쇄성 폐질환 및 당뇨병 등 면역력이 저하된 환자 또는 장기간 중환자실에서 재원한 환자에서 잘 발생하며, 이러한 위험인자가 없는 경우에는 감염을 잘 일으키지 않는 것으로 알려져 있다[1]. 그러나 지역사회에서 획득된 A. baumannii에 의한 폐렴이 국외에서 발생하고 있으며[2], 국내에서도 증례가 보고된 바 있다[3].
A. baumannii에 의한 감염성 심내막염은 호흡기 감염이 동반되어 있거나 정맥 도관을 사용하는 입원 환자에서 드물게 발생한다[4,5]. 지역사회에서 획득된 A. baumannii에 의한 심내막염은 산발적인 보고만 이루어지고 있는데, Falagas 등이 2007년에 232개의 문헌을 검색하여 지역사회 획득 Acinetobacter 감염의 빈도를 조사한 결과, 43명의 지역사회 획득 감염자 중에서 심내막염은 한 증례만을 확인하였다[1]. 국내에서는 아직 지역사회에서 획득된 A. baumannii에 의한 감염성 심내막염이 보고된 바 없다. 저자들은 동반질환을 가지고 있지 않고 침습적 시술을 시행 받은 적이 없는 성인에서 지역사회 획득 A. baumannii에 의하여 자연판막에 발생한 심내막염을 처음 경험하여 보고하는 바이다.
증 례
환 자: 여자, 30세
주증상: 1개월 전부터 발생한 왼쪽 상하지의 근력 감소(weakness)와 구음 장애 및 2일 전부터 지속된 발열
현병력: 1개월 전부터 왼쪽 상하지에 근력이 서서히 감소되고 경미한 구음 장애가 발생하였으며, 2일 전부터 상기 증상이 급격히 악화되면서 발열이 동반되어 타병원에서 시행한 뇌 자기공명영상상 오른쪽 중뇌동맥 영역에 급성 뇌경색이 관찰되어 본원에 입원하였다. 1개월 전부터 신경학적 증상이 발생하였지만 증상이 경미하고 서서히 악화되어 타병원에 내원하여 치료 받은 병력은 없었다.
과거력 및 가족력: 5년 전에 갑상선 기능 항진증을 진단 받고 methimazole을 불규칙하게 복용하였으며, 이외 특이 병력 및 입원력은 없었다.
이학적 소견: 입원 당시의 활력징후는 혈압 133/79 mmHg, 맥박수 94회/분, 호흡수 18회/분, 체온 38.1℃였다. 의식은 명료하였고, 급성 병색을 보였다. 호흡음은 정상이었고, 심음은 규칙적이었으며 흉골좌연에서 수축기 심잡음이 청진되었다. 오른쪽 상하지의 근력은 정상이었지만, 왼쪽 상지 및 하지의 근력이 grade III로 감소되어 있었다. 양쪽 모두에서 심부 건반사의 항진 소견은 관찰되지 않았다.
검사실 소견: 입원 당시 시행한 말초혈액 검사에서 백혈구 10,170/mm3(호중구 43%, 림프구 45.6%, 호산구 0.6%), 혈색소 12.9 g/dL, 적혈구용적률 38.3%, 혈소판 230,000/mm3, 적혈구침강속도 2 mm/hr였다. 면역혈청 검사에서 C-반응성 단백은 13.1 mg/L였으며, 요검사상 단백질 2+ 외에 이상 소견은 관찰되지 않았다. 입원 당시 시행한 흉부 방사선 검사 상 특이 이상소견 보이지 않았으며, 뇌 자기공명영상 혈관조영술(brain MR angiography)에서 오른쪽 내경 동맥(internal carotid artery, ICA) 및 왼쪽 내경 동맥 상상돌기 가지(ICA supraclinoid portion)의 폐색(Fig. 1)과 함께 오른쪽 중대뇌 동맥 영역에서 급성 경색 소견이 관찰되었다(Fig. 2).
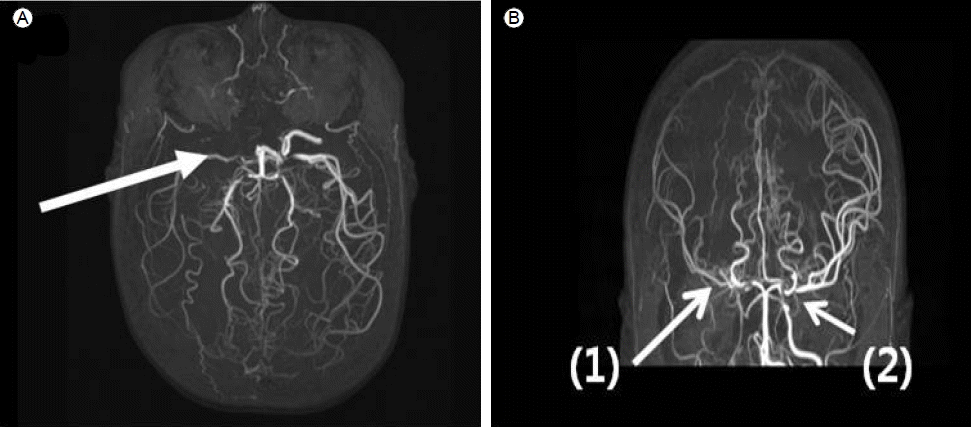
Brain magnetic resonance angiography on admission shows occlusion of the right internal carotid artery (ICA) (A), right middle cerebral artery (1), and left ICA supraclinoid branch (2) (B).

Brain magnetic resonance imaging on admission shows an acute infarction in the right middle cerebral artery territory.
임상경과: 입원 직후 서로 다른 부위의 말초혈관에서 채취한 혈액으로 자동화 혈액배양 및 항균제 감수성 검사 장비인 VITEK 2 system (bioMerieux, Inc., Hazelwood, MO, USA)의 그람음성용 동정카드를 사용하여 배양 검사를 시행하였으며, 입원 4일째 말초 혈액 3쌍 중 2쌍에서 A. baumanni(Confidence level: good Identification, Probability: 91%)가 동정되는 것을 확인하였다. 균혈증의 원인과 급성 뇌경색의 혈관 내 색전 유무를 확인하기 위하여 시행한 경흉부 심초음파 검사에서 전방 승모판 소엽에 0.53 × 0.94 cm의 증식증(vegetation)이 관찰되었고, grade II의 승모판 폐쇄 부전이 동반되어 있었다(Fig. 3). Modified Duke criteria [6]에서 주 진단 기준으로 심초음파에서 증식증의 이상소견이 관찰되었고, 부 진단 기준 중에서 38도 이상의 발열, A. baumanii에 의한 균혈증, 오른쪽 중대뇌 동맥 색전 소견의 세 가지 기준을 만족하여 감염성 심내막염을 진단할 수 있었다.

A transthoracic parasternal long-axis view shows a vegetation (0.53 × 0.94 cm) on the anterior leaflet of the mitral valve. LA, left atrium; LV, left ventricle.
입원 직후 말초혈액에서 동정된 A. baumannii의 시험관 내 항균제 감수성 검사는 VITEK2 system에서 N132 항균제 카드를 사용하여 시행하였고, CLSI (Clinical and Laboratory Standards Institute) [7] 지침을 기준으로 감수성 결과를 판단하였다. A. baumannii는 cefotaxime에 대해서만 최소억제농도가 16 μg/mL로 중등도 내성을 가지고 있었고, ampicillin/sulbactam, ceftazidime, colistimethate sodium, ciprofloxacin, gentamicin, imipenem, levofloxacin, meropenem, minocycline, piperacillin, trimethoprim/sulfamethoxazole, ticarcillin, ticarcillin/clavulanic acid, tobramycin에 모두 감수성을 나타내었다.
경험적 항생제로 ceftezole (2 g/일)을 투여하였고, A. baumannii 균주가 확인된 후에는 ceftazidime 및 ampicillin/sulbactam과 항균 범위가 유사한 cefoperazone/sulbactam (2 g/일, 12시간 간격) 투여를 시작하였으며, 발열이 호전되지 않아 입원 7일째부터 하루 4 g (12시간 간격)으로 증량하였다. 이후 입원 8일째부터 발열은 소실되어, 입원 38일까지 총 35일동안 cefoperazone/sulbactam 사용을 유지하였다. 입원 12일째 시행한 추적 혈액배양 검사에서 A. baumannii는 동정되지 않았다. 입원 21일째 시행한 추적 경흉부 초음파 검사에서 승모판에 증식증은 관찰되지 않았고, 승모판 폐쇄 부전은 grade II에서 grade I으로 호전되었다. 뇌경색 치료를 위하여 aspirin 및 clopidogrel을 복용하고 재활치료를 시행하였으며, 왼쪽 근력 감소는 grade V로 호전되었다. 구음 장애에 대한 재활치료를 지속적으로 시행 받았고 항생제를 중단한 후 28일째 퇴원하였다. 입원 기간 동안 감염 재발의 증거는 없었으며, 퇴원 후 입원 16개월째 시행한 추적 경흉부 심초음파 검사에서 승모판 폐쇄 부전이 경미한 정도로만 남아 있었으며 이외에 이상소견은 관찰되지 않았다.
고 찰
A. baumannii는 의료관련 감염의 중요한 원인균으로 최근 carbapenem 계열을 포함한 대부분의 항생제에 내성을 획득한 다제내성균주에 의한 감염이 증가하고 있다[8]. 그러나 A. baumannii는 환경에서 장기간 생존할 수 있기 때문에 열대 혹은 아열대 지방에서 지역사회 감염의 원인균으로서도 중요성이 증가되고 있다[1]. 본 환자는 최근 국외 또는 국내로 여행한 적이 없었으며, 그 밖의 임상적으로 의미 있는 이상 병력도 없었다. 따라서 본 증례에서는 사람의 손이나 토양 등 주변 환경에서 집락화를 이루고 있던 세균이 체내로 유입되어 지역사회 획득 심내막염을 일으킨 것으로 추정된다.
Falagas 등의 보고에 의하면 지역사회 획득 Acinetobacter 감염은 주로 만성폐쇄성 폐질환, 신장 질환, 당뇨 등과 같은 기저 질환을 갖고 있는 환자에서 주로 발생하는 것으로 보인다[1]. 특히 A. baumannii를 원인 균주로 하는 감염성 심내막염은 흔하지 않은 질환으로, 지금까지 산발적인 보고만 있어 왔다. Olut 등은 인공 판막 치환술을 시행 받은 환자에서 수술 1개월 후에 Acinetobacter에 의하여 심내막염이 발생한 경우를 보고하였으며[5], Bhagan-Bruno 등은 내경 정맥 도관을 통하여 투석을 시행 받은 말기 신부전 환자에서 발생한 경우를 보고한 바 있다[9]. 본 증례는 A. baumannii 감염의 위험인자인 기저 질환을 가지고 있지 않는 젊은 여성에게서 발생한 지역사회 획득 감염성 심내막염의 첫 증례로서 의미가 있다.
본 증례에서 신경학적 이상 증상이 1개월 전부터 발생하였지만 처음에는 경미한 구음 장애 및 근력저하가 발생하였고 근력저하가 서서히 진행되었다. 이러한 신경학적 이상 소견은 작은 우식증의 색전으로 인한 일과성 허혈 발작(transient ischemic attack)이 반복적으로 발생하였기 때문일 가능성이 높을 것으로 판단된다. 2일 전부터 급성 악화된 증상은 작은 다발성의 색전에 의한 주 동맥 폐색으로 급성 뇌경색이 발생하였음을 시사하는 것으로 사료된다. 감염성 심내막염에서 동반될 수 있는 두개내 감염성 동맥류(intracranial mycotic aneurysm)이 파열되어 뇌출혈이 발생할 위험성이 있기 때문에 항응고 치료가 제한되어 왔으나, 최근 발표된 결과에 따르면 혈전 색전성 뇌경색이 발생할 확률이 높거나 발생한 경우 항응고 치료를 병행하는 것이 뇌경색의 발생과 악화를 감소시켜 준다는 보고가 있다[10]. 따라서 본 증례에서는 급성 혈전 색전성 뇌경색에 대해 aspirin 및 clopidogrel로 항응고 치료를 시행하였다.
Acinetobacter에 의한 감염성 심내막염의 경우, 여러 가지 인자들이 예후에 영향을 미칠 수 있는 것으로 생각되고 있다. 그 한 가지가 환자의 판막의 종류이다. Acinetobacter에 의한 감염성 심내막염은 자연 판막, 인공 판막을 가진 환자 모두에서 발생할 수 있다. 보고된 사례들을 고찰해 보았을 때 자연 판막에 발생한 경우가 인공 판막에 발생한 경우에 비하여 전격성으로 진행하는 경우가 많았으며, 예후가 좋지 않아 사망률이 높았다[11]. 따라서 인공 판막에 발생한 심내막염의 경우 중증 기저 심장 질환이 동반되어 있지 않으면 이른 시기에 판막치환술을 시행할 필요는 없는 것으로 사료되지만, 자연 판막의 경우 급속하게 질병이 진행하는 경우가 많아서 판막 치환술의 시행 가능성에 대해 지속적인 감시가 필요한 것으로 생각된다[12]. 또한, A. baumannii의 항생제에 대한 감수성 결과가 예후에 영향을 미칠 수 있다. Rizos 등은 다제 내성이 아닌 A. baumannii에 의한 심내막염을 6주간의 항생제 병용 투여로 성공적으로 치료한 사례를 보고하였으며[12], Menon 등은 다제 내성 A. baumannii에 의한 심내막염 환자에서 항생제 병합 치료를 하였지만 사망한 증례를 보고한 바 있다[13]. A. baumannii에 의하여 발생한 감염성 심내막염에서 병원 획득 감염의 경우 다제 내성 균주 빈도가 69.6%에 이르는 것으로 보고되고 있으며[5] 다제 내성 A. baumannii에 의한 감염성 심내막염은 일반적으로 carbapenem과 aminoglycoside을 병합하여 치료한다[5]. 그러나 지역 사회 획득 A. baumannii 감염성 심내막염에서 다제 내성 균주의 빈도는 높지 않은 것으로 보고되고 있으며[14], 본 증례에서도 지역 사회에서 A. baumannii의 감염이 획득되어 대부분의 항생제에 감수성을 가지고 있었다.
본 증례는 자연 판막에 심내막염이 발생하였지만 지역사회 획득 감염으로 A. baumannii가 우수한 항균제 감수성을 가지고 있었으며, 환자가 기저 질환을 가지고 있지 않았기 때문에 5주 동안의 항생제 치료 중 심내막염에 의한 추가적인 합병증이 발생하지 않고 수술적 치료 없이 항생제 치료만으로 완치할 수 있었던 것으로 사료된다. 병원 내 획득 감염을 주로 일으키는 A. baumannii 균주가 만성 기저 질환이 없는 지역 사회인에서 감염성 심내막염의 원인균이 될 수 있으므로 지역사회획득 A. baumannii 균혈증이 발생하였을 경우 감염성 심내막염을 감별 진단해야 할 것이다.