мДЬ л°†
нПР к∞ДмІИмЭА нПРнПђмЧРмДЬ м£ЉмЬД л™®мДЄ нШИкіА л≤љкєМмІАмЭШ к≥µк∞ДмЭД лІРнХШл©∞, мЧђкЄ∞мЧРлКФ нПРнПђ, нПРнПђмГБнФЉмДЄнПђ, нШИкіАлВінФЉмДЄнПђ, мЭілЯђнХЬ м°∞мІБ мВђмЭімЭШ к≥µк∞Д, нШИкіАм£ЉмЬД л∞П л¶ЉнФД м°∞мІБмЭД нПђнХ®нХЬлЛ§. к∞ДмІИмД± нПРмІИнЩШмЭА м£Љл°Ь к∞ДмІИмЭД мє®л≤ФнХШмЧђ лЛ§мЦСнХЬ нШХнГЬмЭШ мЧЉм¶Эк≥Љ мДђмЬ†нЩФл•Љ міИлЮШнХШлКФ лєДмҐЕмЦСмД±, лєДк∞РмЧЉмД± мІИнЩШмЭД лІРнХЬлЛ§[1]. кЈЄлЯђлВШ к∞ДмІИмД± нПРмІИнЩШмЭШ мҐЕл•ШлКФ лІ§мЪ∞ лЛ§мЦСнХШмЧђ, мИШмИ†м†Б нПР мГЭк≤АмЭД нХШлНФлЭЉлПД мІДлЛ®мЭі мХ†лІ§нХЬ к≤љмЪ∞лПД мЮИлЛ§. лФ∞лЭЉмДЬ к∞ДмІИмД± нПРмІИнЩШмЭА мЮДмГБм†Б, мШБмГБнХЩм†Б, л≥Сл¶ђм°∞мІБнХЩм†Б мЖМк≤ђмЭД мҐЕнХ©нХШмЧђ мІДлЛ®нХШлКФлН∞, мЭЉл∞Шм†БмЬЉл°Ь 2002лЕД лѓЄкµ≠нЭЙлґАнХЩнЪМ/мЬ†лЯљнЭЙлґАнХЩнЪМмЧРмДЬ м†ЬмХИнХЬ л∞©л≤ХмЭД нЖµнХі лґДл•ШнХЬлЛ§[2].
к∞ДмІИмД± нПРмІИнЩШ м§СмЧРмДЬ к∞ДмІИк≥Љ мДЄкЄ∞кіАмІАл•Љ нХ®кїШ мє®л≤ФнХШлКФ мІИнЩШмЬЉл°ЬлКФ мЧђлЯђ к∞АмІАк∞А мЮИлЛ§. нХШмІАлІМ bronchiolitis interstitial pneumonitis (BIP)лКФ нШДмЮђмЭШ м≤ік≥Дл°ЬлКФ лґДл•ШлРШмІА мХКлКФ мГИл°ЬмЭі л≥ік≥†лРЬ лПЕл¶љм†БмЭЄ мІИнЩШкµ∞мЬЉл°Ь к∞ДмІИмД± нПРмЮ•мЧЉк≥Љ мДЄкЄ∞кіАмІАмЧЉмЭі л≥СнХ©лРЬ мІИнЩШмЭілЛ§[3]. к≥Љк±∞мЧРлКФ мДЄкЄ∞кіАмІА мІИнЩШк≥Љ к∞ДмІИмД± мІИнЩШмЭі нХ®кїШ м°імЮђнХЬлЛ§лКФ к∞ЬлЕРмЬЉл°Ь вАШrubric BOOP (bronchiolitis obliterans organizing pneumonia) [3]вАЩлЭЉк≥† нХШмЧђ нПРмЗДмД± мДЄкЄ∞кіАмІАмЧЉ-кЄ∞мІИнЩФ нПРл†і(BOOP)мЬЉл°Ь нЭФнЮИ лґДл•ШлРШмЧИлЛ§[2]. нХШмІАлІМ мµЬкЈЉ 31л™ЕмЭШ нЩШмЮР нПРм°∞мІБ к≤АмВђл•Љ лґДмДЭнХЬ л≥ік≥†мЧРмДЬ л≥Сл¶ђнХЩм†БмЬЉл°Ь нПРмЗДмД± мДЄкЄ∞кіАмІАмЧЉ-кЄ∞мІИнЩФ нПРл†ік≥Љ нЖµмГБнШХ к∞ДмІИмД± нПРл†і(usual interstitial pneumonia, UIP)мЭШ м§Ск∞Дм†БмЭЄ нКємІХмЭД к∞АмІАлКФ мІИнЩШкµ∞мЭД BIPлЭЉлКФ лПЕл¶љм†БмЭЄ мІИнЩШмЬЉл°Ь лґДл•ШнХШмШАлЛ§[3].
м†АмЮРлУ§мЭА 2к∞ЬмЫФ м†ДлґАнД∞ мЛђнХімІД нШЄнЭ° к≥§лЮАмЬЉл°Ь лВімЫРнХЬ 68мДЄ мЧђмЮР нЩШмЮРк∞А нЭЙлґА м†ДмВ∞нЩФлЛ®мЄµміђмШБмЧРмДЬ 6к∞ЬмЫФ м†Дк≥Љ лєДкµРнХШмЧђ мХЕнЩФлРЬ мЖМк≤ђмЭД л≥імЧђ нЭЙк∞Хк≤љмИШмИ†мЭД нЖµнХі мЪ∞нХШмЧљмЭШ мРРкЄ∞ м†Им†ЬмИ†мЭД мЛЬнЦЙнХШмШАмЬЉл©∞ BIPл°Ь мІДлЛ®нХЬ к≤љмЪ∞л•Љ к≤љнЧШнХШмШАлЛ§. кµ≠лВімЧРмДЬлКФ лєДмКЈнХЬ м¶Эл°А л≥ік≥†к∞А мЮИмЧИмІАлІМ, мЭілКФ мК§нЕМл°ЬмЭілУЬ мєШл£М нЫДмЧР нПР м°∞мІБк≤АмВђл•Љ мЛЬнЦЙнХШмЧђ мІДлЛ®лРЬ к≤љмЪ∞л°Ь, л≥Є м¶Эл°АмЩА к∞ЩмЭі мК§нЕМл°ЬмЭілУЬ мєШл£М м†ДмЧР л≥Сл¶ђнХЩм†БмЬЉл°Ь нЩХмЭЄлРЬ мШИк∞А мЧЖмЬЉлѓАл°Ь мЭіл•Љ лђЄнЧМк≥†м∞∞к≥Љ нХ®кїШ л≥ік≥†нХШк≥†мЮР нХЬлЛ§.
м¶Э л°А
нЩШ мЮР: мЧђмЮР, 68мДЄ
м£Љ мЖМ: 8к∞ЬмЫФк∞Д мІАмЖНлРШлКФ кЄ∞мє® л∞П нЭ∞мГЙ к∞ЭлЛі, мµЬкЈЉ 2к∞ЬмЫФ м†ДлґАнД∞ л∞ЬмГЭнХЬ нШЄнЭ° к≥§лЮА
нШДл≥С놕: мХљ 6к∞ЬмЫФ м†Д кЄ∞мє®к≥Љ к∞ЭлЛімЭД м£ЉмЖМл°Ь мЭЄкЈЉ л≥СмЫРмЧР лВімЫРнХШмШАлЛ§. лЛємЛЬ H1N1 к∞РмЧЉмЭі мЭШмЛђлРШмЦі oseltamivir мєШл£Мл•Љ л∞ЫмХШмЬЉлВШ мєШл£М нЫДмЧРлПД м¶ЭмГБ мІАмЖНлРШк≥† лЛ®мИЬ нЭЙлґАмВђмІДмЧРмДЬ мЭімГБмЖМк≤ђмЭі кіАм∞∞лРШмЦі 6к∞ЬмЫФ м†Д л≥ЄмЫРмЬЉл°Ь мЭШлҐ∞лРШмЧИлЛ§. л≥ЄмЫРмЧРмДЬ мЛЬнЦЙнХЬ нЭЙлґА м†ДмВ∞нЩФлЛ®мЄµміђмШБмЧРмДЬ к∞ДмІИмД± нПРл†імЭі мЭШмЛђлРШмЧИмЬЉлВШ, нШЄнЭ°к≥§лЮАмЭі мЧЖк≥† к≥†л†ємЭЄ м†РмЭД к≥†л†§нХШмЧђ нПР м°∞мІБк≤АмВђлКФ мЛЬнЦЙнХШмІА мХКмХШмЬЉл©∞, мЭЄкЈЉ мЭШмЫРмЧРмДЬ лМАм¶ЭмєШл£М нХШл©імДЬ к≤љк≥ЉкіАм∞∞нХШкЄ∞л°Ь нХШмШАлЛ§. нХШмІАлІМ м¶ЭмГБмЭі нШЄм†Д мЧЖмЭі мІАмЖНлРШл©∞, 2к∞ЬмЫФ м†ДлґАнД∞лКФ mMRC (modified Medical Research Council) 3мЭШ нШЄнЭ°к≥§лЮАмЭі л∞ЬмГЭнХШмЧђ лЛ§мЛЬ л≥ЄмЫРмЧР лВімЫРнХШмШАлЛ§.
к≥Љк±∞놕: 2лЕД м†Д нГА л≥СмЫРмЧРмДЬ нПРл†імЬЉл°Ь мЩЄлЮШ мєШл£Мл•Љ л∞ЫмЭА м†БмЭі мЮИмЧИлЛ§.
мВђнЪМ놕: мЭМм£Љ л∞П нЭ°мЧ∞놕 мЧЖмЧИмЭМ.
мІБмЧЕ놕 л∞П к∞А찱놕: нКємЭімВђнХ≠ мЧЖмЭМ.
мІДм∞∞ мЖМк≤ђ: нШИмХХмЭА 120/70 mmHg, лІ•л∞ХмИШ 60нЪМ/лґД, нШЄнЭ°мИШ 20нЪМ/лґД, м≤імШ® 36.5вДГл°Ь мХИм†Хм†БмЭімЧИлЛ§. нЩШмЮРлКФ лІМмД± л≥СмГЙмЭД лЭ†к≥† мЮИмЧИмЬЉлВШ мЭШмЛЭмЭА л™Ел£МнХШмШАмЬЉл©∞, нЭЙлґА мІДм∞∞мЧРмДЬ мЦСмЄ° нПРнХШлґАмЧР нШЄнЭ°мЭМмЭі к∞РмЖМлРШмЦі мЮИмЧИлЛ§. кЈЄ мЩЄ кЄ∞нГА лСРк≤љлґА к≤АмВђ л∞П л≥µлґА мІДм∞∞мЧРмДЬлКФ мЭімГБмЖМк≤ђ мЧЖмЧИмЬЉл©∞, мЛ†к≤љнХЩм†Б к≤АмВђмЧРмДЬлПД нКємЭімЖМк≤ђ мЧЖмЧИлЛ§.
к≤АмВђмЛ§ мЖМк≤ђ: нПР м°∞мІБк≤АмВђл•Љ мЬДнХі мЮЕмЫРнХШл©імДЬ мЛЬнЦЙнХЬ лІРміИнШИмХ° к≤АмВђмЧРмДЬлКФ л∞±нШИкµђ 5,460/mm3 (нШЄм§Скµђ 68%, нШЄмВ∞кµђ 5%), нШИмГЙмЖМ 12.4 g/dL, м†БнШИкµђ мЪ©м†Б땆 35.9%, нШИмЖМнМР 235,000/mm3мЭімЧИлЛ§. мГЭнЩФнХЩм†Б к≤АмВђмЧРмДЬлКФ міЭ лЛ®л∞±мІИ 6.5 g/dL, мХМлґАлѓЉ 3.9 g/dL, міЭ лєМл¶ђл£®лєИ 0.4 mg/dL, мљЬл†ИмК§нЕМл°§ 205 mg/dL, AST 30 IU/L, ALT 24 IU/L, ALP 195 IU/L, LDH 545 IU/L, BUN 16.7 mg/dL, Creatinine 0.87 mg/dL, Glucose 108 mg/dL, Na 142 mEq/L, K 4.1 mEq/LмШАлЛ§. нПРкЄ∞лК• к≤АмВђмЧРмДЬлКФ лŪ놕мД± нПРнЩЬлЯЙ(forced vital capacity, FVC)мЭі 2.65 Lл°Ь мШИмЄ°мєШмЭШ 101%, 1міИк∞Д лŪ놕мД± нШЄкЄ∞лЯЙ(forced expiratory volume in 1 second, FEV1)мЭі 2.02 Lл°Ь мШИмЄ°мєШмЭШ 108%, FEV1/FVCк∞А 76%мШАк≥†, 6к∞ЬмЫФ м†ДмЭШ нПРкЄ∞лК• к≤АмВђмЩА лєДкµРнХШмЧђ нПРнЩХмВ∞лК•(diffusing capacity of the lung for carbon monoxide, DLCO)мЭі мШИмЄ°мєШмЭШ 86%мЧРмДЬ 59%л°Ь к∞РмЖМлРШмЦі мЮИмЧИлЛ§. лШРнХЬ мЖМкЄ∞лПД нПРмЗДмД± мІИнЩШмЭШ м°∞кЄ∞ мІДлЛ®мЧР лѓЉк∞РнХЬ лŪ놕мД± нШЄкЄ∞м§Ск∞ДмЬ†лЯЙ(forced expiratory flow between 25% and 75% of vital capacity, FEF25-75%)лПД 6к∞ЬмЫФ м†Дк≥Љ лєДкµРнХШмЧђ мШИмЄ°мєШмЭШ 90%мЧРмДЬ 76%л°Ь к∞РмЖМлРШмЦі мЮИмЧИлЛ§. кЈЄ мЩЄ л©ФнГАмљЬл¶∞кЄ∞кіАмІАмЬ†л∞Ь к≤АмВђлКФ мЭМмД±мЭімЧИлЛ§. кЄ∞кіАмІАлВімЛЬк≤љ к≤АмВђмЧРмДЬ кЄ∞кіАмІА лВі л≥Сл≥АмЭА кіАм∞∞лРШмІА мХКмХШмЬЉл©∞, кЄ∞кіАмІА мДЄм≤ЩмИ†мЭД нЖµнХі мЦїмЭА к≤Ам≤іл°Ь мЛЬнЦЙнХЬ мДЄкЈ†л∞∞мЦС, к≤∞нХµкЈ† мІСкЈ† л∞П л∞∞мЦС, к≤∞нХµкЈ† PCR к≤АмВђлКФ мЭМмД±мЭімЧИлЛ§. мЪ∞м§СмЧљмЧРмДЬ мЛЬнЦЙнХЬ кЄ∞кіАмІАнПРнПђмДЄм≤ЩмХ° к≤АмВђмЧРмДЬлКФ лЛ§нХµкµђл•Љ нПђнХ®нХЬ лЛ®нХµкµђ 85%, л¶ЉнФДкµђ 15%, м§СмД±кµђ 10%мШАк≥†, CD4/CD8 лєДлКФ 2.75л°Ь мХљк∞Д м¶Эк∞АлРШмЦі мЮИмЧИлЛ§.
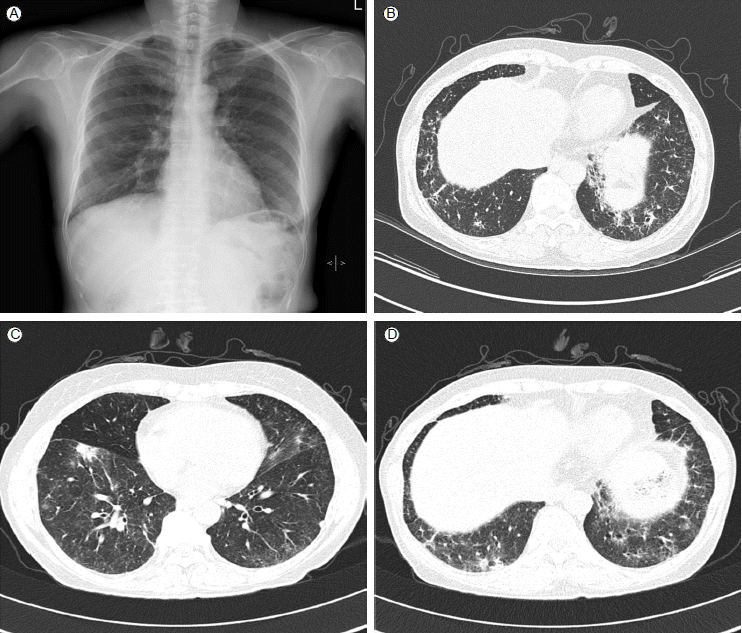
л∞©мВђмД†к≤АмВђ мЖМк≤ђ: 6к∞ЬмЫФ м†Д л≥ЄмЫР м≤Ђ лВімЫР лЛємЛЬ мЛЬнЦЙнХЬ лЛ®мИЬнЭЙлґАмВђмІДмЧРмДЬлКФ м†ДнПРмХЉл°Ь лІЭмГБ к≤∞м†ИнШХ л≥Сл≥АмЭі кіАм∞∞лРШмЧИлЛ§(Fig. 1A). м≤ШмЭМ лВімЫР мЛЬ мЛЬнЦЙнХЬ нЭЙлґА к≥†нХімГБм†ДмВ∞нЩФлЛ®мЄµміђмШБмЧРмДЬлКФ мЦСнПРмХЉмЭШ лІРміИ лґАмЬДл°Ь лІЭмГБ к≤∞м†ИнШХмЭШ л≥Сл≥АмЭі кіАм∞∞лРШмЧИмЬЉл©∞, кЄ∞кіАмІА м£ЉмЬДл°ЬлКФ к∞АмІА л™®мЦСмЭШ мД†мГБ мЭМмШБмЭі л≥імШАлЛ§(Fig. 1B). нХШмІАлІМ 6к∞ЬмЫФ нЫД мЛЬнЦЙнХЬ нЭЙлґА к≥†нХімГБм†ДмВ∞нЩФлЛ®мЄµміђмШБмЧРмДЬлКФ м†Дл∞Шм†БмЬЉл°Ь к≤љк≤∞мД± л≥АнЩФмЩА нХ®кїШ к∞ДмЬ†л¶ђмЦС мЭМмШБмЭі м¶Эк∞АлРШмЦі л™®мЮРмЭінБђ л™®мЦСмЬЉл°Ь мХЕнЩФлРЬ мЖМк≤ђмЭі кіАм∞∞лРШмЧИлЛ§(Fig. 1C and 1D).
м°∞мІБк≤АмВђ мЖМк≤ђ: лєДлФФмШ§ нЭЙк∞Хк≤љмИШмИ†(video assisted thoracoscopic surgery, VATS)мЭД нЖµнХі мЪ∞нХШмЧљмЭШ мРРкЄ∞ м†Им†ЬмИ†мЭД мЛЬнЦЙнХШмШАлЛ§. м°∞мІБк≤АмВђмЧРмДЬ мДЄкЄ∞кіАмІАмЭШ нЩХмЮ•к≥Љ мДЄкЄ∞кіАмІА м£Љл≥А л∞П к∞ДмІИмД± мДђмЬ†нЩФ, нПРмЗДкЄ∞кіАмІА кЄ∞мІИнЩФ нПРл†імЭі кіАм∞∞лРШмЧИлЛ§. лШРнХЬ нЖµмГБнШХ к∞ДмІИмД± нПРл†ік≥Љ мЬ†мВђнХЬ л≤МмІСл™®мЦСмЭШ л≥АнЩФлПД кіАм∞∞нХ† мИШ мЮИмЦі BIPл°Ь мІДлЛ®нХШмШАлЛ§(Fig. 2).
мєШл£М л∞П мЮДмГБк≤љк≥Љ: нЩШмЮРлКФ к≤љкµђ methylprednisolone 16 mgк≥Љ azathioprine 50 mgмЬЉл°Ь мєШл£Мл•Љ мЛЬмЮСнХШмШАлЛ§. MethylprednisoloneмЭА 16 mgмЬЉл°Ь 2к∞ЬмЫФ мВђмЪ© нЫД м†Рм∞® к∞РлЯЙнХШмЧђ міЭ 6к∞ЬмЫФ мВђмЪ©нХШмШАмЬЉл©∞, azathioprineмЭА 100 mgкєМмІА м¶ЭлЯЙнХШмЧђ нШДмЮђкєМмІА мВђмЪ© м§СмЭілЛ§. Methylprednisoloneк≥Љ azathioprineмЭД мЛЬмЮСнХЬ нЫД нШЄнЭ°к≥§лЮА, кЄ∞мє®, к∞ЭлЛі лУ±мЭШ м¶ЭмГБмЭА нШЄм†ДмЭД л≥імШАмЬЉлВШ, мєШл£М 5к∞ЬмЫФ нЫДмЩА 9к∞ЬмЫФ нЫД мЛЬнЦЙнХЬ нЭЙлґА к≥†нХімГБм†ДмВ∞нЩФлЛ®мЄµміђмШБ(Fig. 3)мЧРмДЬлКФ міИкЄ∞мЩА лєДкµРнХШмЧђ нБ∞ л≥АнЩФк∞А кіАм∞∞лРШмІА мХКмХШлЛ§. нШДмЮђлКФ azathioprine 100 mgмЬЉл°Ь 1лЕД 6к∞ЬмЫФмІЄ мєШл£Мл•Љ мЬ†мІАнХШк≥† мЮИмЬЉл©∞, мХЕнЩФ мЖМк≤ђ мЧЖмЭі мЩЄлЮШ мґФм†БкіАм∞∞ м§СмЭілЛ§.
к≥† м∞∞
Bronchiolitis interstitial pneumonitis (BIP)лКФ мµЬкЈЉмЧР м†ЬмЛЬлРЬ мГИл°ЬмЪі к∞ДмІИмД± нПРл†імЭШ нХШлВШл°Ь мДЄкЄ∞кіАмІАмЧЉк≥Љ к∞ДмІИмД± нПРл†імЭі нХ®кїШ м°імЮђнХШл©імДЬлПД нПРнПђ лВіл°ЬлКФ л≥Сл≥АмЭі к±∞мЭШ мє®л≤ФлРШмІА мХКлКФ нКємІХмЭі мЮИлЛ§[3]. м°∞мІБк≤АмВђмЧРмДЬлКФ мДЄкЄ∞кіАмІАмЩА к∞ДмІИмЧР мЧЉм¶Эк≥Љ мДђмЬ†нЩФк∞А мІДнЦЙлРШмЦі мЮИмІАлІМ нПРнПђ лВі кЄ∞мІИнЩФ нПРл†і(intra-alveolar organizing pneumonia)мЭА к±∞мЭШ кіАм∞∞лРШмІА мХКк≥† л≥ім°ілРЬ мЖМк≤ђмЭД л≥імЭЄлЛ§[3].
мЭілЯђнХЬ нКємІХмЭД к∞АмІАлКФ мІИнЩШлУ§л°ЬлКФ нПРмЗДмДЄкЄ∞кіАмІАмЧЉ(bronchiolitis obliterans, BO) нШємЭА нПРмЗДмД± мДЄкЄ∞кіАмІАмЧЉ-кЄ∞мІИнЩФ нПРл†і, нЖµмГБнШХ к∞ДмІИмД± нПРл†і, лєДнКємЭімД± к∞ДмІИмД± нПРл†і(nonspecific interstitial pneumonia, NSIP), кЄ∞лПД-м§СмЛђмД± к∞ДмІИмД± мДђмЬ†нЩФ(airwaycentered interstitial fibrosis, ACIF), кЈЄл¶ђк≥† нКєл∞ЬмД± мДЄкЄ∞кіАмІА-м§СмЛђмД± к∞ДмІИмД± нПРл†і(idiopathic bronchiolocentric interstitial pneumonia, IBCIP) лУ±мЭі мЮИлЛ§. кЈЄ мЩЄмЧРлПД к≥ЉлѓЉмД± нПРл†і(hypersensitivity pneumonitis)к≥Љ мХљлђЉмЧР мЭШнХЬ нПРмІИнЩШ(drug-induced lung disease)лПД мГЭк∞БнХі л≥Љ мИШ мЮИлЛ§[3].
мЭім†ДмЧРлКФ BIPл°Ь лґДл•ШлР† мИШ мЮИлКФ мІИнЩШлУ§мЭі мДЄкЄ∞кіАмІА мІИнЩШк≥Љ к∞ДмІИмД± мІИнЩШмЭі нХ®кїШ м°імЮђнХЬлЛ§лКФ к∞ЬлЕРмЬЉл°Ь мЭЄнХШмЧђ вАШrubric BOOPвАЩлЭЉк≥† нХШмЧђ нПРмЗДмД± мДЄкЄ∞кіАмІАмЧЉ-кЄ∞мІИнЩФ нПРл†імЬЉл°Ь нЭФнЮИ лґДл•ШлРШкЄ∞лПД нХШмШАмІАлІМ[3], BIPлКФ нПРнПђ лВі к≥µк∞ДмЭі л≥ім°ілРЬлЛ§лКФ м†РмЧРмДЬ нПРл†і(pneumonia)мЭі мХДлЛМ нПРмЮ•мЧЉ(pneumonitis)мЬЉл°Ь л≥Љ мИШ мЮИмЬЉл©∞, мЭілКФ нПРмЗДмД± мДЄкЄ∞кіАмІАмЧЉ-кЄ∞мІИнЩФ нПРл†ік≥ЉлКФ мЧДмЧ∞нЮИ лЛ§л•ілЛ§лКФ к≤ГмЭД мЭШлѓЄнХЬлЛ§[3].
BIPлКФ нЖµмГБнШХ к∞ДмІИмД± нПРл†ік≥ЉлПД кµђлґДмЭі лРШлКФлН∞, нЖµмГБнШХ к∞ДмІИмД± нПРл†ік≥Љ лєДкµРнХШмЧђ BIPмЧРмДЬлКФ мДЄкЄ∞кіАмІА л≥Сл≥АмЭі лНФ лЪЬл†ЈнХЬ м∞®мЭім†РмЭі мЮИлЛ§. нЖµмГБнШХ к∞ДмІИмД± нПРл†імЭШ м°∞мІБ мЖМк≤ђмЧРмДЬлКФ нКємІХм†БмЬЉл°Ь м†ХмГБм†БмЭЄ нПР лґАмЬДмЩА л≥СмЖМ лґАмЬДк∞А мДЮмЧђмДЬ мВ∞л∞Ьм†БмЬЉл°Ь лВШнГАлВШк≥† л≥Сл≥А мЮРм≤ілПД к∞ЩмЭА нЩШмЮРмЭШ к∞ЩмЭА нПРмЧљмЧРмДЬ кµРмЫРмІИ мє®м∞©мЭі м£ЉмЖМк≤ђмЭЄ мЛђнХЬ лІРкЄ∞ мДђмЬ†нЩФ л≥Сл≥А(л≤МмІСл™®мЦС л≥АнШХ, honeycomb fibrosis)к≥Љ мДђмЬ†нЩФмЭШ міИкЄ∞ мЖМк≤ђмЭЄ мДђмЬ†л™®мДЄнПђ л≥СмЖМ(fibroblastic foci)к∞А к∞ЩмЭі м°імЮђнХШлКФ мЛЬкЄ∞м†Б мЭімІИмД±(temporal heterogeneity)мЭі кіАм∞∞лРШмІАлІМ[1], BIPмЧРмДЬлКФ мЭілЯђнХЬ мЖМк≤ђмЭі кіАм∞∞лРШмІА мХКлКФлЛ§. кЄЙмД± мХЕнЩФ мЛЬкЄ∞мЭШ нЖµмГБнШХ к∞ДмІИмД± нПРл†імЧРмДЬлКФ кЄ∞мІИнЩФ нПРл†імЭі лПЩл∞ШлР† мИШ мЮИкЄ∞ лХМлђЄмЧР BIPк∞А нЖµмГБнШХ к∞ДмІИмД± нПРл†імЭШ кЄЙмД± мХЕнЩФ мЛЬкЄ∞л°Ь мЧђк≤®мІИ мИШлПД мЮИлЛ§[3]. нХШмІАлІМ кЄЙмД± мХЕнЩФ мЛЬкЄ∞мЭШ нЖµмГБнШХ к∞ДмІИмД± нПРл†імЭШ м°∞мІБмЧРмДЬлКФ лѓЄлІМмД± нПРнПђ лВі мЖРмГБ(diffuse intra-alveolar damage)мЭі кіАм∞∞лРШмІАлІМ BIPмЧРмДЬ нПРнПђ лВілКФ нБ∞ л≥Сл≥А мЧЖмЭі л≥ім°ілРЬлЛ§лКФ м∞®мЭім†РмЭі мЮИлЛ§[3].
мЦілКР нКєм†Х нМ®нДімЧР мЙљк≤М лУ§мЦі лІЮмІА мХКмЭА нКєл∞ЬмД± к∞ДмІИмД± нПРл†імЭШ к≤љмЪ∞мЧРлКФ лґДл•Шк∞А мЙљмІА мХКмХД лХМлХМл°Ь BIPк∞А лєДнКємЭімД± к∞ДмІИмД± нПРл†імЬЉл°Ь мШ§мЭЄлРШкЄ∞лПД нХЬлЛ§. кЈЄлЯђлВШ лєДнКємЭімД± к∞ДмІИмД± нПРл†імЭШ л≥Сл≥АмЭА лєДкµРм†Б кЈ†мЭЉнХШк≤М лВШнГАлВШк≥†, л≥Сл≥АмЭШ мДЄкЄ∞кіАмІА мє®л≤ФмЭі мЧЖлКФ м†РмЧРмДЬ BIPмЩА м∞®мЭік∞А мЮИмЬЉл©∞, л≥Є м¶Эл°АмЧРмДЬлПД лєДнКємЭімД± к∞ДмІИмД± нПРл†імЬЉл°Ь мЭШмЛђнХ† лІМнХЬ лґАлґДмЭА кіАм∞∞лРШмІА мХКмХШлЛ§[3].
кЄ∞лПД-м§СмЛђмД± к∞ДмІИмД± мДђмЬ†нЩФмЧРмДЬ кіАм∞∞лРШлКФ мДЄкЄ∞кіАмІА м£ЉмЬД мДђмЬ†нЩФк∞А BIPмЧРмДЬлКФ кіАм∞∞лРШмІА мХКк≥†[4], нКєл∞ЬмД± мДЄкЄ∞кіАмІА-м§СмЛђмД± к∞ДмІИмД± нПРл†імЭА лєДл°Э мДЄкЄ∞кіАмІА м§СмЛђмД±мЭікЄ∞лКФ нХШмІАлІМ л¶ЉнФДкµђмД± мДЄкЄ∞кіАмІАмЧЉмЭілВШ мДЄкЄ∞кіАмІА м£ЉмЬД мДђмЬ†нЩФл°Ь нСЬнШДлРШлКФ л≥Сл≥АмЭД к∞АмІДлЛ§лКФ м†РмЧРмДЬ BIPмЩА лЛ§л•ілЛ§[5].
л≥Є м¶Эл°АмЭШ кЄ∞кіАмІАнПРнПђмДЄм≤ЩмХ° к≤АмВђмЧРмДЬ м§СмД±кµђмЩА CD4/CD8 лєДк∞А мХљк∞Д м¶Эк∞АлРШмЦі мЮИлКФ мЖМк≤ђмЬЉл°Ь к≥ЉлѓЉмД± нПРл†імЭШ к∞АлК•мД±лПД мГЭк∞БнХі л≥Љ мИШ мЮИлЛ§[1]. нХШмІАлІМ к≥ЉлѓЉмД± нПРл†імЭА мЦілЦ§ мЫРмЭЄ лђЉмІИмЧР мЭШнХЬ к≥ЉлѓЉ л∞ШмЭСмЭілЭЉлКФ л≥СмЭЄл°†м†Б мІДлЛ®мЭі нПђнХ®лРЬ мЪ©мЦімЭіл©∞[3], м°∞мІБнХЩм†Б мЖМк≤ђмЭі м£Љл°Ь мДЄнПђмД± кЄ∞кіАмІАмЧЉ, л¶ЉнФДкµђмД± к∞ДмІИмД± нПРл†і, лєДкіімВђмД± мЬ°мХДмҐЕмЬЉл°Ь лВШнГАлВЬлЛ§лКФ м†РмЧРмДЬ л≥Є м¶Эл°АмЩАлКФ м∞®мЭік∞А мЮИлЛ§[1,6].
мХљлђЉмЧР мЭШнХЬ нПРмІИнЩШлПД к≥†л†§нХі л≥Љ мИШ мЮИлЛ§. л≥Є м¶Эл°АмЧРмДЬлКФ мЫРмЭЄ мХљм†Ьл°Ь oseltamivirл•Љ мГЭк∞БнХі л≥Љ мИШ мЮИмЬЉл©∞, мХљм†ДмЧРлПД лУЬлђЉк≤М нПРл†імЭД мЭЉмЬЉнВђ мИШ мЮИлЛ§к≥† л™ЕмЛЬлРШмЦі мЮИлЛ§. нХШмІАлІМ мХљлђЉмЧР мЭШнХЬ нПРмІИнЩШмЭШ к≤љмЪ∞ мХљлђЉмЭД м°∞кЄ∞ м§СлЛ®нХШл©і нПР мЖРмГБмЭШ нШЄм†ДмЭі к∞АлК•нХЬлН∞, мД±мЭЄмЧРмДЬ oseltamivirл•Љ мВђмЪ©нХ† лХМ нЖµмГБм†БмЬЉл°Ь 75 mg bidл°Ь 5мЭЉк∞Д мІІмЭА кЄ∞к∞Д мВђмЪ©нХШл©∞, л≥Є м¶Эл°АмЧРмДЬлКФ oseltamivirл•Љ м§СлЛ®нХШк≥† мИШк∞ЬмЫФ нЫДмЧР мІИнЩШмЭі мІДнЦЙнХЬ м†РмЬЉл°Ь лѓЄл£®мЦі л≥імХД к∞АлК•мД±мЭі лЦ®мЦімІДлЛ§к≥† нХ† мИШ мЮИк≤†лЛ§[7].
кЈЄ мЩЄ л∞ФмЭілЯђмК§ лУ±мЬЉл°Ь мЭЄнХЬ к∞РмЧЉ нЫДмЭШ нЫДкЄ∞ нХ©л≥См¶ЭмЬЉл°Ь л∞ЬмГЭнХШмШАмЭД к≤љмЪ∞лПД мГЭк∞БнХі л≥Љ мИШ мЮИлЛ§. нХШмІАлІМ мЭілЯ∞ к≤љмЪ∞ лМАлґАлґД мЖМмХДмЧРмДЬ л∞ЬмГЭнХШл©∞, лМАк∞Ь нХЬ м™љ нПРмЧРлІМ л≥Сл≥АмЭі лВШнГАлВЬлЛ§лКФ м†РмЭі л≥Є м¶Эл°АмЩА лЛ§л•ілЛ§[8].
Mark лУ±мЭі кіАм∞∞нХЬ 31мШИмЭШ BIP м¶Эл°АлУ§мЭД л≥іл©і[3], BIPлКФ м°∞мІБнХЩм†Б мЦСмГБк≥Љ лНФлґИмЦі мЮДмГБ м¶ЭмГБ л∞П мШБмГБ мЖМк≤ђмЭі нПРмЗДмД± мДЄкЄ∞кіАмІАмЧЉ-кЄ∞мІИнЩФ нПРл†і нШємЭА нЖµмГБнШХ к∞ДмІИмД± нПРл†ік≥ЉлКФ к∞Бк∞Б кµђл≥ДлРШл©імДЬлПД лєДкµРм†Б м§Ск∞Д м†ХлПДмЭШ нКємІХмЭД мІАлЛМлЛ§к≥† л≥ік≥†нХШк≥† мЮИлЛ§. нПРмЗДмД± мДЄкЄ∞кіАмІАмЧЉ-кЄ∞мІИнЩФ нПРл†імЭА лєДкµРм†Б м†КмЭА 40лМА лШРлКФ 50лМАмЧРмДЬ л∞ЬмГЭнХШл©∞, лМАлґАлґДмЭі 2-3к∞ЬмЫФ м†ДмЧР л∞ЬмЧі, кЄ∞мє® лУ±мЭШ к∞РкЄ∞ л™ЄмВі м¶ЭмГБмЭілВШ нФЉл°Ь-мЗ†мХљк∞Р, м≤ім§С к∞РмЖМ лУ±мЭШ м¶ЭмГБмЬЉл°Ь мЛЬмЮСлРШмЦі мІДнЦЙнХЬлЛ§. мК§нЕМл°ЬмЭілУЬмЧР л∞ШмЭСмЭД мЮШнХШк≥†, мЮРмЧ∞м†БмЬЉл°Ь нШЄм†ДлРШлКФ к≤љмЪ∞лПД мЮИмЦі мШИнЫДлКФ мҐЛмЭА нОЄмЭілЛ§[1]. л∞Шл©і нЖµмГБнШХ к∞ДмІИмД± нПРл†імЭА м£Љл°Ь 50мДЄ мЭінЫДмЧР нШЄл∞ЬнХШл©∞, нЭ°мЧ∞놕к≥Љ кіАк≥Дк∞А мЮИк≥†, 1-2лЕДмЧР к±Єм≥Р лІМмД±м†БмЬЉл°Ь мДЬмДЬнЮИ мІДнЦЙнХШлКФ мІИнЩШмЬЉл°Ь мК§нЕМл°ЬмЭілУЬ мєШл£МмЧР л∞ШмЭСмЭі мҐЛмІА мХКмХД мК§нЕМл°ЬмЭілУЬл•Љ мВђмЪ©нХШмЧђлПД к∞ЭкіАм†БмЬЉл°Ь нШЄм†ДмЭД л≥імЭілКФ к≤љмЪ∞к∞А лУЬлђЉлЛ§[1]. BIP м¶Эл°А л≥ік≥†мЧР лФ∞л•іл©і[3], мЮДмГБ м¶ЭмГБмЬЉл°Ь нШЄнЭ° к≥§лЮАмЭі 18л™Е(69%)мЬЉл°Ь к∞АмЮ• нЭФнЦИмЬЉл©∞, лЛ®мИЬнЭЙлґАмВђмІД мЖМк≤ђмЧРмДЬлКФ к∞ДмІИ мЭМмШБ м¶Эк∞Ак∞А к∞АмЮ• нЭФнЮИ кіАм∞∞(43%)лРШмЧИк≥†, лЛ§мЭМмЬЉл°Ь мЦСмЄ° нПР кЄ∞м†АлґА лІЭмГБ мє®мЬ§мЭі нЭФнХШк≤М кіАм∞∞(28%)лРШмЧИлЛ§. нЭЙлґА м†ДмВ∞нЩФлЛ®мЄµміђмШБмЧРмДЬлКФ лМАлґАлґДмЧРмДЬ к∞ДмІИ л≥Сл≥АмЭі кіАм∞∞(78%)лРШмЧИмЬЉл©∞, лѓЄлІМнШХ к∞ДмЬ†л¶ђмЦС мЭМмШБмЭі нЭФнЮИ кіАм∞∞(39%)лРШмЧИк≥†, лІЭмГБ нПРнПђ лВі мє®мЬ§лПД лЛ§мЖМ кіАм∞∞(17%)лРШмЧИмЬЉлВШ, л≤МмІСл™®мЦС л≥АнШХмЭА лЛ®мІА нХЬ мШИ(5%)мЧРмДЬлІМ кіАм∞∞лРШмЧИлЛ§. мК§нЕМл°ЬмЭілУЬ мєШл£МмЧР лМАнХЬ л∞ШмЭСмЭД л≥іл©і, 12л™Е(63%)мЭШ нЩШмЮРмЧРмДЬлКФ нШЄм†ДмЭД л≥імШАк≥†, 1л™Е(5%)мЭА нБ∞ л≥АнЩФ мЧЖмЭі мХИм†Хм†БмЬЉл°Ь мЬ†мІАлРШмЧИмЬЉлВШ, 6л™Е(32%)мЭА мХЕнЩФлРШмЧИлЛ§к≥† л≥ік≥†нХШк≥† мЮИлЛ§[3].
л≥Є м¶Эл°АмЩА лєДкµРнХі л≥іл©і, нЩШмЮРлКФ 70мДЄмЧР к∞АкєМмЪі лВШмЭімЧР л∞Ьл≥СнХШмШАмІАлІМ, нЭ°мЧ∞놕мЭі мЧЖмЧИк≥†, мШБмГБнХЩм†БмЬЉл°ЬлКФ мЦСмЄ° нПР кЄ∞м†АлґА нШємЭА нПРм£Љл≥АлґАл°Ь мДЄкЄ∞кіАмІА нЩХмЮ•м¶ЭмЭД лПЩл∞ШнХЬ лІЭмГБ к≤∞м†ИнШХмЭШ л≥Сл≥Ак≥Љ к∞ДмЬ†л¶ђ мЭМмШБмЭі кіАм∞∞лРШмЧИмЬЉлВШ, л≤МмІС л™®мЦСмЭШ нПР мДђмЬ†нЩФлКФ кіАм∞∞лРШмІА мХКмХШлЛ§. нШЄнЭ°к≥§лЮАмЭі лєДкµРм†Б мХДкЄЙмД±мЬЉл°Ь мІДнЦЙнХЬ к≤Гк≥Љ мК§нЕМл°ЬмЭілУЬ мєШл£МмЧР лЪЬл†ЈнХЬ нШЄм†ДмЭА мЧЖмЬЉлВШ, мЮДмГБм¶ЭмГБ л∞П л∞©мВђмД† мЖМк≤ђмЭі лНФ мЭімГБ мХЕнЩФ мЧЖмЭі мЬ†мІАлРШк≥† мЮИлКФ м†РмЭА нПРмЗДмД± мДЄкЄ∞кіАмІА-кЄ∞мІИнЩФ нПРл†ік≥Љ нЖµмГБнШХ к∞ДмІИмД± нПРл†імЭШ м§Ск∞Дм†БмЭЄ нКємІХмЭД мІАлЛМ к≤ГмЬЉл°Ь мГЭк∞БлРШл©∞, мЭілКФ BIP 31мШИ л≥ік≥†л•Љ лґДмДЭнХЬ лВімЪ©к≥Љ мЭЉмєШнХЬлЛ§.
кЈЄлЯђлВШ BIPлКФ мХДмІБ нЩХл¶љлРЬ мІИнЩШмЭі мХДлЛИл©∞, мєШл£МмЧР лМАнХЬ л∞ШмЭСлПД лЛ§л•ік≥† мШИнЫДлПД лЛ§л•ілѓАл°Ь лЛ®мЭЉ мІИнЩШмЭілЭЉк≥† м†ХмЭШнХШкЄ∞мЧРлКФ мֳ놧мЫАмЭі мЮИлЛ§. л≥Є м¶Эл°АмЧРмДЬлПД нПРнПђ лВі кЄ∞мІИнЩФ нПРл†іл≥ілЛ§лКФ мДЄкЄ∞кіАмІАмЩА к∞ДмІИмЧР мЧЉм¶Эк≥Љ мДђмЬ†нЩФл•Љ нКємІХмЬЉл°Ь нХШлКФ л≥Сл≥АмЭі м£Љл°Ь л≥імШАмІАлІМ, нПРмЗДмД± мДЄкЄ∞кіАмІА-кЄ∞мІИнЩФ нПРл†ік≥Љ нЖµмГБнШХ к∞ДмІИмД± нПРл†імЭШ нКємІХм†БмЭЄ м°∞мІБ мЖМк≤ђмЭі нХ®кїШ кіАм∞∞лРШмЦі, мЭілКФ BIPмЭШ мЭЉлґА нКємД±мЭЉ мИШлПД мЮИк≥†, л≥АнШХлРЬ нШємЭА нКємЭім†Б нПРмЗДмД± мДЄкЄ∞кіАмІА-кЄ∞мІИнЩФ нПРл†імЭілВШ нЖµмГБнШХ к∞ДмІИмД± нПРл†і к∞АлК•мД±лПД мЮИлЛ§. нХЬнОЄ, мЖМмИШмЭШ м¶Эл°Ал•Љ л∞ФнГХмЬЉл°Ь нХЬ BIPмЭШ л≥ік≥†мЧРмДЬлКФ л∞ШмИШ мЭімГБмЭШ нЩШмЮРк∞А нШЄм†ДмЭД л≥імШАлЛ§к≥† нХШмШАлЛ§. л≥Є м¶Эл°АмЧРмДЬлПД мК§нЕМл°ЬмЭілУЬ мєШл£М нЫД м¶ЭмГБ нШЄм†ДмЭД л≥імЭік≥†, нШДмЮђкєМмІА мЮДмГБм†Б мХЕнЩФ мЧЖмЭі мХИм†Хм†Б к≤љк≥Љл•Љ мЬ†мІАнХШк≥† мЮИмЬЉл©∞, мєШл£М нЫД мґФм†Б нЭЙлґА к≥†нХімГБм†ДмВ∞нЩФлЛ®мЄµміђмШБмЧРмДЬ к≤∞м†И л∞П к∞ДмЬ†л¶ђмЭМмШБмЭі мХљк∞Д к∞РмЖМлРЬ мЖМк≤ђмЭД л≥імЭік≥† мЮИлЛ§. нХШмІАлІМ мЭілЯђнХЬ м†РлІМмЬЉл°Ь мєШл£М нЫД нШЄм†ДмЬЉл°Ь нМРлЛ®нХШкЄ∞мЧРлКФ лґИмґ©лґДнХШлЛ§. кЈЄлЯЉмЧРлПД лґИкµђнХШк≥† л≥Є м¶Эл°АмЭШ мЮДмГБмЦСмГБмЭі мГБкЄ∞ лСР мІИнЩШмЭШ мЦілКР м™љмЬЉл°ЬлПД мєШмЪ∞мєШмІА мХКк≥† м°∞мІБ мЖМк≤ђмЧРмДЬлКФ BIPмЭШ нКємІХм†БмЭЄ мЖМк≤ђлУ§мЭД л™®лСР нПђнХ®нХШк≥† мЮИмЦі BIPл°Ь мІДлЛ®нХ† мИШ мЮИмЭД к≤ГмЬЉл°Ь мГЭк∞БлРЬлЛ§.
мµЬкЈЉ лєДмКЈнХЬ м¶Эл°АмЧР лМАнХЬ кµ≠лВі л≥ік≥†к∞А мЮИмЧИмЬЉлВШ[9], л≥ік≥†лРЬ м¶Эл°АлКФ мК§нЕМл°ЬмЭілУЬ мєШл£М нЫДмЧР м°∞мІБк≤АмВђл•Љ мЛЬнЦЙнХШмШАлЛ§. мК§нЕМл°ЬмЭілУЬ лУ±мЭШ мХљлђЉмєШл£Мк∞А к∞ДмІИмД± нПРмІИнЩШмЭШ мІДлЛ®мЧР нБ∞ мШБнЦ•мЭі мЧЖлЛ§лКФ л≥ік≥†лПД мЮИмІАлІМ, лѓЄкµ≠нЭЙлґАнХЩнЪМ/мЬ†лЯљнЭЙлґАнХЩнЪМмЧРмДЬлКФ мІИл≥СмЭШ лІРкЄ∞лВШ мєШл£М нЫДмЧРлКФ мИШмИ†м†Б мГЭк≤АмЭі лПДмЫАмЭі лРШмІА л™їнХЬлЛ§к≥† нХШмЧђ мєШл£М м†ДмЧР м°∞мІБк≤АмВђл•Љ нХШлПДл°Э кґМмЬ†нХШк≥† мЮИмЬЉл©∞, мЛ§м†Ьл°Ь мК§нЕМл°ЬмЭілУЬ мєШл£М нЫДмЧР м°∞мІБнШХмЭі л∞ФлАР к≤љмЪ∞мЭШ л≥ік≥†лПД мЮИлЛ§[10].
л≥Є м¶Эл°АлКФ нПР мГЭк≤А к≤∞к≥ЉмЩА нХ®кїШ мК§нЕМл°ЬмЭілУЬмЩА л©імЧ≠мЦµм†Ьм†Ь мВђмЪ© нЫД 1лЕД 6к∞ЬмЫФк∞ДмЭШ мґФм†БкіАм∞∞мЧРмДЬ мЮДмГБ м¶ЭмГБк≥Љ л∞©мВђмД† мЖМк≤ђмЭі мХИм†Хм†БмЭЄ мГБнГЬл•Љ л≥імЭік≥† мЮИлКФ м†РмЭД л∞ФнГХмЬЉл°Ь BIPл°Ь мІДлЛ®нХШлКФ к≤ГмЭі нХ©лЛєнХШк≤†лЛ§. BIPлЭЉлКФ мІИнЩШкµ∞мЭі мЖМмИШмЭШ м¶Эл°Ал•Љ л∞ФнГХмЬЉл°Ь мµЬкЈЉмЧР м†ЬмЛЬлРЬ к≤ГмЭімЦімДЬ нКєл∞ЬмД± к∞ДмІИмД± нПРл†імЭШ мЖМкЈЄл£ємЬЉл°Ь лґДл•ШлРШкЄ∞ мЬДнХімДЬлКФ м°∞кЄИ лНФ мґФк∞Ам†БмЭЄ мЧ∞кµђк∞А нХДмЪФнХШк≤†мІАлІМ лґДл•ШлРШмІА мХКлКФ к∞ДмІИмД± нПРмІИнЩШ м§СмЧРмДЬ л≥Є м¶Эл°АмЩА лєДмКЈнХЬ мЖМк≤ђмЭД к∞АмІД к≤љмЪ∞ BIPмЭШ мІДлЛ®мЭД к≥†л†§нХі л≥Љ мИШ мЮИмЭД к≤ГмЬЉл°Ь мГЭк∞БлРЬлЛ§.





 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






