м„ң лЎ
кі мЈјнҢҢ м—ҙм№ҳлЈҢлҠ” мҲҳмҲ мқ„ н• мҲҳ м—ҶлҠ” к°„м„ёнҸ¬м•” нҷҳмһҗм—җкІҢм„ң көӯмҶҢм ҒмңјлЎң мў…кҙҙлҘј м№ҳлЈҢн•ҳкё° мң„н•ҙ нҡЁкіјм Ғмқё мӢңмҲ лЎң м•Ңл Өм ё мһҲмңјлӮҳ[1], мөңк·ј мӢңмҲ мқҳ мҰқк°ҖлЎң н•©лі‘мҰқм—җ лҢҖн•ң л¬ём ңлҸ„ м ңкё°лҗҳм–ҙ мҷ”лӢӨ.
кі мЈјнҢҢ м—ҙм№ҳлЈҢ нӣ„ л°ңмғқн• мҲҳ мһҲлҠ” н•©лі‘мҰқмқҖ нҒ¬кІҢ кі мЈјнҢҢ м—ҙм№ҳлЈҢ мӢң м „к·№мқҳ мң„м№ҳм—җ мқҳн•ң кІғкіј м—ҙмҶҗмғҒм—җ мқҳн•ң кІғмңјлЎң лӮҳлҲҢ мҲҳ мһҲлӢӨ. м „мһҗм—җлҠ” к°җм—ј, м¶ңнҳҲ, мў…м–‘м„ёнҸ¬мқҳ нҢҢкёүкіј кё°нқү л“ұмқҙ мһҲкі , нӣ„мһҗм—җлҠ” мқём ‘ мһҘкё°мқҳ мҶҗмғҒ л°Ҹ м ‘м§Җ к·№м—җ мқҳн•ң нҷ”мғҒмқҙ мһҲлӢӨ[2]. к·ёмӨ‘ к°„лҶҚм–‘мқҖ мЈјмҡ” н•©лі‘мҰқ мӨ‘ к°ҖмһҘ нқ”н•ң кІғмңјлЎң м•Ңл Өм ё мһҲмңјл©°[3], л“ңл¬јкІҢ лӢҙкҙҖкіј мң„мһҘкҙҖ мӮ¬мқҙм—җ лҲ„кіөмқҙ мғқкёё мҲҳлҸ„ мһҲлӢӨ[1].
лҳҗн•ң к°„лҶҚм–‘ мһҗмІҙмқҳ н•©лі‘мҰқмңјлЎң нҡЎкІҪл§ү л°Ҹ к°„ н•ҳл¶Җ лҶҚм–‘, ліөл§үм—ј л“ұмқҙ нқ”нһҲ л°ңмғқн• мҲҳ мһҲмңјлӮҳ, л“ңл¬јкІҢ нӣ„ліөл§ү, мң„, мҶҢмһҘ л“ұмңјлЎң лҲ„кіөмқ„ нҳ•м„ұн•ң ліҙкі к°Җ мһҲкі лҢҖмһҘм—җм„ң лҲ„кіөмқ„ нҳ•м„ұн•ң ліҙкі к°Җ мһҲлӢӨ[4].
м Җмһҗл“ӨмқҖ к°„м„ёнҸ¬м•” м№ҳлЈҢлЎң кі мЈјнҢҢ м—ҙм№ҳлЈҢ нӣ„ к°„лҶҚм–‘мқҙ л°ңмғқн•ҳм—¬ н•ӯмғқм ң м№ҳлЈҢ мӨ‘ м—ҙк°җ л°Ҹ мҳӨн•ңмқҙ мһҲм–ҙ л°ңкІ¬н•ң к°„лҢҖмһҘ лҲ„кіө 1мҳҲлҘј кІҪн—ҳн•ҳкі м№ҳлЈҢн•ҳмҳҖкё°м—җ л¬ён—Ңкі м°°кіј к°ҷмқҙ ліҙкі н•ҳлҠ” л°”мқҙлӢӨ.
мҰқ лЎҖ
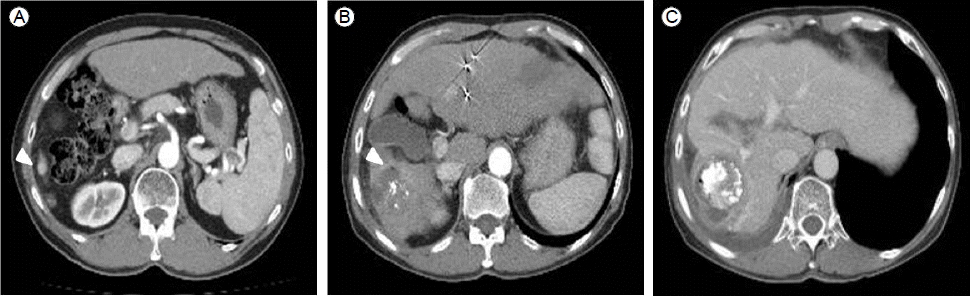
2л…„ м „ Bнҳ• к°„м—ј л°”мқҙлҹ¬мҠӨм—җ мқҳн•ң к°„кІҪліҖкіј к°„м„ёнҸ¬м•”мқ„ 진лӢЁл°ӣмқҖ 58м„ё лӮЁмһҗк°Җ м—ҙк°җкіј мҳӨн•ңмқ„ мЈјмҶҢлЎң лӮҙмӣҗн•ҳмҳҖлӢӨ. к°„м„ёнҸ¬м•”мқҖ 진лӢЁ лӢ№мӢң 6лІҲкіј 7лІҲ к°„ кө¬м—ӯм—җ кұём№ң м•Ҫ 5 Г— 4.7 cm нҒ¬кё°мқҳ мў…кҙҙмҳҖкі мЈјліҖ лҰјн”„м Ҳ м „мқҙлӮҳ мӣҗл°ңмһҘкё°лЎңмқҳ м „мқҙлҠ” м—Ҷм—Ҳмңјл©°, лӢ№мӢң Child Pugh score A, 6м җмңјлЎң кІҪлҸҷл§Ҙ нҷ”н•ҷмғү м „мҲ мқ„ 진лӢЁ лӢ№мӢңмҷҖ 6к°ңмӣ” л’Ө 2нҡҢ мӢңн–үмқ„ н•ҳмҳҖлӢӨ. 추м ҒкІҖмӮ¬мӨ‘ 1л…„ 9к°ңмӣ” л’Ө мӢңн–үн•ң к°„ м—ӯлҸҷм„ұ CTм—җм„ң к°„мҡ°м—Ҫмқҳ мІЁлӢЁкіјмўҢ мҷёмёЎкө¬м—ӯм—җ лҸҷл§Ҙкё°м—җ мЎ°мҳҒмҰқк°•мқҙ лҗҳкі м§Җм—°кё°м—җ мЎ°мҳҒк°җмҶҢк°Җ лҗҳлҠ” кІ°м Ҳмқҙ л°ңкІ¬лҗҳм—ҲлӢӨ(к°Ғк°Ғ м§ҒкІҪ 8 mm, 1 cm). к°Ғ кІ°м Ҳм—җ лҢҖн•ҳм—¬ кі мЈјнҢҢ м—ҙм№ҳлЈҢлҘј мӢңн–үн•ҳмҳҖкі , лӢ№мӢң кёүм„ұ н•©лі‘мҰқмқҖ л°ңмғқн•ҳм§Җ м•Ҡм•ҳлӢӨ(Fig. 1A). 2к°ңмӣ” л’Ө мӢңн–үн•ң CTм—җм„ң 3лІҲк°„ кө¬м—ӯм—җ к°„м„ёнҸ¬м•”мқҳ мһ¬л°ңмқҙ мқҳмӢ¬мқҙ лҗҳлҠ” кІ°м Ҳмқҙ мһҲм–ҙ лӢӨмӢң кі мЈјнҢҢ м—ҙм№ҳлЈҢлҘј мӢңн–үн•ҳмҳҖкі , 6лІҲ к°„ кө¬м—ӯм—җм„ң л¶Ҳк·ңм№ҷн•ң кІҪкі„мқҳ м ҖмқҢмҳҒ л¶Җмң„мҷҖ лҜёлҹүмқҳ кіөкё°мқҢмҳҒмқҙ мһҲм—ҲмңјлӮҳ(Fig. 1B), нҠ№мқҙ мҰқмғҒ л°Ҹ мҰқнӣ„к°Җ м—Ҷм–ҙ, кІҪкіјкҙҖм°°н•ҳмҳҖкі кі мЈјнҢҢ м—ҙм№ҳлЈҢ нӣ„ нҠ№мқҙ кёүм„ұ н•©лі‘мҰқмқҙ м—Ҷмқҙ нҮҙмӣҗн•ҳмҳҖлӢӨ. 2к°ңмӣ” л’Ө мҷёлһҳл°©л¬ёмӢң нҷңл Ҙ징нӣ„лҠ” м•Ҳм •м Ғмқҙм—ҲмңјлӮҳ к°„н—җм Ғмқё л°ңм—ҙкіј мҳӨн•ңмқ„ нҳёмҶҢн•ҳм—¬ к°„ м—ӯлҸҷм„ұ CTлҘј мҙ¬мҳҒн•ҳмҳҖлӢӨ. к°„мҡ°м—Ҫмқҳ мІЁлӢЁм—җ лҸҷл§Ҙкё°м—җ мЎ°мҳҒк°җмҶҢ л°Ҹ кіөкё°мқҢмҳҒмқҙ мһҲкі мЈјліҖл¶Җ кІҪкі„к°Җ мһҲлҠ” к°„ лҶҚм–‘мқҙ л°ңкІ¬лҗҳм–ҙ(Fig. 1C) н•ӯмғқм ңлҘј 2к°ңмӣ”к°„ мӮ¬мҡ© нӣ„ мҷёлһҳ추м Ғмқ„ н•ҳмҳҖлӢӨ.
мқҙнӣ„ нҷҳмһҗмқҳ нҷңл Ҙ징нӣ„лҠ” м•Ҳм •м Ғмқҙм—ҲмңјлӮҳ мқҙн•ҷм Ғ кІҖмӮ¬м—җм„ң мҡ°мғҒліөл¶Җ м••нҶөмқҙ мһҲм—Ҳкі , к°„н—җм ҒмңјлЎң мҡ°мғҒліөл¶Җ нҶөмҰқ, мҳӨн•ңкіј л°ңм—ҙмқҙ мһҲм–ҙ лҶҚм–‘мқҳ м№ҳлЈҢ м—¬л¶ҖмҷҖ к°„м„ёнҸ¬м•”мқҳ мһ¬л°ң м—¬л¶ҖлҘј нҷ•мқён•ҳкё° мң„н•ҙ нҳҲм•ЎкІҖмӮ¬мҷҖ к°„ м—ӯлҸҷм„ұ CTлҘј мҙ¬мҳҒн•ҳмҳҖлӢӨ. нҳҲм•ЎкІҖмӮ¬м—җм„ң л°ұнҳҲкө¬ 5,300/uL, нҳҲмғүмҶҢ 11.6 g/dL, Hematocrit 34.6%, нҳҲмҶҢнҢҗ 167,000/uL, мҙқ лӢЁл°ұ 8.23 g/dL, м•Ңл¶ҖлҜј 3.17 g/dL, мҙқ л№ҢлҰ¬лЈЁл№Ҳ 0.83 mg/dL, AST 48 IU/L, ALT 52 IU/L, prothrombin time INR 1.19, BUN 11.0 mg/dL, creatinine 0.86 mg/dL, sodium 129 mmol/L, potassium 3.74 mmol/L, chloride 98.4 mmol/L, м•ҢнҢҢ нғңм•„лӢЁл°ұ 40.51 ng/mL, CRP 6.9 mg/dL, Entamoeba histolytica IgGлҠ” мқҢм„ұмқҙм—ҲлӢӨ. нҷҳмһҗмқҳ к°„кё°лҠҘмқҖ Child Pugh score 6м җмңјлЎң м–‘нҳён•ҳмҳҖмңјл©°, CRPмқҳ мҰқк°ҖлҠ” к°җм—јмқҙ мһҲмқҢмқ„ мӢңмӮ¬н•ҳмҳҖлӢӨ.
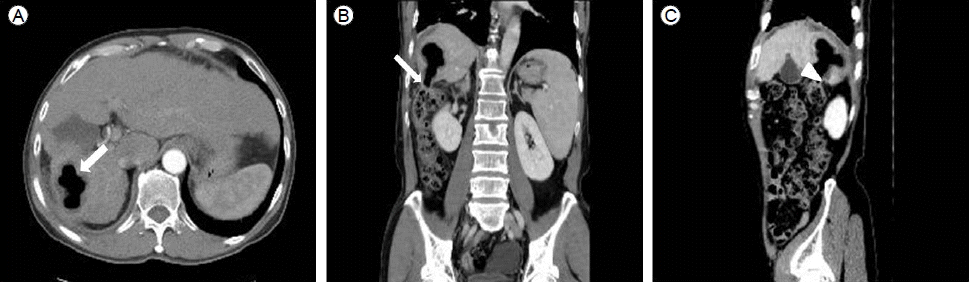
к°„ м—ӯлҸҷм„ұ CTм—җм„ң к°„ мӢӨм§ҲлЎң л‘ҳлҹ¬мӢём—¬ мһҲкі кіөкё°мқҢмҳҒмңјлЎң кҙҖм°°лҗҳлҠ” кіөк°„мқҙ 6лІҲ к°„ кө¬нҡҚм—җм„ң л°ңкІ¬лҗҳм—ҲлӢӨ(Fig. 2). мқҙлҠ” лҢҖмһҘ к°„л§ҢкіЎл¶ҖмҷҖ мқём ‘н•ҙ мһҲм–ҙм„ң к°„лҢҖмһҘлҲ„кіөмқҙ мқҳмӢ¬лҗҳм—Ҳкі мқҙлҘј нҷ•мқён•ҳкё° мң„н•ҳм—¬ лҢҖмһҘлӮҙмӢңкІҪ л°Ҹ нҳ•кҙ‘нҲ¬мӢңлІ•мқ„ мқҙмҡ©н•ҳмҳҖлӢӨ.
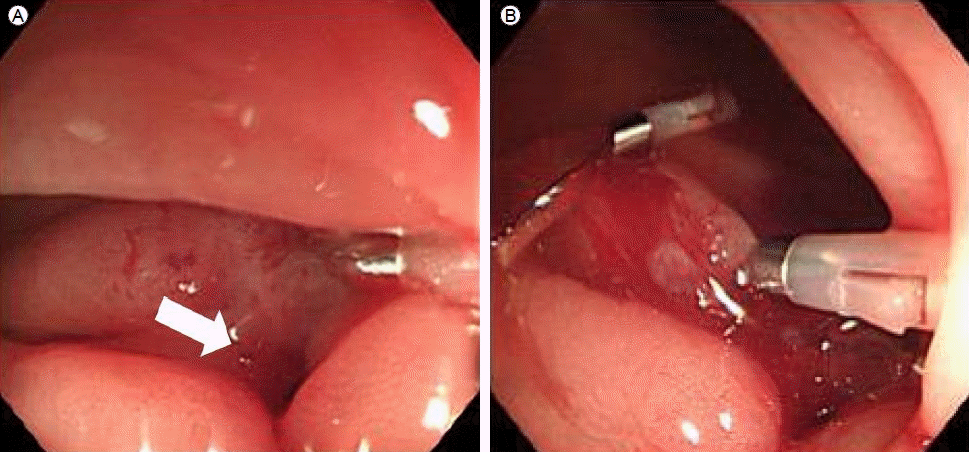
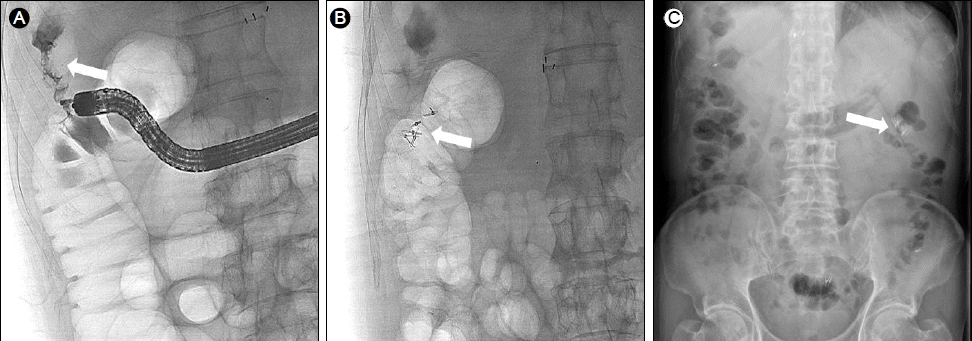
лЁјм Җ лҢҖмһҘлӮҙмӢңкІҪмңјлЎң к°„л§ҢкіЎл¶Җм—җ м ‘к·јн•ҳмҳҖкі кіөкё°л°©мҡёмқҙ ліҙмқҙлҠ” лҲ„кіөмқҙ ліҙм—¬ к°ҖмҠӨнҠёлЎңк·ёлқјн•Җмқ„ лҲ„кіөм—җ мӮ¬м¶ңн•ҳмҳҖкі , мЎ°мҳҒм—җм„ңлҸ„ к°„кіј м—°кІ°лҗҳлҠ” кёёкіј CTмғҒ ліҙмқҙлҠ” кіөлҸҷл¶Җмң„м—җ мЎ°мҳҒм ңк°Җ м°ЁлҠ” кІғмқ„ нҷ•мқён•ҳм—¬ к°„лҢҖмһҘлҲ„кіөмқҙ мһҲмқҢмқ„ 진лӢЁн•ҳмҳҖлӢӨ(Figs. 3 and 4). лӮҙмӢңкІҪм Ғмқё мІҳм№ҳлЎң hemoclipingмқ„ 5нҡҢ мӢңлҸ„н•ҳмҳҖмңјлӮҳ лҲ„кіө мЈјліҖ л¶Җмң„к°Җ лӢЁлӢЁн•ҳм—¬ л‘җ к°ңл§Ң clipingм—җ м„ұкіөн•ҳмҳҖлӢӨ. лӢӨмқҢ лӮ лӢЁмҲң ліөл¶Җ мҙ¬мҳҒмқ„ мӢңн–үн•ҳмҳҖмңјлӮҳ л‘җ к°ңмқҳ clipлҸ„ л–Ём–ҙ진 кІғмңјлЎң нҢҗлӢЁлҗҳм–ҙ(Fig. 4), кёҲмӢқкіј н•ӯмғқм ң мӮ¬мҡ©мқ„ м§ҖмҶҚн•ҳкі мҷёкіјмҷҖ нҳ‘진н•ҳм—¬ лҲ„кіө м Ҳм ңмҲ л°Ҹ 6лІҲ к°„ кө¬нҡҚ м Ҳм ңмҲ нҳ№мқҖ к°„мҡ°м—Ҫмқҳ мІЁлӢЁ м Ҳм ңмҲ мқ„ мӢңн–үн•ҳл Ө н•ҳмҳҖмңјлӮҳ ICG R15мӢңн–ү кІ°кіј 27%лЎң мҲ нӣ„ к°„л¶Җм „мқҳ л°ңмғқк°ҖлҠҘм„ұмқ„ кі л Өн•ҳм—¬ м „мӢ л§Ҳм·Ё л°Ҹ ліөк°•кІҪ мӮҪмһ…н•ҳм—җ лҲ„кіө м Ҳм ңмҲ л°Ҹ мғҒн–үкІ°мһҘ мҗҗкё° м Ҳм ңмҲ мқ„ мӢңн–үн•ҳмҳҖлӢӨ.
мҲҳмҲ мҶҢкІ¬м—җм„ң мғҒн–үкІ°мһҘмқҳ к°„л§ҢкіЎл¶ҖмҷҖ 6лІҲ к°„ кө¬нҡҚ мӮ¬мқҙм—җ м§ҖлҰ„ 3 cm нҒ¬кё°мқҳ лӮӯм„ұ кіөлҸҷмқҙ мһҲкі лҢҖл§қмқҙ л°Җл Ө кіөлҸҷмқ„ мұ„мҡ°кі мһҲм—Ҳмңјл©°, мҗҗкё° м Ҳм ңмҲ мқ„ мӢңн–үн•ң мғҒн–ү кІ°мһҘм—җ лҲ„кіөкҙҖмқҙ кҙҖм°°лҗҳм—ҲлӢӨ. мЎ°м§ҒкІҖмӮ¬мғҒ мғҒн–үкІ°мһҘ мЎ°м§Ғмқҳ м „лІҪмёөмқҳ к¶Өм–‘кіј м§Җл°© кҙҙмӮ¬ мҶҢкІ¬мқҙ ліҙмҳҖкі мқҙлҠ” лҲ„кіөкіј мқјм№ҳн•ҳлҠ” мҶҢкІ¬мқҙм—ҲлӢӨ. нҷҳмһҗлҠ” мқҙнӣ„ м•Ҳм •лҗҳм–ҙ нҮҙмӣҗн•ҳмҳҖкі , нҳ„мһ¬ мҷёлһҳ 추м Ғ мӨ‘мқҙлӢӨ.
кі м°°
кі мЈјнҢҢ м—ҙм№ҳлЈҢлҠ” 1996л…„ мІҳмқҢмңјлЎң к°„м„ёнҸ¬м•”м—җм„ң мқҙмҡ©лҗң нӣ„ мҲҳмҲ мқҙ л¶Ҳк°ҖлҠҘн•ң к°„м„ёнҸ¬м•” нҷҳмһҗм—җкІҢм„ң нҡЁкіјм Ғмқё м№ҳлЈҢлІ•мңјлЎң к°Ғкҙ‘л°ӣкі мһҲкі [1], көӯмҶҢм ҒмңјлЎң л°ңмғқн•ҳкі нҒ¬кё°к°Җ мһ‘мқҖ кІҪмҡ°м—җ м Ғмқ‘мҰқмқҙ лҗ мҲҳ мһҲм–ҙ, к°„мў…м–‘мқҳ көӯмҶҢм Ғ м№ҳлЈҢмӢң м„ұкіјк°Җ лҶ’мқҖ кІғмңјлЎң м•Ңл Өм ё мһҲлӢӨ. н•ҳм§Җл§Ң мӢңмҲ кіј м—°кҙҖлҗң н•©лі‘мҰқмқҙ м—¬лҹ¬ м°ЁлЎҖ ліҙкі лҗҳм—ҲлӢӨ.
Livraghi л“ұ[5]мқҖ лӢӨкё°кҙҖ м—°кө¬м—җм„ң 2,320лӘ…мқҳ нҷҳмһҗм—җм„ң 6мҳҲ(0.3%)мқҳ мӮ¬л§қмқҙ мһҲм—Ҳкі 50мҳҲ(2.2%)м—җм„ң ліөк°•лӮҙ м¶ңнҳҲ, мў…м–‘мқҳ нҢҢмў…, к°„лҶҚм–‘, мһҘмІңкіөмқҳ мЈјмҡ” н•©лі‘мҰқмқ„ ліҙкі н•ҳмҳҖлӢӨ. 2001л…„ Rhim л“ұ[6]мқҖ көӯлӮҙ нҷҳмһҗ 1,520мҳҲмқҳ кі мЈјнҢҢ м—ҙ м№ҳлЈҢ нӣ„ л°ңмғқн•ң мЈјмҡ” н•©лі‘мҰқмқ„ ліҙкі н•ҳмҳҖлҠ”лҚ° мӨ‘ к°„лҶҚм–‘мқҙ 10мҳҲ(0.66%)лЎң мЈјмҡ” к°ҖмһҘ нқ”н•ҳмҳҖмңјл©°, лӢҙкҙҖмң„мһҘлҲ„кіө, лӢҙкҙҖлҲ„кіө, лӢҙкҙҖнқүл§үлҲ„кіө л“ұмқҙ мһҲм—ҲлӢӨ. к·ёлҹ¬лӮҳ көӯлӮҙм—җм„ң к°„лҢҖмһҘлҲ„кіөмқҳ л°ңмғқмқҖ кұ°мқҳ ліҙкі лҗҳм§Җ м•Ҡм•ҳлӢӨ.
к°„лҶҚм–‘мңјлЎң мқён•ң к°„лҢҖмһҘлҲ„кіөмқҳ л°ңмғқмқҖ л§Өмҡ° л“ңл¬јлӢӨ. ліёмӣҗм—җм„ңлҠ” мқҙл¬јм§Ҳм—җ мқҳн•ң к°„лҢҖмһҘлҲ„кіөкіј м—¬кё°м„ң м—ӯн–үм„ұ к°җм—јмңјлЎң к°„лҶҚм–‘мқҙ л°ңмғқн•ң кІҪмҡ°к°Җ мһҲм—ҲмңјлӮҳ[7], л°ҳлҢҖмқҳ кІҪмҡ°лҠ” м§ҖкёҲк№Ңм§Җ ліҙкі лҗң л°”к°Җ л§Өмҡ° м ҒмқҖ кІғмңјлЎң м•Ңл Өм ё мһҲлӢӨ. нҠ№нһҲ нҷ”лҶҚм„ұ к°„лҶҚм–‘м—җм„ң көӯмҶҢ н•©лі‘мҰқмңјлЎң мқём ‘мһҘкё°мҷҖ к°„ мӮ¬мқҙм—җ лҲ„кіөмқҙ мғқкё°лҠ” кІғмқҖ л§Өмҡ° л“ңл¬ё мқјмқҙкі , лҶҚм–‘мқҳ нҢҢм—ҙм—җ мқҳн•ң ліөл§үм—јмқҙ л№ҲлІҲн•ҳкІҢ л°ңмғқн•ңлӢӨ[8]. н•ҳм§Җл§Ң м•„л©”л°”м„ұ к°„лҶҚм–‘мқҳ кІҪмҡ° к°„лҶҚм–‘мқҳ нҢҢм—ҙкіј мқём ‘мһҘкё°лЎңмқҳ мІңкіөмқҙ н•©лі‘мҰқмңјлЎң л°ңмғқн• мҲҳ мһҲлӢӨкі м•Ңл Өм ё мһҲлӢӨ[9].
к°„лҶҚм–‘мқҙ мқҳмӢ¬лҗҳлҠ” нҷҳмһҗм—җм„ң мҳҒмғҒкІҖмӮ¬ мӢң кіөкё°мқҢмҳҒмқҙ к°„м—җм„ң кҙҖм°°лҗңлӢӨл©ҙ к°ҖмҠӨнҳ•м„ұк· мқҳ к°җм—ј, к°„кё°кҙҖм§ҖлҲ„кіөкіј к°„мһҘлҲ„кіөмқҳ л°ңмғқмқ„ кі л Өн•ҙм•ј н•ңлӢӨ[8]. мқҙ мҰқлЎҖм—җм„ңлҠ” к°„ м—ӯлҸҷм„ұ CTкІ°кіј 6лІҲ к°„ кө¬нҡҚм—җ кі мЈјнҢҢ м—ҙм№ҳлЈҢ нӣ„ к°ҷмқҖ мң„м№ҳм—җ к°„лҶҚм–‘мқҙ л°ңмғқн•ҳмҳҖкі , мҶҢлҹүмқҳ кіөкё°мқҢмҳҒмқҙ мһҲм§Җл§Ң мӢңмҲ нӣ„ л‘җ лӢ¬к°„ нҠ№мқҙ мҰқмғҒмқҙ м—Ҷм—Ҳкі , к°„лҢҖмһҘлҲ„кіөмқ„ лӘ…л°ұнһҲ мқҳмӢ¬н• л§Ңн•ң мҳҒмғҒмҶҢкІ¬мқҙ м•„лӢҲм—Ҳкё° л•Ңл¬ём—җ к°ҖмҠӨнҳ•м„ұк· м—җ мқҳн•ң лҶҚм–‘л°ңмғқмқ„ лЁјм Җ мғқк°Ғн•ҳмҳҖкі л‘җ лӢ¬к°„ н•ӯмғқм ңлҘј мӮ¬мҡ©н•ҳмҳҖм§Җл§Ң, к°„н—җм Ғмқё л°ңм—ҙкіј мҡ°мғҒліөл¶Җ ліөнҶөмқҙ мһҲм–ҙ CT кІҖмӮ¬ кІ°кіј лҲ„кіөмқ„ нҷ•мқён•ҳмҳҖлӢӨ.
мқҙ нҷҳмһҗм—җм„ң лҲ„кіөмқҳ л°ңмғқкё°м „мқҖ м„ё к°Җм§ҖлЎң мғқк°Ғн•ҙ ліј мҲҳ мһҲлӢӨ. мІ«м§ёлҠ” кі мЈјнҢҢ м—ҙм№ҳлЈҢм—җ мқҳн•ң м§Ғм ‘м Ғмқё мҶҗмғҒмқҳ к°ҖлҠҘм„ұмқҙлӢӨ. л§Ңмқј мһҘмІңкіөмқҙ м ҖлӘ…н–ҲлӢӨл©ҙ, кёүм„ұмңјлЎң мҰқмғҒмқҙ л°ңмғқн•ҳмҳҖмқ„ кІғмқҙкі ліөл§үмһҗк·№ мҰқмғҒмқҙлӮҳ мһҗмң кіөкё°мқҢмҳҒмқҙ мҳҒмғҒкІҖмӮ¬м—җм„ң л°ңкІ¬лҗҳм—Ҳмқ„ кІғмқҙлӢӨ. к·ёл Үм§Җл§Ң мқҙ нҷҳмһҗм—җм„ңлҠ” мғҒкё° мҰқмғҒмқҙлӮҳ кІҖмӮ¬ мҶҢкІ¬мқҙ м—Ҷм—ҲмңјлҜҖлЎң лҢҖмһҘмқҳ лҜём„ёмІңкіө к°ҖлҠҘм„ұмқ„ мғқк°Ғн•ҙ ліј мҲҳ мһҲкі , мқҙлЎң мқён•ң көӯмҶҢ н•©лі‘мҰқмңјлЎң к°„лҢҖмһҘлҲ„кіөмқҙ л°ңмғқн•ҳкі м—ӯн–үм„ұ к°җм—јмңјлЎң к°„лҶҚм–‘мқҙ л°ңмғқн• к°ҖлҠҘм„ұмқҙ мһҲлӢӨ. л‘җ лІҲм§ёлҠ” к°„лҶҚм–‘кіј к°„лҢҖмһҘлҲ„кіөмқҙ лӘЁл‘җ кі мЈјнҢҢ м—ҙ м№ҳлЈҢм—җ мқҳн•ҙм„ң л°ңмғқн• к°ҖлҠҘм„ұмқҙлӢӨ. к·ёлҹ¬лӮҳ мҳҒмғҒ кІҖмӮ¬ мҶҢкІ¬мқ„ нҶ лҢҖлЎң мғқк°Ғн–Ҳмқ„ л•Ң к°„лҢҖмһҘлҲ„кіөмқҳ нҳ•м„ұмқҙ к°„лҶҚм–‘мқҳ л°ңмғқліҙлӢӨ мқҙм „м—җ л°ңмғқн–Ҳмқ„ к°ҖлҠҘм„ұмқҙ лҶ’лӢӨкі мғқк°Ғн•ңлӢӨ. л§Ҳм§Җл§үмңјлЎң к°„лҶҚм–‘мқҙ лЁјм Җ л°ңмғқн•ҳкі к°„лҶҚм–‘мқҳ м–ҮмқҖ лІҪмқҳ кҙҙмӮ¬лЎң к°„лҢҖмһҘлҲ„кіөмқҙ л°ңмғқн–Ҳмқ„ кІҪмҡ°лҸ„ кі л Өн•ҙ ліј мҲҳ мһҲкІ лӢӨ. мң„м—җм„ң м–ёкёүн•ң к°„лҢҖмһҘ лҲ„кіөмқҳ л°ңмғқ кё°м „мқ„ мғқк°Ғн•ҙ ліј л•Ң, мқҙ нҷҳмһҗм—җм„ңлҠ” к°„ м—ӯлҸҷ CTм—җм„ң лҲ„кіөмқҳ нҳ•м„ұліҙлӢӨ к°„лҶҚм–‘мқҳ л°ңмғқмқҙ лЁјм Җ нҷ•мқёлҗҳм—Ҳкі мқҙнӣ„ л‘җ лӢ¬ нӣ„ CTм—җм„ң лӘ…нҷ•н•ң лҢҖмһҘлҲ„кіөмқҙ л°ңкІ¬лҗҳм—ҲмңјлҜҖлЎң, к°ҖмҠӨнҳ•м„ұк· м—җ мқҳн•ң лҶҚм–‘мқҙ 1к°ңмӣ” мқҙмғҒ м§ҖмҶҚлҗҳкі к·ёлЎң мқён•ң к°„лҶҚм–‘лІҪмқҳ кҙҙмӮ¬лЎң к°„лҢҖмһҘлҲ„кіөмқҙ л°ңмғқн•ң кІғмңјлЎң м¶”м •н• мҲҳ мһҲм—ҲлӢӨ.
мқҙ мҰқлЎҖлҠ” кі мЈјнҢҢ м—ҙм№ҳлЈҢ нӣ„ 2к°ңмӣ”к°„ лҢҖмһҘ мҶҗмғҒм—җ мқҳн•ң мҰқмғҒмқҙ м—Ҷм—Ҳкі , 추м ҒкІҖмӮ¬н•ң CTм—җм„ңлҸ„ к°„лҶҚм–‘мқҳ л°ңмғқмқҖ кҙҖм°°лҗҳм—ҲмңјлӮҳ лҢҖмһҘмқҳ мҶҗмғҒмқ„ мқҳмӢ¬н• мҲҳ мһҲлҠ” мҶҢкІ¬мқҙ м—Ҷм–ҙ лҢҖмһҘ мҶҗмғҒм—җ мқҳн•ң к°„лҶҚм–‘ліҙлӢӨлҠ” кі мЈјнҢҢ м—ҙм№ҳлЈҢм—җ мқҳн•ң нҷ”лҶҚм„ұ к°„лҶҚм–‘мқҳ н•©лі‘мҰқмңјлЎң к°„лҢҖмһҘлҲ„кіөмқҙ л°ңмғқн•ң кІғмңјлЎң м¶”м •лҗҳм—Ҳмңјл©°, н•ӯмғқм ң мӮ¬мҡ©мңјлЎң к°җм—јм—җ мқҳн•ң мҰқмғҒ л°Ҹ 징нӣ„к°Җ к°җм¶°м ё мқҙлҘј 진лӢЁн•ҳлҠ” лҚ° мӢңк°„мқҙ м§ҖмІҙлҗҳм—ҲлҚҳ кІғмңјлЎң мғқк°ҒлҗңлӢӨ. лҳҗн•ң к°ҖлҠҘм„ұмқҖ м Ғм§Җл§Ң мҲҳмҲ мҶҢкІ¬м—җм„ң лҢҖл§қмқҙ к°„лҶҚм–‘мқҙ мһҲлҚҳ кіөлҸҷм—җ л“Өм–ҙк°Җ мһҲлҚҳ кІғмңјлЎң ліҙм•„ мҳҒмғҒкІҖмӮ¬к°Җ к°„лҢҖмһҘлҲ„кіөмқҳ л°ңкІ¬м—җ мӢӨнҢЁн–Ҳмқ„ к°ҖлҠҘм„ұлҸ„ мғқк°Ғн•ҙ ліј мҲҳ мһҲлӢӨ.
кі мЈјнҢҢ м—ҙм№ҳлЈҢлҠ” 비көҗм Ғ м•Ҳм „н•ң мӢңмҲ лЎң м•Ңл Өм ё мһҲлӢӨ. н•ҳм§Җл§Ң 진лӢЁкё°мҲ мқҳ л°ңм „мңјлЎң к°„м„ёнҸ¬м•”мқҳ 진лӢЁмңЁмқҙ лҶ’м•„м§Җкі мһҲкі , кі мЈјнҢҢ м—ҙм№ҳлЈҢк°Җ к°„м„ёнҸ¬м•”мқҳ м№ҳлЈҢлЎң л§Һмқҙ лҸ„мһ…лҗҳкі мһҲмңјлҜҖлЎң к°„лҢҖмһҘлҲ„кіөмқҙ к·№нһҲ л“ңл¬ё н•©лі‘мҰқмқјм§ҖлқјлҸ„ к°„лҶҚм–‘мқҙ л°ңмғқн–Ҳмқ„ кІҪмҡ°м—җлҠ” мқҳмӢ¬н• н•„мҡ”к°Җ мһҲмқ„ кІғмңјлЎң мғқк°ҒлҗңлӢӨ.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






