 |
 |
| Korean J Med > Volume 82(6); 2012 > Article |
|
žöĒžēĹ
ž†ÄžěźŽď§žĚÄ žēÖžĄĪžĘÖžĖĎžúľŽ°ú žė§žĚłŽźėžóąŽćė ŪôĒŽÜ枥Ī Ž≥ĎŽ≥ÄÍ≥ľ ÍįĄ žĻ®Ž≤ĒžĚĄ ŽŹôŽįėŪēú žč†žč§žßąžĚė žóįŽįėž¶ĚžĚĄ 1žėą Í≤ĹŪóėŪēėžėÄÍ≥†, žĚīžóź ŽĆÄŪēú ÍĶ≠Žāī Ž≥īÍ≥†ÍįÄ žóÜžĖī ÍĶ≠ŽāīžóźžĄú Ž≥īÍ≥†Žźú žóįŽįėž¶Ě ž¶ĚŽ°Ä Í≥†žįįÍ≥ľ Ūē®ÍĽė Ž≥īÍ≥†ŪēėŽäĒ ŽįĒžĚīŽč§.
Abstract
Malakoplakia is a chronic inflammatory disorder that usually affects the urinary tract in immunocompromised patients and rarely extends to adjacent organs. Due to its mass-like presentation, malakoplakia is often clinically misdiagnosed as a neoplastic lesion. We describe the case of a 51-year-old female with renal malakoplakia and hepatic extension and large intraperitoneal abscesses that had been misdiagnosed as malignancy. She was diagnosed with myasthenia gravis 12 years prior and had been treated with oral corticosteroids and immunosuppressants. Radical nephrectomy concomitant with abscess drainage was performed. The final pathology was compatible with malakoplakia, and the patient was successfully treated with antibiotics. Although renal malakoplakia is a rare disease, it should be included in the differential diagnosis of patients with a renal mass who have a history of recurrent urinary tract infections or evidence of immunosuppression. (Korean J Med 2012;82:764-768)
žóįŽįėž¶ĚžĚÄ 1902ŽÖĄ Michaelis ŽďĪ[1]žóź žĚėŪēī ž≤ėžĚĆ Ž≥īÍ≥†Žźú ŽßĆžĄĪ žú°žēĄžĘÖžĄĪ žßąŪôėžĚīŽč§. žĚī žßąŪôėžĚÄ žĄłÍ∑†ÍįźžóľÍ≥ľ ÍīÄŽ†®Ūēú ŽĆÄžčĚžĄłŪŹ¨žĚė ŪÉźžčĚžěĎžö© žě•žē†Ž°ú žĚłŪēī ŽįúžÉĚŪēėŽäĒ Í≤ÉžúľŽ°ú žÉĚÍįĀŽźėÍ≥† žěąžúľŽ©į Ž©īžó≠žĖĶž†úž†ú Ž≥Ķžö© ŽįŹ Ž©īžó≠Í≤įŪēćžßąŪôė, žä§ŪÖĆŽ°úžĚīŽďúžĚė žě•Íłį Ž≥Ķžö©žĚīŽāė žěźÍįÄ Ž©īžó≠ žßąŪôėžĚĄ ÍįÄžßÄÍ≥† žěąŽäĒ Í≤Ĺžöį ŽįúžÉĚŽ•†žĚī ŽÜížĚÄ Í≤ÉžúľŽ°ú žēĆŽ†§ž†ł žěąŽč§[2]. žóįŽįėž¶ĚžĚÄ ž†Ąžč† žó¨Žü¨ Ž∂ÄžúĄžóźžĄú ŽįúžÉĚŪē† žąė žěąžúľŽāė ž£ľŽ°ú žöĒŽ°úÍ≥Ąžóź ŪėłŽįúŪēėŽ©į Žį©ÍīĎ ŽįŹ žöĒŽŹĄŽ•ľ ŪŹ¨Ūē®Ūēú ŪēėŽ∂Ä žöĒŽ°úÍ≥Ąžóź ŽćĒ ŪėłŽįúŪēúŽč§. žč† žč§žßąžĚĄ žĻ®Ž≤ĒŪēėŽäĒ žóįŽįėž¶ĚžĚÄžÉĀŽĆÄž†ĀžúľŽ°ú ŽďúŽ¨ľÍ≤Ć ŽįúžÉĚŪēėŽ©į žĚī ž§ĎžóźžĄúŽŹĄ žč† žč§žßąžĚė žóįŽįėž¶ĚžĚī Žč§Ž•ł žě•ÍłįžĚė žĻ®Ž≤ĒžĚĄ ŽŹôŽįėŪēú Í≤ĹžöįŽäĒ ŽćĒ ŽįúžÉĚŽĻąŽŹĄÍįÄ ŽāģžēĄ ÍĶ≠ŽāīžóźžĄúŽäĒ Ūēú žėąŽßĆžĚī Ž≥īÍ≥†ŽźėžĖī žěąŽč§[3]. žĚīžóź ž§Ďž¶Ě Í∑ľŽ¨īŽ†•ž¶ĚžúľŽ°ú žě•ÍłįÍįĄ Ž©īžó≠žĖĶž†úž†úŽ•ľ Ž≥Ķžö© ž§ĎžĚīŽćė 51žĄł žó¨žěź ŪôėžěźžóźžĄú žēÖžĄĪžĘÖžĖĎžúľŽ°ú žė§žĚłŽźėžóąŽćė ÍįĄ žĻ®Ž≤Ē ŽįŹ Ž≥ĶÍįē Žāī ŽÜćžĖϞ̥ ŽŹôŽįėŪēú žč† žč§žßąžĚė žóįŽįėž¶ĚžĚė žā¨Ž°ÄŽ•ľ Ž≥īÍ≥†ŪēėÍ≥†žěź ŪēúŽč§.
Ūôė žěź: ž†Ą„Äá„Äá, žó¨žěź 51žĄł
ž£ľ žÜĆ: žöįžł° žł°žôÄŽ∂Ä ŪÜĶž¶Ě, žĘÖÍīī
ŪėĄŽ≥ĎŽ†•: Žāīžõź 1ž£ľžĚľ ž†Ą žčúžěĎŪēėžó¨ ž†źžį® žßĄŪĖČŪēėŽäĒ žöįžł° žł°žôÄŽ∂ÄžĚė ŪÜĶž¶ĚÍ≥ľ žĘÖÍīīŽ•ľ ž£ľžÜĆŽ°ú ŽāīžõźŪĖąŽč§. ŪôėžěźŽäĒ 12ŽÖĄ ž†Ą ŪĚČžĄ†žĘÖžúľŽ°ú ŪĚČžĄ† ž†ąž†úžą† žčúŪĖČ ŪõĄ ž∂Ēž†ĀÍīÄžįį ž§ĎžĚīžóąŽč§. Žāīžõź 5ÍįúžõĒ ž†Ą žčúŪĖČŪēú ž†ĄžāįŪôĒ Žč®žłĶ žī¨žėĀžóźžĄú žöįžł° Ž∂Äžč† ž£ľŽ≥ÄžúľŽ°ú 5 √ó 3 cmžĚė žĘÖÍīīÍįÄ ŪôēžĚłŽźėžĖī ž°įžßĀÍ≤Äžā¨Ž•ľ ŽįõÍłį žúĄŪēī žěÖžõź žėąž†ēžĚīžóąžúľŽāė žěÖžõź ž†Ą žöįžł° žł°žôÄŽ∂ÄžĚė ŪÜĶž¶ĚžĚī ŽßéžĚī žēÖŪôĒŽźėžĖī žôłŽ∂Ä Ž≥Ďžõź žĚĎÍłČžč§ Žį©Ž¨ł ŪõĄ Ž≥łžõźžúľŽ°ú ž†ĄžõźŽźėžóąŽč§. Žāīžõź ŽčĻžčú ŪôėžěźŽäĒ ŪÜĶž¶ĚžĚī Žß§žöį žč¨Ūēī žõÄžßĀžĚīÍłį žĖīŽ†§žöī žÉĀŪÉúžėÄžúľŽ©į ž†Ąžč† žá†žēĹÍįźÍ≥ľ ÍįĄŪ󟞆ĀžĚł žė§ŪēúžĚĄ ŽŹôŽįėŪēėÍ≥† žěąžóąŽč§. žł°žôÄŽ∂Ä ŪÜĶž¶Ě žôł ÍĶ¨žó≠, ÍĶ¨Ū܆Žāė ŽĻąŽá®, žěĒŽá®, ž†ąŽįēŽá® ŽďĪžĚė Žč§Ž•ł ž¶ĚžÉĀžĚÄ žóÜžóąŽč§.
Í≥ľÍĪįŽ†•: ŪôėžěźŽäĒ Žāīžõź 12ŽÖĄ ž†Ą žā¨žßÄžúĄžēĹÍ≥ľ žēąÍ≤ÄŪēėžąėŽ°ú ŽāīžõźŪēėžó¨ ŪĚČžĄ†žĘÖ ŽįŹ ž§Ďž¶Ě Í∑ľŽ¨īŽ†•ž¶ĚžĚĄ žßĄŽč®ŽįõÍ≥† ŪĚČžĄ† ž†ąž†úžą†žĚĄ žčúŪĖČŽįõžēėžúľŽ©į Žāīžõź 2ŽÖĄ ž†Ą ŪĚČžĄ†žĘÖžĚė ŪŹźž†ĄžĚīÍįÄ ŪôēžĚłŽźėžĖī žöįŪēėžóĹ ž†ąž†úžą†žĚĄ ŽįõžĚÄ Í≥ľÍĪįŽ†•žĚī žěąžóąŽč§. žĚīŪõĄ ŪėĄžě¨ÍĻĆžßÄ Í≤ĹÍĶ¨ prednisolone 20 mgÍ≥ľ cyclosporin 50 mgžĚĄ Žß§žĚľ žßÄžÜ枆ĀžúľŽ°ú Ž≥Ķžö©ŪēėÍ≥† žěąŽäĒ žÉĀŪÉúžėÄŽč§.
ÍįÄž°ĪŽ†•: ŪäĻžĚīžÜĆÍ≤¨ žóÜžĚĆ.
žā¨ŪöĆŽ†•: ŪĚ°žóįŽ†• ŽįŹ žĚĆž£ľŽ†• žóÜžĚĆ.
žĚīŪēôž†Ā žßĄžįį žÜĆÍ≤¨: žěÖžõź ŽčĻžčú ŪôúŽ†• žßēŪõĄŽäĒ Ūėąžēē 150/76 mmHg, Žß•Žįē 70ŪöĆ/Ž∂Ą, ž≤īžė®žĚÄ 36.6‚ĄÉžėÄžúľŽ©į ͳȞĄĪ Ž≥ĎžÉȞ̥ ŽĚĄžóąŽč§. Í≤įŽßČžĚÄ žįĹŽįĪŪĖąžúľŽ©į žč¨žĚĆ, ŪĚČŽ∂Äž≤≠žßĄžĚÄ ž†ēžÉĀžĚīžóąŽč§. Ž≥ĶŽ∂Ä žßĄžįįžóźžĄú žöįžł° žł°žôÄŽ∂Ä žīČžßÄ žčú Žč®Žč®ŪēėÍ≥† žēēŪÜĶžĚĄ ŽŹôŽįėŪēėŽäĒ žĘÖÍīīÍįÄ žěąžóąžúľŽ©į ŽįėŽįúŪÜĶžĚÄ ŽŹôŽįėŽźėžßÄ žēäžēėÍ≥† žě•žĚĆžĚÄ ÍįźžÜĆŽźėžĖī žěąžóąŽč§.
Í≤Äžā¨žč§ žÜĆÍ≤¨: Ūėąžē° Í≤Äžā¨žóźžĄú ŽįĪŪėąÍĶ¨ žąė 20.9 √ó 103/mm3, ŪėąžÜĆŪĆź žąė 377 √ó 103/mm3Ž°ú ž¶ĚÍįÄŽźėžĖī žěąžóąžúľŽ©į ŪėąžÉČžÜĆŽäĒ 8.6 g/dLŽ°ú ÍįźžÜĆŽźėžĖī žěąžóąŽč§. CRPÍįÄ 12.49 mg/dLŽ°ú ž¶ĚÍįÄŽźėžĖī žěąžóąžúľŽāė Í∑łŽįĖžóź ŪĀ¨Ž†ąžēĄŪčįŽčĆžĚīŽāė ÍįĄŪö®žÜĆ žąėžĻėžĚė žÉĀžäĻžĚÄ žóÜžóąŽč§. žöĒÍ≤Äžā¨žóźžĄúŽäĒ ŽįĪŪėąÍĶ¨ žąėžĻėÍįÄ ž¶ĚÍįÄŽźėžĖī žěąžóąžúľŽ©į žě†ŪėąžĚī ŪôēžĚłŽźėžóąŽč§.
Žį©žā¨žĄ† žÜĆÍ≤¨: Ž≥ĶŽ∂Ä ž†ĄžāįŪôĒ Žč®žłĶžī¨žėĀžóźžĄú žöįžł° Ž∂Äžč† ŽįŹ žč†žě•žĚĄ žĻ®Ž≤ĒŪēú žĘÖÍīīÍįÄ ÍįĄ ŽįŹ ŽčīŽā≠ÍĻĆžßÄ ŽčŅžēĄžěąŽäĒ Í≤ÉžĚī ŪôēžĚłŽźėžóąžúľŽ©į žĘÖÍīīŽäĒ Žč§žąėžĚė ž§ĎÍ≤©žúľŽ°ú ÍĶ¨žĄĪŽźėžĖī žěąžóąŽč§. žĘÖÍīīžĚė ŽāīŽ∂ÄžóźŽäĒ Í≥ĶÍłįŽ•ľ Ūē®žú†ŪēėÍ≥† žěąŽäĒ žßĀÍ≤Ĺ 27.4 cm, žě•Í≤Ĺ 11.2 cmžĚė ÍĪįŽĆÄŪēú ŽÜćžĖĎžĚī ŽŹôŽįėŽźėžĖī žÉĀŪĖČÍ≤įžě•žĚī Žāīžł°žúľŽ°ú žĚīŽŹôŪēú žĖĎžÉĀžĚĄ Ž≥īžėÄÍ≥†, Žį©ÍīĎ ž£ľŽ≥Äž°įžßĀÍĻĆžßÄ Ž≥ĎŽ≥ÄžĚī ŪôēžāįŽźėžĖī žěąžóąŽč§. žĘÖÍīīŽäĒ ž°įžėĀž†ú ž£ľžěÖ žčú Ž∂ąÍ∑úžĻôŪēú ž°įžėĀ ž¶ĚÍįēžĚĄ Ž≥īžėÄŽč§(Fig. 1).
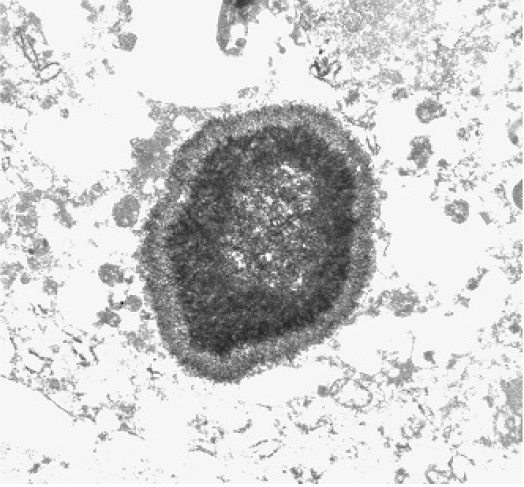
žěĄžÉĀÍ≤ĹÍ≥ľ: žĘÖÍīī ŽāīŽ∂ÄžĚė Žįįžē°žĚĄ žúĄŪēī Í≤ĹŪĒľž†Ā ŽįįŽÜćžą†žĚī žčúŪĖČŽźėžóąžúľŽ©į ŽįįŽÜ掟ú Í≤Äž≤īžóźžĄú Escherichia coliÍįÄ ŽįįžĖĎŽźėžóąŽč§. Ž∂ĄŽ¶¨Žźú E. coliŽäĒ ampicillinžóź ŽāīžĄĪžĚĄ ÍįÄžßÄÍ≥† žěąžóąžúľŽāė cefazolin, cefuroxime, cefotaxime, ciprofloxacinžóźŽäĒ ÍįźžąėžĄĪžĚī žěąŽäĒ Í∑†ž£ľŽ°ú ŪôēžĚłŽźėžóąŽč§. ŪôėžěźÍįÄ žě•ÍłįÍįĄ Ž©īžó≠žĖĶž†úž†úŽ•ľ Ž≥Ķžö©Ūēú Í≥ľÍĪįŽ†• ŽįŹ ŪėźÍłįÍ∑† Ž≥ĶŪē© ÍįźžóľžĚĄ Í≥†Ž†§Ūēėžó¨ cefepime 2 g ŪēėŽ£® 3ŪöĆ, metronidazole 500 mg ŪēėŽ£® 3ŪöĆ ž†ēŽß• Ūą¨žó¨Ž•ľ žčúžěĎŪĖąžúľŽ©į ŽÜćžĖĎ ŽāīŽ∂Äžóź žāĹžěÖŪēú Žįįžē°ÍīÄžĚÄ Í≥ĄžÜć žú†žßÄŪēėÍłįŽ°ú ŪēėžėÄŽč§. žāĹžěÖŽźú Žįįžē°ÍīÄžúľŽ°ú ŪēėŽ£® 100-150 cc ÍįÄŽüČžĚė ŽÜćžĖĎžĚī Žįįžē°ŽźėžóąŽč§. 2ž£ľ ŪõĄ ž∂Ēž†ĀŪēú Ž≥ĶŽ∂Ä ž†ĄžāįŪôĒ Žč®žłĶ žī¨žėĀžóźžĄú žĘÖÍīīžĚė ŪĀ¨ÍłįÍįÄ žĻėŽ£ĆŽ•ľ žčúžěĎŪēėÍłį ž†ĄÍ≥ľ ŽĻĄÍĶź žčú Í∑ł ŪĀ¨ÍłįÍįÄ ŽĻĄžä∑Ūēėžó¨ žĘÖÍīī ŽāīŽ∂ÄžĚė ŽÜćžĖĎžĚī Ūö®Í≥ľž†ĀžúľŽ°ú Žįįžē°ŽźėžßÄ žēäŽäĒ Í≤ÉžúľŽ°ú ŪĆźŽč®ŽźėžóąŽč§. žēÖžĄĪ žĘÖžĖĎ ŽďĪžĚė ÍįźŽ≥ĄžĚĄ žúĄŪēú ž°įžßĀ Í≤Äžā¨, ŽįįŽÜćžĚĄ žúĄŪēú žąėžą†žĚī žčúŪĖČŽźėžóąžúľŽ©į ŪõĄŽ≥ĶÍįē ÍįúŽ≥Ķ žčú žöįžł° žč†žě• ŪõĄŽį©žúľŽ°ú Žč§ŽüČžĚė ŽÜćžĚī Žįįžē°ŽźėžóąŽč§. žöįžł° Ž∂Äžč†Í≥ľ žč†žě•žĚė žč¨Ūēú žóľž¶ĚžĄĪ Ž≥ÄŪôĒžôÄ žĄ¨žú†ŪôĒŽ•ľ ŽŹôŽįėŪēú žĘÖÍīīÍįÄ žč≠žĚīžßÄžě•žĚė žĚľŽ∂ÄžôÄ ÍįĄžĚė ŽĮłžÉĀžóĹ, ŪõĄžóĹÍĻĆžßÄ žĻ®Ž≤ĒŪēėÍ≥† žěąŽäĒ Í≤ÉžĚī ŪôēžĚłŽźėžóąŽč§. Ž≥ĎŽ≥Äžóź žĚłž†ĎŪēú ŪõĄŽ≥ĶÍįēŽßČžĚė žĚľŽ∂Ğ󟞥ú ŽŹôÍ≤į žÉĚÍ≤Ğ̥ žčúŪĖČŪēú Í≤įÍ≥ľ ÍłįžõźžĚī Ž∂ĄŽ™ÖŪēėžßÄ žēäžĚÄ žēÖžĄĪ žĘÖžĖĎ ÍįÄŽä•žĄĪžĚī Ž≥īÍ≥†ŽźėžóąŽč§. žĚīŽü¨Ūēú ŽŹôÍ≤į žÉĚÍ≤Ä ž°įžßĀ Í≤Äžā¨ Í≤įÍ≥ľŽ•ľ ŽįĒŪÉēžúľŽ°ú žöįžł° Ž∂Äžč† ŽįŹ žč†žě•žóźžĄú ÍłįžõźŪēú žēÖžĄĪ žĘÖžĖĎžĚī Ž≥ĶŽßČÍĻĆžßÄ ž†ĄžĚīŽźėžĖī Í∑ľžĻėž†Ā ž†ąž†úŽäĒ žĖīŽ†§žöł Í≤ÉžúľŽ°ú ŪĆźŽč®Ūēėžó¨ ŪÜĶž¶Ě ÍįźžÜĆ ŽįŹ žóľž¶Ěž°įžßĀ ž†úÍĪįžôÄ ŽįįŽÜćžĚĄ žúĄŪēī žöįžł° žč†ž†ąž†úžą† ŽįŹ žúĄ-Í≥Ķžě• Ž¨łŪē©žą†žĚĄ žčúŪĖČŪĖąžúľŽ©į ÍįĄžĚĄ žĻ®Ž≤ĒŪēú Ž≥ĎŽ≥ÄžĚÄ ž†úÍĪįŪēėžßÄ žēäžĚÄ žÉĀŪÉúŽ°ú žąėžą†žĚĄ žĘÖŽ£ĆŪēėžėÄŽč§. žĶúžĘÖ Ž≥ĎŽ¶¨žÜĆÍ≤¨žÉĀ žĘÖÍīīŽäĒ žč†žąėžßąžĚĄ žĻ®Ž≤ĒŪēėÍ≥† žěąžóąžúľŽ©į Ūô©žÉČžĚė žú°žēĄžĘÖžĄĪ Ž≥ĎŽ≥Ä, ÍĶ≠žÜĆžĄĪ ž∂úŪėą ŽįŹ žĄ¨žú†ŪôĒÍįÄ žßĄŪĖČŽźú Ž∂ÄžúĄŽ•ľ ŽŹôŽįėŪēėÍ≥† žěąžóąÍ≥† žēÖžĄĪ žĘÖžĖĎ žĄłŪŹ¨ŽäĒ ÍīÄžįįŽźėžßÄ žēäžēėŽč§. žč† ž°įžßĀžĚÄ žĄłŪŹ¨žßąžĚĄ Žč§ŽüČ Ūē®žú†ŪēėÍ≥† žěąŽäĒ ŽĆÄžčĚžĄłŪŹ¨ÍįÄ ÍĶįžßϞ̥ žĚīŽ£®Í≥† žěąžóąžúľŽ©į Žč§žąėžĚė žóľž¶ĚžĄłŪŹ¨ÍįÄ žāįžě¨ŽźėžĖī žěąžóąŽč§. ŽĆÄžčĚžĄłŪŹ¨ŽäĒ žĄłŪŹ¨žßą Žāī ŽßéžĚÄ žĖĎžĚė ŪėłžāįÍĶ¨žĄĪ Í≥ľŽ¶Ĺ ŽįŹ žĚľŽ∂Ä ŪėłžóľžĄĪ Í≥ľŽ¶ĹžĚī ÍīÄžįįŽźėžĖī ‚ÄúVon Hansemann‚ÄĚ žĄłŪŹ¨Ž°ú žÉĚÍįĀŽźėžóąžúľŽ©į ž†Ąžěź ŪėĄŽĮłÍ≤Ĺ žÉĀ Prucian blue ŽįŹ von-Kossa stainžóź žĖĎžĄĪžĚĄ Ž≥īžĚīŽäĒ Ž¨īÍłįžßąžĚī žĻ®žį©Žźú Michaelis-Gutmann bodyÍįÄ ŪôēžĚłŽźėžĖī žĶúžĘÖž†ĀžúľŽ°ú žč† žč§žßąžĚė žóįŽįėž¶ĚžúľŽ°ú žßĄŽč®ŽźėžóąŽč§(Figs. 2 and 3). ž†ąž†úŽźú ž°įžßĀžĚė ŽįįžĖĎ Í≤Äžā¨žóźžĄú Í∑†žĚÄ Ž∂ĄŽ¶¨ŽźėžßÄ žēäžēėžúľŽ©į, ž°įžßĀžúľŽ°úžĚė žĻ®Ūą¨Ž†•žĚĄ Í≥†Ž†§Ūēėžó¨ Ūē≠žÉĚž†úŽ•ľ cefepimeÍ≥ľ metronidazoležóźžĄú ciprofloxacin 400 mg ŪēėŽ£® 2ŪöĆ ž†ēŽß• Ūą¨žó¨Ž°ú Ž≥ÄÍ≤ĹŪĖąŽč§. Íłįž°īžóź Ūą¨žēĹ ž§ĎžĚīŽćė Ž©īžó≠žĖĶž†úž†ú cyclosporinžĚÄ 50 mgžóźžĄú 25 mgžúľŽ°ú ÍįźŽüČŪĖąžúľŽ©į prednisolonežĚÄ 20 mgžĚĄ Í∑łŽĆÄŽ°ú žú†žßÄŪēėžėÄŽč§. žĚīŪõĄ ŪôėžěźžĚė žÉĀŪÉúŽäĒ ž†źžį® Ūėłž†ĄŽźėžĖī Žāīžõź 12ž£ľ ŪõĄ ciprofloxacin 500 mg ŪēėŽ£® 2ŪöĆ Í≤ĹÍĶ¨ž†úž†úŽ°ú Ž≥ÄÍ≤ĹŪēėžó¨ ŪáīžõźŪĖąŽč§. ŪôėžěźŽäĒ Ūáīžõź ŪõĄžóźŽŹĄ Í≤ĹÍĶ¨ Ūē≠žÉĚž†úŽ•ľ žßÄžÜ枆ĀžúľŽ°ú Ž≥Ķžö©ŪĖąžúľŽ©į Ūáīžõź 1ÍįúžõĒ ŪõĄ žôłŽěėžóźžĄú ž∂Ēž†ĀŪēú Ž≥ĶŽ∂Ä ž†ĄžāįŪôĒ Žč®žłĶžī¨žėĀžóźžĄú ÍįĄžúľŽ°ú ŪĆĆͳȎźėžóąŽćė Ž≥ĎŽ≥Ä ŽįŹ Ž≥ĶÍįē Žāī ŽÜćžĖĎžĚė ŪĀ¨ÍłįÍįÄ ÍįźžÜĆŪēú Í≤ɞ̥ ŪôēžĚłŪē† žąė žěąžóąŽč§.
žóįŽįėž¶ĚžĚÄ ŪĚĒŪēėžßÄ žēäžĚÄ ŽßĆžĄĪ žú°žēĄžĘÖžĄĪ žóľž¶Ě žßąŪôėžúľŽ°ú žě¶žĚÄ žöĒŽ°ú ÍįźžóľžĚė Í≥ľÍĪįŽ†•žĚī žěąŽäĒ ž§ĎŽÖĄ žó¨žĄĪžóźžĄú ŪėłŽįúŪēėŽäĒ Í≤ÉžúľŽ°ú žēĆŽ†§ž†ł žěąŽč§[2]. 1900ŽÖĄŽĆÄ žīą Žį©ÍīϞ󟞥ú ŽįúžÉĚŪēú žóįŽįėž¶ĚžĚī žĶúžīąŽ°ú Ž≥īÍ≥†Žźú žĚīŪõĄ Žč§žĖĎŪēú Ž∂ÄžúĄžĚė žóįŽįėž¶ĚžĚī Ž≥īÍ≥†ŽźėÍ≥† žěąžúľŽāė ŽĻĄŽá®žÉĚžčĚÍ≥ĄžĚė žĻ®Ž≤ĒžĚī ÍįÄžě• ŪĚĒŪēėŽ©į žÜĆŪôĒÍłįÍ≥Ą, ŪõĄŽ≥ĶÍįēžĚė žąúžúľŽ°ú ŽįúžÉĚŪēúŽč§. 153Ž™ÖžĚė žā¨Ž°ÄŽ•ľ Ž∂ĄžĄĚŪēú StantonžĚė žóįÍĶ¨žóźžĄúŽäĒ ŽĻĄŽá®žÉĚžčĚÍ≥ĄžóźžĄúžĚė ŽįúžÉĚžĚī 58%Ž•ľ žį®žßÄŪēėžėÄÍ≥†, žĚī ž§Ď 40%ŽäĒ Žį©ÍīĎ, 11%ŽäĒ žöĒŽŹĄ, 10%ŽäĒ žč†žöįžóźžĄú ŽįúžÉĚŪēú Í≤ÉžĚī Ž≥īÍ≥†Žźú ŽįĒ žěąŽč§[4]. žĚīŽ≤ą ž¶ĚŽ°ÄžôÄ ÍįôžĚÄ žč† žč§žßąžĚė žóįŽįėž¶ĚžĚÄ ž†Ą žĄłÍ≥Ąž†ĀžúľŽ°ú žēĹ 75žėąÍįÄ Ž≥īÍ≥†ŽźėžóąžúľŽ©į[2,5] ÍĶ≠ŽāīžóźžĄúŽäĒ ŪėĄžě¨ÍĻĆžßÄ Ž≥ł ž¶ĚŽ°ÄŽ•ľ ŪŹ¨Ūē®Ūēėžó¨ žēĹ 10žėąÍįÄ Ž≥īÍ≥†ŽźėžĖī žěąŽč§[3,6]. ÍĶ≠Žāīžóź Ž≥īÍ≥†ŽźėžóąŽćė ŪôėžěźŽď§žĚė ŪŹČÍ∑† ŽāėžĚīŽäĒ žēĹ 55žĄłžėÄžúľŽ©į, 10žėąžĚė ž¶ĚŽ°Ä ž§Ď žó¨žĄĪžóźžĄú ŽįúžÉĚŪēú Í≤ĹžöįÍįÄ 8žėą, Žā®žĄĪžóźžĄú ŽįúžÉĚŪēú Í≤ĹžöįÍįÄ 2žėąŽ°ú ÍĶ≠ŽāīžóźžĄúŽŹĄ ž§ĎŽÖĄ žó¨žĄĪžóźžĄú ŪėłŽįúŪēėŽäĒ Í≤ĹŪĖ•žĚĄ Ž≥īžėÄŽč§[3,6]. žč† žč§žßąžĚė žóįŽįėž¶ĚžĚÄ Žč§žĖĎŪēú ž¶ĚžÉĀžĚĄ Ž≥īžĚľ žąė žěąžúľŽ©į ŽįúžóīžĚī ÍįÄžě• ŪĚĒŪēėÍ≥†(42%) žĘÖÍīīžĚė žīČžßÄ, Žč§Žá®, ŽĻąŽá®, Ž≥ĶŪÜĶ, žł°žôÄŽ∂Ä ŪÜĶž¶Ě ŽďĪžĚė ž¶ĚžÉĀžĚī ŽāėŪÉÄŽā† žąė žěąŽč§[2]. Ž≥ł ž¶ĚŽ°ÄžĚė ŪôėžěźŽäĒ žł°žôÄŽ∂Ä ŪÜĶž¶Ě ŽįŹ žĘÖÍīīžĚė žīČžßÄŽ•ľ ž£ľŽ°ú ŪėłžÜĆŪĖąŽč§.
žóįŽįėž¶ĚžĚė ŽįúžÉĚÍłįž†ĄžĚÄ žēĄžßĀ Ž∂ĄŽ™ÖŪēėžßÄ žēäžßÄŽßĆ 1965ŽÖĄ Terner ŽďĪžĚī E. coližóź žĚėŪēú žöĒŽ°ú ÍįźžóľžĚī žěąŽćė ŪôėžěźžóźžĄú žóįŽįėž¶ĚžĚī ŪėłŽįúŪēúŽč§ŽäĒ žÉĀÍīÄžĄĪžĚĄ Ž≥īÍ≥†Ūēú žĚīŪõĄ[7], E. coli endotoxin-antigen complexŽ•ľ ž•źžĚė žč†žě• ŽįŹ Í≥†Ūôėžóź ž£ľžěÖŪēú ŽŹôŽ¨ľ žč§ŪóėžóźžĄú žóįŽįėž¶ĚžóźžĄú ÍīÄžįįŽźėŽäĒ ŪäĻžßēž†ĀžĚł žÜĆÍ≤¨žĚł ‚ÄĚVon Hansemann‚ÄĚ žĄłŪŹ¨ ŽįŹ ‚ÄúMichaelis-Gutmann body‚ÄĚžôÄ žú†žā¨Ūēú Ž¨ľžßąžĚī ŪėēžĄĪŽźėŽäĒ Í≤ÉžĚī ÍīÄžįįŽźėžĖī žĚī žóįÍīÄžĄĪžĚĄ ŽćĒžöĪ Ží∑ŽįõžĻ®ŪĖąŽč§[8]. žĚīŽü¨Ūēú ŪėĄžÉĀžĚė Íłįž†ĄžĚÄ ŪėĄžě¨ÍĻĆžßÄ Žč®ŪēĶžĄłŪŹ¨žĚė ÍłįŽä•žě•žē†ÍįÄ ÍįÄžě• žú†Ž†•Ūēú žõźžĚłžúľŽ°ú žÉĚÍįĀŽźėÍ≥† žěąŽč§. žóįŽįėž¶Ě ŪôėžěźžĚė Žč®ŪēĶžĄłŪŹ¨ŽäĒ ž†ēžÉĀžĚłžóź ŽĻĄŪēī žĄłŪŹ¨ Žāī cyclic-guanosine monophosphate (cGMP)ÍįÄ ÍįźžÜĆŽźėžĖī Žč®ŪēĶžĄłŪŹ¨ Žāī žö©Ūēī žÜĆž≤īŽ•ľ Ž∂ĄŽĻĄŪēėŽäĒŽćį ž§ĎžöĒŪēú žĄłŪŹ¨Žāī žÜĆÍīÄ(intracellular microtubule)žĚė ÍłįŽä•žě•žē†ÍįÄ ŽįúžÉĚŪēėŽ©īžĄú ŪÉźžčĚŽźú žĄłÍ∑†žĚī Ž∂ąžôĄž†ĄŪēėÍ≤Ć žö©ŪēīŽźėžĖī Í∑ł žĚľŽ∂ÄÍįÄ žĄłŪŹ¨Žāī ž∂ēž†ĀŽźėŽ©īžĄú žóįŽįėž¶ĚžĚī ŽįúžÉĚŪēúŽč§ŽäĒ Í≤ÉžĚīŽč§[9].
ÍįźžóľŽźú žĄłÍ∑†žĚė žĘÖŽ•ėŽŹĄ žóįŽįėž¶ĚžĚė ŽįúžÉĚÍ≥ľ žÉĀÍīÄÍīÄÍ≥ĄÍįÄ žěąŽäĒ Í≤ÉžúľŽ°ú žÉĚÍįĀŽźėÍ≥† žěąŽč§. 93Ž™ÖžĚė žóįŽįėž¶Ě ŪôėžěźŽ•ľ Ž∂ĄžĄĚŪēú Ūēú žóįÍĶ¨žóźžĄú 89%ÍįÄ coliform bacteriažóź ÍįźžóľŽźú Í≤ÉžĚī ŪôēžĚłŽźėžóąžúľŽ©į coliform bacteria ž§ĎžóźžĄúŽäĒ E. coliÍįÄ 72%Ž°ú ÍįÄžě• ŽßéžēėÍ≥† Í∑łŽįĖžóź lebsiella, Enterobacter, Proteus, Pseudomonas species ŽďĪžĚī žěąžóąŽč§[4]. Ž©īžó≠ ÍłįŽä• žě•žē† žó≠žčú žóįÍīÄžĚī žěąŽäĒ Í≤ÉžúľŽ°ú žēĆŽ†§ž†ł žěąžĖī žēÖžĄĪ žĘÖžĖĎ, Ž©īžó≠Í≤įŪēćžßąŪôė, žěźÍįÄŽ©īžó≠žßąŪôė ŽďĪžĚė žßąŪôėžĚīŽāė žč†žě• žĚīžčĚ Ūôėžěź, žä§ŪÖĆŽ°úžĚīŽďúŽ•ľ žě•Íłį Ž≥Ķžö©ŪĖąŽćė ŪôėžěźžóźžĄú ŽįúžÉĚŪēėŽäĒ Í≤ĹŪĖ•žĚī žěąŽč§[4]. žóįŽįėž¶ĚžĚė žßĄŽč®žĚÄ žČĹžßÄ žēäžúľŽ©į žēÖžĄĪ žĘÖžĖĎžúľŽ°ú žė§žßĄŽźėŽäĒ Í≤ĹžöįŽŹĄ ŽďúŽ¨ľžßÄ žēäŽč§. ÍįźŽ≥Ą žßĄŽč®žĚĄ žúĄŪēī Žč§žĖĎŪēú žėĀžÉĀ Í≤Äžā¨Žď§žĚī žĚīžö©ŽźėžßÄŽßĆ žĶúžĘÖž†ĀžúľŽ°úŽäĒ ž°įžßĀÍ≤Äžā¨Ž•ľ ŪÜĶŪēī ŪôēžßĄŽźėŽäĒ Í≤ÉžĚī Ž≥īŪÜĶžĚīŽč§. Ž≥ł ŪôėžěźžóźžĄúŽŹĄ Žāīžõź 5ÍįúžõĒ ž†Ą ž≤ėžĚĆ ŽįúÍ≤¨Žźú Ž∂Äžč† ž£ľžúĄžĚė žĘÖÍīīÍįÄ Žāīžõź ŽčĻžčú ž†ĄžāįŪôĒ Žč®žłĶ žī¨žėĀžóźžĄúŽäĒ Í∑ł Ž≤ĒžúĄÍįÄ Žß§žöį Ūôēžě•ŽźėžĖī Ž∂ąÍ∑úžĻôŪēú ž°įžėĀ ž¶ĚÍįēžĚĄ Ž≥īžĚīŽäĒ žč†žě•žĚė žĘÖÍīīÍįÄ žč†ž£ľŽ≥Ä ŽįŹ ÍįĄžúľŽ°ú ž†ĄžĚīŽźú žĖĎžÉĀžĚĄ Ž≥īžėÄŽč§. žĚī Ž≥ĎŽ≥ÄžĚÄ žąėžą† ž§Ď ŽŹôÍ≤į žÉĚÍ≤Ğ󟞥ú žēÖžĄĪ žĄłŪŹ¨Ž°ú ŪôēžĚłŽźėžĖī ž≤ėžĚĆžóźŽäĒ žč†žĄłŪŹ¨žēĒ ŽďĪžĚė žēÖžĄĪ žĘÖžĖϞ̥ žĚėžč¨ŪĖąžóąžúľŽāė žĶúžĘÖž†ĀžĚł Ž≥ĎŽ¶¨žÜĆÍ≤¨žóźžĄú žč† žč§žßąžĚė žóįŽįėž¶ĚžúľŽ°ú ŪôēžĚłŽźėžóąŽč§. ŽėźŪēú žĘÖÍīī ŽāīŽ∂Äžóź Íīīžā¨Ž•ľ ŽŹôŽįėŪēú ŪôĒŽÜ枥Ī Ž≥ĎŽ≥ÄžĚī žěąžóąŽäĒŽćį, žĚīŽäĒ žĚīž†Ąžóź Ž≥īÍ≥†Žźú žč† žč§žßąžĚė žóįŽįėž¶ĚžóźžĄú Ž≥īÍ≥†Žźú ž†ĀžĚī žóÜŽäĒ žÜĆÍ≤¨žúľŽ°ú Ž©īžó≠ž†ÄŪēėžěźžóźžĄú ŪôĒŽÜ枥Ī Ž≥ĎŽ≥Ğ̥ ŽŹôŽįėŪē† žąė žěąŽäĒ Íįźžóľ, žēÖžĄĪ žĘÖžĖĎÍ≥ľ ÍįôžĚÄ žßąŪôėžĚė ÍįźŽ≥Ąžóź žóįŽįėž¶Ě ŽėźŪēú Í≥†Ž†§Ūē† ŪēĄžöĒÍįÄ žěąžĚƞ̥ Ž≥īžó¨ž§ÄŽč§. ž°įžßĀÍ≤Äžā¨ŽäĒ žú†žĚľŪēú ŪôēžßĄ žąėŽč®žúľŽ°ú ‚ÄĚVon Hansemann‚ÄĚ žĄłŪŹ¨Ž°ú Ž∂ąŽ¶¨ŽäĒ ŪėłžāįžĄĪ Í≥ľŽ¶ĹžĚĄ Žč§ŽüČ Ūē®žú†ŪēėÍ≥† žěąŽäĒ žĄłŪŹ¨žßąžĚī ŪíćŽ∂ÄŪēú ŽĆÄžčĚžĄłŪŹ¨ ŽįŹ žĚī žĄłŪŹ¨ ŽāīžôłŽ∂Äžóź ž≤†Í≥ľ žĻľžäėžĚī žĻ®žį©Žźú ÍĶ¨ŪėēžĚė žłĶžÉĀ ÍĶ¨ž°įŽ¨ľžĚł ‚ÄúMichaelis-Gutmann body‚ÄĚÍįÄ ŪôēžĚłŽźėŽäĒ Í≤Ĺžöį žóįŽįėž¶ĚžúľŽ°ú žßĄŽč® Ūē† žąė žěąŽč§[4].
žóįŽįėž¶ĚžĚė žĻėŽ£ĆŽäĒ žēĄžßĀ ž†ēŽ¶ĹŽźú žĻėŽ£Ć Žį©žĻ®žĚī žóÜŽäĒ žÉĀŪÉúžĚīŽāė ŪĀ¨Í≤Ć Ūē≠žÉĚž†ú žĻėŽ£Ć ŽįŹ žąėžą†ž†Ā žĻėŽ£ĆŽ°ú ŽāėŽąĆ žąė žěąŽč§. žĚīž†ĄžóźŽäĒ žąėžą†ž†Ā žĻėŽ£ĆÍįÄ ŽßéžĚī žčúŪĖČŽźėžóąžúľŽāė 1990ŽÖĄ žīą ciprofloxacin Žč®ŽŹÖžĻėŽ£ĆŽ•ľ žčúŪĖČŪēú žóįŽįėž¶Ě ŪôėžěźžĚė žĄĪÍ≥Ķž†ĀžĚł žĻėŽ£Ć žā¨Ž°ÄÍįÄ ž≤ėžĚĆžúľŽ°ú Ž≥īÍ≥†Žźú žĚīŪõĄ[10], žĄłŪŹ¨ŽāīŽ∂ÄŽ°úžĚė žĻ®Ūą¨ÍįÄ žöįžąėŪēú trimethoprim/sulfamethoxazole, rifampin, fluoroquinolone ŽďĪžĚė Ūē≠žÉĚž†úŽ•ľ žĚīžö©Ūēú žĻėŽ£ĆÍįÄ ŽßéžĚī žčúŪĖČŽźėÍ≥† žěąŽč§. Ūą¨žēĹ ž§ĎžĚł Ž©īžó≠žĖĶž†úž†úŽ•ľ ÍįźŽüČŪēėÍĪįŽāė ž§ĎŽč®ŪēėŽäĒ Í≤ÉŽŹĄ žĻėŽ£Ćžóź ž§ĎžöĒŪēėŽč§[2]. Ž≥ł ŪôėžěźžóźžĄúŽŹĄ Ž©īžó≠žĖĶž†úž†ú ÍįźŽüČ ŽįŹ Í≤ĹÍĶ¨ ciprofloxacinžĚĄ žú†žßÄŪēėŽ©īžĄú ž†źžį® Ūėłž†ĄŽźėŽäĒ Í≤ĹÍ≥ľŽ•ľ Ž≥īžėÄŽč§.
ž≤ėžĚĆ žóįŽįėž¶ĚžĚī Ž≥īÍ≥†Žźú žĚīŽěė žĚī žßąŪôėžĚė žėąŪõĄŽäĒ ŽßéžĚī ÍįúžĄ†ŽźėžóąžßÄŽßĆ žó¨ž†ĄŪěą ŽĻĄÍįÄžó≠ž†ĀžĚł žč†ÍłįŽä• žě•žē†žôÄ ÍįôžĚÄ žč¨ÍįĀŪēú ŪõĄ žú†ž¶ĚžĚĄ žú†ŽįúŪē† žąė žěąŽč§. 1990ŽÖĄŽĆÄ žĚīŪõĄ žėĀžĖīŽ°ú Ž≥īÍ≥†Žźú žč† žč§žßąžĚė žóįŽįėž¶Ě žā¨Ž°ÄŽď§žĚė žėąŪõĄŽ•ľ Ž∂ĄžĄĚŪēú žóįÍĶ¨žóź ŽĒįŽ•īŽ©ī žīĚ 25žėąž§Ď 23žėąžĚė ŪôėžěźÍįÄ žÉĀŪÉúÍįÄ Ūėłž†ĄŽźėžĖī ŪáīžõźŪĖąžúľŽ©į Žč® 2Ž™ÖŽßĆžĚī žā¨ŽßĚŪĖąŽč§. Í∑łŽü¨Žāė ŽĻĄÍįÄžó≠ž†ĀžĚł žč†ÍłįŽä• žě•žē†ÍįÄ 6žėą(24%)žóźžĄú ŽįúžÉĚŪĖąÍ≥†, žĚīž§Ď žßÄžÜ枆ĀžĚł žč† ŽĆÄžĻė žĻėŽ£ĆŽ•ľ ŪēĄžöĒŽ°ú Ūēú Í≤ĹžöįÍįÄ 3žėąŽ°ú Ž≥īÍ≥†ŽźėžóąŽč§[11]. žĚīŽü¨Ūēú Ūē©Ž≥Ďž¶ĚžĚĄ žėąŽį©ŪēėÍ≥† žč† ÍłįŽä•žĚė žēÖŪôĒŽ•ľ žĶúžÜĆŪôĒ ŪēėÍłį žúĄŪēīžĄúŽäĒ žč† ž°įžßĀ Í≤Äžā¨Ž•ľ ŪÜĶŪēú ž°įÍłį žßĄŽč®Í≥ľ ž†Āž†ąŪēú Ūē≠žÉĚž†úžĚė žā¨žö©žĚī ž§ĎžöĒŪēėŽč§. ŽĒįŽĚľžĄú ŽĻĄŽ°Ě ŽįúžÉĚŽ•†žĚī ŽÜížßÄ žēäžĚÄ žßąŪôėžĚīžßÄŽßĆ žč†žě•žĚė žĘÖÍīīžĄĪ Ž≥ĎŽ≥Ğ̥ ž£ľžÜĆŽ°ú ŽāīžõźŪēú ŪôėžěźÍįÄ ŽįėŽ≥ĶŽźú žöĒŽ°úÍ≥Ą ÍįźžóľžĚė Í≥ľÍĪįŽ†•žĚī žěąÍĪįŽāė Ž©īžó≠ ÍłįŽä•žĚī ž†ÄŪēėŽźėžĖī žěąŽč§Ž©ī ÍįźŽ≥ĄŪēīžēľ Ūē† žßąŪôėžóź žóįŽįėž¶Ěžóź ŽĆÄŪēú Í≥†Ž†§ŽŹĄ ŪēĄžöĒŪē† Í≤ÉžúľŽ°ú žÉĚÍįĀŽźúŽč§.
REFERENCES
1. Michaelis L, Gutmann C. Uber einschl√ľsse in blasentumoren. Z Klin Med 1902;47:208‚Äď215.
2. Dobyan DC, Truong LD, Eknoyan G. Renal malacoplakia reappraised. Am J Kidney Dis 1993;22:243‚Äď252.


3. Sung DE, Yu E, Kim CS, Ro JY. Renal malakoplakia with secondary hepatic extension: a case report. Korean J Pathol 2003;37:199‚Äď203.
4. Stanton MJ, Maxted W. Malacoplakia: a study of the literature and current concepts of pathogenesis, diagnosis and treatment. J Urol 1981;125:139‚Äď146.


5. Daroux M, Frimat M, Mirault T, et al. Renal malakoplakia: an underestimate cause of renal failure. Nephrol Ther 2011;7:111‚Äď116.


6. Jo YI, Yoo TS, Heo WM, et al. A case of renal malakoplakia with renal insufficiency. Korean J Med 1996;51:843‚Äď849.
7. Terner JY, Lattes R. Malakoplakia of colon and retroperitoneum: report of a case with a histochemical study of the Michaelis-Gutman inclusion bodies. Am J Clin Pathol 1965;44:20‚Äď31.


8. Abdou NI, NaPombejara C, Sagawa A, et al. Malakoplakia: evidence for monocyte lysosomal abnormality correctable by cholinergic agonist in vitro and in vivo. N Engl J Med 1977;297:1413‚Äď1419.


9. Oliver JM. Impaired microtubule function correctable by cyclic GMP and cholinergic agonists in the Chediak-Higashi syndrome. Am J Pathol 1976;85:395‚Äď418.


(A) Abdominal computed tomography revealed a heterogeneous irregular peripheral enhancing mass with an air-containing lesion. (B) The mass extended to the peritoneal space and adjacent liver.
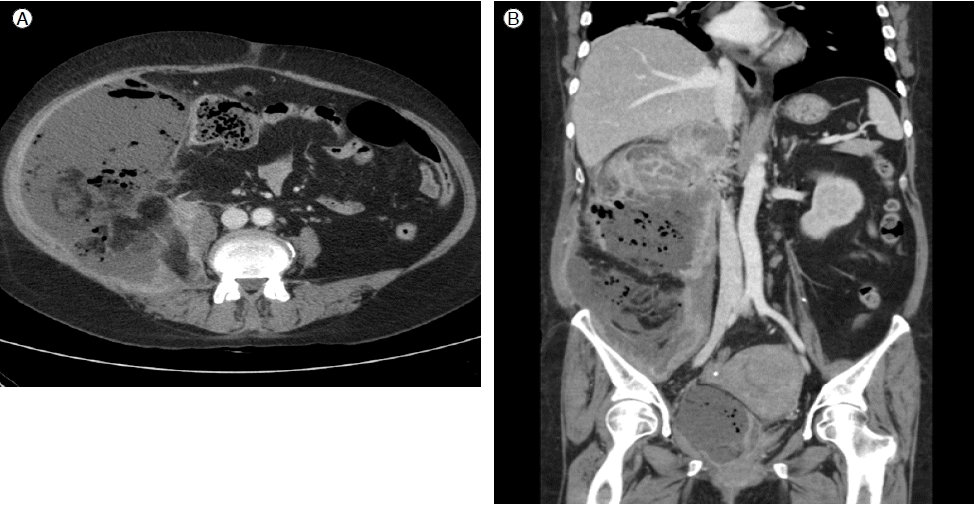
Figure 1.
(A) Abundant eosinophilic granular cytoplasm with round intracytoplasmic basophilic bodies, round nuclei with dispersed chromatin, and small conspicuous nucleoli. (B) An intracytoplasmic round basophilic body was positively stained on von Kossa staining, consistent with a Michaelis-Gutmann body (original magnification √ó 400).
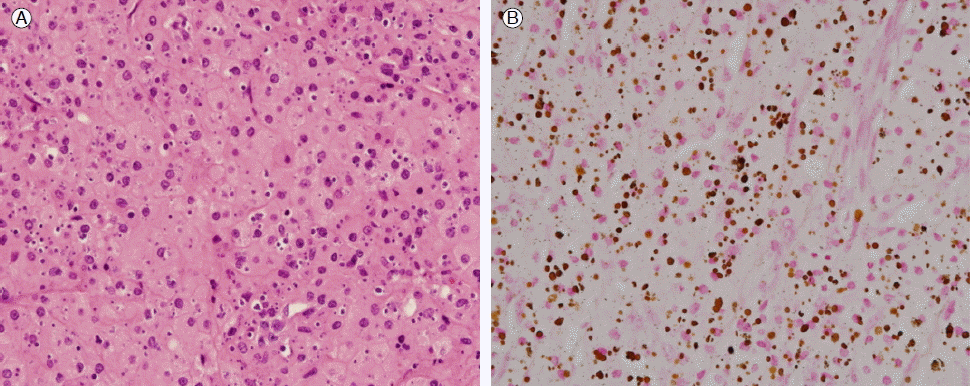
Figure 2.
-
METRICS

-
- 1 Crossref
- 0 Scopus
- 6,645 View
- 68 Download



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



