 |
 |
| Korean J Med > Volume 82(4); 2012 > Article |
|
мҡ”м•Ҫ
м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҖ кёүм„ұ лҢҖлҸҷл§Ҙ мҰқнӣ„кө°мқҳ мқјл¶ҖлЎң лҢҖлҸҷл§Ҙмқҳ нҢҢм—ҙ мң„н—ҳмқҙ мҰқк°Җн•ҳлҠ” м§ҲнҷҳмқҙлӢӨ. м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘ нҷҳмһҗм—җкІҢ мһҲм–ҙм„ң мҰқмғҒмқҙ м§ҖмҶҚлҗҳкұ°лӮҳ м җм°Ё нҒ¬кё°к°Җ мҰқк°Җн•ҳм—¬ нҢҢм—ҙмқҳ мң„н—ҳмқҙ мһҲмқ„ л•Ң мҲҳмҲ м Ғ м№ҳлЈҢ лҳҗлҠ” нҳҲкҙҖ лӮҙ мҠӨн…җнҠё мқҙмӢқнҺё мӮҪмһ… мӢңмҲ мқҙ н•„мҡ”н•ҳлӢӨ. ліё мҰқлЎҖлҠ” 78м„ё лӮЁмһҗ нҷҳмһҗк°Җ ліөл¶Җ л¶ҲнҺёк°җмқ„ мЈјмҶҢлЎң лӮҙмӣҗн•ҳм—¬ мҲҳмҲ м Ғ м№ҳлЈҢк°Җ н•„мҡ”н•ң ліөл¶Җ лҢҖлҸҷл§ҘлҘҳк°Җ 진лӢЁлҗҳм—Ҳмңјл©° мқҙм—җ лҸҷл°ҳлҗң нҒ° нҒ¬кё°мқҳ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҙ кҙҖм°°лҗң нҷҳмһҗмқҙлӢӨ. мҲҳмҲ м „ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘м—җ лҢҖн•ҳм—¬ нҳҲкҙҖ лӮҙ мҠӨн…җнҠё мқҙмӢқнҺё мӮҪмһ…н•ҳмҳҖкі мқҙнӣ„ ліөл¶Җ лҢҖлҸҷл§ҘлҘҳм—җ лҢҖн•ҳм—¬ мҲҳмҲ м Ғ м№ҳлЈҢлҘј мӢңн–үн•ҳм—¬ м„ұкіөм ҒмңјлЎң нҷҳмһҗлҘј м№ҳлЈҢн•ң мҳҲлҘј кІҪн—ҳн•ҳмҳҖкё°м—җ л¬ён—Ңкі м°°кіј н•Ёк»ҳ ліҙкі н•ҳлҠ” л°”мқҙлӢӨ.
Abstract
Penetrating aortic ulcers (PAUs) are part of acute aortic syndrome and can cause aortic rupture. We report a case of abdominal aortic aneurysm (AAA) with a PAU in the thoracic aorta. The patient was treated with thoracic aortic endovascular repair (TEVAR) for the PAU and open repair for the AAA. A 78-year-old man was admitted due to abdominal discomfort. Computed tomography (CT) showed a 6.8-cm AAA with a short neck and a large (4.2 Г— 3.3 cm) thoracic PAU. The patient was scheduled for AAA repair. Due to the risk of rupture of the thoracic PAU, TEVAR was performed in the PAU before surgery for the AAA. After stent graft insertion, the patient underwent surgery to repair the AAA. A follow-up CT scan showed no endoleakage or thrombus formation in the PAU. The patient had no specific symptoms during 1 year of follow-up. (Korean J Med 2012;82:481-486)
м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҖ 1934л…„ Shennanм—җ мқҳн•ҳм—¬ мІҳмқҢ кё°мҲ лҗң м§ҲнҷҳмңјлЎң лҢҖлҸҷл§Ҙ л°•лҰ¬мҰқ, лҢҖлҸҷл§Ҙ лІҪлӮҙ нҳҲмў… л“ұкіј н•Ёк»ҳ кёүм„ұ лҢҖлҸҷл§Ҙ мҰқнӣ„кө°мқҳ мқјл¶Җмқё м§ҲнҷҳмқҙлӢӨ[1,2]. мқҙм „ м—°кө¬м—җ л”°лҘҙл©ҙ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҖ кёүм„ұ лҢҖлҸҷл§Ҙ мҰқнӣ„кө° мӨ‘ 2.3-7.6%лҘј м°Ём§Җн•ҳлҠ” кІғмңјлЎң м•Ңл Өм ё мһҲмңјл©° лҢҖнҳҲкҙҖ лӮҙл§үмқҳ мЈҪмғҒнҢҗ лҚ®к°ң(atherosclerotic plaques)мқҳ к¶Өм–‘кіј лҜёлһҖмңјлЎң мқён•ҳм—¬ лҢҖнҳҲкҙҖ лӮҙл§үмқҳ кІ°мҶҗмқҙ л°ңмғқн•ҳм—¬ лҢҖнҳҲкҙҖ мӨ‘л§үмқҙ л…ём¶ңлҗҳм–ҙ л°ңмғқн•ҳлҠ” м§ҲнҷҳмқҙлӢӨ[3]. мқҙлҹ¬н•ң м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҖ нҳҲкҙҖ мҷёл§үк№Ңм§Җ нҢҢкёүлҗҳм–ҙ мң„ лҸҷл§ҘлҘҳлҘј л°ңмғқмӢңнӮӨкұ°лӮҳ кІҪмҡ°м—җ л”°лқј лҢҖлҸҷл§Ҙмқҳ нҢҢм—ҙмқ„ м•јкё°н• мҲҳ мһҲлӢӨ[4]. м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘м—җм„ң лҢҖлҸҷл§Ҙ нҢҢм—ҙмқҳ л°ңмғқлҘ мқҖ лҢҖлҸҷл§Ҙ л°•лҰ¬мҷҖ лҢҖлҸҷл§Ҙ лІҪ лӮҙ нҳҲмў…кіј 비көҗн–Ҳмқ„ л•Ң ліҙлӢӨ лҶ’мқҖ кІғмңјлЎң м•Ңл Өм ё мһҲлӢӨ[5]. м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҳ м№ҳлЈҢм—җ лҢҖн•ҳм—¬ лӘ…нҷ•нһҲ м •лҰҪлҗң м§Җм№ЁмқҖ нҳ„мһ¬к№Ңм§Җ м—ҶлӢӨ. к·ёлҹ¬лӮҳ н•ҳн–ү лҢҖлҸҷл§Ҙмқҳ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҳ м№ҳлЈҢлҠ” мҰқмғҒмқҙ м—ҶлҠ” кІҪмҡ° мІҳмқҢм—җлҠ” нҳҲм•• мЎ°м Ҳ л“ұ ліҙм „м Ғ м№ҳлЈҢлҘј мҡ°м„ м ҒмңјлЎң мӢңн–үн•ҳлӮҳ мҰқмғҒмқҙ м§ҖмҶҚлҗҳлҠ” кІҪмҡ°, к¶Өм–‘мқҳ нҒ¬кё°к°Җ м§ҖмҶҚм ҒмңјлЎң мҰқк°Җн•ҳм—¬ нҢҢм—ҙмқҳ мң„н—ҳм„ұмқҙ мһҲлҠ” кІҪмҡ°, лҢҖлҸҷл§ҘлҘҳк°Җ нҒ¬кІҢ нҳ•м„ұлҗҳлҠ” кІҪмҡ° л“ұм—җм„ңлҠ” мҲҳмҲ м Ғ м№ҳлЈҢ лҳҗлҠ” нҳҲкҙҖ лӮҙ мҠӨн…җнҠё мқҙмӢқнҺё мӮҪмһ…мқ„ кі л Өн•ҙм•ј н•ңлӢӨ[6]. м Җмһҗл“ӨмқҖ мӢ лҸҷл§Ҙ 6 mm м•„лһҳм—җ нҳҲм „мқҙ м№ЁлІ”лҗҳм–ҙ мһҲлҠ” 6.8 cm м§ҒкІҪмқҳ ліөл¶Җ лҢҖлҸҷл§ҘлҘҳмҷҖ 4.3 cm м§ҒкІҪмқҳ нқүл¶Җ лҢҖлҸҷл§Ҙ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҙ лҸҷмӢңм—җ мһҲлҠ” нҷҳмһҗм—җм„ң нқүл¶Җ лҢҖлҸҷл§Ҙ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘м—җ лҢҖн•ҳм—¬ нҳҲкҙҖ лӮҙ мҠӨн…җнҠё мқҙмӢқнҺё мӮҪмһ… мӢңмҲ мқҙнӣ„ ліөл¶Җ лҢҖлҸҷл§ҘлҘҳм—җ мҲҳмҲ м Ғ м№ҳлЈҢлҘј мӢңн–үн•ҳм—¬ м№ҳлЈҢн•ң 1мҳҲлҘј ліҙкі н•ңлӢӨ.
78м„ё лӮЁмһҗк°Җ мөңк·ј мҰқк°Җн•ҳлҠ” ліөл¶Җ л¶ҲнҺёк°җкіј ліөл¶Җ нҢҪл§Ңк°җмқ„ мЈјмҶҢлЎң лӮҙмӣҗн•ҳмҳҖлӢӨ. мғҒкё° нҷҳмһҗлҠ” нҸүмҶҢ кі нҳҲм••мқҳ лі‘л Ҙмқҙ мһҲм—Ҳмңјл©° 8л…„ м „м—җ н—ҲнҳҲм„ұ мӢ¬м§ҲнҷҳмңјлЎң кҙҖмғҒлҸҷл§Ҙ мӨ‘мһ¬мҲ мқ„ мӢңн–үн•ҳмҳҖкі , лҳҗн•ң лӮҙкІҪлҸҷл§Ҙ нҳ‘м°©мңјлЎң кІҪлҸҷл§Ҙ мҠӨн…җнҠё мӮҪмһ… мӢңмҲ нӣ„ мҷёлһҳ кІҪкіјкҙҖм°° мӨ‘мқҙм—ҲлӢӨ. кҙҖмғҒлҸҷл§Ҙ мӨ‘мһ¬мҲ мӢңн–ү лӢ№мӢң мӢ лҸҷл§Ҙ(renal artery) н•ҳл°© ліөл¶Җ лҢҖлҸҷл§Ҙмқҳ 50% к°Җлҹүмқҳ нҳ‘м°© мҶҢкІ¬мқ„ ліҙмҳҖмңјлӮҳ лҢҖлҸҷл§ҘлҘҳлҠ” ліҙмқҙм§Җ м•Ҡм•ҳкі лӢ№мӢң мһ„мғҒ мҰқмғҒ ліҙмқҙм§Җ м•Ҡм•„ кІҪкіјкҙҖм°°н•ҳкё°лЎң н•ҳмҳҖлҚҳ 분мқҙлӢӨ.
нҷҳмһҗлҠ” лӮҙмӣҗ м „ мҲҳк°ңмӣ”к°„ ліөл¶Җ л¶ҲнҺёк°җ л°Ҹ ліөл¶Җ нҢҪл§Ңк°җмқҙ мҰқк°Җн•ҳлҠ” мҰқмғҒмқ„ ліҙм—¬ м „мӮ°нҷ” лӢЁмёө мҙ¬мҳҒ мӢңн–үн•ҳмҳҖкі , ліөл¶Җ лҢҖлҸҷл§Ҙм—җм„ң мӢ лҸҷл§Ҙ н•ҳл°©м—җм„ң мҙқ мһҘкіЁ лҸҷл§Ҙ 분м§Җ(common iliac artery bifurcation) л¶Җмң„м—җ мқҙлҘҙлҠ” м§ҒкІҪ 6.8 cm л°Ҹ кёёмқҙ 11 cmмқҳ ліөл¶Җ лҢҖлҸҷл§ҘлҘҳк°Җ кҙҖм°°лҗҳм—Ҳмңјл©°(Fig. 1), 9лІҲ лҠ‘кіЁ лҶ’мқҙмқҳ нқүл¶Җ лҢҖлҸҷл§Ҙм—җм„ң м§ҒкІҪ 4.2 cm л°Ҹ кёёмқҙ 3.3 cmмқҳ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҙ кҙҖм°°лҗҳм—ҲлӢӨ(Fig. 2). нҷҳмһҗмқҳ ліөл¶Җ лҢҖлҸҷл§ҘлҘҳлҠ” мҷјмӘҪ мӢ лҸҷл§Ҙ м•„лһҳ 6 mm м •лҸ„м—җм„ң мӢңмһ‘лҗҳм—Ҳкі мқҙ л¶Җмң„м—җ нҳҲм „мқҙ м№ЁлІ”н•ҙ мһҲм–ҙм„ң ліөл¶ҖлҢҖлҸҷл§ҘлҘҳм—җ лҢҖн•ң мҠӨн…җнҠё мқҙмӢқнҺё мӮҪмһ…мҲ мқ„ мӢңн–үн• мҲҳ м—ҶлҠ” мғҒнғңмҳҖлӢӨ(Fig. 1). к·ёлҹ¬лҜҖлЎң, ліөл¶Җ лҢҖлҸҷл§ҘлҘҳмқҳ мҲҳмҲ м Ғ м№ҳлЈҢлҘј мң„н•ҳм—¬ ліёмӣҗ нқүл¶Җмҷёкіјм—җ мһ…мӣҗн•ҳмҳҖлӢӨ. мһ…мӣҗ мӢң нҷҳмһҗмқҳ нҷңл Ҙ 징нӣ„лҠ” нҳҲм•• 140/100 mmHg, л§Ҙл°• 36нҡҢ/분, нҳёнқЎ 20нҡҢ/분, мІҙмҳЁ 36в„ғмҳҖлӢӨ. мӢ мІҙкІҖмӮ¬м—җм„ң нҠ№мқҙ мҶҢкІ¬мқҖ л°ңкІ¬лҗҳм§Җ м•Ҡм•ҳлӢӨ. мһ…мӣҗ лӢ№мӢң кІҖмӮ¬ мҶҢкІ¬м—җм„ң нҳҲмғүмҶҢ 11.5 g/dL, л°ұнҳҲкө¬ 3,640/mm3, нҳҲмҶҢнҢҗ 95,000/mm3мҳҖмңјл©°, мғқнҷ”н•ҷ кІҖмӮ¬м—җм„ң AST 22IU/L, ALT 21IU/L, BUN 2.38 mg/dL, Creatinine 1.5 mg/dL, C л°ҳмқ‘м„ұ лӢЁл°ұм§Ҳ 0.01 mg/dLмқҙм—ҲлӢӨ. нҷҳмһҗлҠ” нҸүмҶҢ Aspirin (AstrixВ®, Boryung, Seoul, Korea) 100 mg, Clopidogrel (PlavixВ®, Sanofi-Aventis, Paris, France) 75 mg, Candesartan (AtacandВ®, AstraZeneca, London, UK) 16 mg, Rosuvastatin (CrestorВ®, AstraZeneca) 10 mg, Bisoprolol (ConcorВ®, Merck, Darmstadt, Germany) 2.5 mgмқ„ мҷёлһҳм—җм„ң ліөмҡ© мӨ‘мқҙм—ҲлӢӨ.
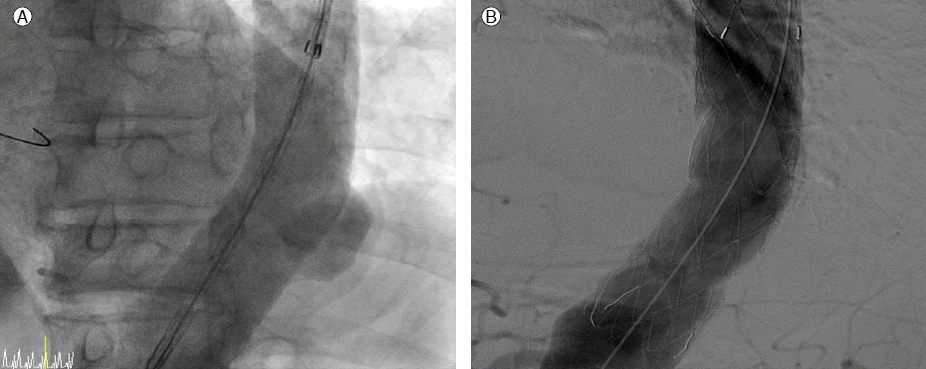
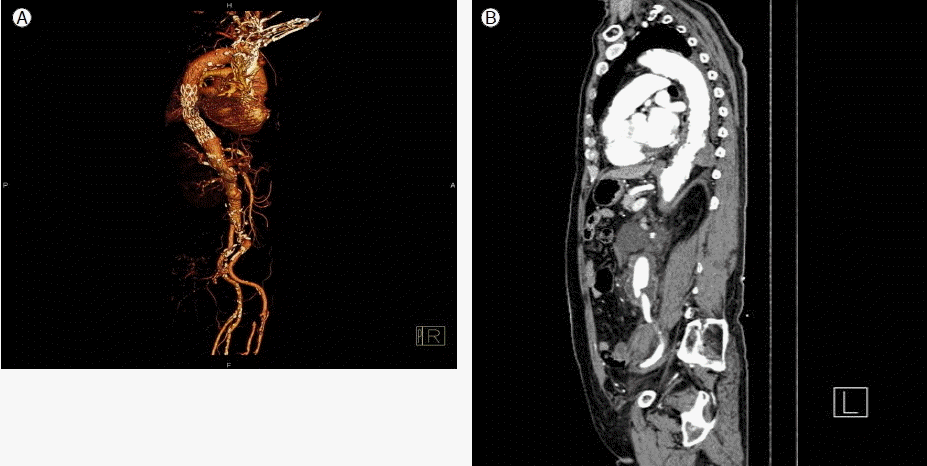
м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҳ м№ҳлЈҢ м—Ҷмқҙ ліөл¶Җ лҢҖлҸҷл§ҘлҘҳ мҲҳмҲ мқ„ мӢңн–ү мӢң мҲҳмҲ лҸ„мӨ‘ мӢ лҸҷл§Ҙ м•„лһҳмқҳ лҢҖлҸҷл§Ҙ нҳҲкҙҖмқ„ мқјмӢңм ҒмңјлЎң кІ°м°°н•ҳлҠ”лҚ° мқҙл•Ң нқүл¶Җ лҢҖлҸҷл§Ҙ лӮҙмқҳ м••л Ҙмқҳ мғҒмҠ№мңјлЎң мқён•ҳм—¬ нқүл¶Җ лҢҖлҸҷл§Ҙмқҳ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҳ нҢҢм—ҙ мң„н—ҳмқҙ мһҲм–ҙ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҳ м№ҳлЈҢ нӣ„ ліөл¶Җ лҢҖлҸҷл§ҘлҘҳ мҲҳмҲ мқ„ мӢңн–үн•ҳкё°лЎң н•ҳмҳҖлӢӨ. нқүл¶Җ лҢҖлҸҷл§Ҙ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқ„ мҷёкіјм Ғ мҲҳмҲ мӢңм—җлҠ” мҲҳмҲ мӢңк°„мқҖ кёёкі , мҲҳмҲ мӮ¬л§қлҘ лҸ„ лҶ’кі , мһҘкё° м„ұм Ғмқҙ мўӢм§Җ м•Ҡмңјл©°, нҷҳмһҗк°Җ 추к°ҖлЎң ліөл¶Җ лҢҖлҸҷл§ҘлҘҳ мҲҳмҲ мқ„ л°ӣм•„м•ј н•ҳлҠ” мғҒнҷ©мқҙм–ҙм„ң ліөл¶Җ лҢҖлҸҷл§ҘлҘҳ мҲҳмҲ м „м—җ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘м—җ лҢҖн•ҳм—¬ нҳҲкҙҖ лӮҙ мҠӨн…җнҠё мқҙмӢқнҺё(thoracic endovascular aortic repair, TEVAR)мқ„ мӢңн–үн•ҳкё°лЎң кІ°м •н•ҳмҳҖлӢӨ. мһ…мӣҗ 2мқјм§ё, нҳҲкҙҖ мЎ°мҳҒмҲ л°Ҹ TEVARлҘј мӢңн–үн•ҳмҳҖлӢӨ. мӢңмҲ мқҖ м „мӢ л§Ҳм·ЁлЎң 진н–үлҗҳм—Ҳмңјл©° мҷјмӘҪ лҢҖнҮҙлҸҷл§Ҙмқ„ мҷёкіјм Ғ нҳҲкҙҖ л…ём¶ң(surgical cutdown)мқ„ н•ҳмҳҖкі , мҳӨлҘёмӘҪ лҢҖнҮҙлҸҷл§Ҙмқ„ лҸҷл§ҘмІңмһҗ нӣ„ 6 French sheathлҘј л„ЈмқҖ нӣ„ marked pigtail (COOK Medical, Bloomington, IN, USA)мқ„ нҶөн•ҳм—¬ лҢҖлҸҷл§Ҙ мЎ°мҳҒмҲ мқ„ мӢӨмӢңн•ҳм—¬ н•ҳн–ү нқүл¶Җ лҢҖлҸҷл§Ҙм—җм„ң м „мӮ°нҷ” лӢЁмёө мҙ¬мҳҒм—җм„ң кҙҖм°°лҗң м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҳ мң„м№ҳлҘј нҷ•мқён•ҳмҳҖлӢӨ. мҷјмӘҪ лҢҖнҮҙлҸҷл§Ҙм—җ 5 French radial sheathлҘј л„ЈмқҖ нӣ„ 7 French femoral sheathлЎң л°”кҫёл©ҙм„ң м җм°Ём ҒмңјлЎң нҳҲкҙҖмқ„ нҷ•мһҘмӢңмј°кі мҠӨн…җнҠё мқҙмӢқнҺёмқҳ мӣҗнҷңн•ң нҶөкіјлҘј мң„н•ҳм—¬ 035-inch Lundquest stiffwire (COOK Medical)лҘј мғҒн–үлҢҖлҸҷл§Ҙк№Ңм§Җ л„ЈмқҖ нӣ„м—җ 16 French inner sheathлҘј мҷјмӘҪ мһҘкіЁлҸҷл§Ҙк№Ңм§Җ мҳ¬лҰ¬л©ҙм„ң мҠӨн…җнҠё мқҙмӢқнҺёмқҙ мһҳ нҶөкіј н• мҲҳ мһҲлҸ„лЎқ нҳҲкҙҖмқ„ нҷ•мһҘн•ҳмҳҖлӢӨ. м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘ л¶Җмң„м—җ м§ҒкІҪ 36 mm, кёёмқҙ 11 cmмқҳ мҠӨн…җнҠё мқҙмӢқнҺё(SEALв“Ү thoracic limb stent graft, S&G Biotech., Seoul, Korea)мқ„ мӮҪмһ…н•ҳмҳҖлӢӨ(Fig. 3). лҢҖлҸҷл§Ҙ мЎ°мҳҒмҲ м—җм„ң endoleakлҠ” м—Ҷм—Ҳкі мӢңмҲ м „нӣ„ нҠ№мқҙ н•©лі‘мҰқ л°ңмғқмқҖ м—Ҷм—ҲлӢӨ. мӢңмҲ мӢңн–ү 5мқј мқҙнӣ„ нҷҳмһҗлҠ” нқүл¶Җмҷёкіјм—җм„ң ліөл¶Җ лҢҖлҸҷл§ҘлҘҳм—җ лҢҖн•ҳм—¬ Aorto-biiliac bifurcation grafting мҲҳмҲ мқ„ мӢңн–ү л°ӣм•ҳлӢӨ. мҲҳмҲ лҸ„мӨ‘мқҙлӮҳ мҲҳмҲ мқҙнӣ„ нҷҳмһҗлҠ” нҠ№мқҙ н•©лі‘мҰқ л°ңмғқ м—Ҷмқҙ нҡҢліөлҗҳм—Ҳмңјл©° мҲ нӣ„ 8мқјм§ё м „мӮ°нҷ” лӢЁмёө мҙ¬мҳҒмқ„ мӢңн–үн•ҳмҳҖкі нқүл¶Җ лҢҖлҸҷл§Ҙмқҳ мҠӨн…җнҠё мқҙмӢқнҺё л¶Җмң„ л°Ҹ ліөл¶Җ лҢҖлҸҷл§ҘлҘҳмқҳ мҲҳмҲ л¶Җмң„мқҳ нҳҲм•Ў мң м¶ң мҶҢкІ¬ м—Ҷмқҙ м№ҳлЈҢлҗң кІғмқ„ нҷ•мқён•ҳмҳҖлӢӨ(Fig. 4). мқҙнӣ„ нҷҳмһҗлҠ” нҠ№мқҙ н•©лі‘мҰқ м—Ҷмқҙ мҲҳмҲ 13мқјм§ё нҮҙмӣҗн•ҳмҳҖкі , мқҙнӣ„ нҳ„мһ¬к№Ңм§Җ мҷёлһҳм—җм„ң 1л…„ лҸҷм•Ҳ мқҙмғҒ мҶҢкІ¬ м—Ҷмқҙ кІҪкіјкҙҖм°° мӨ‘мқҙлӢӨ.
нқүл¶Җ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘ нҷҳмһҗм—җкІҢм„ң м§ҖмҶҚм Ғмқҙкі л°ҳліөм Ғмқё нҶөмҰқмқҙ м§ҖмҶҚлҗҳкұ°лӮҳ мҳҒмғҒн•ҷм ҒмңјлЎң к¶Өм–‘мқҳ нҒ¬кё°к°Җ м§ҖмҶҚм ҒмңјлЎң мҰқк°Җн•ҳм—¬ нҢҢм—ҙмқҳ мң„н—ҳм„ұмқҙ мҰқк°Җн•ҳлҠ” кІҪмҡ°, нҒ¬кё°к°Җ нҒ° лҢҖлҸҷл§ҘлҘҳк°Җ л°ңмғқн•ҳлҠ” кІҪмҡ°м—җлҠ” м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘м—җ лҢҖн•ң мҲҳмҲ м Ғ м№ҳлЈҢк°Җ н•„мҡ”н•ҳлӢӨ[6]. к·ёлҹ¬лӮҳ л§ҺмқҖ мҲҳмқҳ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘ нҷҳмһҗл“ӨмқҖ кі л №кіј лҸҷл°ҳлҗң лӢӨлҘё м§Ҳнҷҳ л“ұмңјлЎң мқён•ҳм—¬ мҲҳмҲ кіј лҸҷл°ҳлҗң мң„н—ҳм„ұмқҙ лҶ“мқҖ кІғмңјлЎң м•Ңл Өм ё мһҲмңјл©° мҲҳмҲ кіј кҙҖл Ён•ң мӮ¬л§қлҘ мқҙ 5-20%к№Ңм§Җ м•Ңл Өм ё мһҲлӢӨ[7]. к·ёлҰ¬кі м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘ нҷҳмһҗм—җм„ң мҲҳмҲ м Ғ м№ҳлЈҢ нӣ„мһҘкё°к°„ кІҪкіјлҘј кҙҖм°°н•ҳмҳҖмқ„ л•Ң м•Ҫл¬јм№ҳлЈҢліҙлӢӨ мўӢмқҖ мһ„мғҒкІ°кіјлҘј ліҙмқҙм§Җ м•Ҡм•ҳкі м•Ҫл¬јм№ҳлЈҢмҷҖ 비мҠ·н•ң мһҘкё° мҳҲнӣ„лҘј ліҙмҳҖлӢӨ[8]. к·ёлһҳм„ң 1994л…„ Dake л“ұм—җ мқҳн•ҳм—¬ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘м—җ лҢҖн•ң нҳҲкҙҖ лӮҙ мҠӨн…җнҠё мқҙмӢқнҺё мӮҪмһ… мӢңмҲ мқҙ мІҳмқҢ мӮ¬мҡ©лҗң мқҙлһҳ мөңк·ј нҳҲкҙҖ лӮҙ мҠӨн…җнҠё мқҙмӢқнҺё мӮҪмһ… мӢңмҲ мқҙ м№ЁнҲ¬м„ұ к¶Өм–‘м—җ лҢҖн•ң м№ҳлЈҢ л°©лІ•мңјлЎң л§Һмқҙ мӮ¬мҡ©лҗҳкі мһҲлӢӨ[9]. мқҙлҹ¬н•ң нҳҲкҙҖ лӮҙ мҠӨн…җнҠё мқҙмӢқнҺё мӮҪмһ… мӢңмҲ мқҖ мҲҳмҲ м Ғ м№ҳлЈҢм—җ 비н•ҳм—¬ м Ҳк°ң л¶Җмң„к°Җ мһ‘кі мҲҳмҲ мӢңк°„мқҙ 짧мңјл©° лҢҖлҸҷл§Ҙмқ„ кІ°м°°н•ҳм§Җ м•Ҡмңјл©° 비침мҠөм Ғмқё мӢңмҲ лЎң мқён•ҳм—¬ мҲҳмҲ м—җ 비н•ҳм—¬ лҸҷл°ҳлҗң мӮ¬л§қлҘ л°Ҹ мқҙнҷҳмңЁмқҳ к°җмҶҢлҘј к°Җм ёмҷ”лӢӨ. Brinster л“ұмқҖ 21лӘ…мқ„ лҢҖмғҒмңјлЎң н•ң м—°кө¬м—җм„ң м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘ нҷҳмһҗм—җм„ң нҳҲкҙҖ лӮҙ мқҙмӢқнҺё мӢңмҲ мқ„ мӢңн–үн•ҳм—¬ 100%мқҳ мӢңмҲ м„ұкіөлҘ мқ„ ліҙмҳҖмңјл©° 4.8%мқҳ мӮ¬л§қлҘ мқ„ ліҙмҳҖлӢӨ[10]. м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҖ н•ҳн–ү нқүл¶Җ лҢҖлҸҷл§Ҙм—җ л§Һмқҙ л°ңмғқн•ҳл©° мқҙ л¶Җмң„лҠ” лҢҖлҸҷл§Ҙ мҲҳмҲ нӣ„ мІҷмҲҳ мҶҗмғҒмңјлЎң мӮ¬м§Җ л§Ҳ비к°Җ л§Һмқҙ л°ңмғқн•ҳлҠ” л¶Җмң„лӢӨ. нҳҲкҙҖ лӮҙ мқҙмӢқнҺё мӢңмҲ мқҖ лҢҖлҸҷл§Ҙ мҲҳмҲ м—җ 비н•ҳм—¬ мӮ¬м§Җ л§Ҳ비мқҳ мң„н—ҳлҸ„ м ҒмқҖ кІғмңјлЎң м•Ңл Өм ё мһҲлӢӨ[11]. мӮ¬м§Җл§Ҳ비мқҳ мң„н—ҳ л•Ңл¬ём—җ нҳҲкҙҖлӮҙ мқҙмӢқнҺё мӢңмҲ мӢңм—җ к°ҖлҠҘн•ң 짧кІҢ л„ЈлҠ” кІғмқҙ мӮ¬м§Җл§Ҳ비мқҳ мң„н—ҳмқ„ мӨ„мқҙлҠ” кІғмңјлЎң м•Ңл Өм ё мһҲлӢӨ.
мқҙлҹ¬н•ң лҢҖлҸҷл§Ҙм—җ лҢҖн•ң нҳҲкҙҖлӮҙ мқҙмӢқнҺё мӢңмҲ лЎң м№ҳлЈҢн•ң көӯлӮҙ мҰқлЎҖлЎң 2003л…„ Lee л“ұм—җ мқҳн•ҳм—¬ нқүл¶Җ лҢҖлҸҷл§ҘлҘҳм—җ мқҳн•ң лҢҖлҸҷл§Ҙ кё°кҙҖм§Җ лҲ„кіөмқҳ м№ҳлЈҢмқҳ мҳҲк°Җ мһҲм—Ҳмңјл©°[12], 2004л…„ лҢҖлҸҷл§ҘлҘҳ нҢҢм—ҙлЎң мқён•ң лҢҖлҸҷл§Ҙ н•ҳлҢҖм •л§ҘлЈЁ л°ңмғқмқ„ мҠӨн…җнҠё мқҙмӢқнҺёмңјлЎң м№ҳлЈҢн•ң мҳҲк°Җ мһҲм—ҲлӢӨ[13].
ліё мҰқлЎҖлҠ” ліөл¶Җ лҢҖлҸҷл§ҘлҘҳ мҲҳмҲ мқҙ мҳҲм •лҗң нҷҳмһҗм—җкІҢм„ң лҸҷл°ҳлҗң м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘ нҷҳмһҗм—җкІҢм„ң ліөл¶Җ лҢҖлҸҷл§ҘлҘҳ мҲҳмҲ м „ нҳҲкҙҖ лӮҙ мҠӨн…җнҠё мқҙмӢқнҺё мӮҪмһ… мӢңмҲ мқ„ мӢңн–үн•ң мҰқлЎҖмқҙлӢӨ. нҷҳмһҗлҠ” ліөл¶Җ лҢҖлҸҷл§ҘлҘҳм—җ лҢҖн•ң мҰқмғҒмқҖ мһҲм—ҲмңјлӮҳ нқүл¶Җ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҖ мҰқмғҒ м—Ҷмқҙ ліөл¶Җ лҢҖлҸҷл§ҘлҘҳм—җ лҢҖн•ң нҸүк°Җ мӨ‘ л°ңкІ¬лҗң мҰқлЎҖлЎң ліөл¶Җ лҢҖлҸҷл§ҘлҘҳлҠ” мҲҳмҲ м Ғмқ‘мҰқмқҙ лҗҳм—Ҳкі , нқүл¶Җ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘лҸ„ м§ҒкІҪ 4.2 cm л°Ҹ кёёмқҙ 3.3 cmлЎң к¶Өм–‘мқҳ нҒ¬кё°к°Җ м»Өм„ң мҲҳмҲ мқҙлӮҳ мӢңмҲ м Ғ м№ҳлЈҢк°Җ н•„мҡ”н•ң мғҒнғңмҳҖлӢӨ. Ganaha л“ұм—җ л”°лҘҙл©ҙ м§ҒкІҪ 2.1 cm, к№Ҡмқҙ 1.2 cmмқҙ л„ҳлҠ” нқүл¶Җ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘кіј нҒ¬кё°к°Җ м җм°Ё мҰқк°Җн•ҳлҠ” кІҪмҡ°лҠ” мҳҲнӣ„к°Җ мўӢм§Җ м•ҠмқҖ кІғмңјлЎң ліҙкі н•ҳмҳҖлӢӨ[14]. нқүл¶Җ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘ мҲҳмҲ кіј ліөл¶Җ лҢҖлҸҷл§ҘлҘҳ мҲҳмҲ мқ„ лҸҷмӢңм—җ мӢңн–үн•ҳлҠ” кІғмқҖ мҲҳмҲ мӢң мӮ¬л§қлҘ мқҙ лҶ’кі , нқүл¶Җ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҳ м№ҳлЈҢ м—Ҷмқҙ ліөл¶Җ лҢҖлҸҷл§ҘлҘҳ мҲҳмҲ мқҙ мӢңн–үлҗңлӢӨл©ҙ мҲҳмҲ лҸ„мӨ‘ мқјмӢңм ҒмңјлЎң лҢҖлҸҷл§Ҙ кІ°м°° мӢңм—җ нқүл¶Җ лҢҖлҸҷл§Ҙмқҳ м••л Ҙмқҙ мғҒмҠ№н•ҳм—¬ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҳ нҢҢм—ҙ мҡ°л Өк°Җ мһҲлӢӨ. к·ёлһҳм„ң нқүл¶Җ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘м—җ лҢҖн•ҳм—¬ нҳҲкҙҖ лӮҙ мҠӨн…җнҠё мқҙмӢқнҺё мӮҪмһ… мӢңмҲ мқҙнӣ„ ліөл¶Җ лҢҖлҸҷл§ҘлҘҳм—җ лҢҖн•ң мҲҳмҲ м Ғ м№ҳлЈҢлҘј н•ҳкё°лЎң кІ°м •н•ҳмҳҖкі н•©лі‘мҰқ м—Ҷмқҙ мӢңмҲ кіј мҲҳмҲ мқҙ мӢңн–үлҗҳм—ҲлӢӨ.
мқҙлҹ¬н•ң мҲҳмҲ мң„н—ҳм„ұмқ„ мӨ„мқҙкё° мң„н•ҳм—¬ ліөл¶Җ, нқүл¶Җ лӢӨл°ңм„ұ лҢҖлҸҷл§Ҙ м§Ҳнҷҳм—җ лҢҖн•ҳм—¬ лҸҷмӢңм—җ лҳҗлҠ” мӢңмҲ к°„м—җ мӢңк°„мқ„ л‘җкі нҳҲкҙҖ лӮҙ мҠӨн…җнҠё мқҙмӢқнҺё мӮҪмһ… мӢңмҲ мқ„ к°Ғк°Ғ мӢңн–үн•ҳлҠ” кІҪмҡ°лҸ„ мһҲлӢӨ[15]. к·ёлҹ¬лӮҳ ліөл¶Җ лҢҖлҸҷл§ҘлҘҳк°Җ мӢңмҲ м—җ м Ғн•©н•ҳм§Җ м•ҠмқҖ мӢ лҸҷл§Ҙм•„лһҳмқҳ лҢҖлҸҷл§Ҙмқ„ к°Җм§Җкі (нҳҲкҙҖ м§ҒкІҪ, нҳҲкҙҖмқҳ н•ҙл¶Җн•ҷм Ғ кө¬мЎ°), мһҘкіЁлҸҷл§Ҙмқҙ мӢңмҲ н•ҳкё°м—җ мһ‘кі , м„қнҡҢнҷ”к°Җ мӢ¬н•ң кІҪмҡ°м—җлҠ” нҳҲкҙҖ лӮҙ мҠӨн…җнҠё мқҙмӢқнҺё мӮҪмһ… мӢңмҲ мқҙ нһҳл“ кІҪмҡ°лҸ„ мһҲлӢӨ. мқҙлҹ¬н•ң кІҪмҡ°м—җ нқүл¶Җ лҢҖлҸҷл§Ҙ лі‘ліҖмқҖ нҳҲкҙҖ лӮҙ мҠӨн…җнҠё мқҙмӢқнҺё мӮҪмһ… мӢңмҲ лЎң м№ҳлЈҢн•ҳкі к·ё нӣ„ ліөл¶Җ лҢҖлҸҷл§ҘлҘҳ мҲҳмҲ мқ„ мӢңн–үн•ҳлҠ” кІғлҸ„ м№ҳлЈҢмқҳ н•ң к°Җм§Җ л°©лІ•мңјлЎң м ңмӢңлҗ мҲҳ мһҲлӢӨ. мқҙ нҷҳмһҗмқҳ кІҪмҡ°м—җлҠ” мўҢмёЎ мӢ лҸҷл§Ҙ 6 mm м•„лһҳм—җм„ң ліөл¶Җ лҢҖлҸҷл§ҘлҘҳк°Җ мӢңмһ‘лҗҳкі нҳҲм „мқҙ м№ЁлІ”н•ҳм—¬м„ң нҳҲкҙҖ лӮҙ мҠӨн…җнҠё мқҙмӢқнҺё мӮҪмһ… мӢңмҲ мқ„ н•ҳкё° мң„н•ң мӢ лҸҷл§Ҙ м•„лһҳл¶Җмң„м—җм„ң ліөл¶ҖлҢҖлҸҷл§ҘлҘҳмқҳ мӢңмһ‘к№Ңм§Җмқҳ мөңмҶҢ кұ°лҰ¬ 15 mmмҷҖ нҳҲм „мқҙ м№ЁлІ”н•ҳм§Җ м•Ҡм•„м•ј н•ҳлҠ” мӢңмҲ мЎ°кұҙмқҙ лҗҳм§Җ м•Ҡм•„м„ң мҲҳмҲ мқ„ мӢңн–үн•ҳмҳҖлӢӨ.
мқҙм—җ м Җмһҗл“ӨмқҖ мӢ лҸҷл§Ҙ м•„лһҳ л¶Җмң„мқҳ ліөл¶Җ лҢҖлҸҷл§ҘлҘҳмҷҖ нҒ° нҒ¬кё°мқҳ нқүл¶Җ лҢҖлҸҷл§Ҙ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘мқҙ лҸҷмӢңм—җ мһҲлҠ” нҷҳмһҗм—җкІҢм„ң нқүл¶Җ лҢҖлҸҷл§Ҙ м№ЁнҲ¬м„ұ лҸҷл§Ҙ кІҪнҷ”м„ұ к¶Өм–‘м—җ лҢҖн•ҳм—¬ нҳҲкҙҖ лӮҙ мҠӨн…җнҠё мқҙмӢқнҺё мӮҪмһ… мӢңмҲ мқҙнӣ„ ліөл¶Җ лҢҖлҸҷл§ҘлҘҳм—җ мҲҳмҲ м Ғ м№ҳлЈҢлҘј мӢңн–үн•ҳм—¬ нҡЁкіјм ҒмңјлЎң м№ҳлЈҢлҗң 1мҳҲлҘј ліҙкі н•ңлӢӨ.
REFERENCES
1. Shennan T. Dissecting Aneurysms: Special Report Series No. 193London: Medical Research Council; 1934.
2. Ahmad F, Cheshire N, Hamady M. Acute aortic syndrome: pathology and therapeutic strategies. Postgrad Med J 2006;82:305вҖ“312.



3. Eggebrecht H, Plicht B, Kahlert P, Erbel R. Intramural hematoma and penetrating ulcers: indications to endovascular treatment. Eur J Vasc Endovasc Surg 2009;38:659вҖ“665.


4. Baikoussis NG, Apostolakis EE. Penetrating atherosclerotic ulcer of the thoracic aorta: diagnosis and treatment. Hellenic J Cardiol 2010;51:153вҖ“157.

5. Coady MA, Rizzo JA, Elefteriades JA. Pathologic variants of thoracic aortic dissections: penetrating atherosclerotic ulcers and intramural haematomas. Cardiol Clin 1999;17:637вҖ“657.


6. Troxler M, Mavor AI, Homer-Vanniasinkam S. Penetrating atherosclerotic ulcers of the aorta. Br J Surg 2001;88:1169вҖ“1177.


7. Brinster DR. Endovascular repair of the descending thoracic aorta for penetrating atherosclerotic ulcer disease. J Card Surg 2009;24:203вҖ“208.


8. Tittle SL, Lynch RJ, Cole PE, et al. Midterm follow-up of penetrating ulcer and intramural hematoma of the aorta. J Thorac Cardiovasc Surg 2002;123:1051вҖ“1059.


9. Dake MD, Miller DC, Semba CP, Mitchell RS, Walker PJ, Liddell RP. Transluminal placement of endovascular stent-grafts for the treatment of descending thoracic aortic aneurysms. N Engl J Med 1994;331:1729вҖ“1734.


10. Brinster DR, Wheatley GH 3rd, Williams J, Ramaiah VG, Diethrich EB, Rodriguez-Lopez JA. Are penetrating aortic ulcers best treated using an endovascular approach? Ann Thorac Surg 2006;82:1688вҖ“1691.


11. Stone DH, Brewster DC, Kwolek CJ, et al. Stent-graft versus open-surgical repair of the thoracic aorta : mid-term results. J Vasc Surg 2006;44:1188вҖ“1197.


12. Lee JH, Park CB, Roh JH, et al. A case of aortobronchial fistula caused by thoracic aortic aneurysm and successfully treated with an endovascular stent graft. Korean J Med 2003;65(Suppl 3):S721вҖ“S726.
13. Sin SJ, Kim JW, Kim HS, et al. Endovascular stent-graft repair of aortocaval fistula complicated by the rupture of abdominal aortic aneurysm. Korean J Med 2004;67(Suppl 3):S746вҖ“S751.
Computed tomography image showing an abdominal aortic aneurysm (6.8 cm diameter) with an angulated, short-necked aorta (6 mm) and a thrombus below the renal artery.
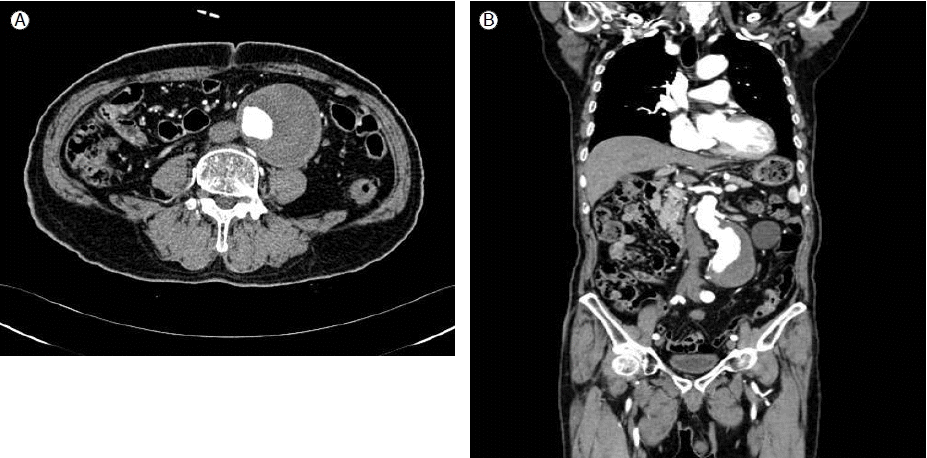
FigureВ 1.
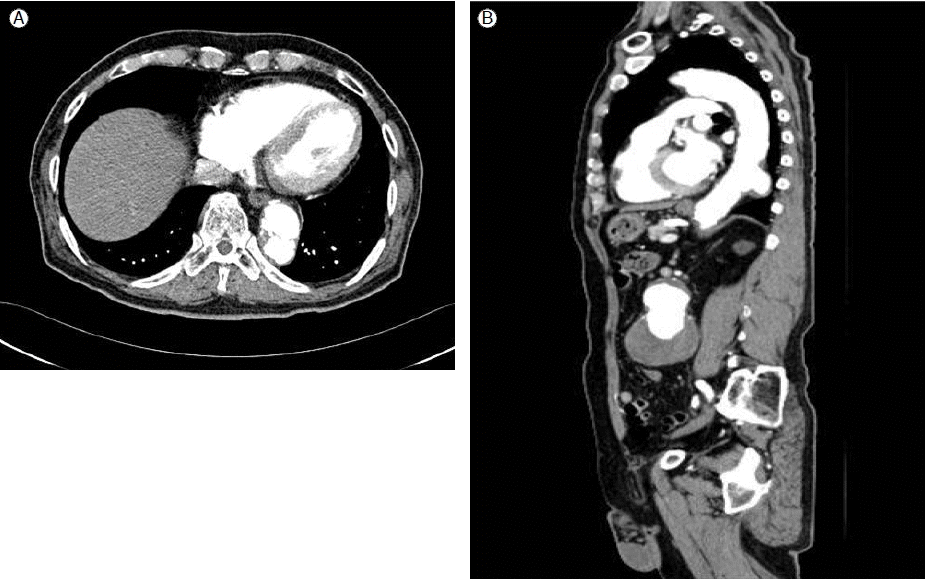
Computed tomography image showing a 4.2 Г— 3.3-cm thoracic penetrating aortic ulcer in the descending thoracic aorta.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




