ņä£ ļĪĀ
ļīĆļÅÖļ¦źĻČü ĒśłņĀä ļ░£ņāØņØĆ 1966ļģäļČĆĒä░ 2011ļģä Ēśäņ×¼Ļ╣īņ¦Ć, ļ¼ĖĒŚīņØ┤ ļ│┤Ļ│ĀļÉ£ Ļ▓ĮņÜ░ļŖö 58ņśł ņĀĢļÅäļĪ£ ļ¦żņÜ░ ļō£ļ¼Ė ņ¦łĒÖśņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[1]. ļīĆļÅÖļ¦źĻČü ĒśłņĀäņØĆ ņÜ░ņŚ░Ē׳ ļ░£Ļ▓¼ļÉśļŖö Ļ▓ĮņÜ░ļ│┤ļŗżļŖö ļćīĒśłĻ┤ĆĻ│ä ļśÉļŖö ļ¦Éņ┤łĒśłĻ┤ĆņŚÉ ņāēņĀäņØä ņ£Āļ░£ĒĢ┤ņä£ ņøÉņØĖņØä ņ░ŠļŖö ņżæņŚÉ ļ░£Ļ▓¼ĒĢśļŖö Ļ▓ĮņÜ░Ļ░Ć ļīĆļČĆļČäņØ┤ļŗż[2]. ĒśłņĢĪņØæĻ│Ā ņØĖņ×ÉņØś ņĪ┤ņ×¼ ļō▒ņ£╝ļĪ£ ņØĖĒĢ£ ĒśłņĢĪ Ļ│╝ņØæĻ│Ā ņāüĒā£ ļ░Å ļÅÖļ¦ź Ļ▓ĮĒÖöļ░ś ļō▒ņØ┤ ņŻ╝ ņ£äĒŚśņØĖņ×ÉļĪ£ ņĢīļĀżņĀĖ ņ׳ņ£╝ļ®░, ņ╣śļŻīņŚÉ ņ׳ņ¢┤ņä£ļŖö Ēśäņ×¼Ļ╣īņ¦Ć ņŚ¼ņĀäĒ׳ ļģ╝ļ×ĆņØ┤ ņ׳ņ£╝ļéś, ĒĢŁņØæĻ│Ā ņ╣śļŻīļéś ĒśłņĀäņÜ®ĒĢ┤ ņ╣śļŻī ļō▒ņØś ļé┤Ļ│╝ņĀü ņĢĮļ¼╝ņ╣śļŻīļź╝ ņÜ░ņäĀņĀüņ£╝ļĪ£ ņŗ£Ē¢ēĒĢśļ®░, ļ¦īņØ╝ ņØ┤ļ¤¼ĒĢ£ ņ╣śļŻīņŚÉļÅä ņāēņĀäņ£╝ļĪ£ ņØĖĒĢ£ ņŚ¼ļ¤¼ ĒĢ®ļ│æņ”ØņØ┤ ļ░£ņāØĒĢśĻ▒░ļéś, ļīĆļÅÖļ¦źĻČü ĒśłņĀäņØ┤ ņ£ĀļÅÖņä▒ņØĖ Ļ▓ĮņÜ░ļō▒ņŚÉļŖö ņłśņłĀņØ┤ ņäĀĒāØņĀü ņ╣śļŻīļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[1,3]. ļ│Ė ņĀĆņ×ÉļōżņØĆ ļ░śļ│ĄņĀüņØĖ ņé¼ņ¦Ć ĒŚłĒśł ļ░Å ņāēņĀäņ”ØņäĖļĪ£ ļé┤ņøÉĒĢ£ 59ņäĖ ļé©ņ×É ĒÖśņ×ÉņŚÉņä£ ļīĆļÅÖļ¦źĻČü ĒśłņĀäņ£╝ļĪ£ ņ¦äļŗ©ļÉ£ ņ”ØļĪĆļź╝ Ļ▓ĮĒŚśĒĢśņśĆĻĖ░ņŚÉ ļ¼ĖĒŚīĻ│Āņ░░Ļ│╝ ĒĢ©Ļ╗ś ļ│┤Ļ│ĀĒĢśļŖö ļ░öņØ┤ļŗż.
ņ”Ø ļĪĆ
ĒÖś ņ×É: 59ņäĖ, ļé©ņ×É
ņŻ╝ ņåī: ņóīņĖĪ ĒīöņØ┤ ļ¼Ąņ¦üĒĢśĻ│Ā ņĀĆļ”¼ļ®░ ņŗ£ļ”░ ļŖÉļéīņØ┤ ņ׳ņØī.
Ēśäļ│æļĀź: ĒÖśņ×ÉļŖö ņóīņĖĪ ĒīöņØ┤ ļ¼Ąņ¦üĒĢśĻ│Ā ņĀĆļ”¼Ļ│Ā ņŗ£ļ”░ ļŖÉļéīņØ┤ļōĀļŗżļ®░, Ļ░£ņØĖļ│æņøÉņŚÉ ļ░®ļ¼ĖĒĢśņŚ¼ ņĀĢļ░ĆĻ▓Ćņé¼ļź╝ ņ£äĒĢ┤ ļ│ĖņøÉņŚÉ ļé┤ņøÉĒĢśņśĆļŗż.
Ļ│╝Ļ▒░ļĀź ļ░Å ņé¼ĒÜīļĀź: 2ļģä ņĀä ļ░Å 4ļģä ņĀäņŚÉ Ļ░üĻ░ü ĒĢ£ņ░©ļĪĆņö® ņóīņĖĪ ĒĢśņ¦Ć ĒåĄņ”ØĻ│╝ ĒĢśņ¦ĆļČĆņóģ ņåīĻ▓¼ņØä ļ│┤ņŚ¼, ĒāĆ ļ│æņøÉņŚÉņä£ ĒśłņĀäņÜ®ĒĢ┤ ņ╣śļŻīļź╝ ņŗ£Ē¢ēņØä ļ░øņØĆ ļ│æļĀźņØ┤ ņ׳ņŚłļŗż.
ĒØĪņŚ░ļĀź: ņŚåņØī.
Ļ░ĆņĪ▒ļĀź: ļČĆļ¬©ļŗś ļæÉ ļČä ļ¬©ļæÉņŚÉņä£ ļćīņĪĖņżæņØ┤ ņ׳ļŗż.
ņØ┤ĒĢÖņĀü ņåīĻ▓¼: ļé┤ņøÉ ļŗ╣ņŗ£ ĒÖ£ļĀźņ¦ĢĒøäļŖö ĒśłņĢĢ 120/81 mmHg, ļ¦źļ░Ģ 70ĒÜī/ļČä, ĒśĖĒØĪņłś 20ĒÜī/ļČä, ņ▓┤ņś© 35.8ŌäāņśĆļŗż. ņØśņŗØņØĆ ļ¬ģļŻīĒĢśņśĆĻ│Ā Ēö╝ļČĆņŚÉ ļ░£ņ¦äņØĆ ņŚåņŚłļŗż. ĒØēļČĆ ņ▓Łņ¦äņŚÉņä£ ņ¢æņ¬Į ĒÅÉņĢ╝ ņĀäļ░śņŚÉ Ļ▒Ėņ│É ņłśĒżņØī ņåīĻ▓¼ņØĆ ņŚåņŚłņ£╝ļ®░ ņŗ¼ņØī ļśÉĒĢ£ ņĀĢņāüņØ┤ņŚłļŗż. ļ│ĄļČĆņ┤ēņ¦äņāü ĒŖ╣ņØ┤ņåīĻ▓¼ ņŚåņŚłņ£╝ļ®░ ņ¢æņ¬Į ĒĢśņ¦ĆņŚÉņä£ ļČĆņóģņåīĻ▓¼ Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśĻ│Ā ņŗĀĻ▓ĮĒĢÖņĀü Ļ▓Ćņé¼ņāü ļśÉĒĢ£ ĒŖ╣ņØ┤ ņåīĻ▓¼ ņŚåņŚłļŗż. ņóīņĖĪ ņāüņ¦ĆņØś ņĀĆļ”╝Ļ░ÉņØä ņŻ╝ļĪ£ ĒśĖņåīĒĢśņŚ¼, ņ¢æņĖĪ ņāüņ¦ĆņØś ĒśłņĢĢņ░©ņØ┤ļź╝ ĒÖĢņØĖĒĢśņśĆņ£╝ļéś ĒŖ╣ļ│äĒĢ£ ļ│ĆĒÖö ņåīĻ▓¼ņØĆ ņŚåņŚłļŗż.
Ļ▓Ćņé¼ņŗż ņåīĻ▓¼: ļ¦Éņ┤łĒśłņĢĪĻ▓Ćņé¼ņŚÉņä£ ļ░▒ĒśłĻĄ¼ 7,350/mm3, Ēśłņāēņåī 16.3 g/dL, ĒŚżļ¦łĒåĀĒü¼ļ”┐ 42%, ĒśłņåīĒīÉ 316,000/mm3ļĪ£ ņĖĪņĀĢļÉśņŚłļŗż. Ēśłņ▓Ł ņāØĒÖöĒĢÖ Ļ▓Ćņé¼ņŚÉņä£ļŖö AST 31 IU/L, ALT 34 IU/L, ņ┤Ø ļ╣īļ”¼ļŻ©ļ╣ł 0.7 mg/dL, ĒśłņżæņÜöņåīņ¦łņåī 11.4 mg/dL, Ēü¼ļĀłņĢäĒŗ░ļŗī 0.93 mg/dL, C-ļ░śņØæ ļŗ©ļ░▒ņ¦ł: 0.26 mg/dL, ņ┤Ø ņĮ£ļĀłņŖżĒģīļĪż 167 mg/dL, ņżæņä▒ņ¦Ćļ░® 109 mg/dL, Ļ│Āļ░ĆļÅä ņ¦Ćļŗ©ļ░▒ņ¦ł 54 mg/dL, ņĢäĒż ļŗ©ļ░▒ņ¦ł A1 138 mg/dL, ņĢäĒż ļŗ©ļ░▒ņ¦ł B 122 mg/dL, ļ”¼Ēżļŗ©ļ░▒ņ¦ł 72 mg/dL ļō▒ņ£╝ļĪ£ ņĀĢņāüņåīĻ▓¼ņØä ļ│┤ņśĆņ£╝ļ®░, ĒśĖļ¬©ņŗ£ņŖżĒģīņØĖ 8.8 ╬╝mol/L, Ēö╝ļĖīļ”¼ļģĖĻ▓É 239 mg/dL, Antithrombin III ĒĢŁņ▓┤ 105%, C ļŗ©ļ░▒ņ¦ł 134%, S ļŗ©ļ░▒ņ¦ł 113%, Lupus anticoaugulant ĒĢŁņ▓┤ ņØīņä▒, Cardiolipine Ab ĒĢŁņ▓┤ ņØīņä▒ņåīĻ▓¼ņ£╝ļĪ£ ļ¬©ļæÉ ņĀĢņāü ļ▓öņ£äļź╝ ļéśĒāĆļé┤ņŚłĻ│Ā, ņĀĆļ░ĆļÅä ņ¦Ćļŗ©ļ░▒ņ¦łļ¦ī 167 mg/dLļĪ£ ņāüņŖ╣ņåīĻ▓¼ņØä ļ│┤ņśĆļŗż.
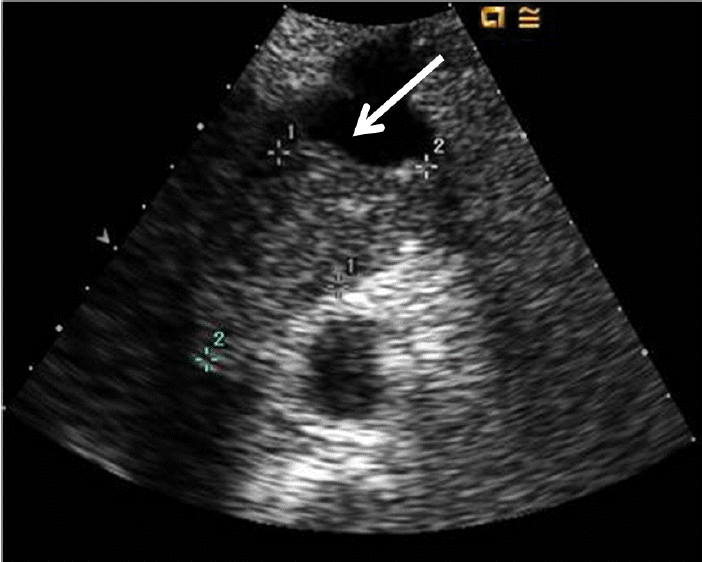
ņŗ¼ņן ņ┤łņØīĒīī ņåīĻ▓¼: Ļ▓ĮĒØēļČĆ ņŗ¼ņןņ┤łņØīĒīīņŚÉņä£ ļīĆļÅÖļ¦źĻČüņŚÉ ļČĆņ░®ļÉśņ¢┤ ņĀ£ĒĢ£ņĀüņØĖ ņøĆņ¦üņ×äņØä ļ│┤ņØ┤ļŖö 3.0 ├Ś 6.0 cm Ēü¼ĻĖ░ņØś ņóģĻ┤┤, ļŹ®ņ¢┤ļ”¼Ļ░Ć Ļ┤Ćņ░░ļÉśņŚłļŗż(Fig. 1).
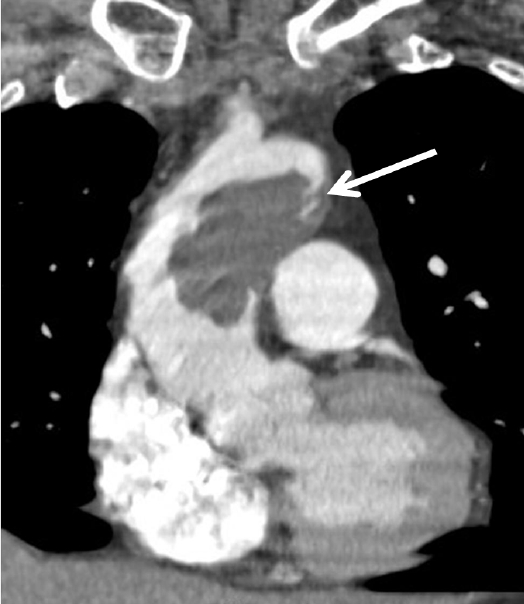
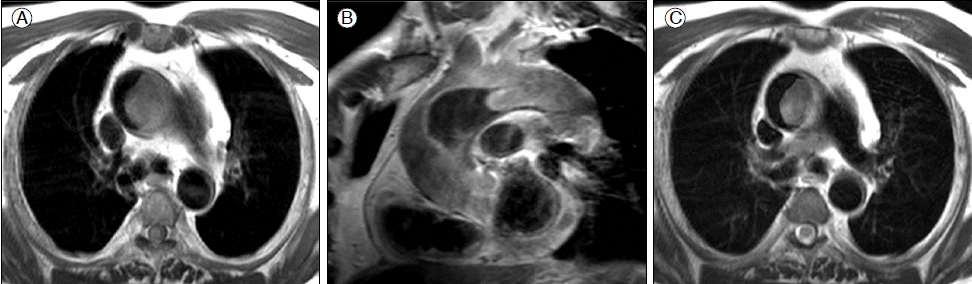
ņśüņāüņØśĒĢÖĻ│╝ Ļ▓Ćņé¼ ņåīĻ▓¼: ĒØēļČĆņĀäņé░ĒÖö ļŗ©ņĖĄņ┤¼ņśü Ļ▓Ćņé¼Ļ▓░Ļ│╝ ņĪ░ņśü ņ”ØĻ░ĢĒøä ļÅÖļ¦źĻ░Ģ ļé┤ņØś ņāüĒ¢ēļīĆļÅÖļ¦źņŚÉņä£ ļīĆļÅÖļ¦źĻČü ļČĆņ£äņŚÉ ņČ®ļ¦īĻ▓░ņåÉņØä ļ│┤ņØ┤ļŖö ļČĆņ£äĻ░Ć Ļ┤Ćņ░░ļÉśņŚłĻ│Ā(Fig. 2), ņ×ÉĻĖ░Ļ│Ąļ¬ģ ņśüņāüĻ▓Ćņé¼ņŚÉņä£ļŖö T1ņśüņāüņŚÉņä£ļŖö ņāüĒ¢ē ļīĆļÅÖļ¦źļČĆņ£äņŚÉ ņĀĆĻ░ĢļÅä ņåīĻ▓¼Ļ│╝ ņĪ░ņśüņ”ØĻ░Ģ ĒøäņŚÉļÅä ņóģĻ┤┤ ļé┤ļĪ£ ņĪ░ņśüņĀ£Ļ░Ć ĒØĪņłśļÉśņ¦Ć ņĢŖļŖö ņåīĻ▓¼ņØä ļ│┤ņśĆĻ│Ā, T2ņśüņāüņŚÉņä£ļŖö Ļ│ĀĻ░ĢļÅä ņóģĻ┤┤ņåīĻ▓¼ņØä ļ│┤ņśĆļŗż(Fig. 3). ņóīņĖĪ ņāüņ¦ĆņØś ņĀĆļ”╝ņ”ØņäĖļź╝ ņŻ╝ņåīļĪ£ ļé┤ņøÉĒĢśņśĆĻĖ░ņŚÉ ņóīņĖĪ ņćäĻ│©ĒĢś ļÅÖļ¦źļČĆĒä░ ņāüņÖäļÅÖļ¦ź ļō▒ņØś ĒśłĻ┤ĆņØä ļ®┤ļ░ĆĒ׳ Ļ┤Ćņ░░ĒĢ£ Ļ▓░Ļ│╝ Ēśæņ░®ņØ┤ļéś ņāēņĀäļō▒ņØś ņåīĻ▓¼ņØĆ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśļŗż.
ņĪ░ņśüņĀ£ ņŻ╝ņ×ģ ņĀäņŚÉ ņŗ£Ē¢ēĒĢ£ ņĀäņé░ĒÖö ļŗ©ņĖĄņ┤¼ņśüĻ▓Ćņé¼ņŚÉņä£ ņāüĒ¢ēļīĆļÅÖļ¦ź ņóģĻ┤┤ļČĆņ£äņØś ņĢłņ¬ĮņŚÉ Ļ│Āļ░ĆļÅäņØś ņäØĒÜīņ╣©ņ░®ņåīĻ▓¼Ļ│╝ ņ¢æņĀäņ×É ņĀäņé░ ļŗ©ņĖĄ ņ┤¼ņśüĻ▓Ćņé¼(PET-CT)ņŚÉņä£ ņóģĻ┤┤ ļé┤ļĪ£ FDGĻ░Ć ņäŁņĘ©ļÉśņ¦Ć ņĢŖļŖö ņåīĻ▓¼ ļō▒ņØä ņóģĒĢ®ņĀüņ£╝ļĪ£ Ļ│ĀļĀżĒĢ┤ ļ│╝ ļĢī, ĒśłņĀäņØä ņŗ£ņé¼ĒĢśļŖö ņåīĻ▓¼ņ£╝ļĪ£ ņóģņ¢æņØś Ļ░ĆļŖźņä▒ņØĆ ļ░░ņĀ£ļÉśņŚłļŗż.
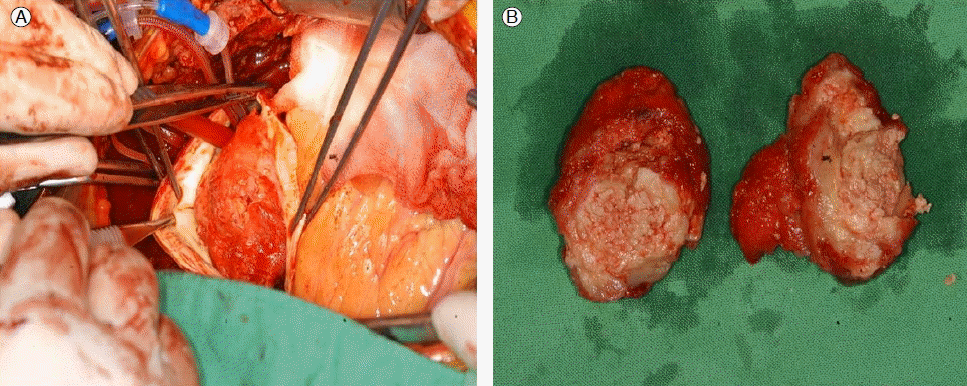
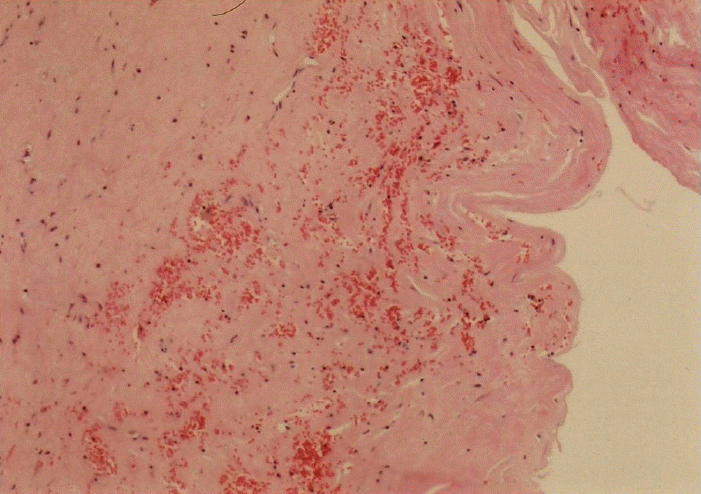
ņ╣śļŻī ļ░Å ņ×äņāü Ļ▓ĮĻ│╝: ņāüĻĖ░ ĒÖśņ×ÉļŖö ĒśłņĀä ņĀ£Ļ▒░ņłĀ ļ░Å ļīĆļÅÖļ¦ź ņ╣śĒÖśņłĀņØä ņŗ£Ē¢ēĒĢśņśĆĻ│Ā(Fig. 4), ĒÖśņ×É ņóīņĖĪ ĒīöņØ┤ ņĀĆļ”¼Ļ│Ā ņŗ£ļ”░ ņ”ØņäĖļŖö ĒśĖņĀäļÉśņŚłļŗż. ņłśņłĀ Ēøä ņŗ£Ē¢ēĒĢ£ ņĪ░ņ¦üļ│æļ”¼Ļ▓Ćņé¼ņŚÉņä£ Ēö╝ļĖīļ”░ ļ¼╝ņ¦łĻ│╝ ņŗĀņäĀĒĢ£ ņČ£Ēśłņä▒ļ░śņØ┤ Ļ┤Ćņ░░ļÉśņ¢┤(Fig. 5), ļīĆļÅÖļ¦źĻČüņŚÉ ĒśĢņä▒ļÉ£ ĒśłņĀäņ£╝ļĪ£ ĒÖĢņ¦äļÉśņŚłļŗż.
ņāüĻĖ░ ĒÖśņ×ÉļŖö ņÖĆĒīīļ”░ņØä ņ╣śļŻīļ¬®Ēæ£ INR 2-3ņØä ņ£Āņ¦ĆĒĢśļ®┤ņä£ ņÖĖļל ļé┤ņøÉ ņżæņØ┤ļ®░ ĒŖ╣ļ│äĒĢ£ ĒĢ®ļ│æņ”ØņØĆ ļ░£ņāØĒĢśņ¦Ć ņĢŖņĢśĻ│Ā ņ¦ĆņåŹņĀüņ£╝ļĪ£ ņÖĖļלņŚÉņä£ ņČöņĀüĻ┤Ćņ░░ ņżæņØ┤ļŗż.
Ļ│Ā ņ░░
ļīĆļÅÖļ¦źĻČü ĒśłņĀäņØĆ ņĀäņŗĀ ņāēņĀäņ”ØņØś ļō£ļ¼Ė ņøÉņØĖ ņżæņØś ĒĢśļéśņØ┤ļŗż. ļÅÖļ¦źĻ▓ĮĒÖöņ”Ø, ļīĆļÅÖļ¦ź ļ░Ģļ”¼, ņĢģņä▒ ņóģņ¢æ, ņÖĖņāü, ĒśłĻ┤Ć ļé┤Ēö╝ņäĖĒż ņ¦łĒÖś, ļ░Å ĒśłņĢĪ Ļ│╝ņØæĻ│Ā ņāüĒā£ ļō▒ņØ┤ ņØ┤ļ¤¼ĒĢ£ ļīĆļÅÖļ¦źĻČü ĒśłņĀä ĒśĢņä▒ņØś ņ£äĒŚśņØĖņ×ÉļĪ£ ņĢīļĀżņĀĖ ņ׳ņ£╝ļ®░[4], ĒØĪņŚ░ņØ┤ Ļ┤ĆņāüļÅÖļ¦źĻ│╝ Ļ▓ĮļÅÖļ¦ź, ĻĘĖļ”¼Ļ│Ā ļīĆļÅÖļ¦źņŚÉ ņŚ╝ņ”ØņØä ņ£Āļ░£ĒĢĀ ņłś ņ׳ļŖö ņ£äĒŚśņØĖņ×ÉļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[5]. ļīĆļÅÖļ¦źĻČü ĒśłņĀäņØĆ ļīĆļćī, ļ│ĄļČĆņןĻĖ░ ļ░Å ņé¼ņ¦ĆļČĆņ£äņŚÉ ĒżĒĢ©ĒĢ£ ņāēņĀäņ”ØņāüņØ┤ ļéśĒāĆļé£ ĒøäņŚÉ ņøÉņØĖņØä ņ░ŠļŖö Ļ▓Ćņé¼ļź╝ ĒåĄĒĢ┤ ļ░£Ļ▓¼ļÉśļŖö Ļ▓ĮņÜ░Ļ░Ć ļīĆļČĆļČäņØ┤ļ®░, ņÜ░ņŚ░Ē׳ ļ░£Ļ▓¼ļÉśļŖö Ļ▓ĮņÜ░ļŖö ļō£ļ¼╝ļŗż[2].
ļ¬ćļ¬ć ņĀĆņ×ÉļōżņØĆ ņŖżĒģīļĪ£ņØ┤ļō£ņØś ņןĻĖ░ļ│ĄņÜ®ņØ┤ ĒśłņĀäĒśĢņä▒ņØś ņøÉņØĖņØ┤ ļÉĀ ņłś ņ׳ļŗżĻ│Ā ņŻ╝ņןĒĢśļŖöļŹ░, ņŖżĒģīļĪ£ņØ┤ļō£Ļ░Ć ĒśłĻ┤Ćļé┤Ēö╝ņäĖĒżņØś ņ”ØņŗØ ļ░Å ņåÉņāüņØä ņ£Āļ░£ĒĢśņŚ¼ ļīĆļÅÖļ¦źņŚÉ ĒśłņĀäņØ┤ ĒśĢņä▒ļÉśĻ│ĀņØ┤ļĪ£ ņØĖĒĢ┤ ņĀäņŗĀ ņāēņĀäņ”ØņØ┤ ņ£Āļ░£ļÉśļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉ£ ļ░ö ņ׳ļŗż[6,7].
ļīĆļÅÖļ¦źĻČü ĒśłņĀäņØś ņ×ÉņŚ░ņĀüņØĖ ļ│æĒā£ņāØļ”¼ļŖö ņל ņĢīļĀżņĀĖ ņ׳ņ¦Ć ņĢŖņ¦Ćļ¦ī, ļīĆļČĆļČäņØś Ļ▓ĮņÜ░ ļÅÖļ¦ź Ļ▓ĮĒÖöļ░śņØ┤ ĻĖ░ņøÉņØ┤ ļÉśĻ│Ā, ņØ┤Ļ││ņŚÉņä£ ĒśłņĀäņØ┤ ļ░£ĒśäļÉśĻ│Ā ņ”ØņŗØĒĢśņŚ¼, ļīĆļČĆļČäņØ┤ ņØ┤ņ░©ņĀüņ£╝ļĪ£ ļ░£ņāØĒĢśļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[7,8]. Schneiderman ļō▒ņØĆ ļČłņĢłņĀĢĒĢ£ Ļ▓ĮĒÖöļ░śņØ┤ ĒśĢņä▒ļÉśņ¢┤ ņØ┤Ļ││ņŚÉņä£ ņØ╝ņŗ£ņĀüņ£╝ļĪ£ ĒśłņĀäņØ┤ ĒśĢņä▒ļÉśņ¢┤ ļīĆļÅÖļ¦źĻČü ĒśłņĀäņØ┤ ņāØņä▒ļÉĀ ņłś ņ׳ņ£╝ļ®░, ņŚ¼ĻĖ░ņŚÉ ļ¦īņØ╝ ņ×Āņ×¼ņĀüņØĖ Ļ│╝ņØæĻ│Ā ņāüĒā£ņØś ņ¦łĒÖśņØ┤ ļÅÖļ░śļÉśņŚłņØä ļĢī ļŹöņÜ▒ļŹö ņĪ░ņןļÉĀ ņłś ņ׳ļŗżĻ│Ā ņŻ╝ņןĒĢśņśĆļŗż[9]. Geha ļō▒ņØĆ 1966ļģäļČĆĒä░ 2003ļģäĻ╣īņ¦Ć 38ļ¬ģņØś ļīĆļÅÖļ¦źĻČü ĒśłņĀäĒÖśņ×Éļź╝ ļīĆņāüņ£╝ļĪ£ ļ¼ĖĒŚīĻ│Āņ░░ņØä ņŗ£Ē¢ēĒĢśņśĆļŖöļŹ░, ļŗ╣ļć©, Ļ│ĀĒśłņĢĢ, Ļ│Āņ¦ĆĒśłņ”Ø, ļ░Å ĒØĪņŚ░ņØś ņŗ¼ĒśłĻ┤ĆĻ│ä ņ£äĒŚśņØĖņ×É ņżæņŚÉņä£ ĒĢ£ Ļ░Ćņ¦Ć ņØ┤ņāüņØś ņ£äĒŚśņØĖņ×Éļź╝ ĒżĒĢ©ĒĢśļŖö Ļ▓ĮņÜ░Ļ░Ć 89.5%ņŚÉ ĒĢ┤ļŗ╣ļÉśņŚłĻ│Ā, ĻĖēņä▒ ņāēņĀäņ”ØņØĆ 92%ņŚÉņä£ ļ░£ņāØĒĢśņśĆļŗż[1]. ļ│Ė ņ”ØļĪĆņØś Ļ▓ĮņÜ░ļŖö ĒśłņĢĪ Ļ│╝ņØæĻ│Ā ņāüĒā£ņØś ņåīĻ▓¼ņØĆ ņĀäĒśĆ ņŚåņŚłņ£╝ļ®░, ļŗżļźĖ ĒśłņĀäņØś ņ£äĒŚśņØĖņ×É ļśÉĒĢ£ ĒĢ┤ļŗ╣ļÉśņ¦Ć ņĢŖņĢśļŗż. ļŗ©ņ¦Ć ņĀĆļ░ĆļÅä ņĮ£ļĀłņŖżĒģīļĪżņØ┤ ņ”ØĻ░ĆļÉśņ¢┤ ņ׳ņŚłĻ│Ā, ļīĆļÅÖļ¦źĻČü ĒśłņĀä ņĀ£Ļ▒░ņłĀņØä ņŗ£Ē¢ē ĒøäņŚÉ, ĒśłņĀäņØ┤ ļīĆļÅÖļ¦ź ļČĆņ░®ļČĆņ£äņŚÉ ļŗ©ļŗ©Ē׳ Ļ│ĀņĀĢļÉśņ¢┤ ņ׳ļŖö Ļ▓ĮĒÖöļ░ś ĒśĢņä▒ņØä ĒÖĢņØĖĒĢśņŚ¼ ļÅÖļ¦źĻ▓ĮĒÖöļ░śņØ┤ ļīĆļÅÖļ¦źĻČü ĒśłņĀäņØś ņøÉņØĖņ£╝ļĪ£ Ļ│ĀļĀżļÉśņŚłļŗż.
ņāüĒ¢ēļīĆļÅÖļ¦źņØ┤ļéś, ĻĘ╝ņ£äļČĆ ļīĆļÅÖļ¦źĻČü ļČĆņ£äļŖö Ļ▓ĮņŗØļÅä ņ┤łņØīĒīīĻ▓Ćņé¼ļĪ£ ĒśłņĀäņØś ļČĆņ░®ļČĆņ£ä, Ļ▓ĮĒÖöļ░śņØś ļ░ĆļÅä ļ░Å ņäØĒÜīĒÖö ļō▒ņØä ĒÅēĻ░ĆĒĢśĻĖ░Ļ░Ć ņłśņøöĒĢśļ®░, ņäĀļ│äĻ▓Ćņé¼ļĪ£ļÅä ņĄ£ņĀüņØś Ļ▓Ćņé¼ļĪ£ ņØ┤ņÜ®ļÉśĻ│Ā ņ׳ļŗż[1]. ĻĘĖļ¤¼ļéś ņøÉņ£äļČĆ ļīĆļÅÖļ¦źĻČüņØ┤ļéś, ĒØēļČĆ ļīĆļÅÖļ¦źļČĆņ£äļŖö Ļ▓ĮņŗØļÅä ņ┤łņØīĒīīļĪ£ ĒÅēĻ░ĆĒĢśĻĖ░Ļ░Ć ņ¢┤ļĀżņÜ░ļ®░, ņŗ¼ņן ļČĆņ£ä ņØ┤ņÖĖņØś ĒĢ┤ļČĆĒĢÖņĀü ĒÅēĻ░ĆņŚÉļŖö ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāü(MRI)ņØ┤ļéś, ĒØēļČĆ ņ╗┤Ēō©Ēä░ ņĀäņé░ ņ┤¼ņśü(CT) ļō▒ņØ┤ Ļ▓ĮņŗØļÅä ņ┤łņØīĒīīļ│┤ļŗż ļ»╝Ļ░ÉļÅä ļō▒ņØ┤ ļŹö ļø░ņ¢┤ļé£ Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[10]. ļīĆļÅÖļ¦źĻČü ĒśłņĀäņØĆ ļīĆļČĆļČäņØ┤ ĒøäĒ¢źņĀüņØĖ ņŚ░ĻĄ¼ļé┤ņÜ®Ļ│╝ ļō£ļ¼Ė ņ”ØļĪĆļĪ£ ņØĖĒĢ┤ ņ╣śļŻīņŚÉļŖö ņĢäņ¦üĻ╣īņ¦Ć ļģ╝ļ×ĆņØ┤ ļ¦ÄņØĆ ņāüĒā£ņØ┤ļ®░, ļö░ļØ╝ņä£ Ēæ£ņżĆņĀüņØĖ ņ╣śļŻīņ¦Ćņ╣©ļÅä ņĀĢĒĢ┤ņĀĖ ņ׳ņ¦Ć ņĢŖļŗż. ļ¬ćļ¬ć ņĀĆņ×ÉļŖö ĒśłņĀäņØś Ēü¼ĻĖ░Ļ░Ć 0.5-3 cm ņĀĢļÅäļĪ£ ņ×æĻ▒░ļéś, ļ¼┤ņ”ØņāüņØś Ļ▓ĮņÜ░ņŚÉļŖö ĒśłņĀäņÜ®ĒĢ┤ņ╣śļŻīļéś ĒĢŁņØæĻ│Ā ņ╣śļŻī ļō▒ņØś ļé┤Ļ│╝ņĀü ņĢĮļ¼╝ņ╣śļŻīļź╝ ņŻ╝ņןĒĢśņśĆļŗż[8,11].
ĻĘĖļ¤¼ļéś ļé┤Ļ│╝ņĀü ņĢĮļ¼╝ņ╣śļŻīņØś Ļ▓ĮņÜ░ ĒśłņĀäņØś ļČĆļČäņĀü ņÜ®ĒĢ┤ļĪ£ ņØĖĒĢ┤ Ēśłļźśļź╝ ĒāĆĻ│Ā ĒśłņĀäņØś ņØ╝ļČĆĻ░Ć ļ¢©ņ¢┤ņĀĖ ļéśĻ░Ć ņøÉņ£äļČĆ ņāēņĀäņØä ņśżĒ׳ļĀż ņĪ░ņןĒĢĀ ņłś ņ׳ļŗżĻ│Ā ņĢīļĀżņĀĖ ņ׳ņ£╝ļ®░[8,9], Bowdish ļō▒[12]ņØĆ ĒĢŁņØæĻ│Ā ņ╣śļŻīļź╝ ļ░øņØĆ 23ļ¬ģ ņżæņŚÉ 15ļ¬ģļ¦īņØ┤(65%) ĒśłņĀäņØś ņÖäņĀäĻ┤ĆĒĢ┤ļź╝ ļ│┤ņśĆļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆĻ│Ā, ļśÉ ļŗżļźĖ ņŚ░ĻĄ¼ņŚÉņä£ļŖö 9ļ¬ģ ņżæ 4ļ¬ģ(44%)ņŚÉņä£ ņÖäņĀäĻ┤ĆĒĢ┤ļź╝ ļ│┤Ļ│ĀĒĢ£ ļ░ö ļ░śļ│ĄļÉśļŖö ņāēņĀäņØś ĒĢ®ļ│æņ”ØņØ┤ ņ╣śļŻīņĀü ļ¼ĖņĀ£ļĪ£ ņ¦ĆņĀüļÉśņ¢┤, Ļ▓░ĻĄŁņŚÉļŖö ļīĆļÅÖļ¦źĻČüņŚÉ ĒśłņĀäņØś ļČĆņ░®ļČĆņ£äļź╝ ņÖäņĀäĒ׳ ņĀ£Ļ▒░ĒĢśĻĖ░ ņ£äĒĢ┤ņä£ļŖö ņłśņłĀņĀü ļ░®ļ▓ĢņØ┤ ĒĢäņłśņĀüņ×äņØä ņØ╝ļČĆ ņĀĆņ×ÉļōżņØĆ ņŻ╝ņןĒĢ£ļŗż[13,14]. ņłśņłĀņĀü ņ╣śļŻīņŚÉ ņ׳ņ¢┤ņä£ Ļ░Ćņן Ēü░ ļ¼ĖņĀ£ņĀÉņØĆ ĒśłņĀä ņĀ£Ļ▒░ņłĀ, ĒśłņĀäļé┤ļ¦ē ņĀłņĀ£ņłĀ ļ░Å ļīĆļÅÖļ¦ź ņ╣śĒÖśņłĀ ļō▒ņØä ņŗ£Ē¢ēĒĢ£ Ēøä ļ░£ņāØĒĢśļŖö ļīĆļćīņ¦łĒÖśņØś ļåÆņØĆ ĒĢ®ļ│æņ”Ø ļ░Å ņØ┤ĒÖśņ£©ļĪ£ ļ¦ÄņØĆ Ļ▓ĮņÜ░ņŚÉ 29%Ļ╣īņ¦Ć ļ│┤Ļ│ĀĒĢśļŖö Ļ▓ĮņÜ░ļÅä ņ׳ņ£╝ļéś, ņĄ£ĻĘ╝ņŚÉļŖö ņłśņłĀņĀü ņ╣śļŻī Ēøä ņé¼ļ¦ØļźĀ ļ░Å ņØ┤ĒÖśņ£©ņØä ņāüļīĆņĀüņ£╝ļĪ£ 2.6%Ļ╣īņ¦Ć ļé«ņČ░ ļ│┤Ļ│ĀĒĢ£ Ļ▓ĮņÜ░ļÅä ņ׳ļŗż[15]. ļö░ļØ╝ņä£ ņłśņłĀņĀü ņ╣śļŻīļŖö ļīĆļÅÖļ¦źĻČüņŚÉ ļÅÖļ¦źĻ▓ĮĒÖöļ░śņØ┤ ĻĄŁņåīņĀüņ£╝ļĪ£ Ļ│ĀņĀĢļÉśņ¢┤ ņ׳Ļ▒░ļéś ĒśłņĀäņØ┤ ļé┤Ļ▓ĮņØä ĒśĢņä▒ĒĢśĻ▒░ļéś ļ¦żņÜ░ ņ£ĀļÅÖņĀüņ£╝ļĪ£ ņøĆņ¦üņØ┤ļŖö Ļ▓ĮņÜ░, ĻĘĖļ”¼Ļ│Ā ļé┤Ļ│╝ņĀü ņĢĮļ¼╝ņ╣śļŻī ĒøäņŚÉļÅä ĒśłņĀäņØ┤ ņ¦ĆņåŹņĀüņ£╝ļĪ£ ļé©ņĢäņ׳Ļ▒░ļéś ļ░śļ│ĄņĀüņØĖ ņāēņĀäņØä ņ£Āļ░£ĒĢśļŖö Ļ▓ĮņÜ░ņŚÉ ņŗ£Ē¢ēļÉśņ¢┤ņĢ╝ ĒĢ£ļŗżĻ│Ā ņŻ╝ņןĒĢ£ļŗż[1,3]. Karalis ļō▒[16]ņØĆ 36ļ¬ģņØś ļīĆļÅÖļ¦ź ĒśłņĀäĒÖśņ×É ņżæņŚÉņä£ ĒśłņĀäņØ┤ ļé┤Ļ▓ĮņØä ĒśĢņä▒ĒĢśĻ▒░ļéś, ļ¦żņÜ░ ņ£ĀļÅÖņĀüņ£╝ļĪ£ ņøĆņ¦üņØ┤ļŖö 11ļ¬ģņØś ĒÖśņ×É ņżæņŚÉņä£ 8ļ¬ģ(73%)ņŚÉņä£ ņāēņĀäņØ┤ ņ£Āļ░£ĒĢśņśĆĻ│Ā, ņØ┤ņÖĆ ļ░śļīĆļĪ£ ĒśłņĀäņØ┤ Ļ│Āņ░®ļÉśņ¢┤ ņ׳ļŖö Ļ▓ĮņÜ░ 25ļ¬ģ ņżæņŚÉņä£ ņśżņ¦ü 3ļ¬ģ(12%)ļ¦īņØ┤ ņāēņĀäņØ┤ ļ░£ņāØĒĢśņśĆņØīņØä ļ│┤Ļ│ĀĒĢśņŚ¼ ņ£äņØś ņŻ╝ņןņØä ļÆĘļ░øņ╣©ĒĢśņśĆļŗż. ļ│Ė ņ”ØļĪĆņØś Ļ▓ĮņÜ░, ļīĆļÅÖļ¦źĻČüņŚÉ ļČĆņ░®ļÉ£ ĒśłņĀä ņżæ ņØ╝ļČĆĻ░Ć ņÖ╝ņ¬Į ņāüņ¦ĆļČĆņ£äļĪ£ ļ¢©ņ¢┤ņĀĖ ļéśĻ░Ć ņāēņĀä ņ”ØņāüņØä ņ£Āļ░£ĒĢśņŚ¼ ņåÉņØś ņĀĆļ”╝ņ”ØņäĖļź╝ ņ£Āļ░£Ē¢łņØä Ļ▓āņ£╝ļĪ£ ņČöņĖĪļÉ£ļŗż. Ļ░Ćņן ņĄ£ĻĘ╝ņŚÉ ĻĄŁļé┤ņŚÉņä£ ĒĢŁņØæĻ│Ā ņ╣śļŻīļź╝ ņäĀĒāØĒĢśņŚ¼ ņāēņĀä ļō▒ņØś ĒĢ®ļ│æņ”Ø ņŚåņØ┤ ņä▒Ļ│ĄņĀüņ£╝ļĪ£ ĒśłņĀäņØś ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢ£ ņ”ØļĪĆļź╝ ļ│┤Ļ│ĀĒĢśņśĆļŖöļŹ░[17], ļ│Ė ņ”ØļĪĆņÖĆ ļ╣äĻĄÉ ņŗ£ņŚÉ 3 cm ņØ┤ņāüņØś Ēü¼ĻĖ░ņÖĆ ļ¦żņÜ░ ņøĆņ¦üņ×äņØ┤ Ļ░ĢĒĢ£ ņ£ĀļÅÖņä▒ņŚÉņä£ļŖö Ļ│ĄĒåĄņĀÉņØä ļ│┤ņśĆĻ│Ā, ļ│Ė ņ”ØļĪĆņŚÉņä£ ļ░śļ│ĄļÉśļŖö ņāēņĀäņ”ØņāüņØä ļéśĒāĆļéĖ ņĀÉņØ┤ ņ░©ņØ┤ņĀÉņØ┤ļØ╝ ĒĢĀ ņłś ņ׳ņŚłļŗż. ņĢ×ņä£ ņ¢ĖĻĖēĒĢ£ ņŚ¼ļ¤¼ ļ¼ĖĒŚī ļō▒ņØä ņóģĒĢ®ĒĢ£ Ļ▓░Ļ│╝, ļ│Ė ņ”ØļĪĆņØś ļīĆļÅÖļ¦źĻČü ĒśłņĀäņØĆ 4 cm ņØ┤ņāüņØś Ēü¼ĻĖ░ņÖĆ ļé┤Ļ▓ĮņØä ĒśĢņä▒ĒĢ£ ņĀÉ, ĻĘĖļ”¼Ļ│Ā ņ£ĀļÅÖņä▒Ļ│╝ ļ░śļ│ĄļÉśļŖö ņāēņĀä ņ¢æņāü ļō▒ņ£╝ļĪ£ ļīĆļÅÖļ¦źĻČü ņ╣śĒÖśņłĀņØś ņłśņłĀņĀü ņ╣śļŻīĻ░Ć ņäĀĒāØļÉśņŚłļŗż.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






