서 론
심방세동은 전 인구의 약 2% 정도에서 나타나는 가장 흔한 부정맥 중 하나로 연령이 높아질수록 증가하여 65세 이상인 경우에는 약 5%의 유병률을 보인다. 모든 뇌경색 환자의 약 15-20%는 심방세동이 그 원인으로 알려져 있다. 미국의 Framingham Heart Study에 의하면 55-59세의 심방세동 환자에서 1년간 발생하는 뇌졸중은 1.5%이지만 80-89세의 노인에서는 23.5%로 증가한다[1]. 심방세동에 의한 뇌경색은 다른 원인에 의한 것보다 뇌경색의 범위가 크며 동반된 심질환으로 인하여 조기 및 만기 사망률이 높다. 그러나 심방세동에 의한 뇌졸중은 항응고제를 사용함으로써 예방이 가능하며 뇌졸중의 여러 원인들 중에서 가장 예방효과가 뚜렷한 유형이다[2]. 항응고제 중 와파린을 가장 많이 사용하고 있으나, 여러 가지 문제로 그 사용이 제한되어 있다. 하지만 최근에는 새로운 항응고제가 개발되거나 개발 중에 있으며, 이러한 약물들은 와파린을 보완할 수 있을 것으로 기대된다.
본 론
심방세동 환자에서 경구용 항응고 치료
류마티스 열에 의한 판막질환에서 동반된 심방세동의 경우 정상 대조군에 비해 뇌졸중의 위험이 17배 가량 증가하는 것으로 알려져 있으며, 뇌졸중 예방을 위하여 항응고제 투여는 전향적인 비교 연구결과는 없지만 지금까지 일반적인 관행으로 받아 들여졌다.
항혈전제 비교
항응고제와 위약 비교
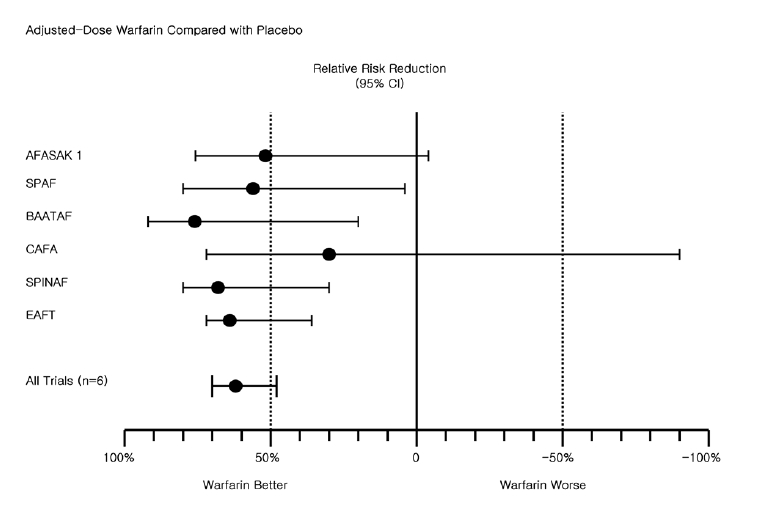
비판막성 심방세동 환자에서 색혈전증 일차 예방을 위한 5개의 연구(AFASAK I, SPAF, BAATAF, CAFA, SPINAF)와 이차 예방을 위한 1개의 연구(EAFT)를 포함하여 분석을 하여 보면, 모든 뇌졸중의 연간 발생 빈도가 항응고제를 사용한 군에서 위약을 사용한 군과 비교하였을 때 64% (95% CI, 49-74%) 감소하였다. 이러한 감소 효과는 일차 및 이차 예방 모두 비슷하게 나왔다. 또한 항응고제를 사용한 군이 총사망율을 26% 감소시키는 효과가 있었다(Fig. 1) [2]. 이러한 결과들은 뇌졸중의 위험을 갖고 있는 환자들은 특별한 금기가 없는 한 항응고제를 사용해야 하는 임상적인 배경이 되었다.
항혈소판제와 위약 비교
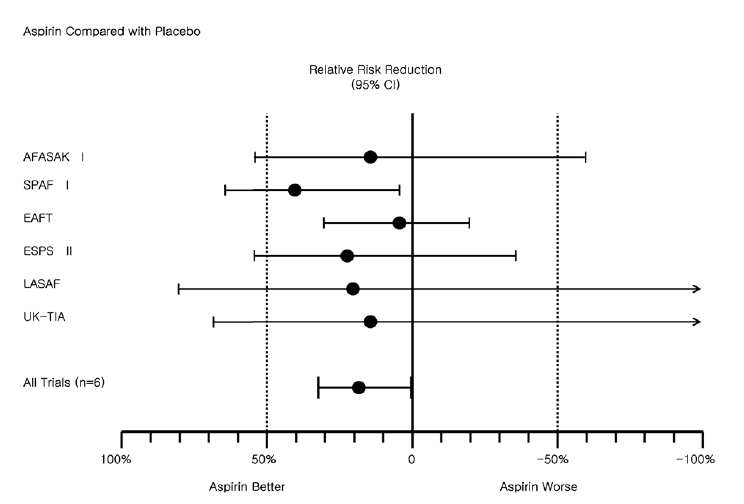
심방세동을 갖는 환자에서 색혈전증 예방을 위하여 아스피린을 사용한 연구(AFASAK I, SPAF I, EAFT, ESPS II, LASAF, UK-TIA)를 분석하여 보면, 모든 뇌졸중의 발생 빈도가 아스피린 사용한 군에서 위약을 사용한 군과 비교하여 19% (95% CI, 1-35%) 감소하였으며, 허혈성 뇌졸중은 21% (95% CI, 1-38%) 감소하였다(Fig. 2) [2]. 이 연구들에서 아스피린의 하루 용량은 50 mg에서 1,300 mg으로 다양하였지만, 약리학적으로 아스피린 75 mg이 거의 완전히 혈소판 억제를 하며, 저용량의 아스피린(< 100 mg)이 고용량의 아스피린(> 300 mg)보다 출혈의 위험성이 적으므로, 만약 아스피린을 사용한다면 저용량 아스피린이 권장된다.
항혈소판제 2제 요법과 단독 요법의 비교
ACTIVE-A 연구에서 1년간 주요 혈관질환 사고율이 아스피린과 클로피도그렐 병합 사용군 6.8%, 아스피린 단독 사용군 7.8%로 아스피린과 클로피도그렐 병합 사용군에서 주요 혈관질환 사고율이 11% (RR 0.89; 95% CI, 0.81-0.98) 감소하였다[12]. 이 차이는 주로 뇌졸중의 감소 때문이었는데 1년간 뇌졸중의 발생률은 아스피린과 클로피도그렐 병합 사용군 2.4%, 아스피린 단독군 3.3%로 병합 사용군에서 28% 감소하였다. 1년간 중요한 출혈은 아스피린과 클로피도그렐 병합 사용군 2.0%, 아스피린 단독군 1.3%로 병합 사용군에서 57% (RR 1.57; 95% CI, 1.29-1.92) 증가하였다. 그리고 총 출혈은 아스피린과 클로피도그렐 병합 사용군 9.7%, 아스피린 단독군 5.7%로 68% 증가하였다. 이러한 결과는 심방세동이 있으면서 항응고 치료가 필요하지만, 항응고제를 사용할 수 없을 때 아스피린 단독요법보다는 아스피린과 클로피도그렐을 같이 쓰면 효과적이라는 것을 보여준다. 그러나 클로피도그렐을 같이 사용 시 출혈이 증가할 수 있으므로 주의를 요한다.
항혈소판제와 항응고제 비교
항응고제인 와파린의 장기적인 투여는 필연적으로 출혈과 관련된 합병증을 동반할 수 있으며 이를 피하기 위하여 정기적으로 혈액검사를 실시하여야 한다. 이러한 문제점의 해결방안으로 항응고제 대신 항혈소판제의 사용을 고려할 수 있다.
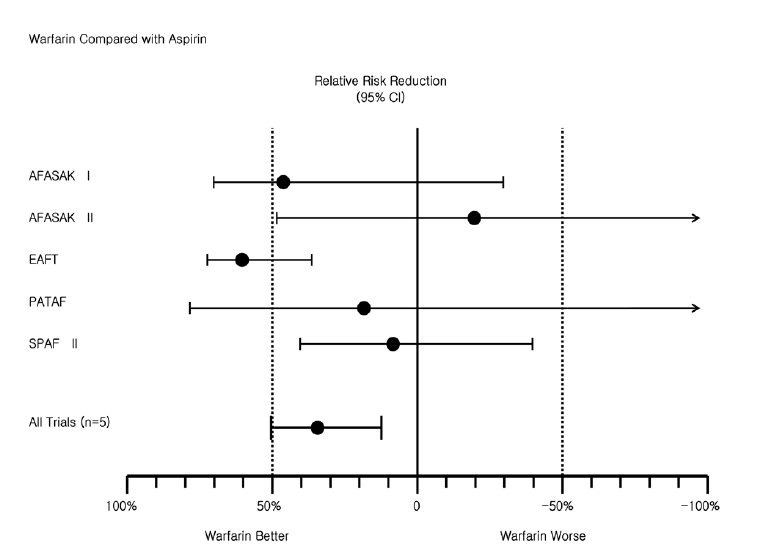
항응고제와 아스피린의 직접적인 비교 연구에서 항응고제가 중증 뇌졸중(뇌허혈성, 출혈성), 혈전증 예방에 39-52% 더 우수하였으며, 주된 출혈에서는 차이가 없었다(Fig. 3) [2].
ACTIVE-W 연구에서 아스피린과 클로피도그렐을 동시에 사용한 군보다 항응고제를 단독으로 사용한 군에서 뇌졸중 위험도가 40% (95% CI, 18-56%) 감소하였고, 출혈 합병증은 차이가 없었다[13]. 이러한 결과들은 항혈소판제 단독 요법이든 병합요법이든 모두가 항응고제보다는 효과가 약하므로, 항혈전 치료가 필요한 경우에는 특별한 금기가 없는 한 항응고제를 사용하여야 된다.
새로운 경구용 항응고제
현재 널리 사용되고 있는 항응고제인 와파린은 좁은 치료 범위, 긴 반감기에 의해 효과가 늦게 나타나는 점, 약물 및 음식물과의 상호 작용 등에 의해 INR을 일정하게 유지하기 힘들며, 자주 INR 감시를 해야 하는 단점이 있다. 최근에 부작용은 최소화 하면서, 효과는 같거나 더 좋은 작용을 나타내며, 용량 조절 및 감시가 필요하지 않는 새로운 항응고제 들이 개발되어 임상연구가 활발히 진행되고 있다(Table 1). 이러한 항응고제들은 Xa 차단제와 트롬빈 억제제로 나누어 이야기할 수 있다(Fig. 4).
Dabigatran
Dabigatran은 경구용 직접적인 트롬빈 억제제(direct thrombin inhibitor)로 반감기는 14-17시간이고 음식물과 상호 작용이 없으며 신장으로 배설된다. 이러한 약리 효과는 INR 감시가 필요 없으며, 고정된 용량을 투여할 수 있는 장점이 있다. 심방세동 환자에서 와파린과의 직접 비교 연구[14]에서 dabigatran 110 mg 하루 2번 투여는 와파린과 비교하여 뇌졸중의 예방 효과에서는 비슷(non-inferior)하며, 출혈성 부작용은 적었다. 150 mg 하루 2번 복용은 뇌졸중 예방 효과에서는 와파린보다 우수하였으며(RR 0.66; 95% CI, 0.53-0.82; p < 0.001 for superiority), 출혈의 위험성은 비슷하였다. 2011년 미국 심장학회에서는 심방세동 환자에서 뇌졸중과 전신성 색전증의 위험성을 갖고 있는 경우에는 이를 예방하기 위해 와파린 대신 dabigatran를 대체해서 사용할 수 있음을 제시하였다[5]. 하지만, 판막질환자, 기계성 판막 치환자에서 dabigatran 효과에 대한 임상연구는 아직 없으므로 이런 환자에서의 사용은 주의를 요한다.
Rivaroxaban
Rivaroxaban은 하루에 1번 복용하는 direct factor Xa inhibitor로서 반감기는 9-13시간이고, 음식물과 상호 작용이 없는 장점을 갖고 있다. 심방세동 환자에서 와파린과 직접 비교한 연구[15]에서 rivaroxaban 20 mg은 뇌졸중 및 전신 색전증 예방에 있어서 와파린과 비슷(non-inferior)한 결과를 보였으며(HR 0.79; 95% CI, 0.66-0.96; p < 0.001 for non-inferiority), 출혈의 위험성은 비슷하였다.
Apixaban
Apixaban은 경구용 direct factor Xa inhibitor로서 반감기는 9-14시간이고, 음식물과 상호작용이 없는 약물로, 심부 정맥 혈전증의 치료에 사용된다. 심방세동의 환자에 있어서는 아스피린과의 직접 비교한 연구[16]에서 와파린을 사용할 수 없는 환자들을 대상으로 apixaban 5 mg 하루 2번 사용한 경우 아스피린 81-324 mg을 사용한 경우보다 뇌졸중을 예방하는 효과가 뛰어나며, 출혈의 위험성은 비슷한 결과를 보였다. 와파린과의 직접적인 비교 연구[17]에서는 뇌졸중 및 전신성 색전증 예방에 있어서 더 우수하였으며(RR 0.79; 95% CI, 0.66-0.95; p < 0.001 for non-inferiority; p = 0.01 for superiority), 출혈(RR 0.69; 95% CI, 0.60-0.80; p < 0.001) 및 사망(RR 0.89; 95% CI, 0.80-0.99; p = 0.047)의 위험성이 더 적었다.
색혈전증 위험인자의 계층화 및 치료 전략
심방세동 환자에서 뇌졸중의 위험인자는 나이, 성별, 고혈압, 허혈성 또는 류마티스 심장질환, 기계판막, 심부전, 뇌졸중 또는 일과성 허혈성 발작의 병력, 색혈전증 병력, 심장 내 혈전의 증거, 당뇨병 등이다(Table 2).
2010년 유럽 치료 지침에 의하면 고위험군(‘Major’ risk factors)은 뇌졸중이나 일과성 허혈성 발작의 병력, 색혈전증, 75세 이상의 고령, 승모판막 협착증, 기계 심장 판막이며, 중등도 위험군(‘clinically relevant non-major’ risk factors)은 심부전(좌심실 구혈률 40% 이하), 고혈압, 당뇨병, 여성, 65-74세 고령, 혈관 질환(심근경색증, 복합성 대동맥 플라크, 사지 혈관 질환)이다. 이러한 중등도 위험인자들이 2개 이상 존재할 경우에는 고위험군으로 판단한다(Table 3).
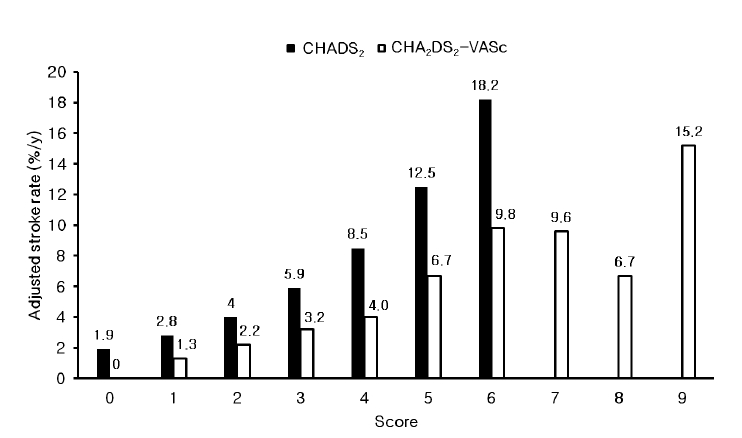
심방세동 환자에서 항혈전 치료는 뇌졸중 및 색혈전증에 대한 위험인자의 유무에 따라 결정된다. CHADS2 (congestive heart failure, hypertension, age > 75 years, diabetes mellitus, previous TIA or stroke) 점수를 이용한 방법은 간단하게 적용할 수 있는 장점이 있으므로, 환자의 첫 치료적 접근방법으로 사용할 수 있고, 이는 부정맥을 전공하지 않은 일차 진료 기관에서도 쉽게 사용할 수 있다. 최근에는 이를 세분화한 CHA2DS2-VASc 점수를 이용한 치료적 접근 방법도 사용되어진다(Table 4). CHADS2 점수 및 CHA2DS2-VASc 점수가 높을수록 뇌졸중의 위험도는 증가한다(Fig. 5).
항혈전 치료는 미국, 캐나다 및 유럽 모두 CHADS2 점수 2 이상인 경우에는 금기증이 없는 한 항응고제(INR 2.0-3.0) 사용을 권장하고 있다(Table 5). CHADS2 점수 0-1인 경우에는 좀 더 상세히 위험도를 평가하여 적절한 치료 방법을 선택해야 한다. CHA2DS2-VASc 점수를 이용하면 CHADS2 점수가 2점 미만인 환자들을 좀 더 상세히 구별해 낼 수 있겠지만, 아직까지 CHA2DS2-VASc 점수를 이용한 치료가 CHADS2 점수를 이용한 치료보다 우월하다는 증거는 없다.
출혈의 위험성
항응고제 사용 시 심각한 출혈이 0.1-6.0% 정도로 발생하므로, 약물을 사용하기 전 출혈의 위험성에 대한 평가가 필요하다. 와파린 사용 시 출혈의 위험성은 INR 값과 밀접한 관련이 있는데, 3.0 이상인 경우에 출혈의 위험성이 현저하게 증가한다. 뇌출혈 예측인자로는 고령, 뇌졸중 병력, 고혈압 등이다. 이 중 고령과 뇌졸중 병력은 변형시킬 수 없는 인자이므로, 혈압의 조절과 INR의 적극적 감시가 뇌출혈을 최소화 할 수 있다. 특히 제산제, 항부정맥제, 항우울제, 아스피린, NSAID, 스타틴과 같은 새로운 약을 추가 시에는 약물 상호 작용에 대한 주의가 필요하다.
적절한 INR 유지
AFFIRM [19]과 RACE [20] 연구에서 뇌졸중이 발생하였던 환자 군을 분석하여 보면 항응고제 사용이 중단되었거나 항응고 수치가 낮았던 경우가 대부분이었다. RACE 연구에서 색혈전증을 경험하였던 환자 35명 중 23명(66%)은 INR < 2.0이었다. AFFIRM 연구에서도 허혈성 뇌졸중이 발생하였던 175명 중 113명(72%)은 항응고제 사용이 중단되었거나 INR < 2.0이었으며, 율동 조절(rhythm control)군에서 색혈전증이 발생한 환자의 75%는 정상 동율동으로 유지되고 있는 중에 발생하였다. 이러한 결과는 심실 반응수를 조절하든지 또는 동율동으로 전환하여 유지하든지 경구용 항응고제를 사용하여 INR 2.0-3.0 사이로 조절하는 것이 필요함을 보여준다.
비판막성 심방세동 환자에서 와파린을 사용할 때 일반적으로 INR을 2-3으로 유지하면 출혈의 위험성을 높이지 않으면서 뇌졸중 및 전신적인 혈전증을 예방할 수 있다. 하지만, 와파린에 대한 반응은 개인차가 심하고, 약물 및 음식물과의 상호작용이 심하기 때문에 적절한 수준의 INR을 유지하는 것이 매우 힘들다. 발표된 임상연구들을 보더라도 60-65% 정도에서만 INR이 2.0-3.0 정도로 유지되므로, 실제 임상에서는 50% 미만일 것으로 추정된다. 출혈의 위험성 때문에 고령에서 INR을 1.8-2.5 정도로 낮게 유지하는 것이 제시되기도 하는데, 이는 임상 증거가 없으며, 코호트 연구에서 INR 1.5-2.0은 뇌졸중이 2배 정도 증가하므로, INR을 2 이하로 유지하는 것은 권장되지 않는다.
특수 상항에서 항혈전 치료
발작성 심방세동에서 항혈전 치료
발작성 심방세동에서 뇌졸중 및 색혈전증에 대한 위험 및 예방에 대한 것은 정립이 덜 되어있기는 하지만 뇌졸중에 대한 위험도는 지속성 및 영구형 심방세동과 큰 차이가 없다. 그래서 발작성 심방세동에서 항혈전 치료는 지속성 및 영구형 심방세동과 동일하게 뇌졸중의 위험도에 따른 치료를 원칙으로 한다.
수술 전후 항응고 치료
항응고제를 복용하고 있는 환자 중 수술 또는 침습적인 시술 전에 약물을 일시적으로 중지해야 할 경우가 있다. 많은 수술 의사들은 수술 전에 INR이 1.5 이하 또는 정상 수치로 유지하기를 원한다. 와파린은 반감기가 36-42시간이므로 INR이 적절한 정도까지 떨어지려면 수술 5일 전부터 중지해야 한다. 적절한 지혈이 되었다면 수술 후 그날 저녁 또는 다음날 아침부터는 평상시 사용하던 용량의 와파린을 투여하기 시작한다.
기계판막으로 치환 받은 환자나 색혈전증에 대한 고위험군 환자는 와파린을 끓는 동안에 헤파린(LMWH 또는 UFH)를 사용하는 ‘bridging’ 치료를 고려해봐야 한다.
만성 혈관 질환이 동반된 환자에서 항혈전 치료
항응고제를 복용하고 있는 많은 심방세동 환자들이 관상동맥, 경동맥 또는 사지동맥의 혈관 질환들을 동반하고 있다. 이러한 환자들 중 상당수가 항응고제에 항혈소판제(일반적으로 아스피린)를 복합하여 사용하고 있다. 하지만 이러한 복합 치료가 뇌졸중 및 혈관 사고(심근경색증 포함)에 대한 위험성을 감소시키지 못하며, 오히려 출혈을 유의하게 증가시킨다.
급성 관상동맥 증후군 또는 관동맥중재술 후 항혈전 치료
스텐트를 시술 받은 관동맥 질환 환자에서 아스피린과 클로피도그렐을 이용한 이제요법은 스텐트 혈전증을 예방하기 위한 항혈소판치료의 표준이다. Bare-metal 스텐트 경우에는 시술 후 4주, 약물 용출성 스텐트 경우에는 시술 후 6-12개월, 급성 관동맥증후군은 스텐트 종류에 관계없이 9-12개월 동안 이제요법을 일반적으로 사용하고 있다.
스텐트를 시술 받는 환자의 5-7%는 중등도 이상의 혈전색전증 위험이 동반된 심방세동 환자들인데 이들에게는 스텐트 혈전증 예방을 위한 항혈소판제뿐만 아니라 뇌졸중 예방을 위한 항응고제 치료가 필요하다. 심방세동이 동반된 관동맥 질환 환자들은 일반 환자들에 비해 주요심장사고 발생률이 높다. 삼제 요법(와파린, 아스피린, 클로피도그렐)을 한 경우에 30일 출혈 유병률은 2.6-4.6%로 크게 증가하지 않으나, 12개월 출혈 유병률은 7.4-10.3%로 증가하게 된다. 그래서 삼제요법을 하는 경우에는 위험성과 이익을 따져서 그 기간과 방법을 결정해야 한다.
혈전색전증의 위험이 낮다면(CHADS2 score < 2) 짧은 기간(예, 1개월) 동안에 이제 항혈소판 요법이 항응고제를 대치할 수도 있다. 하지만 혈전색전증의 위험도가 중등도 이상(CHADS2 score ≥ 2)이라면 항혈소판제에 항응고제를 추가하는 것이 좋다. 삼제요법은 스텐트 혈전증과 전신 혈전색전증을 예방할 수 있는 가장 좋은 방법이다. 따라서 스텐트 시술 후 스텐트내 내막이 다시 생성되는 초기에는 삼제요법을 쓰는 것이 좋다. 다만, 삼제요법은 장기간 사용 시 출혈의 위험성이 증가하므로 스텐트 삽입 시 개개인마다 출혈의 위험성을 평가하여 스텐트 종류 및 약물 사용 시기 등을 결정하여야 한다. 삼제요법을 사용할 경우 출혈의 위험성을 줄이기 위해 INR은 되도록 낮게 유지한다(INR 2.0-2.5). 출혈의 위험성이 높으면 bare-metal 스텐트를 시술하여야 하고, 이후 삼제요법을 2주 정도로 줄여 쓸 수도 있다. 또한 스텐트 시술 없이 풍선도자를 이용한 혈관성혈술만 실시한 후 아스피린과 항응고제만 쓸 수도 있다. 삼제요법 후에는 항응고제에 항혈소판제 1개를 이용한 이제요법이 사용되는데, 아스피린과 클로피도그렐 중 어느 것이 더 나은지에 대한 자료는 없다(Table 7).
심방세동 동율동 전환 시 항혈전 치료
심방세동이 발생한 지 48시간 이내이면 항응고제 사용 없이 동율동 전환을 즉시 시행할 수 있다. 그러나 심방세동 발생시점이 병력상 명확하지 않거나 48시간 이상 지속되었을 경우에는 동율전 전환 전 최소한 3주 이상의 항응고제를 사용(INR 2-3)하여야 하며, 전기적 또는 약물적 동율동으로의 전환 후 최소한 4주간 항응고제를 사용하여야 한다.
동율동 전환하기 위하여 3주간 항응고 치료를 하는 대신 경식도 초음파를 시행하여 혈전의 증거가 없으면 율동 전환 전에 헤파린(UFH 또는 LMWH)을 투여한 후 동율동 전환을 시도하고, 경구용 항응고제는 동율동 전환 후 4주간 사용한다.
경식도 심초음파에 의해 혈전이 발견된 경우에는 경구용 항응고제로 최소한 3주간 치료(INR 2-3)를 실시한 후 혈전을 확인 후 동율동 전환을 시도한다.
뇌졸중 예방을 위한 비약물적 방법
좌심방 appendage가 심방 혈전증의 주된 장소이다. 그래서 좌심방 appendage의 입구를 막으면 심방의 혈전증이 감소하고, 이는 뇌졸중의 발생을 감소시킬 수 있을 것으로 예측된다. 특히, 항응고제의 장기간 사용이 힘든 환자에서 좋은 적응증이 되리라 생각된다. PROTECT AF연구[21]에서 WATCHMAN 기구를 이용하여 좌심방 appendage의 입구를 막은 환자와 와파린을 사용한 환자에서 뇌졸중, 심혈관계 사망, 전신적인 색전증을 비교하였는데, 두 군 간에 비슷한 결과를 얻었다. 하지만, 시술과 관련된 안전성 등 아직 해결해야 할 부분들이 남아 있다.
결 론
현재 경구용 항응고 치료는 색혈전증의 고위험군인 심방세동 환자에서 뇌졸중을 예방하는 가장 효과적인 방법이다. 최근에는 와파린과 비교하여 효과는 비슷하면서 INR검사가 필요 없으며, 약물 간 상호작용이 없는 새로운 항응고제들이 개발되어 임상 연구가 한창이다. 특히 dabigatran을 포함한 몇몇 약물들은 와파린을 대체할 수 있을 것으로 기대된다. 아스피린 단독요법 및 아스피린과 클로피도그렐 복합요법은 모두 와파린보다 뇌졸중 예방 효과가 떨어지므로 경도 및 중등도의 위험군에 제한적으로 사용할 수 있다. 현재 많은 의사들이 와파린의 사용상 제한점 때문에 이의 적절한 사용을 간과하는 경우가 많은데 항상 주의를 기울어야 하겠다.




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






