서 론
만성적인 통증은 암 환자에서 매우 흔한 증상으로 극심한 통증은 삶의 질을 크게 손상시킨다[1-3]. 1990년도 세계보건기구(WHO)는 암성 통증 관리를 위한 진통제 치료 지침인 ‘진통제 사다리(Analgesic ladder)’를 만들었다[4]. 삼단계 진통제는 비마약성, 약한 마약성 진통제(weak opioids) 마지막으로 강한 마약성 진통제(strong opioids)로 나누어진다. 진통제를 이용한 통증 조절은 환자의 통증 강도에 따른 적절한 약물 선택이 중요하지만 아직도 의료진의 경우 강한 마약성 진통제의 사용을 꺼리는 경향이 있다. 하지만 최근에 들어서 비마약성 진통제가 효과가 없을 때 가급적 빨리 마약성 진통제 투약을 시작하는 것이 좋다는데 많은 전문가들이 의견을 모으고 있다[5].
염산히드로모르폰은 모르핀에서 합성된 강한 마약성 진통제의 하나로 1921년에 개발되었다[6]. 염산히드로모르폰의 경우 옥시코돈의 2~3배, 모르핀의 5~7.5배의 역가를 보여 소량으로 강력한 진통효과를 보이고 시토크롬(cytochrome) P450을 거의 거치지 않고 glucuronidation을 통해 대사 되므로 시토크롬 P450과 관련된 약물과 상호 작용이 적고 또한 활성화되는 대사 산물이 없어 안전하고 내약성이 우수하다고 하겠다[6,7]. 최근에 한국에서 발매된 염산히드로모르폰 서방정(상품명: 저니스타 서방정)은 2006년에 개발되어 유럽에서 널리 사용되고 있는 1일 1회의 강한 마약성 진통제로 삼투압으로 조절되는 펌프를 통해 약물이 24시간 동안 천천히 방출되어 위 운동이나 산도, 음식물 섭취 등이 약물의 흡수에 큰 영향을 미치지 않는 것으로 알려져 있다[8-10].
현재까지 기존의 마약성 진통제를 사용하던 환자를 대상으로 진행된 암성 통증 조절에 대한 임상 연구 결과는 있으나, 강한 마약성 진통제(예를 들면 옥시코돈, 펜타닐 패치) 투약 경험이 없는 환자에게서 염산히드로모르폰 서방정을 이용한 암성 통증 조절에 대한 임상 자료는 없다. 그러므로 본 연구에서는 강한 마약성 진통제 투약 경험이 없는 한국인 암환자에서 염산히드로모르폰 서방정의 유효성과 안전성을 알아보고 환자 만족도를 조사하였다.
대상 및 방법
대상
2009년 1월부터 2009년 3월까지 최근 1달 이내에 강한 마약성 진통제 투약 경험이 없는 만 20세 이상의 중등도(숫자 통증 등급 4점 이상, Numberic rating scale, NRS) 이상의 암성 통증을 호소하는 화순전남대학교병원에 내원한 외래 및 입원 환자를 대상으로 시행하였다. 과거 혹은 현재 약물이나 알코홀 남용의 기왕력이 있는 환자, 경구용 진통제 작용을 방해할 정도의 심한 소화기계 질환을 가진 피험자로 연하곤란, 구토, 장운동 없음, 장 폐쇄, 심한 장협착 등의 경구투약 약물의 흡수 및 통과에 영향을 미칠 수 있는 질환을 가진 환자, 염산히드로모르폰에 과민성이 있는 환자, 모노아민 산화효소 저해제를 투약 중이거나 투약을 중단한지 2주 이내인 환자, 심한 호흡곤란을 호소하는 환자, 임상적으로 심각한 간이나 신장 부전이 있는 환자, 가임기 여성으로 임신 중이거나 본 임상 연구 기간 동안 임신 가능성이 있는 피험자, 남성의 경우 시험기간 중 성관계를 자제할 의지가 없는 남성 피험자임에도 불구하고 그들의 파트너가 효과적인 피임법을 행하지 않는 피험자, 연구자의 의견으로 본 연구에 참여할 수 없는 상태인 경우의 환자 등은 제외하였다.
방법
염산히드로모르폰 서방정 8 mg으로 투약을 시작하여 1일 1회 매일 일정한 시간대에 복용하도록 하였다. 용량 조절은 매 2일 간격으로 시행하여 지난 24시간 동안 4회 이상의 돌발성 통증 치료제 투약이 있었던 경우 시험약의 용량을 8 mg 단위로 증량하였다. 다만 이상반응으로 인하여 용량 증가가 의학적으로 바람직하지 않다고 판단될 경우 현재 투약 중인 용량을 유지하거나 중단 혹은 감량하도록 하였다. 연구기간 동안 연속 3일 이상 시험약을 투약하지 않은 피험자는 탈락하도록 하였으며 마지막 평가 직전 하루와 평가 당일에는 반드시 시험약을 투약하도록 하였다. 돌발성 통증 치료제로는 속효성 옥시코돈 5 mg (상품명: IR codon 5 mg) 혹은 모르핀 15 mg 제재(상품명: S-morphine 15 mg)를 사용하였다. 투약 첫날 및 투약 8일째, 투약 15일째는 직접 방문하도록 하여 통증의 강도, 이상반응, 일반적인 마약성 진통제의 부작용, 만족도 등을 확인하였으며 방문외 평가는 2일 간격으로 입원 환자의 경우 직접 면담, 외래 환자의 경우 전화문의를 통하여 통증의 강도, 이상반응, 일반적인 마약성 진통제의 부작용, 만족도 등을 확인하였다. 평가 변수로 1차 방문과 마지막 방문에서의 지난 24시간 평균 숫자 통증 등급(NRS) 감소 정도(%) (투약 전 NRS minus 마지막 방문에서의 평균 NRS/투약 전 NRS), 연구기간 동안 지난 24시간 NRS 변화 추이, 1차 방문 이후 안정적인 통증 조절에 도달하는 피험자 비율(안정적인 통증 조절: 연속 2일 동안 지난 24시간 평균 통증 강도가 NRS 3점 이하로 유지되고 돌발성 통증 마약성 진통제 투약 횟수가 3회 이하로 유지되는 경우), 일반적인 마약성 진통제 부작용 발생 빈도, 통증 치료에 대한 피험자 만족도, 연구자의 전반적인 평가를 보고자 하였다. 통증치료에 대한 피험자 만족도는 1 = 매우만족, 2 = 만족, 3 = 보통, 4 = 불만족, 5 = 매우 불만족 5단계로 평가하였으며, 연구자의 전반적인 평가 또한 1 = 효과적이지 못함, 2 = 보통, 3 = 효과적이었음, 4 = 매우 효과적이었음, 4단계로 평가하였다.
통계 방법
히드로모르폰 서방정을 한 번이라도 투약한 환자는 약물의 효과와 안전성을 평가하는데 포함하였다. 인구통계학적 기초자료 및 유효성 평가변수에 대해 연속형 변수의 경우 기술통계량(평균, 표준편차)을 제시하였고, 범주형 변수에 대해서는 빈도와 비율을 제시하였다. 유효성 평가 변수에 대한 분석방법으로 치료 전과 치료 후 효과의 차이를 보기 위한 분석 방법으로 연속형 변수의 경우 Wilcoxon signed rank test를 사용하였다. 모든 통계적 분석은 SPSS version 16.0 (SPSS Inc., Chicago, IL, USA)을 이용하였고, 검정의 유의 수준은 0.05로 하였다.
결 과
총 23명의 고형암 환자가 참여하였고, 그 중 3명이 동의 철회 및 협조 부족으로 중도에 탈락되었다. 22명(95.7%)의 환자가 4기 환자였으며 참여한 환자들의 인구통계학적 특성은 표 1에 기술하였다.
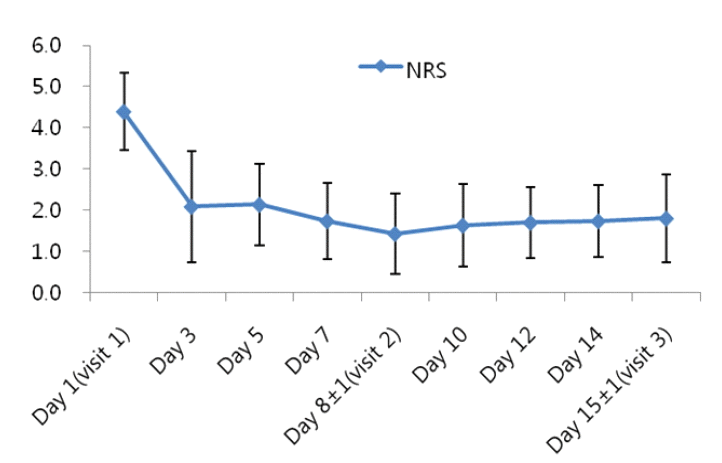
1차 방문과 마지막 방문에서의 지난 24시간 평균 숫자 통증 등급(NRS) 감소 정도(%)는 59.1%로 현저한 감소를 보였다. 또한 연구기간 동안 지난 24시간 NRS 변화 추이도 1차 방문 시 NRS 4.4에서 3일째 NRS 2.1로 감소하였고, 그후 NRS 2 이하로 유지되었으며 마지막 3차 방문 시에는 1.8로 감소를 보였다(Table 2, Fig. 1). 약물을 투여 후 3일째 통계학적으로 의의있게 NRS 값이 2.1로 조기에 감소하였으며(p< 0.01) 통계학적으로 의의 있는 통증의 감소는 시험기간 동안 유지되었다. 또한 1차 방문 이후, 안정적인 통증 조절에 도달하는 피험자 비율은 100%였다. 통증 치료에 대한 피험자의 만족도는 매우 만족, 만족한다고 응답한 피험자가 26.1%, 47.8%였다(Table 3). 시험자의 전반적인 평가 역시 43.5%의 시험자가 통증 조절에 대한 약물의 작용이 매우 효과적이라고 평가하였으며 30.4%의 시험자가 효과적이었다고 평가하였다(Table 4). 총 2명(8.7%)의 환자에서 용량의 증가가 관찰되었다. 용량 변경이 있었던 환자 중 한 환자는 12일째 16 mg으로 용량을 증량하여 16 mg을 연구 종료 시까지 복용하였고, 다른 환자는 3일째 16 mg, 5일째 24 mg, 7일째 32 mg으로 용량을 증량하여 32 mg을 연구 종료 시까지 유지하였다. 약물 관련 부작용은 16명(69.6%)의 환자에서 발생하였으며 가장 흔히 호소하는 부작용은 경도의 오심, 변비, 어지러움, 졸림이었다. 용량의 증가가 있었던 2명의 환자에서 용량의 증가와 관련된 부작용 발생의 증가는 관찰되지 않았다. 총 연구기간 동안 관찰되었던 부작용을 표 5에 기술하였다. 약물과 관련된 매우 심한 부작용은 1명(4.3%)의 환자에서 발생하였으며 매우 심한 졸림을 호소하여 약물을 중단하였다.
고 찰
암성 통증은 말기암 환자에서 삶의 질을 심각하게 손상시키는 가장 큰 인자로 암성 통증의 조절은 삶의 질을 향상시키고 전반적인 활동도(performance status)를 향상시키는데 큰 역할을 한다[11]. 만성 허리 통증이나 암성 통증에 대한 염산히드로모르폰의 연구를 살펴보면 대부분 기존의 마약성 진통제를 사용하던 환자를 대상으로 동등 용량의 염산히드로모르폰으로 전환하거나 기존의 마약성 진통제와의 비교를 통해 통증조절에 대한 연구가 진행되어 효과 및 안정성을 입증한 연구가 대부분이다[11-14]. Wallace 등[11]은 만성 허리 통증을 호소하는 환자를 대상으로 황산 모르핀으로 통증을 조절한 후 동등 용량의 염산히드로모르폰으로 황산 모르핀이 안정적으로 전환될 수 있음을 발표하였고, Hanna 등[13]도 만성 암성 통증을 호소하는 환자들에서 황산 모르핀이 염산히드로모르폰으로 안정적으로 전환될 수 있음을 발표하였었다. 본 연구에서는 기존 연구와는 다르게 강한 마약성 진통제 투약 경험이 없는 한국인 암환자에서 염산 히드로모르폰 서방정의 효과 및 안정성을 알아보고자 하였다. 본 연구에서 사용한 염산히드로모르폰 서방정은 1일 1회 복용하며 삼투압으로 조절되는 펌프를 통해 약물이 24시간 동안 천천히 방출되도록 고안되어 있다. 황산모르핀과 염산히드로모르핀과의 동등 용량 역가는 3:1에서 7.5:1 정도로 알려져 있으며 기존의 대부분의 연구는 5:1 정도의 역가를 사용하였다[6,15-17].
본 연구에서 약물 복용 후 숫자 통증 등급이 3일 만에 2.1로 조기에 의의있게 감소하였으며 마지막 방문시까지 의의있는 숫자 통증 등급 감소가 지속 되어 약물의 효과가 매우 빠르게 나타나고 지속됨을 알 수 있었다. 만성 허리 통증을 호소하는 환자를 대상으로 한 Wallace 등이 발표한 연구에서도 약물 복용 후 3일째에 의의있는 통증 감소 효과를 보였으며 효과가 지속되어 염산히드로모르폰의 우수한 효과를 시사하였다[11]. 추가적으로 Wallace 등은 염산히드로모르폰을 약 1년 정도 투약을 지속하였을 때에도 통증 조절의 효과가 우수하고 부작용도 단기간 사용하였을 때와 크게 다르지 않는 빈도로 발생하여 장기간 사용하는데 내약성이 우수함을 발표하였다[18].
지속성 마약성 진통제의 부작용은 속효성 마약성 진통제의 부작용과 유사하다고 알려져 있다[19]. 기존의 연구를 살펴보면 염산히드로모르폰의 부작용은 일반적인 마약성 진통제와 유사하게 소화기계와 신경계통에 집중되어 있고, 심각한 부작용은 약 10%에서 20% 정도에서 발생한다. 가장 흔한 부작용은 연구마다 약간의 차이는 있지만 대부분 경도에서 중등도의 오심, 변비, 구토, 졸림, 어지러움 등으로 본 연구에서 염산히드로모르폰의 부작용도 기존의 연구들과 크게 다르지 않았다[6,11,13,14,16]. 기존의 연구들에서는 대부분 오심, 구토 변비 등의 심각한 소화기계 부작용으로 약물을 중단하는 경우가 대부분이었고, 드물게 섬망을 호소하여 약물을 중단해야 하는 경우도 있었다[14]. 본 연구에서는 1명의 환자가 약물 투약 후 무기력을 심하게 호소하여 약물을 중단하였고, 옥시코돈제재로 약물을 전환하였다. 전환 후에도 경도의 무기력을 호소하였지만 항암 치료 후 질환이 호전되면서 마약성 진통제를 중단할 수 있었다. 통증 치료에 대한 피험자 및 시험자의 만족도도 통증조절에 만족 혹은 효과적이라고 응답한 경우가 73.9%로 환자, 의사 모두 약물의 효과에 만족한 것으로 판단할 수 있었다. 본 연구의 제한점으로는 대상 환자 수가 적고 기간이 짧으며 개방적이라는 데 있겠다. 또한 염산히드로모르폰과 다른 약제 혹은 위약과의 비교 연구도 시행하지 않았다. 하지만 마약성 진통제를 사용한 적이 없는 한국인 환자를 대상으로 염산히드로모르폰의 우수한 효과 및 내약성을 입증했다는데 의의가 있겠다.
염산히드로모르폰 서방정은 삼투압성 펌프를 이용하여 약물의 농도가 24시간 동안 유지되는 하루 한 번 복용하는 약물로서 강한 마약성 진통제를 사용한 적이 없는 한국인 환자에서 매우 효과가 좋고 안전한 약물이라고 하겠다.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






