|
 |
| Korean J Med > Volume 80(1); 2011 > Article |
|
요약
목적:
TSH 분비 뇌하수체 선종은 모든 뇌하수체종양의 1~2%를 차지하는 매우 드문 질환으로써 빠르고 정확하게 진단하여 부적절한 치료를 피하고 적극적인 치료를 하는 것이 중요하다. 저자들은 TSH 분비 뇌하수체 선종으로 진단받은 8명의 환자들의 임상적, 생화학적 특징과 치료에 대해서 비교분석하였다.
결과:
신촌 세브란스 병원에서 종양절제술을 받은 484명의 환자들 중 8명(1.65%)가 TSH 분비 뇌하수체 선종이었다. 성별은 5명이 여자, 3명이 남자였고, 연령 분포는 28세에서 55세까지 평균 40.6세였다. 증상이 발생하고 나서 진단되기까지의 평균 기간은 17개월이었다. 초기 증상은 4명의 환자에서는 갑상선기능항진증의 전형적인 증상을 보였고, 2명의 환자에서는 시야 결손을 보였다. 생화학적 검사상에서는 하시모토갑상선염을 동반한 환자 2명을 제외한 6명에서 갑상선호르몬은 증가되어 있으나 TSH가 적절하게 억제되지 않았다. 또한 2명의 환자에서 유리알파아단위와 유리알파아단위/TSH의 몰농도비를 측정하였고, 모두 증가되어 있었다. 터키안 자기공명영상에서는 6명의 환자에서 거대선종이 관찰되었고, 2명의 환자에서 미세선종이 관찰되었다. 8명의 환자가 모두 완전한 종양절제술을 시행받았고, 7명의 환자에서 수술 후 얻은 조직으로 면역조직화학검사를 시행하였다. 6명의 환자가 TSH 양성 소견을 보였고, 그 중 2명의 환자에서 동시에 성장호르몬, 유즙분비호르몬에 양성 소견을 보였으며 1명의 환자에서 유즙분비호르몬에 양성 소견을 보였다. 수술 전 뇌하수체 전엽 기능부전증을 가지고 있단 5명의 환자 중 3명의 환자는 수술 후 기능이 회복되었다. 또한 병원에 내원하지 않은 3명의 환자를 제외한 5명의 환자 모두 평균 30.8개월의 기간 동안 갑상선기능항진증과 종양 재발의 증거는 없었다.
Abstract
Background/Aims:
Thyrotropin (TSH)-secreting pituitary adenoma (TSHoma) is rare and represents 1~2% of all pituitaryadenomas. TSHoma should be distinguished from the thyroid hormone resistance syndrome. Patients with TSHoma may bemisdiagnosed with primary hyperthyroidism and often receive inappropriate thyroid gland treatment.
Methods:
We assessed the clinical characteristics of patients with TSHoma who presented to Severance Hospital at the YonseiUniversity College of Medicine, Seoul, Korea between 2005 and 2009.
Results:
Of 484 patients who underwent pituitary tumor resection, eight (1.65%; five women and three men) were found to haveTSHoma. The mean age was 40.6±8.9 years at diagnosis (range, 28~55 years). The median duration from onset of symptoms todiagnosis was 17 months (range, 4~60 months). Four patients had overt symptoms of hyperthyroidism and two had visual fielddefect. Six patients had elevated free thyroxine (FT4) levels with elevated or inappropriately normal TSH levels, and two patientshad symptoms associated with Hashimoto’s thyroiditis. The serum levels of free α-subunit measured in two patients were elevated.Six of the tumors were macroadenomas (>10 mm) and two were microadenomas. Complete tumor removal was achieved in allpatients. Five patients had preoperative anterior pituitary dysfunction; three patients recovered from this after surgery. Threepatients were lost to follow up and five patients showed no evidence of recurrence or hyperthyroidism in the follow-up period(mean, 30.8 months, range, 3~57).
갑상선자극호르몬(TSH) 분비 뇌하수체 선종은 매우 드문 질환으로 모든 뇌하수체종양의 2% 미만이고, 발생률은 백만 명당 한 명으로 알려져 있다. 갑상선기능항진증이 있으나, 대부분의 경우와는 달리 TSH가 부적절하게 정상이거나 높은 경우 의심해 볼 수 있다. 종양으로부터 TSH가 분비되는 양상은 자율적이기 때문에 갑상선호르몬 수치가 증가해도 음성 되먹임 기전에 반응이 없게 된다. 그 후 TSH는 갑상선의 분비에 기여하게 되어 갑상선호르몬이 지속적으로 과분비된다. 그러므로 이러한 형태의 갑상선기능항진증을 중심성 갑상선기능항진증으로 분류한다. 1960년대 생물학적 검정법을 통한 혈청 TSH 측정으로 TSH 분비 뇌하수체 선종이 처음 발표된 이래 1970년에는 Hamilton 등이 방사면역측정법을 이용하여 TSH를 비정상적으로 과분비하는 뇌하수체 선종을 보고하였다[1,2]. 현재는 TSH 측정을 위한 극도로 민감한 면역계량검사가 발전하면서 이런 중심성 갑상선기능항진증, 즉 TSH 분비 뇌하수체종양이 거대선종이 되기 전에 더욱 일찍 발견되어 TSH 분비 뇌하수체종양 환자의 진단율이 급증하고 있다[3]. 국내에서도 1986년 윤 등에 의한 첫 보고 이후 이에 대한 관심이 높아짐에 따라 현재까지 약 11예가 보고되었다[3,4]. 중심성 갑상선기능항진증이 진단되면, TSH 분비 뇌하수체 선종과갑상선호르몬에 대한 뇌하수체저항성증후군을 감별하는 것이 매우 중요하다. 감별은 임상양상, 유리알파아단위 수치, 영상검사, T3 억제검사 등을 통해 하게 된다. 만약 감별 진단하지 못할 경우, TSH 분비 뇌하수체 종양 환자에게 부적절한 갑상선 절제나, 갑상선호르몬에 대한 뇌하수체저항성증후군을 가지고 있는 환자에게 불필요한 뇌하수체 수술을 하게 된다[5].
TSH 분비 뇌하수체 선종이 정확히 진단되어도 진단이 지연되는 경우가 많고 따라서 진단 당시 종양의 크기가 크고 침습적이기 때문에 보통 치료가 힘든 경우가 많다. 이러한 TSH 분비 뇌하수체 선종을 빨리, 그리고 정확하게 진단하는 것은 종양이 커져서 누르는 효과로 생기는 신경내분비적 합병증, 즉 두통, 시야 결손, 뇌하수체 기능 저하증이 생기는 것을 방지할 수 있고 그럼으로써 치료율을 향상시킬 수 있다[6].
저자들은 한국인에서의 TSH 분비 뇌하수체 선종의 임상양상과 특성을 살펴보기 위해 세브란스 병원에서 TSH 분비 뇌하수체 선종으로 진단받은 8명의 환자의 임상양상, 생화학적 특징, 치료에 대해 보고하고자 한다.
2005년부터 2009년까지 세브란스 병원에 내원하여 뇌하수체종양을 진단받고 절제술을 받은 환자 484명 중, 8명(1.65%)이 TSH 분비 뇌하수체 선종으로 진단받았다. 이 환자들을 의무기록에 의거하여 후향적으로 분석하였다. 환자들의 나이, 성별, 과거력, 진단받을 당시 증상, 증상이 나타난 후 진단되기까지의 기간, 진찰 소견, 수술 전후 갑상선 기능 검사 및 복합 뇌하수체 검사 결과, 치료 후 경과를 분석하였다.
TSH (immunoradiometric assay, Diasorin, Stillwater, Minnesota, U.S.A), 유리 T4 (immunoradiometric assay, Trinity Biotech plc, co.wicklow, Ireland), 항갑상선글로불린항체(radioimmunoassay, BRAHMS, Hennigsdorf, Germany), 항갑상선과산화효소항체(radioimmunoassay, BRAHMS, Hennigsdorf, Germany), 복합뇌하수체기능검사를 수술 전, 수술 후 추적관찰하면서 시행하였고, 2명의 환자에서 수술 전 유리알파아단위(IRAM-α-subunit, Immunotech, France) 및 유리알파아단위/TSH의 몰농도비를 측정하였다. 복합뇌하수체검사방법 및 해석은 표 1과 같이 시행하였고, 유리알파아단위는 gamma counter를 이용하여 측정하였다.
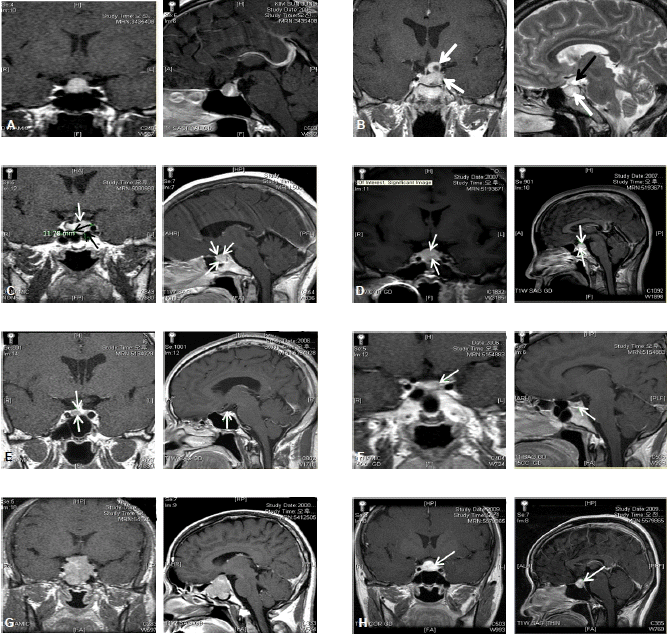
8명의 환자 모두에서 진단 당시 터키안 자기공명영상 검사가 시행되었고, 각각 종양의 크기 및 침입 정도가 분석되었다. 또한 수술 후 추적관찰하면서 내분비검사와 함께 터키안 자기공명영상 검사를 시행하여 병의 치유 및 재발 여부를 평가하였다.
수술 전 TSH 분비 뇌하수체 선종의 진단은 갑상선 호르몬 수치가 올라가 있으면서 TSH가 부적절하게 억제되지 않는 검사실 소견과 터키안 자기공명영상상 뇌하수체종양의 존재 유무에 기초하였다. 또한 TSH 분비 뇌하수체 선종의 진단에 도움을 얻기 위해 복합 뇌하수체 자극 검사(TRH 자극검사)도 같이 시행하였다.
2005년부터 2009년까지 세브란스 병원에 내원하여 뇌하수체 종양 절제술을 받은 484명의 환자 중에서, 8명의 환자(1.65%)가 TSH 분비 뇌하수체 선종이었다. 평균 연령은 진단 시 40.6±8.9세(범위 28~55세)였고, 5명은 여자, 3명은 남자였다. 임상증상을 살펴보면, 심계항진, 과도한 발한, 체중 감소, 피로와 같은 갑상선기능항진증의 전형적인 증상을 가지고 있는 환자는 4명, 두통, 안구통증, 시야결손 같은 신경학적 증상이 동반된 환자가 3명, 나머지 한 명은 갑상선기능저하증을 진단받고 지속적인 갑상선호르몬 보충요법을 받았으나 TSH가 적절히 억제되지 않아 뇌하수체종양을 의심했던 증례였다. 또한 2명의 환자에서 일차성 갑상선기능항진증으로 치료 받았던 과거력이 있었고, 한 명의 환자는 갑상선 암으로 수술 및 방사선 동위원소 치료를 받았던 과거력이 있었다. 환자들이 첫 증상 이후 진단되기까지의 평균 기간은 17개월(범위 4~60개월)이었다(표 2).
수술 후 얻은 조직으로 면역조직화학검사가 7명의 환자에서 시행되었다. 그 중 6명의 환자에서 TSH 양성 소견을 보였고, 나머지 1명은 모든 호르몬에 음성 소견을 보였다. TSH 양성 소견을 보였던 6명의 환자 중 3명의 환자가 동시에 다른 뇌하수체 전엽 호르몬에도 양성 소견을 보였으며, 1명의 환자는 유즙분비호르몬(prolactin)에 나머지 2명의 환자는 성장호르몬과 유즙분비호르몬에 양성 소견을 보였다(표 4).
2명의 환자를 제외한 6명의 환자에서 보였던 갑상선기능항진증은 수술 후 모두 회복되었다. 또한, 5명의 환자가 수술 전 뇌하수체 전엽 기능 부전증을 보였고, 그 중 3명이 수술 후 기능이 회복되었으며, 나머지 2명은 수술 후 병원에 내원하지 않았다(표 4).
수술 후 추적관찰이 되지 않은 3명의 환자를 제외한 나머지 5명의 환자 모두 평균 30.8±19.8개월(range, 3~57개월) 동안 재발의 증거는 없었다.
TSH 분비 뇌하수체 종은 중심성 갑상선기능항진증의 드문 원인 중 하나이다. 최근 극도로 예민한 면역계량검사가 발전하면서 중심성 갑상선기능항진증과 일차성 갑상선기능항진증 사이의 진단학적 혼란이 줄어들었고, 결국 초기 단계의 TSH 분비 뇌하수체 선종의 진단율을 높이게 되었다[7]. 이로 인해 TSH 분비 뇌하수체 선종의 발생률이 과거에 알려진 것 보다 높은 것으로 생각되고 있다.
TSH 분비 뇌하수체 선종은 갑상선기능항진증의 증상과 더불어 종양에 의한 주위 구조 압박에 의한 증상으로 두통, 시야 결손, 뇌하수체 기능 저하증이 같이 나타나는 경우가 흔하며, 다른 뇌하수체 전엽 호르몬, 즉 성장호르몬, 유즙분비호르몬, 성선자극호르몬 등을 같이 분비하는 종양일 경우 말단비대증, 성선 장애와 같은 증상이 생길 수도 있다. 또한 많은 환자들이 그레이브스병으로 잘못 진단되고 그 중 30%의 환자는 부적절한 갑상선절제술이나 방사선동위원소 치료를 받게 되며 이들에게서 침습적 거대 선종의 발생률이 높은 것으로 알려져 있다[6]. 본 연구에서는 그레이브스병으로 잘못 진단되어 부적절한 항갑상선 요법을 받았던 환자가 2명(25%)이었다. 또한 이전의 TSH 분비 뇌하수체종양을 진단받았던 환자들에 대한 연구들에서는 첫 증상 이후 진단되기까지의 평균 기간을 2.5~9년으로 보고하였으나, 본 연구에서는 17개월(범위 4~60개월)로 지금까지의 연구들보다 증상 발현부터 진단까지의 시기가 짧아진 것을 알 수 있다[8-11]. 이와 같이 진단 검사 방법이 발달하면서 빠르고 좀 더 정확한 진단이 가능해진 것으로 볼 수 있다.
TSH 분비 뇌하수체 선종은 갑상선기능항진증이 있으면서 부적절하게 TSH가 억제되지 않을 때 의심해 볼 수 있다. 하지만 이러한 경우 TSH나 갑상선호르몬에 대한 항체 같은 요소뿐만 아니라 비정상적인 알부민에 의해 중심성 갑상선기능항진증의 생화학적인 특징을 나타내는 경우도 있으므로 이런 요소들을 배제해야 한다. 지속적으로 중심성 갑상선기능항진증의 소견을 보일 경우 TSH 분비 뇌하수체 선종이나 갑상선호르몬에 대한 뇌하수체저항성증후군을 의심해야 하며, 이 두 질환을 감별해야 한다. 첫 번째 방법으로 유리알파아단위와 유리알파아단위/TSH의 몰농도비를 구하는 것이다. TSH은 당단백 호르몬으로 알파-, 베타-의 두 가지 아단위의 비공유 결합으로 이루어져 있다. 알파아단위는 황체형성호르몬(luteinizing hormone, LH), 난포자극호르몬(follicular stimulating hormone, FSH), 인형융모성성선자극호르몬(human chorionic gonadotropin, hCG) 등의 모든 당단백 호르몬에 있어 동일한 구조를 가지고 있다. 베타아단위는 각기 서로 다른 구조를 가지며 각각의 당단백 호르몬에 대한 면역학적, 생물학적 특이성을 가진다. TSH 분비 뇌하수체 선종은 알파아단위가 특이적으로 증가하며 80% 이상의 환자에서 유리알파아단위/TSH의 몰농도비가 1 이상으로 증가하는 것이 특징적인 소견으로 알려져 있다[12]. 하지만 최근 TSH 분비 뇌하수체 선종 환자들의 경우 60% 이상에서 정상 범위의 유리알파아단위 소견을 보이고 거대선종보다는 미세선종에서 더 빈번하게 그런 소견을 보이는 것으로 알려져있다[8]. 본 연구에서는 두 명의 환자에서 유리알파아단위를 측정하였으며, 모두 유리알파아단위가 증가되어 있었고, 유리알파아단위/TSH의 몰농도비가 1 이상으로 증가되어 있었으며, 이 사람들은 모두 거대선종이었다. 두 번째 방법으로는 영상학적 검사로써 MRI 검사를 시행해서 뇌하수체 종양을 찾는 것이다. 대부분 주변 구조로 침범하는 뇌하수체 거대선종의 단계에서 발견되는 것으로 알려져 있으나 최근 들어 영상학적 방법의 발전으로 미세선종의 진단율이 많게는 15%까지 증가하였다[6]. 본 연구에서는 MRI상 2명(25%)의 환자가 미세선종이었으며, 3명(37.5%)의 환자가 주변 구조의 침범이 없었다. 따라서 생화학적 진단방법이 발전하면서 빨리 의심하고 영상학적 검사가 발전함에 따라서 미세선종의 진단율이 높아졌음을 알 수 있다. 세 번째 방법으로는 T3 억제검사나 갑상선자극호르몬 분비호르몬(TRH) 자극검사(민감도 71%, 특이성 96%)와 같은 역동적인 검사 방법이 있다[11]. TSH 분비 뇌하수체 선종의 경우 두 검사에 대한 반응이 없으나, 갑상선 호르몬에 대한 뇌하수체저항성증후군의 경우 반응이 있는 것이 특징적이다. 본 연구에서는 TRH 자극검사를 시행하였으며, 8명 중 5명의 환자에서 반응이 없었다.
드물게는 장기간 갑상선기능저하증을 가지고 있던 환자에서도 TSH 분비 뇌하수체 선종이 발생한 예가 보고된 적이 있고[13], 본 연구에서도 4번 환자의 경우, 장기간 갑상선기능저하증으로 갑상선 호르몬을 복용하였으나, TSH가 적절하게 억제되지 않아 뇌하수체 선종을 의심했던 증례였다. 장기간 갑상선기능저하증이 있는 경우 되먹이기 기전에 의해 갑상선자극호르몬 분비 세포가 증식되어 뇌하수체의 미만성 비대를 초래할 수 있으므로 진짜 선종과 감별을 요한다. 4번 환자의 경우, 오랜 기간 동안의 갑상선호르몬 대체 요법에도 불구하고 TSH가 적절하게 억제되지 않아 시행한 터키안 자기공명영상에서 1.3 cm의 거대선종이 명확하게 보였었다.
TSH 분비 뇌하수체 선종은 경접형동 종양절제술이 일선의 치료이고, 이 치료의 목적은 종양의 완전한 절제와 갑상선기능의 완전한 회복이다. 하지만 이 종양은 섬유모세포성장인자(fibroblast growth factor)의 높은 발현으로 인해 현저하게 섬유화가 많이 진행되고 국소적으로 침습적인 특징을 가졌기 때문에 종양의 완전한 절제가 불가능한 경우가 많다[14]. 수술이 어려울 경우 뇌하수체 방사선 치료를 고려해 볼 수 있다. 지금까지 연구들의 치료 성적을 종합해 보면 약 1/3의 환자에서 종양의 완전 절제 및 갑상선 기능이 완전히 정상화되었다. TSH 분비 뇌하수체 선종의 조기 진단이 늘어나면서 수술적 치료율이 향상되었지만 수술이 어렵거나 수술 후 완전한 절제가 되지 않았거나 갑상선 기능이 정상화되지 않았을 경우에는 약물치료가 필요할 수 있다. 최근 약물치료는 주로 지속성 소마토스타틴(somatostatin) 유사체를 사용하며, 이의 효용성은 여러 연구에 의해서 증명되었다[8,9,11,15-21]. 본 연구에서 하시모토 갑상선염과 동반된 2명의 환자를 제외한 6명의 환자들은 수술 후 갑상선기능항진증이 모두 회복되었고, 수술 전 뇌하수체 전엽 기능 부전증을 가지고 있었던 5명의 환자들 중 3명이 수술 후 기능이 회복되었다. 수술 후 8명의 환자들 중 3명의 환자가 병원에 내원하지 않았으며, 이후 추적관찰이 가능했던 5명의 환자는 모두 평균 30.8±19.8개월(범위, 3~57개월)의 기간 동안 터키안 자기공명영상에서 종양의 재발 및 호르몬 검사상 갑상선기능항진의 증거는 없었다. 물론 장기적인 추적관찰이 필요할 것이며, 단정짓기는 어려우나 조기에 좀 더 정확하게 진단하여 적극적인 치료를 할 경우 예후를 향상시킬 수 있을 것으로 생각된다.
TSH 분비 뇌하수체 선종의 25%에서 다른 뇌하수체 전엽호르몬들, 주로 성장 호르몬 또는 유즙분비호르몬을 같이 분비하고, 이 세 가지 호르몬들은 공통적인 전사조절인자, 즉 PROP-1, Pit-1및 HESX-1을 공유하는 것으로 알려져 있다[6]. 본 연구에서는 8명의 환자 중 2명의 환자에서 성장호르몬, 유즙분비호르몬을 같이 분비하였고, 1명의 환자에서 유즙분비 호르몬을 같이 분비하였다.
실제로 더 많은 예의 TSH 분비 뇌하수체 선종 환자가 있을 것으로 생각되며, 조기 발견을 위해서는 TSH가 부적절하게 억제되지 않았을 때 의심해 보는 것이 중요하고, 확진을 위해서 유리알파아단위, 유리알파아단위/TSH의 몰농도비, TRH 자극검사 또는 T3 억제검사, 터키안 자기공명영상 등의 검사가 필요할 것이다. 이러한 방법으로 조기에 정확한 진단을 하여 종양의 크기가 비교적 작을 때 외과적 절제를 함으로써 완치율을 높일 수 있을 것이며, 수술로 완치가 불가능 할 때에는 지속성 소마토스타틴유사체나 방사선 치료를 병합하여 적극적 치료를 함으로써 예후를 향상시킬 수 있을 것으로 생각된다.
REFERENCES
1. Jailer JW, Holub DA. Remission of Graves' disease following radiotherapy of a pituitary neoplasm. Am J Med 1960;28:497–500.


2. Hamilton CR Jr, Adams LC, Maloof F. Hyperthyroidism due to thyrotropin-producing pituitary chromophobe adenoma. N Engl J Med 1970;283:1077–1080.


3. Sung JK, Kim EM, Nam SM, et al. A TSH-secreting pituitary microadenoma diagnosed with inferior petrosal sinus sampling: case report. Korean J Med 2009;76:752–757.
4. Kim CH, Kim GS, Kim HK, et al. Piruitray thyrotropin-secreting tumors in Korean. J Korean Soc Endocrinol 1997;12:165–175.
5. Beck-Peccoz P, Brucker-Davis F, Persani L, Smallridge RC, Weintraub BD. Thyrotropin-secreting pituitary tumors. Endocr Rev 1996;17:610–638.


6. Beck-Peccoz P, Persani L, Mannavola D, Campi I. Pituitary tumours: TSH-secreting adenomas. Best Pract Res Clin Endocrinol Metab 2009;23:597–606.


7. Beck-Peccoz P, Persani L. Medical management of thyrotropinsecreting pituitary adenomas. Pituitary 2002;5:83–88.


8. Socin HV, Chanson P, Delemer B, et al. The changing spectrum of TSH-secreting pituitary adenomas: diagnosis and management in 43 patients. Eur J Endocrinol 2003;148:433–442.


9. Kienitz T, Quinkler M, Strasburger CJ, Ventz M. Long-term management in five cases of TSH-secreting pituitary adenomas: a single center study and review of the literature. Eur J Endocrinol 2007;157:39–46.


10. Ness-Abramof R, Ishay A, Harel G, et al. TSH-secreting pituitary adenomas: follow-up of 11 cases and review of the literature. Pituitary 2007;10:307–310.


11. Brucker-Davis F, Oldfield EH, Skarulis MC, Doppman JL, Weintraub BD. Thyrotropin-secreting pituitary tumors: diagnostic criteria, thyroid hormone sensitivity, and treatment outcome in 25 patients followed at the national institutes of health. J Clin Endocrinol Metab 1999;84:476–486.


12. Lee EJ, Kim KR, Lee KM, et al. Thyrotropin-secreting pituitary microadenoma. Yonsei Med J 1992;33:368–373.

13. Smallridge RC. Thyrotropin-secreting pituitary tumors. Endocrinol Metab Clin North Am 1987;16:765–792.

14. Ezzat S, Horvath E, Kovacs K, Smyth HS, Singer W, Asa SL. Basic fibroblast growth factor expression by two prolactin and thyrotropin-producing pituitary adenomas. Endocr Pathol 1995;6:125–134.


15. Lee EJ, Kim KR, Kim HM, et al. Thyrotropin secreating pituitary adenoma. J Korean Soc Endocrinol 1992;7:331–342.
16. Bertherat J, Brue T, Enjalbert A, et al. Somatostatin receptors on thyrotropin-secreting pituitary adenomas: comparison with the inhibitory effects of octreotide upon in vivo and in vitro hormonal secretions. J Clin Endocrinol Metab 1992;75:540–546.


17. Gancel A, Vuillermet P, Legrand A, Catus F, Thomas F, Kuhn JM. Effects of a slow-release formulation of the new somatostatin analogue lanreotide in TSH-secreting pituitary adenomas. ClinEndocrinol (Oxf) 1994;40:421–428.


18. Chanson P, Weintraub BD, Harris AG. Octreotide therapy for thyroid-stimulating hormone-secreting pituitary adenomas: a follow-up of 52 patients. Ann Intern Med 1993;119:236–240.


19. Kuhn JM, Arlot S, Lefebvre H, et al. Evaluation of the treatment of thyrotropin-secreting pituitary adenomas with a slow release formulation of the somatostatin analog lanreotide. J Clin Endocrinol Metab 2000;85:1487–1491.


Table 1.
Combined pituitary function test
Table 2.
Initial symptoms, thyroid function test, thyroid antibodies, and free alpha subunit
|
Patient No. |
Age/Sex | Initial Symptoms |
Initial |
Thyroid Ab |
Free α subunit* |
Free α subunit/ TSH molar ratio |
||
|---|---|---|---|---|---|---|---|---|
| fT4* | TSH* | TgAb* | TPO* | |||||
| 1 | 31/F | Headache, visual field defect | 0.79 | 2.34 | 224.660 | 785.950 | ||
| 2 | 28/M | Hyperthyroidism | 4.3 | 5.13 | ‐ | ‐ | ||
| 3 | 55/F | Hyperthyroidism | 2.79 | 3.4 | ‐ | ‐ | ||
| 4 | 49/F | Inadequate suppression of TSH during LT4 replacement | 1.2 | 5.26 | 75.70 | 2,663.7 | ||
| 5 | 43/M | Headache, visual field defect | 2.02 | 2.22 | 15.28 | <5.5 | ||
| 6 | 36/F | Hyperthyroidism | 2.88 | 11.70 | 5.60 | <5.5 | ||
| 7 | 42/M | Headache, bitemporal hemianopsia | 3.94 | 67.09 | ‐ | ‐ | >9.50 | >1.35 |
| 8 | 41/F | Hyperthyroidism | 3.30 | 9.66 | 106.05 | <5.5 | 2.95 | 2.91 |
Table 3.
Preoperative and postoperative thyroid function and pituitary function
| Patient No. |
Preoperative thyroid function |
Postoperative thyroid function |
Preoperative pituitary function | Postoperative ituitary function | ||
|---|---|---|---|---|---|---|
| fT4* | TSH* | fT4* | TSH* | |||
| 1 | 0.79 | 2.34 | 1.52 | 0.26 | Anterior hypopituitarism (GH, TSH, FSH, LH: flat) | Normal |
| 2 | 4.3 | 5.13 | 0.51 | 1.32 | Anterior hypopituitarism (GH, PRL, TSH: flat) | Lost to follow up |
| 3 | 2.79 | 3.4 | 1.52 | 0.21 | Anterior hypopituitarism (TSH: flat) | Normal |
| 4 | 1.2 | 5.26 | 1.23 | 0.05 | Normal | Normal |
| 5 | 2.02 | 2.22 | 0.86 | 0.14 | Anterior hypopituitarism (TSH: flat) | Normal |
| 6 | 2.88 | 11.70 | 0.77 | 0.52 | Normal | Normal |
| 7 | 3.94 | 67.09 | 1.11 | 3.11 | Anterior hypopituitarism (TSH: flat) | Lost to follow up |
| 8 | 3.30 | 9.66 | 0.95 | <0.04 | TSH: overstimulation | Lost to follow up |
| PRL: hypersecretion | ||||||
Table 4.
MRI findings and immunohistochemical staining
- TOOLS
-
 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link XML Download
XML Download Full text via DOI
Full text via DOI-
 Download Citation
Download Citation
 Print
Print-
Share :