 |
 |
| Korean J Med > Volume 96(5); 2021 > Article |
|
Abstract
The most important thing for the management of drug susceptible pulmonary tuberculosis is to diagnose active pulmonary tuberculosis as soon as possible and prevent the occurrence of new patients through appropriate treatment. Therefore, it should be a priority to quickly detect tuberculosis mycobacterium and quickly exclude drug-resistant tuberculosis before treatment begins. To this end, recent guidelines recommend the general use of Mycobacterium tuberculosis (MTB) polymerase chain reaction (PCR) tests, Xpert MTB/RIF tests, and rapid sensitivity tests through line probe assay (LPA). In addition, if the results of the test are positive, it is important to establish an in-hospital reporting system so that rapid reporting can be made. The treatment principle for drug susceptible pulmonary tuberculosis is 2 months of initial intensive phase (isoniazid, rifampin, ethambutol, pyrazinamide) followed by 4 months of maintenance phase (isoniazid, rifampin). Despite global efforts to shorten the duration of the treatment, the treatment of drug susceptible pulmonary tuberculosis has not changed for more than 35 years, and problems such as increased side effects and reduced drug adherence are serious obstacles to tuberculosis management. Therefore, efforts have been steadily made to shorten the treatment period through the combination of new drugs worldwide, and after many failures, they are finally paying off. A recently published Study 31/A5349 study found that 4 months short-term regimen using rifapentine (RPT) and moxifloxacin (MFX) demonstrated non-inferiority in existing standard regimen, as the result, a revision of World Health Organization guidelines is scheduled that 4 months short-term regimen using RPT and MFX may be an alternative. However, it is unlikely that RPT/MFX 4 months short-term regimen will be applied immediately in Korea because the use of RPT is currently limited in Korea due to the high frequency of side effects.
ņĄ£ĻĘ╝ ļŗżņĀ£ļé┤ņä▒ Ļ▓░ĒĢĄņØś ņ¦äļŗ©Ļ│╝ ņ╣śļŻīļŖö ļ¦żņÜ░ ļ╣ĀļźĖ ņåŹļÅäļĪ£ ļ░£ņĀäĒĢ┤ņÖöĻ│Ā, ĻĘĖņŚÉ ļö░ļØ╝ ņ¦äļŻīņ¦Ćņ╣©ņØ┤ ņłśņ░©ļĪĆ Ļ░£ņĀĢļÉśņŚłņ£╝ļ®░, ņ×Āļ│ĄĻ▓░ĒĢĄ ļ░Å ļ╣äĻ▓░ĒĢĄ ĒĢŁņé░ĻĘĀ ĒÅÉņ¦łĒÖśņØś ņ¦äļŗ© ļ░Å ņ╣śļŻī ņŚŁņŗ£ ļ¦ÄņØĆ ļ│ĆĒÖöĻ░Ć ņ׳ņŚłļŗż. ĻĘĖļ¤¼ļéś Ļ░Éņłśņä▒ Ļ▓░ĒĢĄņØś 1ņ░© ņ╣śļŻīņØĖ 4ņĀ£ ļŗ©ĻĖ░ņÜöļ▓Ģ(isoniazid [INH], rifampicin [RIF], ethambutol [EMB]Ļ│╝ pyrazinamide [PZA])ņØĆ Ļ│╝Ļ▒░ 35ļģä ļÅÖņĢł ļ│ĆĒĢśņ¦Ć ņĢŖņĢśĻ│Ā, ņ╣śļŻī ĻĖ░Ļ░äņØĆ ņŚ¼ņĀäĒ׳ ņĄ£ņåī 6Ļ░£ņøöņØ┤ Ļ▒Ėļ”░ļŗż. ņØ┤ļĀćļō» ĻĖ┤ ņ╣śļŻīņÜöļ▓ĢņØĆ Ļ▓░ĒĢĄ Ļ┤Ćļ”¼ņŚÉ ņ׳ņ¢┤ ņŗ¼Ļ░üĒĢ£ ņןņĢĀļ¼╝ņØ┤ĻĖ░ ļĢīļ¼ĖņŚÉ ņäĖĻ│äņĀüņ£╝ļĪ£ ņØ┤ ņ╣śļŻī ĻĖ░Ļ░äņØä ļŗ©ņČĢņŗ£ĒéżļĀżļŖö ļģĖļĀźņØ┤ ĻŠĖņżĆĒ׳ ņ¦äĒ¢ēļÉśņ¢┤ ņÖöņ£╝ļ®░, ņĄ£ĻĘ╝ņŚÉ ļō£ļööņ¢┤ ĻĘĖ Ļ▓░ņŗżņØä ļ│┤ņØ┤Ļ│Ā ņ׳ļŗż. ņØ┤ ĻĖĆņŚÉņä£ļŖö Ļ░Éņłśņä▒ Ļ▓░ĒĢĄ ņ¦äļŗ©ņØś ņĄ£ņŗĀ ņ¦ĆĻ▓¼, ĒŖ╣Ē׳ ņżæĒĢ®ĒÜ©ņåīņŚ░ņćäļ░śņØæ(polymerase chain reaction, PCR) Ļ▓Ćņé¼ ļ░Å ņŗĀņåŹ Ļ░Éņłśņä▒ Ļ▓Ćņé¼ ņé¼ņÜ®ņØś ņĄ£ĻĘ╝ ņ¦Ćņ╣©, ņĢĮņĀ£ Ļ░Éņłśņä▒ ĒÅÉĻ▓░ĒĢĄ ņ╣śļŻīņØś ņŚŁņé¼ ļ░Å ņ╣śļŻī ĻĖ░Ļ░äņØä ļŗ©ņČĢņŗ£ĒéżĻĖ░ ņ£äĒĢ┤ ņØ┤ļ»Ė ņÖäļŻīļÉśņŚłĻ▒░ļéś Ēśäņ×¼ ņ¦äĒ¢ē ņżæņØĖ ņ×äņāü ņŚ░ĻĄ¼, ņØ┤ļź╝ ĻĘ╝Ļ▒░ļĪ£ ĒĢ£ ņäĖĻ│äļ│┤Ļ▒┤ĻĖ░ĻĄ¼(World Health Organization, WHO) ņ¦Ćņ╣© Ļ░£ņĀĢĻ│╝ Ļ░ÖņØĆ ņĄ£ņŗĀ ņ¦ĆĻ▓¼ņØä ņé┤ĒÄ┤ļ│┤Ļ│Āņ×É ĒĢ£ļŗż. ĒÅÉņÖĖ Ļ▓░ĒĢĄ ļ░Å ņĢĮņĀ£ ļé┤ņä▒Ļ▓░ĒĢĄņØś ņ¦äļŗ©Ļ│╝ ņ╣śļŻīļŖö ļ│ĖĻ│ĀņŚÉņä£ ņĀ£ņÖĖĒĢśņśĆļŗż.
Ļ▓░ĒĢĄ Ļ┤Ćļ”¼ļź╝ ņ£äĒĢ┤ Ļ░Ćņן ņżæņÜöĒĢ£ Ļ▓āņØĆ ĒÖ£ļÅÖņä▒ ĒÅÉĻ▓░ĒĢĄ ĒÖśņ×Éļź╝ Ļ░ĆļŖźĒĢ£ ĒĢ£ ļ╣©ļ”¼ ņ¦äļŗ©ĒĢśĻ│Ā ņĀüņĀłĒĢ£ ņ╣śļŻīļź╝ ĒåĄĒĢ┤ Ļ▓░ĒĢĄĻĘĀ ņĀäĒīīļĪ£ ņØĖĒĢ£ ņāłļĪ£ņÜ┤ ĒÖśņ×ÉņØś ļ░£ņāØņØä ļ¦ēļŖö Ļ▓āņØ┤ļŗż. ĻĘĖļ¤¼ļéś Ļ▓░ĒĢĄņØĆ ļŗżņ¢æĒĢ£ ņ×äņāü ņåīĻ▓¼ņØä ļ│┤ņØ┤ļ®░ ĒØēļČĆ ļ░®ņé¼ņäĀ Ļ▓Ćņé¼ļ¦īņ£╝ļĪ£ ĒÖĢņ¦äņØ┤ ĒלļōżĻ│Ā, Ļ▓Ćņ▓┤ļź╝ ņ¢╗ņØä ņłś ņŚåļŖö Ļ▓ĮņÜ░ļÅä ļ¦ÄņØä ļ┐ÉļŹöļ¤¼ ņ¦äļŗ©ņØä ņ£äĒĢ┤ ņĀäĒåĄņĀüņ£╝ļĪ£ ņŗ£Ē¢ēļÉśņ¢┤ ņś© ĒĢŁņé░ĻĘĀ ļÅäļ¦É Ļ▓Ćņé¼ņØś Ļ▓ĮņÜ░ ņĄ£ĻĘ╝ ļ╣łļÅäĻ░Ć ņ”ØĻ░Ć ņČöņäĖņØĖ ļ╣äĻ▓░ĒĢĄĒĢŁņé░ĻĘĀĻ│╝ Ļ░Éļ│äĒĢĀ ņłś ņŚåņ¢┤ ļ»╝Ļ░ÉļÅäĻ░Ć ļ¢©ņ¢┤ņ¦äļŗż[1,2]. ĒÖĢņ¦äņØä ņ£äĒĢ£ ĒĢŁņé░ĻĘĀ ļ░░ņ¢æ Ļ▓Ćņé¼ņØś Ļ▓ĮņÜ░ ņ×ÉļÅÖĒÖö ņĢĪņ▓┤ļ░░ņ¦Ć(BACTEC460)ļź╝ ļÅÖņŗ£ņŚÉ ņé¼ņÜ®ĒĢśņŚ¼ļÅä 2-6ņŻ╝ ņĀĢļÅäņØś ĻĖ┤ ņŗ£Ļ░äņØ┤ ņåīņÜöļÉśĻĖ░[3] ļĢīļ¼ĖņŚÉ ņ¦äļŗ©ņØ┤ ļŖ”ņ¢┤ņ¦ĆļŖö Ļ▓ĮņÜ░Ļ░Ć ļ¦ÄļŗżļŖö Ļ▓āļÅä ļ¼ĖņĀ£ņØ┤ļŗż. ņĄ£ĻĘ╝ņŚÉ ĒĢŁņé░ĻĘĀ ļÅäļ¦É Ļ▓Ćņé¼ļ│┤ļŗż ļ»╝Ļ░ÉļÅäĻ░Ć ļåÆņ£╝ļ®┤ņä£ ĻĖ░ņĪ┤ņØś ļ░░ņ¢æ Ļ▓Ćņé¼ļ│┤ļŗż ļ╣Āļź┤Ļ▓ī Ļ▓░ĒĢĄņØä ĒÖĢņ¦äĒĢĀ ņłś ņ׳ņ£╝ļ®░, ņĢĮņĀ£ļé┤ņä▒ ņŚ¼ļČĆļź╝ ĒĢ©Ļ╗ś ĒÅēĻ░ĆĒĢĀ ņłś ņ׳ļŖö ņŚ¼ļ¤¼ Ļ░Ćņ¦Ć Ļ▓Ćņé¼ļ▓ĢņØ┤ Ļ░£ļ░£ļÉśņ¢┤ ņ×äņāüņĀü ņżæņÜöņä▒ņØ┤ ņ”ØĻ░ĆĒĢśĻ│Ā ņ׳ļŗż.
Ļ▓░ĒĢĄĻĘĀ ļČäņ×É ņ¦äļŗ© Ļ▓Ćņé¼ļŖö Ļ▓░ĒĢĄĻĘĀņŚÉļ¦ī ĒŖ╣ņØ┤ĒĢśĻ▓ī ņĪ┤ņ×¼ĒĢśļŖö DNAļéś RNAņØś ĒŖ╣ņĀĢ ņŚ╝ĻĖ░ņä£ņŚ┤ņØä PCRņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņ”ØĒÅŁĒĢśņŚ¼ ĒÖĢņØĖĒĢśļŖö Ļ▓Ćņé¼ņØ┤ļŗż. ļČäņ×É ņ¦äļŗ© Ļ▓Ćņé¼ļŖö ĒĢŁņé░ĻĘĀ ļÅäļ¦É ļ░Å ļ░░ņ¢æĻ▓Ćņé¼ņŚÉ ļ╣äĒĢ┤ ļ╣äņÜ®ņØ┤ ļ¦ÄņØ┤ ļōżņ¦Ćļ¦ī, ļ»╝Ļ░ÉļÅäņÖĆ ĒŖ╣ņØ┤ļÅäĻ░Ć ļåÆĻ│Ā, Ļ▓░Ļ│╝ļź╝ ņ¢╗ĻĖ░Ļ╣īņ¦ĆņØś ņŗ£Ļ░äņØ┤ 24-48ņŗ£Ļ░äņ£╝ļĪ£ ņ¦¦ņØĆ ņןņĀÉņØ┤ ņ׳ļŗż[4]. Ļ▓░ĒĢĄĻĘĀ ļČäņ×É ņ¦äļŗ© Ļ▓Ćņé¼ņŚÉļŖö ļŗżņ¢æĒĢ£ ļ░®ļ▓ĢņØ┤ ņ׳ņ£╝ļ®░ ņ¦Ćļé£ 10ņŚ¼ļģäĻ░ä ņāłļĪ£ņÜ┤ ļČäņ×É ņ¦äļŗ© Ļ▓Ćņé¼Ļ░Ć ļ¦ÄņØ┤ Ļ░£ļ░£ļÉśņŚłņ£╝ļ®░ PCRņØä ĒåĄĒĢ£ Ļ▓░ĒĢĄĻĘĀ ĒĢĄņé░ ņ”ØĒÅŁ Ļ▓Ćņé¼(nucleic acid amplification tests, NAATs)ļŖö Ļ▓░ĒĢĄĻĘĀņØä ĒÖĢņØĖĒĢśļŖö ĻĖ░ļŖź ņÖĖņŚÉļÅä Ļ▓░ĒĢĄ ņ╣śļŻīņŚÉ ĒĢĄņŗ¼ņØ┤ ļÉśļŖö ņĢĮņĀ£ļōżņŚÉ ļīĆĒĢ£ ļé┤ņä▒ ņŚ¼ļČĆĻ╣īņ¦Ć ņĀäĒåĄņĀü ņĢĮņĀ£ Ļ░Éņłśņä▒ Ļ▓Ćņé¼ļ│┤ļŗż ļ╣Āļź┤Ļ▓ī ĒÖĢņØĖĒĢĀ ņłś ņ׳ļŗż[5]. Ēśäņ×¼Ļ╣īņ¦Ć WHOņŚÉņä£ ņŖ╣ņØĖļÉ£ NAATsņŚÉļŖö line probe assay (LPA), Xpert MTB/RIF, loop-mediated isothermal amplification (LAMP), Truelab ļō▒ņØ┤ ņ׳ņ£╝ļéś[5] ĻĄŁļé┤ņŚÉņä£ļŖö LAMP, TruelabņŚÉ ļīĆĒĢ£ ĒÅēĻ░ĆņÖĆ ĻĘ╝Ļ▒░Ļ░Ć ļČĆņĪ▒ĒĢśļŗż. ĻĄŁļé┤ Ļ▓░ĒĢĄ ņ¦äļŻīņ¦Ćņ╣©ņŚÉņä£ 2011ļģä(ņ┤łĒīÉ)ņŚÉļŖö 1) ĒÅÉĻ▓░ĒĢĄņØ┤ ņØśņŗ¼ļÉśļéś ļÅäļ¦É Ļ▓Ćņé¼Ļ░Ć ņØīņä▒ņØ╝ ļĢī Ēś╣ņØĆ 2) ĒĢŁņé░ĻĘĀ ļÅäļ¦É Ļ▓Ćņé¼Ļ░Ć ņ¢æņä▒ņØ┤ņ¦Ćļ¦ī ļ╣äĻ▓░ĒĢĄ ĒĢŁņé░ĻĘĀņØś Ļ░ĆļŖźņä▒ņØ┤ ņ׳ņØä ļĢī ņŗżņŗ£ĒĢĀ Ļ▓āņØä ĻČīĻ│ĀĒĢśņśĆļŗż[6]. ĒĢśņ¦Ćļ¦ī 2017ļģä(3ĒīÉ)ļČĆĒä░ Ļ▓░ĒĢĄņØ┤ ņØśņŗ¼ļÉĀ ļĢī ĒĢŁņé░ĻĘĀ ļÅäļ¦É ļ░Å ļ░░ņ¢æ Ļ▓Ćņé¼ņÖĆ ĒĢ©Ļ╗ś PCR Ļ▓Ćņé¼ļź╝ ļ░śļō£ņŗ£ ņŗ£Ē¢ēņØä ĒĢ┤ņĢ╝ ĒĢ£ļŗżĻ│Ā ļ¬ģņŗ£ĒĢśĻ│Ā ņ׳ļŗż[7]. ĻĄŁļé┤ņŚÉņä£ļŖö ļ»╝Ļ░ÉļÅäņÖĆ ĒŖ╣ņØ┤ļÅäĻ░Ć ļåÆņØĆ ŌĆśņŗżņŗ£Ļ░ä ņżæĒĢ® ĒÜ©ņåī ņŚ░ņćä ļ░śņØæ(real-time PCR)ŌĆÖņØ┤ ņŻ╝ļĪ£ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ņ£╝ļ®░ ņØ┤ļź╝ ņé¼ņÜ®ĒĢ£ ļ░®ļ▓ĢņŚÉļŖö ĒåĄņāüņĀüņØĖ ļ░®ļ▓ĢĻ│╝ Xpert MTB/RIF Ļ▓Ćņé¼ļ▓Ģ(Xpert)ņØ┤ ņ׳ļŗż.
XpertļŖö ņ×ÉļÅÖĒÖöļÉ£ real-time PCR Ļ▓Ćņé¼ļĪ£ ņłÖļĀ©ļÉ£ Ļ▓Ćņé¼ņ×ÉĻ░Ć ņĢäļŗłļŹöļØ╝ļÅä Ļ▓Ćņ▓┤ļź╝ ļ░öļĪ£ Ļ▓Ćņé¼ ĒéżĒŖĖņŚÉ ņĀüņÜ®ĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ Ļ▓Ćņé¼ Ļ│╝ņĀĢņØ┤ ļŗ©ņł£ĒĢśļ®░ ņĢĮ 2ņŗ£Ļ░ä ļé┤ņŚÉ Ļ▓░Ļ│╝ļź╝ ĒÖĢņØĖĒĢĀ ņłś ņ׳ļŖö ņןņĀÉņØ┤ ņ׳ņ£╝ļéś ĒåĄņāüņĀüņØĖ real-time PCRņŚÉ ļ╣äĒĢśņŚ¼ Ļ▓Ćņé¼ ĒéżĒŖĖņÖĆ ņןļ╣äĻ░Ć Ļ│ĀĻ░ĆļØ╝ļŖö ļŗ©ņĀÉņØ┤ ņ׳ļŗż[8]. ĒĢśņ¦Ćļ¦ī XpertļŖö Ļ▓░ĒĢĄĻĘĀņØś ņĪ┤ņ×¼ ĒÖĢņØĖĻ│╝ ļÅÖņŗ£ņŚÉ RIF ļé┤ņä▒ ņŚ¼ļČĆļź╝ Ļ░ÖņØ┤ Ļ▓Ćņé¼ĒĢĀ ņłś ņ׳ņ¢┤ ņŗĀņåŹĒĢ£ Ļ▓░ĒĢĄņØś ņ¦äļŗ© ļ░Å RIF ļé┤ņä▒ Ļ▓░ĒĢĄņØś ņ¦äļŗ©ņØ┤ ļ¬©ļæÉ Ļ░ĆļŖźĒĢśņŚ¼ ņĄ£ĻĘ╝ ĻĄŁļé┤ ļ¦ÄņØĆ ļ│æņøÉņŚÉņä£ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŗż.
ĻĄŁļé┤ Ļ▓░ĒĢĄ ņ¦äļŻīņ¦Ćņ╣©ņŚÉņä£ļŖö 2014ļģä(2ĒīÉ)ļČĆĒä░ Xpert Ļ▓Ćņé¼ņŚÉ ļīĆĒĢ┤ 1) ņ×¼ņ╣śļŻīņÖĆ Ļ░ÖņØ┤ ļŗżņĀ£ļé┤ņä▒Ļ▓░ĒĢĄņØś Ļ░ĆļŖźņä▒ņØ┤ ļåÆņØĆ Ļ▓ĮņÜ░ Ēś╣ņØĆ 2) ņżæņ”Ø Ļ▓░ĒĢĄņØ┤ļéś ņØĖņ▓┤ļ®┤ņŚŁĻ▓░ĒĢŹļ░öņØ┤ļ¤¼ņŖż Ļ░ÉņŚ╝ņØĖņŚÉņä£ ļ░£ņāØĒĢ£ Ļ▓░ĒĢĄņ▓śļ¤╝ ņĢĮņĀ£ļé┤ņä▒ ņŚ¼ļČĆļź╝ ņŗĀņåŹĒĢśĻ▓ī ĒÖĢņØĖĒĢ┤ņĢ╝ ĒĢśļŖö Ļ▓ĮņÜ░ Ēś╣ņØĆ 3) ĻĘĖ ņÖĖ ņāüĒÖ®ņŚÉņä£ ļŗżņĀ£ļé┤ņä▒ Ļ▓░ĒĢĄņØä Ļ▓ĆņČ£ĒĢśĻĖ░ ņ£äĒĢ£ ļ¬®ņĀüņ£╝ļĪ£ ņŗżņŗ£ĒĢĀ ņłś ņ׳ļŗżĻ│Ā ĻČīĻ│ĀĒĢśņśĆļŗż[9]. ĒĢśņ¦Ćļ¦ī 2020ļģäņŚÉ Ļ░£ņĀĢļÉ£ 4ĒīÉņŚÉņä£ļŖö 1) ļŗżņĀ£ļé┤ņä▒ Ļ▓░ĒĢĄņØ┤ ņØśņŗ¼ļÉśļŖö Ļ▓ĮņÜ░ Ēś╣ņØĆ 2) ņŗĀņåŹĒĢśĻ▓ī ļé┤ņä▒ ņŚ¼ļČĆļź╝ ĒÖĢņØĖĒĢ┤ņĢ╝ ĒĢśļŖö Ļ▓ĮņÜ░ ļ░śļō£ņŗ£ ņŗ£Ē¢ēĒĢ┤ņĢ╝ ĒĢ£ļŗżĻ│Ā ļ¬ģņŗ£ĒĢśņśĆĻ│Ā, 3) ņŗĀņåŹĒĢ£ Ļ▓░ĒĢĄ ņ¦äļŗ©ņØ┤ ĒĢäņÜöĒĢ£ Ļ▓ĮņÜ░ ņŗ£Ē¢ēĒĢĀ ņłś ņ׳ļŗżĻ│Ā ĻČīĻ│ĀĒĢśĻ│Ā ņ׳ļŗż[10]. 2014ļģäņŚÉ ļ░£Ēæ£ļÉ£ XpertņØś ņ¦äļŗ© ņĀĢĒÖĢļÅäņŚÉ ļīĆĒĢ£ ņ▓┤Ļ│äņĀü ļ¼ĖĒŚīĻ│Āņ░░ Ļ▓░Ļ│╝, ļÅäļ¦É ļ░Å ļ░░ņ¢æņ¢æņä▒ Ļ▓Ćņ▓┤ņŚÉņä£ ļ»╝Ļ░ÉļÅäĻ░Ć 98%ņśĆĻ│Ā ļÅäļ¦É ņØīņä▒ ļ░Å ļ░░ņ¢æ ņ¢æņä▒Ļ▓Ćņ▓┤ņŚÉņä£ ļ»╝Ļ░ÉļÅäļŖö 67%ļĪ£ ĒÖĢņØĖļÉśņŚłļŗż[11]. ņØ┤ļ¤¼ĒĢ£ ļÅäļ¦É ņØīņä▒ Ļ▓Ćņ▓┤ņŚÉņä£ņØś ļé«ņØĆ ļ»╝Ļ░ÉļÅäļź╝ Ē¢źņāüņŗ£ĒéżĻĖ░ ņ£äĒĢ┤ Xpert MTB/RIF ultraĻ░Ć Ļ░£ļ░£ļÉśņŚłņ£╝ļ®░ 2017ļģäļČĆĒä░ WHOņŚÉ ņŖ╣ņØĖņØä ļ░øņĢśĻ│Ā, 2021ļģäņŚÉ ļ░£Ēæ£ļÉ£ Xpert MTB/RIF ultraņØś ņ¦äļŗ© ņĀĢĒÖĢļÅäņŚÉ Ļ┤ĆĒĢ£ ņ▓┤Ļ│äņĀü ļ¼ĖĒŚīĻ│Āņ░░ Ļ▓░Ļ│╝ ĻĖ░ņĪ┤ņØś XpertņÖĆ ļ╣äĻĄÉĒĢśņśĆņØä ļĢī ĒÅÉĻ▓░ĒĢĄ ņ¦äļŗ©ņØś ļ»╝Ļ░ÉļÅä ļ░Å ĒŖ╣ņØ┤ļÅä(95% ņŗĀļó░ĻĄ¼Ļ░ä)ļŖö Xpert MTB/RIF UltraņŚÉņä£ 90.9% (86.2-94.7), 95.6% (93.0-97.4)ņśĆĻ│Ā, XpertņŚÉņä£ 84.7% (78.6-89.9), 98.4% (97.0-99.3)ļĪ£ ļ»╝Ļ░ÉļÅäļŖö 6.2% Ē¢źņāüļÉśņŚłņ£╝ļéś ĒŖ╣ņØ┤ļÅäĻ░Ć 2.8% Ļ░ÉņåīĒĢ£ Ļ▓░Ļ│╝ļź╝ ļ│┤ņśĆļŗż. ļÅäļ¦É ņØīņä▒ ļ░Å ļ░░ņ¢æ ņ¢æņä▒ Ļ▓Ćņ▓┤ņŚÉņä£ ņ¦äļŗ© ļ»╝Ļ░ÉļÅäļŖö Xpert MTB/RIF ultraņŚÉņä£ 77.5%ļĪ£ ĻĖ░ņĪ┤ņØś XpertņØś 60.6%ļ│┤ļŗż 16.9%ļĪ£ ņøöļō▒ĒĢ£ ņ”ØĻ░Ćļź╝ ļ│┤ņśĆļŗż[12]. ņĄ£ĻĘ╝ņŚÉļŖö RIFļ┐Éļ¦ī ņĢäļŗłļØ╝ fluoroquinolone (FQ) ļ░Å ņŻ╝ņé¼ņĀ£ņŚÉ ļīĆĒĢ£ ļé┤ņä▒Ļ╣īņ¦Ć ĒÖĢņØĖĒĢĀ ņłś ņ׳ļŖö Xpert XDRņØ┤ Ļ░£ļ░£ļÉśņŚłļŗż.
Ļ▓░ĒĢĄ Ļ┤Ćļ”¼ņŚÉņä£ ļ╣ĀļźĖ ņ¦äļŗ©Ļ│╝ ĒĢ©Ļ╗ś ņżæņÜöĒĢ£ ņØ┤ņŖłļŖö ņĢĮņĀ£ļé┤ņä▒ņØ┤ļŗż. ļ│ĖĻ│ĀņŚÉņä£ļŖö ņĢĮņĀ£ Ļ░Éņłśņä▒ ĒÅÉĻ▓░ĒĢĄņØä ņŻ╝ļĪ£ ļŗżļŻ©Ļ│Ā ņ׳ņ£╝ļéś ņĢĮņĀ£ Ļ░Éņłśņä▒ ĒÅÉĻ▓░ĒĢĄņØä ņ╣śļŻīĒĢśĻĖ░ ņ£äĒĢ┤ņä£ļŖö ņ╣śļŻī ņŗ£ņ×æ ņĀäņŚÉ ņĢĮņĀ£ ļé┤ņä▒Ļ▓░ĒĢĄņØä ļ░░ņĀ£ĒĢśļŖö Ļ▓āņØ┤ ņÜ░ņäĀņĀüņ£╝ļĪ£ ņØ┤ļŻ©ņ¢┤ņĀĖņĢ╝ ĒĢ£ļŗż. ņĀäĒåĄņĀüņ£╝ļĪ£ ĒĢŁĻ▓░ĒĢĄ ņĢĮņĀ£ Ļ░Éņłśņä▒ Ļ▓Ćņé¼ļŖö Ļ│Āņ▓┤ Ēś╣ņØĆ ņĢĪņ▓┤ļ░░ņ¦Ćļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ĒŖ╣ņĀĢ ĒĢŁĻ▓░ĒĢĄņĢĮņĀ£ļź╝ ĒżĒĢ©ĒĢ£ ļ░░ņ¦ĆņŚÉ ĻĘĀņØä ņĀæņóģĒĢ£ ļÆż ļ░░ņ¢æ ņŚ¼ļČĆļź╝ Ļ┤Ćņ░░ĒĢśļŖö ļ░®ļ▓Ģņ£╝ļĪ£, Ļ│Āņ▓┤ļ░░ņ¦Ćļź╝ ņé¼ņÜ®ĒĢśļŖö Ļ▓ĮņÜ░ Ļ▓░Ļ│╝ ļ│┤Ļ│ĀĻ╣īņ¦Ć ņĢĮ 3Ļ░£ņøö ņØ┤ņāü ņåīņÜöļÉśļŖö ļŗ©ņĀÉņØ┤ ņ׳ļŗż. ļö░ļØ╝ņä£ ļé┤ņä▒ņŚ¼ļČĆļź╝ ņŗĀņåŹĒĢśĻ▓ī ĒÖĢņØĖĒĢśĻ│Āņ×É ĒĢŁĻ▓░ĒĢĄņĢĮņĀ£ņØś ļé┤ņä▒ņŚÉ Ļ┤ĆņŚ¼ĒĢśļŖö ĒŖ╣ņĀĢ ņ£ĀņĀäņ×É ļÅīņŚ░ļ│ĆņØ┤ļź╝ ĒÖĢņØĖĒĢśļŖö ļČäņ×ÉņāØļ¼╝ĒĢÖņĀü ļ░®ļ▓ĢņØ┤ ļÅäņ×ģļÉśņŚłņ£╝ļ®░, RIFņÖĆ INHņŚÉ ļīĆĒĢ£ ņŗĀņåŹ Ļ░Éņłśņä▒ Ļ▓Ćņé¼ņØĖ LPAĻ░Ć ļ│┤ĒÄĖĒÖöļÉśņ¢┤ ļŗżņĀ£ļé┤ņä▒ Ļ▓░ĒĢĄņØś ņ¦äļŗ©ņŚÉ ņØ┤ņÜ®ļÉśĻ│Ā ņ׳ļŗż. LPAļŖö ļÅäļ¦Éņ¢æņä▒ņØĖ Ļ▓Ćņ▓┤ņÖĆ ļ░░ņ¢æļÉ£ ĻĘĀņŻ╝ ļ¬©ļæÉļĪ£ ņŗ£Ē¢ēĒĢĀ ņłś ņ׳ņ£╝ļ®░ 2-3ņØ╝ ļé┤ņŚÉ Ļ▓░Ļ│╝ ĒÖĢņØĖņØ┤ Ļ░ĆļŖźĒĢśļŗż. ĻĄŁļé┤ņŚÉņä£ ņé¼ņÜ® ņżæņØĖ Ļ▓Ćņé¼ļ▓ĢņØĆ GenoType MTBDRplus (Hain Lifesciences-Bruker, Nehren, Germany)ņØ┤ļ®░ RIF ļé┤ņä▒ņØś ņ¦äļŗ©ņØĆ rpoB ņ£ĀņĀäņ×ÉņØś ļÅīņŚ░ļ│ĆņØ┤ļź╝, INH ļé┤ņä▒ņØś ņ¦äļŗ©ņØĆ katG, inhA ņ£ĀņĀäņ×ÉņØś ļÅīņŚ░ļ│ĆņØ┤ļź╝ Ļ▓ĆņČ£ĒĢśņŚ¼ ļé┤ņä▒ ņŚ¼ļČĆļź╝ ņ¦äļŗ©ĒĢ£ļŗż[13]. ļ®öĒāĆļČäņäØ Ļ▓░Ļ│╝ INH ļé┤ņä▒, RIF ļé┤ņä▒, ļŗżņĀ£ļé┤ņä▒ Ļ▓░ĒĢĄņØś ņ¦äļŗ© ļ»╝Ļ░ÉļÅäļŖö 91%, 96%, 91%ņØ┤Ļ│Ā, ĒŖ╣ņØ┤ļÅäļŖö 99%, 98%, 99%ņśĆļŗż[14]. ņĄ£ĻĘ╝ņŚÉļŖö GenoType MTBDRslņØ┤ Ļ░£ļ░£ļÉśņ¢┤ INHņÖĆ RIF ļ┐Éļ¦ī ņĢäļŗłļØ╝ FQ, EMB, kanamycin, amikacinņŚÉ ļīĆĒĢ£ ļé┤ņä▒ņØä ĒÖĢņØĖĒĢśņŚ¼ Ļ│Āļ¼┤ņĀüņØĖ Ļ▓░Ļ│╝ļź╝ ļ│┤ņŚ¼ņŻ╝Ļ│Ā ņ׳ļŗż[15].
ĻĄŁļé┤ Ļ▓░ĒĢĄņ¦äļŻīņ¦Ćņ╣©ņŚÉņä£ļŖö 2011ļģä(ņ┤łĒīÉ)ļČĆĒä░ 1) ļŗżņĀ£ļé┤ņä▒Ļ▓░ĒĢĄņØ┤ ņØśņŗ¼ļÉśļŖö Ļ▓ĮņÜ░ Ēś╣ņØĆ 2) ņ×¼ņ╣śļŻī ņŗ£ņŚÉ ņŗĀņåŹ ļé┤ņä▒ Ļ▓Ćņé¼ņŗ£Ē¢ēņØä ĻČīĻ│ĀĒĢśņśĆņ£╝ļ®░, 2014ļģä(2ĒīÉ)ļČĆĒä░ļŖö 1) ņ×¼ņ╣śļŻīņÖĆ Ļ░ÖņØ┤ ļŗżņĀ£ļé┤ņä▒ Ļ▓░ĒĢĄņØś Ļ░ĆļŖźņä▒ņØ┤ ļåÆņØĆ Ļ▓ĮņÜ░ ļÅäļ¦É ņ¢æņä▒ Ļ▓Ćņ▓┤ Ēś╣ņØĆ ļ░░ņ¢æļÉ£ Ļ▓░ĒĢĄĻĘĀņŻ╝ļź╝ ļīĆņāüņ£╝ļĪ£ ņŗĀņåŹ ļé┤ņä▒ Ļ▓Ćņé¼ ņŗ£Ē¢ēņØä ĻČīĻ│ĀĒĢśņśĆļŗż[6]. ĻĘĖļ¤¼ļéś 2017ļģä(3ĒīÉ) ņØ┤Ēøä 1) ņ×¼ņ╣śļŻī ļō▒ ļŗżņĀ£ļé┤ņä▒ Ļ▓░ĒĢĄņØ┤ ņØśņŗ¼ļÉśļŖö Ļ▓ĮņÜ░ ļÅäļ¦É ņ¢æņä▒ Ļ▓Ćņ▓┤ Ēś╣ņØĆ ļ░░ņ¢æļÉ£ Ļ▓░ĒĢĄĻĘĀņŻ╝ļź╝ ļīĆņāüņ£╝ļĪ£ ņŗĀņåŹ ļé┤ņä▒ Ļ▓Ćņé¼ļź╝ ļ░śļō£ņŗ£ ņŗ£Ē¢ēĒĢ┤ņĢ╝ ĒĢ£ļŗżĻ│Ā ļ¬ģņŗ£ĒĢśņśĆĻ│Ā[7], 2020ļģä(4ĒīÉ)ļČĆĒä░ļŖö 1) ļ¬©ļōĀ Ļ▓░ĒĢĄ ĒÖśņ×ÉņØś ņ▓½ ļ░░ņ¢æĻĘĀņŻ╝ņŚÉ ļīĆĒĢ┤ ņŗĀņåŹ Ļ░Éņłśņä▒ Ļ▓Ćņé¼ņÖĆ ĒåĄņāü Ļ░Éņłśņä▒ Ļ▓Ćņé¼ļź╝ ĒĢ©Ļ╗ś ņŗ£Ē¢ēĒĢ┤ņĢ╝ ĒĢśļ®░, 2) ĒĢŁņé░ĻĘĀ ļÅäļ¦É ņ¢æņä▒ņØĖ Ļ▓Ćņ▓┤ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņŗĀņåŹ Ļ░Éņłśņä▒ Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢĀ ņłś ņ׳ņ£╝ļ®░, 3) INH ļśÉļŖö RIFņŚÉ ļé┤ņä▒ņØ┤ Ļ▓ĆņČ£ļÉ£ Ļ▓ĮņÜ░ FQņØä ĒżĒĢ©ĒĢ£ ņØ┤ņ░© ĒĢŁĻ▓░ĒĢĄņĀ£ņŚÉ ļīĆĒĢ£ ņŗĀņåŹ Ļ░Éņłśņä▒ Ļ▓Ćņé¼ņÖĆ ĒåĄņāü Ļ░Éņłśņä▒ Ļ▓Ćņé¼ļź╝ ĒĢ©Ļ╗ś ņŗ£Ē¢ēĒĢ┤ņĢ╝ ĒĢ£ļŗżĻ│Ā Ļ░£ņĀĢĻČīĻ│ĀĒĢśņśĆļŗż[10].
ĒÅÉĻ▓░ĒĢĄņØś ļ╣ĀļźĖ ņ¦äļŗ©Ļ│╝ ņ╣śļŻīļź╝ ņ£äĒĢ┤ņä£ļŖö ņ£äņŚÉņä£ ņ¢ĖĻĖēĒĢ£ ņŗĀņåŹĒĢ£ Ļ▓Ćņé¼ ļ░®ļ▓Ģ ņ×Éņ▓┤ļÅä ņżæņÜöĒĢśņ¦Ćļ¦ī ĻĘĖ Ļ▓Ćņé¼ Ļ▓░Ļ│╝Ļ░Ć ņ¢æņä▒ņØ╝ ļĢī ņ×äņāüņØśĻ░Ć ļ╣Āļź┤Ļ│Ā ņĀüņĀłĒĢ£ ņ▓śņ╣śļź╝ ĒĢĀ ņłś ņ׳ļÅäļĪØ ņŗĀņåŹĒĢ£ ļ│┤Ļ│Āņ▓┤Ļ│äļź╝ Ļ░¢ņČöļŖö Ļ▓ā ņŚŁņŗ£ ļ¦żņÜ░ ņżæņÜöĒĢśļŗż. Ļ▓░ĒĢĄņØś ņ¦äļŗ© ļ░Å ņ╣śļŻīņØś ņ¦ĆņŚ░ņØĆ ĒÖśņ×ÉņØś ņé¼ļ¦ØļźĀņØä ņ”ØĻ░Ćņŗ£ĒéżĻ│Ā, Ļ▓░ĒĢĄĻĘĀņØś ņĀäĒīīļź╝ ņ”ØĻ░Ćņŗ£Ēé¼ ņłś ņ׳ļŗż. ĒŖ╣Ē׳ ļ░ĆĒÅÉļÉ£ Ļ│ĄĻ░äņŚÉņä£ ĒÖśņ×ÉļōżņØ┤ ņ¦æļŗ©ņāØĒÖ£ņØä ĒĢśĻ│Ā ņ׳ļŖö ņØśļŻīĻĖ░Ļ┤ĆņŚÉņä£ Ļ│ĄĻĖ░ ļ¦żĻ░£ņä▒ ņĀäņŚ╝ļ│æņØĖ ĒÅÉĻ▓░ĒĢĄ ĒÖśņ×ÉĻ░Ć ļ░£ņāØĒĢĀ Ļ▓ĮņÜ░, ņŻ╝ņ£ä ĒÖśņ×ÉņŚÉĻ▓ī Ļ▓░ĒĢĄĻĘĀņØ┤ Ļ░ÉņŚ╝ļÉśĻĖ░ ņē¼ņÜ░ļ®░ ĒÖ£ļÅÖņä▒ Ļ▓░ĒĢĄņ£╝ļĪ£ ņ¦äĒ¢ēĒĢĀ ņ£äĒŚśņä▒ ļ░Å ņżæņ”Ø Ļ▓░ĒĢĄņØ┤ ļ░£ņāØĒĢĀ ņ£äĒŚśņä▒ļÅä ņ”ØĻ░ĆĒĢ£ļŗż. Ļ▓░ĒĢĄņØś ņ¦äļŗ© ļ░Å ņ╣śļŻīĻ░Ć ņ¦ĆņŚ░ļÉśļŖö ņøÉņØĖņØĆ Ēü¼Ļ▓ī ĒÖśņ×É ņłśņ¦ä ņ¦ĆņŚ░Ļ│╝ ņØśņé¼ ņ¦äļŗ© ņ¦ĆņŚ░ņ£╝ļĪ£ ĻĄ¼ļČäĒĢĀ ņłś ņ׳ļŖöļŹ░, ņØśņé¼ ņ¦äļŗ© ņ¦ĆņŚ░ņØĆ 1) ĒÖśņ×ÉĻ░Ć ļé┤ņøÉĒĢ£ ļÆż Ļ▓░ĒĢĄ Ļ▓Ćņé¼ ņŗ£Ē¢ēĻ╣īņ¦Ć, 2) Ļ▓░ĒĢĄ Ļ▓Ćņé¼ Ēøä ņ¦äļŗ©Ļ╣īņ¦Ć, 3) ņ¦äļŗ©ļÉ£ Ēøä ņ╣śļŻī ņŗ£ņ×æĻ╣īņ¦Ć ļō▒ņ£╝ļĪ£ ļéśļłī ņłś ņ׳ņ£╝ļ®░[16] ĻĘĖņżæ ļ│æņøÉ ņ▓┤Ļ│äļĪ£ ņ¦ĆņŚ░ņØä ņśłļ░®ĒĢĀ ņłś ņ׳ļŖö ļŗ©Ļ│äĻ░Ć 3) ņ¦äļŗ©ļÉ£ Ēøä ņ╣śļŻī ņŗ£ņ×æņØ┤ļØ╝Ļ│Ā ļ│╝ ņłś ņ׳ļŗż.
ļö░ļØ╝ņä£ ļ│æņøÉ ļé┤ņŚÉņä£ ņŗ£Ē¢ēĒĢ£ Ļ░Øļŗ┤ Ļ▓░ĒĢĄĻĘĀ Ļ▓Ćņé¼ņŚÉņä£ ĻĘĀņ¢æņä▒(ļÅäļ¦É/ļ░░ņ¢æ/PCR)ņØ┤ ĒÖĢņØĖļÉśļŖö Ļ▓ĮņÜ░ ĻĘĖ Ļ▓░Ļ│╝ļŖö ņ”ēņŗ£ ļŗ┤ļŗ╣ņØśņé¼ņŚÉĻ▓ī ļ│┤Ļ│ĀļÉśņ¢┤ņĢ╝ ĒĢ£ļŗż. ļ╣ĀļźĖ ļ│┤Ļ│Āļź╝ ņ£äĒĢ£ ņŚ¼ļ¤¼ Ļ░Ćņ¦Ć ļ░®ļ▓ĢņØ┤ ņŗ£ļÅäļÉśņ¢┤ ņÖöņ£╝ļ®░, ĻĘĖ ļīĆĒæ£ņĀüņØĖ ļ░®ļ▓ĢņØ┤ ņ£äĒŚśņłśņżĆ Ļ▓Ćņé¼ Ļ▓░Ļ│╝ļ│┤Ļ│Ā(critical value report, CVR)ņØ┤ļŗż. Ļ│╝Ļ▒░ņŚÉļŖö ņĀäĒÖöļĪ£ ļ│æļÅÖņŚÉ ņŚ░ļØĮĒĢśļŹś ļ░®ņŗØņŚÉņä£ ņĄ£ĻĘ╝ņŚÉļŖö ņøÉļé┤ ņĀäņé░ņØ┤ļéś Ļ░£ņØĖ ĒĢĖļō£ĒÅ░ ļ®öņŗ£ņ¦Ć ļō▒ņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņŗżņŗ£Ļ░äņ£╝ļĪ£ ļŗ┤ļŗ╣ņØśņé¼ņŚÉĻ▓ī ņ¦üņĀæ ļ│┤Ļ│ĀĒĢśļŖö ļ░®ļ▓Ģņ£╝ļĪ£ ļ│ĆĒÖöĒĢśĻ│Ā ņ׳ļŗż. ņĄ£ĻĘ╝ ĻĄŁļé┤ņŚÉņä£ ļ░£Ēæ£ļÉ£ ņŚ░ĻĄ¼ņŚÉ ņØśĒĢśļ®┤ ņäżļ¼ĖņŚÉ ņØæļŗĄĒĢ£ ņ┤Ø 64Ļ░£ ņØśļŻīĻĖ░Ļ┤Ć ņżæ 12Ļ░£ņØś ņØśļŻīĻĖ░Ļ┤ĆņŚÉņä£ ĒĢŁņé░ĻĘĀ ļÅäļ¦É Ļ▓Ćņé¼ ņ¢æņä▒ Ļ▓░Ļ│╝ļź╝ CVRņŚÉ ĒżĒĢ©ņŗ£ņ╝£ ņŗĀņåŹĒĢśĻ▓ī ļ│┤Ļ│ĀĒĢśļŖö Ļ▓āņ£╝ļĪ£ ĒÖĢņØĖļÉśņŚłļŗż. ņĢäņ¦üĻ╣īņ¦Ć CVRņŚÉ Ļ┤ĆĒĢ£ ĻĄŁļé┤ņ¦Ćņ╣©ņØĆ ņŚåļŖö ņāüĒÖ®ņØ┤ļéś ņĀĆņ×ÉļōżņØĆ ļ│æņøÉņŚÉņä£ Ļ╝Ł ĒĢäņÜöĒĢ£ CVRņŚÉ ĒĢŁņé░ĻĘĀ ļÅäļ¦É Ļ▓Ćņé¼ ņ¢æņä▒ ĒĢŁļ¬®ņØ┤ ļ░śļō£ņŗ£ ĒżĒĢ©ļÉśņ¢┤ņĢ╝ ĒĢ£ļŗżĻ│Ā ņĀ£ņĢłĒĢśņśĆļŗż[17]. Ē¢źĒøä ļ¬©ļōĀ ņØśļŻīĻĖ░Ļ┤ĆņŚÉņä£ ĒĢŁņé░ĻĘĀ ļÅäļ¦É Ļ▓Ćņé¼ ļ┐Éļ¦ī ņĢäļŗłļØ╝ ĒĢŁņé░ĻĘĀ ļ░░ņ¢æ Ļ▓Ćņé¼ ļ░Å MTB PCR Ļ▓Ćņé¼ ĒĢŁļ¬® ņŚŁņŗ£ CVRņŚÉ ĒżĒĢ©ņŗ£ĒéżļŖö Ļ▓āņØ┤ ĒĢäņÜöĒĢĀ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
ĒÜ©Ļ│╝ņĀüņØĖ ĒÖöĒĢÖņÜöļ▓ĢņØ┤ Ļ░£ļ░£ļÉśĻĖ░ ņĀä, Ļ▓░ĒĢĄ ņ╣śļŻīļŖö ņŗĀņäĀĒĢ£ Ļ│ĄĻĖ░ņÖĆ Ē¢ćļ╣øņØä ņɼļ®░ ņÜöņ¢æņøÉņŚÉņä£ ļ│┤ņĪ┤ņĀüņ£╝ļĪ£ ņ╣śļŻīĒĢśļŖö Ļ▓āņØ┤ ņĀäļČĆņśĆļŗż. ĒÖöĒĢÖņÜöļ▓Ģņ£╝ļĪ£ņä£ņØś Ļ▓░ĒĢĄ ņ╣śļŻīļŖö 1944ļģä streptomycin (SM)Ļ│╝ para-aminosalicylic acid (PAS)Ļ░Ć ļ░£Ļ▓¼ļÉśļ®┤ņä£ ļ╣äļĪ£ņåī ņŗ£ņ×æļÉśņŚłļŗż. British Medical Research CouncilņØĆ ĒÖ£ļÅÖņä▒ ĒÅÉĻ▓░ĒĢĄ ĒÖśņ×ÉņŚÉĻ▓ī PAS ļśÉļŖö SM ļŗ©ļÅģņ╣śļŻī ļ░Å PAS + SM ļ│æĒĢ® ņ╣śļŻīļź╝ ļ╣äĻĄÉĒĢ£ ņĄ£ņ┤łņØś ļ¼┤ņ×æņ£ä ļīĆņĪ░ ņŚ░ĻĄ¼ļź╝ ņłśĒ¢ēĒĢśņśĆņ£╝ļ®░ Ļ▓░Ļ│╝ PAS + SM ļ│æĒĢ® ņ╣śļŻīĻ░Ć ņ╣śļŻī ņä▒Ļ│Ą ļ░Å ņĢĮņĀ£ļé┤ņä▒ ļ░£ņāØ ņśłļ░®ņŚÉ ļŹö ĒÜ©Ļ│╝ņĀüņØ┤ļØ╝Ļ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż[18]. ņØ┤Ēøä 1952ļģäļČĆĒä░ 1960ļģäļīĆ ņżæļ░śņŚÉ INHĻ░Ć ņČöĻ░Ć Ļ░£ļ░£ļÉśļ®┤ņä£ 3ņĀ£ ņ╣śļŻī Ļ░£ļģÉņØ┤ ĒśĢņä▒ļÉśņŚłĻ│Ā, 24Ļ░£ņøöĻ░äņØś INH/SM/PAS ļ│æĒĢ® ņ╣śļŻīļĪ£ 90-95%ņØś ņÖäņ╣śņ£©ņØä ļ│┤ņśĆļŗż[19]. 1960ļģäļīĆ EMBĻ░Ć PASļź╝ ļīĆņ▓┤ĒĢśļ®┤ņä£ ņĢĮņĀ£ņł£ņØæļÅäĻ░Ć ļåÆņĢäņĪīņ£╝ļ®░ ņ╣śļŻī ĻĖ░Ļ░äņØä 24Ļ░£ņøöņŚÉņä£ 18Ļ░£ņøöļĪ£ ļŗ©ņČĢņŗ£ņ╝░ļŗż[20]. 1970ļģäļīĆ RIFĻ░Ć ņČöĻ░ĆļÉśļ®┤ņä£ INHņØś ņé┤ĻĘĀĒÜ©Ļ│╝ņŚÉ ļŹöĒĢśņŚ¼, Ļ░ĢļĀźĒĢ£ ļ®ĖĻĘĀĒÜ©Ļ│╝ļź╝ ļ│┤ņØ┤ļ®░ ņ╣śļŻī ĻĖ░Ļ░äņØ┤ 18Ļ░£ņøöņŚÉņä£ 9Ļ░£ņøöļĪ£ ļŗ©ņČĢļÉśņŚłĻ│Ā[21,22], ņØ┤Ēøä ņ┤łĻĖ░ 2Ļ░£ņøöĻ░ä PZAļź╝ ņé¼ņÜ®ĒĢśņśĆņØä ļĢī Ļ│ĄļÅÖļé┤ņØś ņé░ņä▒ĒÖśĻ▓ĮņŚÉņä£ ĒÖ£ļ░£ĒĢ£ ļ®ĖĻĘĀĒÜ©Ļ│╝ļź╝ ļ│┤ņØ┤ļ®░ 4ņĀ£ 6Ļ░£ņøö ņ╣śļŻīņØś ņä▒ņĀüņØ┤ ņ×ģņ”ØļÉśņŚłļŗż[22-24]. ĻĘĖ Ļ▓░Ļ│╝ļĪ£ INH/RIF/EMB/PZA 6Ļ░£ņøö 4ņĀ£ņÜöļ▓Ģ Ēś╣ņØĆ ņØ┤ņØś ļ│ĆĒśĢņØ┤ ņĀä ņäĖĻ│äņØś ņ┤łņ╣śļŻī Ēæ£ņżĆņ▓śļ░®ņ£╝ļĪ£ ĒÖĢļ”ĮļÉśņŚłĻ│Ā, ņØ┤Ēøä ņāłļĪ£ņÜ┤ ĒĢŁĻ▓░ĒĢĄņĢĮņĀ£ņØś Ļ░£ļ░£ņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā ņØ┤ ņ┤łņ╣śļŻīņÜöļ▓ĢņØĆ 1980ļģäļīĆ ņØ┤ļלļĪ£ 35ļģä ņØ┤ņāü ļ│ĆĒÖöĻ░Ć ņŚåņŚłļŗż(Fig. 1) [25]. ņØ┤ ĒÅÉĻ▓░ĒĢĄņŚÉ ļīĆĒĢ£ 6Ļ░£ņøö Ēæ£ņżĆ ņ╣śļŻīņØś ņÖäņ╣śņ£©ņØĆ 90-95%ļĪ£ ļåÆņ£╝ļ®░, ņ╣śļŻī 24Ļ░£ņøö Ēøä ņ×¼ļ░£ļźĀņØĆ 1-2%ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż.
Ļ░Éņłśņä▒ Ļ▓░ĒĢĄņØś ņ╣śļŻīņŚÉ ļīĆĒĢ┤ ņäĖĻ│äņĀüņ£╝ļĪ£ ĒåĄņÜ®ļÉśļŖö ņ¦äļŻīņ¦Ćņ╣©ņØĆ WHOņŚÉņä£ ņ¦Ćļé£ 2017ļģäņŚÉ ņĀ£ņĢłĒĢ£ ņ¦Ćņ╣©ņØ┤ ļ│┤ĒÄĖņĀüņØ┤ļŗż[26]. ņĄ£ņåī 6Ļ░£ņøöņØ┤ Ļ▒Ėļ”¼ļŖö 4ņĀ£ Ēæ£ņżĆ ņ╣śļŻīņØś ĻĖ░Ļ░äņØĆ ņĢäņ¦üĻ╣īņ¦Ć ļŗ©ņČĢļÉśņ¦Ć ļ¬╗ĒĢśĻ│Ā ņ׳ņ£╝ļ®░ ņןĻĖ░Ļ░äņØś ņ╣śļŻīļĪ£ ņØĖĒĢ£ ņ╣śļŻī ņł£ņØæļÅäņØś Ļ░ÉņåīļŖö Ļ▓░ĒĢĄ ņ╣śļŻīņØś Ļ░Ćņן Ēü░ ņןņĢĀļ¼╝ņØ┤ļŗż. ļö░ļØ╝ņä£ ņł£ņØæļÅäļź╝ ļåÆņØ┤ĻĖ░ ņ£äĒĢ┤ ņ¦üņĀæ Ļ┤Ćņ░░ĒĢś ļ│ĄņĢĮ ņ╣śļŻī(directly observed therapy, DOT) Ļ░£ļģÉņØ┤ ņäĖĻ│äņĀüņ£╝ļĪ£ ļäÉļ”¼ ņŖ╣ņØĖļÉśņŚłņ£╝ļ®░, ņØ┤ļź╝ ņÜ®ņØ┤ĒĢśĻ▓ī ĒĢśĻĖ░ ņ£äĒĢ┤ 4ņĀ£ Ļ│ĀņĀĢņÜ®ļ¤ē ļ│ĄĒĢ®ņĀ£(fixed dose combination, FDC)ņØś ņé¼ņÜ® ļ░Å ņŻ╝ 2-3ĒÜīņØś Ļ░äĒŚÉ ņ╣śļŻīņÜöļ▓ĢņØ┤ ņŗ£ļÅäļÉśņŚłĻ│Ā, ņØ┤ļź╝ ļ░öĒāĢņ£╝ļĪ£ Ļ░Éņłśņä▒ Ļ▓░ĒĢĄ Ēæ£ņżĆ ņ╣śļŻīņ¦Ćņ╣©ņØ┤ ļ¦īļōżņ¢┤ņĪīļŗż(Table 1) [26].
WHO ņ¦äļŻīņ¦Ćņ╣©ņŚÉ ļö░ļźĖ Ļ░Éņłśņä▒ Ļ▓░ĒĢĄ ņ┤łņ╣śļŻīņØś Ēæ£ņżĆņ▓śļ░®ņØĆ 2Ļ░£ņøöņØś ņ┤łĻĖ░ ņ¦æņżæ ņ╣śļŻīĻĖ░(initial intensive phase)ņÖĆ 4Ļ░£ņøöņØś ĒøäĻĖ░ ņ£Āņ¦Ć ņ╣śļŻīĻĖ░(maintenance phase)ļĪ£ ĻČīĻ│ĀĒĢ£ļŗż(2HREZ/4HR). 2010ļģä ņ¦äļŻīņ¦Ćņ╣©ņŚÉņä£ 2017ļģäņŚÉ ņāłļĪŁĻ▓ī ļ│ĆĻ▓ĮļÉ£ ļé┤ņÜ®ņØĆ ņŻ╝ 3ĒÜīņØś Ļ░äĒŚÉ ņ╣śļŻī ņÜ®ļ¤ēņØĆ ņ£Āņ¦Ć ņ╣śļŻīĻĖ░ ļ┐Éļ¦ī ņĢäļŗłļØ╝ ņ¦æņżæ ņ╣śļŻīĻĖ░ ļ¬©ļæÉņŚÉņä£ ĻČīĻ│ĀļÉśņ¦Ć ņĢŖņ£╝ļ®░, ĻĖ░ņĪ┤ņØś Ļ░£ļ│äņĢĮņĀ£ ņ▓śļ░®ļ│┤ļŗż ļ│ĄņÜ®ĒĢ┤ņĢ╝ ĒĢĀ ņĢĮņØś Ļ░£ņłśļź╝ ņżäņØĖ FDCņØś ņé¼ņÜ®ņØä ļŹö ĻČīĻ│ĀĒĢśņśĆļŗż. ļśÉĒĢ£, FQļź╝ ĒżĒĢ©ĒĢ£ 4Ļ░£ņøö ļŗ©ĻĖ░ņÜöļ▓ĢņØĆ ņĀłļīĆ ņé¼ņÜ®ĒĢ┤ņä£ļŖö ņĢł ļÉ£ļŗżĻ│Ā ĻČīĻ│ĀĒĢśņśĆļŗż. ĻĘĖ ļ░░Ļ▓Įņ£╝ļĪ£ļŖö 2013ļģä, 2014ļģäņŚÉ ļ│┤Ļ│ĀļÉ£ 4Ļ░£ņØś FQļź╝ ĒżĒĢ©ĒĢ£ 4Ļ░£ņøö ļŗ©ĻĖ░ņÜöļ▓ĢņŚÉ ļīĆĒĢ£ ļ¼┤ņ×æņ£ä ļīĆņĪ░ ņŚ░ĻĄ¼ņŚÉņä£ ļ¬©ļæÉ 4ņĀ£ 6Ļ░£ņøö Ēæ£ņżĆ ņ╣śļŻīņŚÉ ļīĆĒĢ£ ļ╣äņŚ┤ļō▒ņä▒ņØä ņ×ģņ”ØĒĢśņ¦Ć ļ¬╗ĒĢśņśĆĻ│Ā, ļŹö ļåÆņØĆ ņ×¼ļ░£ļźĀņØä ļ│┤ņśĆņ£╝ļ®░ ļČĆņ×æņÜ®ņØś ļ╣łļÅäļź╝ ņżäņØ┤ņ¦Ć ļ¬╗ĒĢśņśĆĻĖ░ ļĢīļ¼ĖņØ┤ļŗż[27-30]. ĻĘĖļ¤¼ļéś, 2021ļģä 6ņøö WHOņŚÉņä£ ļ░£Ēæ£ĒĢ£ ņŗĀņåŹ ĻĄÉņŗĀ(rapid communication)ņŚÉņä£ļŖö rifapentine (RPT)Ļ│╝ moxifloxacin (MFX)ņØä ņé¼ņÜ®ĒĢ£ 4Ļ░£ņøö ļŗ©ĻĖ░ņÜöļ▓ĢņØ┤ ĻĖ░ņĪ┤ 4ņĀ£ 6Ļ░£ņøöņÜöļ▓ĢņŚÉ ņŚ┤ļō▒ĒĢśņ¦Ć ņĢŖņĢä ĻĖ░ņĪ┤ ņ╣śļŻīņÜöļ▓ĢņØś ļīĆņĢłņØ┤ ļÉĀ ņłś ņ׳ļŗżĻ│Ā ņ¢ĖĻĖēĒĢśņŚ¼[31], ļ©Ėņ¦ĆņĢŖņĢä ņŚģļŹ░ņØ┤ĒŖĖļÉ£ WHO ņ¦äļŻīņ¦Ćņ╣©ņØ┤ ļéśņś¼Ļ▓āņ£╝ļĪ£ ĻĖ░ļīĆļÉ£ļŗż.
ĻĄŁļé┤ Ļ▓░ĒĢĄņ¦äļŻīņ¦Ćņ╣©ņŚÉņä£ļÅä Ļ░äĒŚÉ ņ╣śļŻīņÜöļ▓ĢņØĆ ĻČīņןĒĢśņ¦Ć ņĢŖņ£╝ļ®░ Ļ░Éņłśņä▒ Ļ▓░ĒĢĄ ņ┤łņ╣śļŻīņØś Ēæ£ņżĆņ▓śļ░®ņØĆ 2HREZ/4HR(E)ņØ┤Ļ│Ā, ņĢĮņĀ£ Ļ░Éņłśņä▒ Ļ▓░Ļ│╝ INH ļ░Å RIFņŚÉ Ļ░Éņłśņä▒ Ļ▓░ĒĢĄņ£╝ļĪ£ ĒÖĢņØĖļÉ£ Ļ▓ĮņÜ░ņŚÉļŖö ņ╣śļŻī 2Ļ░£ņøö ĒøäļČĆĒä░ EMBņØś ņżæļŗ©ņØä Ļ│ĀļĀżĒĢśļØ╝Ļ│Ā ĻČīĻ│ĀĒĢ£ļŗż[10]. ņĄ£ĻĘ╝ ĻĄŁļé┤ ņŚ░ĻĄ¼ņŚÉņä£ 1) ņ┤łĻĖ░ ņ¦æņżæ ņ╣śļŻīĻĖ░ļź╝ ļ¦łņ╣śĻĖ░ ņĀä GenoType MTBDRplus assay Ļ▓░Ļ│╝ņŚÉ ļö░ļØ╝ ņĪ░ĻĖ░ņŚÉ EMBļź╝ ņżæļŗ©ĒĢ£ ĻĄ░Ļ│╝ 2) ņ┤łĻĖ░ ņ¦æņżæ ņ╣śļŻīĻĖ░ ļÅÖņĢł EMBļź╝ ņ£Āņ¦ĆĒĢ£ ĻĄ░ņØś ņ╣śļŻī ņä▒Ļ│ĄļźĀĻ│╝ ņ×¼ļ░£ļźĀņØä ļ╣äĻĄÉĒĢ£ Ļ▓░Ļ│╝ GenoType MTBDRplus assay Ļ▓░Ļ│╝ņŚÉ ļö░ļźĖ EMBņØś ņĪ░ĻĖ░ ņżæļŗ©ņØ┤ ņ╣śļŻīņØś Ļ▓░Ļ│╝ņŚÉ ņśüĒ¢źņØä ļ»Ėņ╣śņ¦Ć ņĢŖņĢśļŗż[32]. ļö░ļØ╝ņä£ EMBņØś ņ╣śļŻī ĻĖ░Ļ░äņØä 2Ļ░£ņøö ļ»Ėļ¦īņ£╝ļĪ£ ļŗ©ņČĢĒĢĀ ņłś ņ׳ņØä Ļ░ĆļŖźņä▒ņØä ņĀ£ņŗ£ĒĢśņśĆļŗż. ļśÉĒĢ£, ņ╣śļŻī ņŗ£ņ×æ ņŗ£ ĒØēļČĆ XņäĀņŚÉņä£ Ļ│ĄļÅÖņØ┤ ņ׳Ļ│Ā, ņ╣śļŻī 2Ļ░£ņøö ņØ┤Ēøä ņŗ£Ē¢ēĒĢ£ Ļ░Øļŗ┤ ļ░░ņ¢æņØ┤ ņ¢æņä▒ņØĖ Ļ▓ĮņÜ░ņŚÉļŖö ņ£Āņ¦Ć ņ╣śļŻī ĻĖ░Ļ░äņØś ņŚ░ņןņØä Ļ│ĀļĀżĒĢĀ ņłś ņ׳ļŗżĻ│Ā ĻČīĻ│ĀĒĢ£ļŗż[10]. ĻĘĖ ĻĘ╝Ļ▒░ļĪ£ 2014ļģä ļ░£Ēæ£ļÉ£ ĻĄŁļé┤ ļŗ©ņØ╝ĻĖ░Ļ┤Ć ĒøäĒ¢źņĀü ņŚ░ĻĄ¼ Ļ▓░Ļ│╝ 1) ĒØēļČĆ XņäĀņŚÉņä£ Ļ│ĄļÅÖņØ┤ ņĪ┤ņ×¼, 2) 2Ļ░£ņøö ņ¦æņżæ ņ╣śļŻī Ēøä ņŗ£Ē¢ēĒĢ£ Ļ░Øļŗ┤ ļ░░ņ¢æ ņ¢æņä▒ņØ┤ ļÅÖņŗ£ņŚÉ ņĪ┤ņ×¼ĒĢśļŖö Ļ▓ĮņÜ░Ļ░Ć ņ╣śļŻī ņóģļŻī 1ļģä ņØ┤ļé┤ ņ×¼ļ░£ ņ£äĒŚśņØĖņ×ÉļĪ£ ĒÖĢņØĖļÉśņŚłĻĖ░ ļĢīļ¼ĖņØ┤ļéś, ņØ┤ ņŚ░ĻĄ¼ļŖö ņ×¼ļ░£ ĒÖśņ×ÉņłśĻ░Ć ļ¦Äņ¦Ć ņĢŖĻ│Ā(6ļ¬ģ), 3Ļ░£ņøö ņŚ░ņן ņ╣śļŻīņŚÉ ļīĆĒĢ£ Ļ▓░Ļ│╝Ļ░Ć ņŚåĻĖ░ ļĢīļ¼ĖņŚÉ ņ£Āņ¦Ć ņ╣śļŻī ĻĖ░Ļ░äņØś ņŚ░ņןņØä Ļ│ĀļĀżĒĢĀ ņłś ņ׳ļÉś, Ļ░£ļ│ä ĒÖśņ×ÉņØś ņāüĒÖ®ņØä Ļ░ÉņĢłĒĢśņŚ¼ ĒīÉļŗ©ĒĢśļÅäļĪØ ņ¢ĖĻĖēĒĢśņśĆļŗż[33].
ņ╣śļŻī ĻĖ░Ļ░äņØś ļŗ©ņČĢņØĆ Ļ▓░ĒĢĄ Ļ┤Ćļ”¼ņŚÉ ņ׳ņ¢┤ ņ╣śļŻī ņł£ņØæļÅäļź╝ ļåÆņØ┤Ļ│Ā ļČĆņ×æņÜ® ļ░£ņāØļźĀņØä ļé«ņČöĻ│Ā ņ╣śļŻī ļ╣äņÜ®ņØä ņĀłĻ░ÉĒĢĀ ņłś ņ׳ļŖö ļ¦żņÜ░ ņżæņÜöĒĢ£ ļ¬®Ēæ£ņØ┤ļŗż. 2009ļģäņŚÉ Ļ│ĄļÅÖņØ┤ ņŚåĻ│Ā ņ╣śļŻī 2Ļ░£ņøö Ēøä ņŗ£Ē¢ēĒĢ£ Ļ░Øļŗ┤ ļ░░ņ¢æ ņØīņä▒ņØĖ ĒÅÉĻ▓░ĒĢĄ ĒÖśņ×Éļź╝ ļīĆņāüņ£╝ļĪ£ HREZļĪ£ 2Ļ░£ņøö ņ¦æņżæ ņ╣śļŻī Ēøä HRļĪ£ ņ£Āņ¦Ć ņ╣śļŻīĻĖ░ļź╝ 2Ļ░£ņøöļĪ£ ļŗ©ņČĢĒĢśņŚ¼ ņ┤Ø 4Ļ░£ņøöĻ░ä ņ╣śļŻī ņóģļŻīĒĢ£ ĻĄ░ņØś 24Ļ░£ņøö Ēøä ņ×¼ļ░£ļźĀņØä 6Ļ░£ņøö Ēæ£ņżĆ ņ╣śļŻīĒĢ£ ĻĄ░Ļ│╝ ļ╣äĻĄÉĒĢ£ Ļ▓░Ļ│╝, 4Ļ░£ņøö ļŗ©ņČĢ ņ╣śļŻīĻĄ░ņŚÉņä£ ļåÆņØĆ ņ×¼ļ░£ļźĀņØ┤ Ļ┤Ćņ░░ļÉśņ¢┤(7.0% vs. 1.6%; risk difference 0.054; 95% confidence interval with Hauck-Anderson correction 0.01-0.10) ņŚ░ĻĄ¼Ļ░Ć ņĪ░ĻĖ░ ņóģļŻī ļÉśņŚłļŗż[34]. ļö░ļØ╝ņä£ ĒÜ©Ļ│╝ņĀüņ£╝ļĪ£ ņ╣śļŻī ĻĖ░Ļ░äņØä ļŗ©ņČĢņŗ£ĒéżĻĖ░ ņ£äĒĢ┤ņä£ļŖö ĻĖ░ņĪ┤ ņ╣śļŻīņÖĆ ņ░©ļ│äĒÖöļÉ£ ļ░®ļ▓ĢņØ┤ ĒĢäņÜöĒĢśņśĆņ£╝ļ®░ ņØ┤ļź╝ ņ£äĒĢ£ ņĄ£ĻĘ╝ņØś ļģĖļĀźņØĆ FQ Ēś╣ņØĆ ņŗĀņĢĮņØä ņé¼ņÜ®ĒĢśĻ▒░ļéś Ēśäņ×¼ ĻČīĻ│ĀņÜ®ļ¤ēļ│┤ļŗż Ļ│ĀņÜ®ļ¤ēņØś rifamycinņØä ņé¼ņÜ®ĒĢśļŖö ļŹ░ ņ┤łņĀÉņØä ļ¦×ņČöĻ│Ā ņ׳ļŗż.
2013-2014ļģäņŚÉ ļäż Ļ░£ņØś ļīĆĻĘ£ļ¬© ņ×äņāü ņŚ░ĻĄ¼Ļ░Ć FQļź╝ ĒżĒĢ©ĒĢśņŚ¼ 6Ļ░£ņøöņØś ņ╣śļŻī ĻĖ░Ļ░äņØä 4Ļ░£ņøöļĪ£ ļŗ©ņČĢĒĢśĻ│Āņ×É ĒĢśņśĆņ£╝ļéś FQ ĒżĒĢ©ĻĄ░ņŚÉņä£ ņ╣śļŻī 2Ļ░£ņøö Ēøä Ļ░Øļŗ┤ ļ░░ņ¢æ ņØīņĀäņ£©ņØ┤ ļŹö ļåÆņĢśņØīņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā ņ×¼ļ░£ļźĀņØ┤ ļåÆņĢä ļ¬©ļōĀ ņŚ░ĻĄ¼ņŚÉņä£ 6Ļ░£ņøö Ēæ£ņżĆ ņ╣śļŻīņŚÉ ļīĆĒĢ£ ļ╣äņŚ┤ļō▒ņä▒ņØä ņ×ģņ”ØĒĢśņ¦Ć ļ¬╗ĒĢśņśĆņ£╝ļ®░ ļČĆņ×æņÜ® ļ╣łļÅä ļ░Å ņé¼ļ¦ØļźĀņØś ņ░©ņØ┤ ņŚŁņŗ£ ļ│┤ņŚ¼ņŻ╝ņ¦Ć ļ¬╗ĒĢśņśĆļŗż[27-30]. 1) 2013ļģä ļ░£Ēæ£ļÉ£ ļ¼┤ņ×æņ£ä ļīĆņĪ░ĻĄ░ ņŚ░ĻĄ¼ņŚÉņä£ ņ¦æņżæ ņ╣śļŻīĻĖ░ ļĢī EMBļź╝ MFX 400 mg (2HRMZ/2HRM) Ēś╣ņØĆ gatifloxacin (GFX) 400 mg (2HRGZ/2HRG)ņ£╝ļĪ£ ļīĆņ▓┤ĒĢśĻ│Ā ņ£Āņ¦Ć ņ╣śļŻīĻĖ░ ļĢī FQļź╝ ņ£Āņ¦ĆĒĢśņŚ¼ ņŻ╝ 3ĒÜī ņ┤Ø 4Ļ░£ņøö ņ╣śļŻī Ēøä ļīĆņĪ░ĻĄ░(2HREZ/4HR)Ļ│╝ ļ░░ņ¢æņØīņĀäņ£©Ļ│╝ ņ×¼ļ░£ļźĀņØä ļ╣äĻĄÉĒĢ£ Ļ▓░Ļ│╝ ņ╣śļŻī Ēøä ņ×¼ļ░£ļźĀņØ┤ 6Ļ░£ņøö Ēæ£ņżĆ ņ╣śļŻīņØś 6%ņŚÉ ļ╣äĒĢśņŚ¼ GFXĻĄ░ņØ┤ 16%, MFXĻĄ░ņØ┤ 10%ļĪ£ ļŹö ļåÆņĢä ņŚ░ĻĄ¼Ļ░Ć ņĪ░ĻĖ░ ņóģļŻī ļÉśņŚłļŗż[27]. 2014ļģäņŚÉ New England Journal of Medicine (NEJM)ņŚÉ 6Ļ░£ņøö Ēæ£ņżĆ ņ╣śļŻīļź╝ ļīĆņĪ░ĻĄ░ņ£╝ļĪ£ FQ ĒżĒĢ© 4Ļ░£ņøö ļŗ©ĻĖ░ņÜöļ▓ĢņŚÉ ļīĆĒĢ£ 3Ļ░£ņØś ļīĆĻĘ£ļ¬© ļ¼┤ņ×æņ£ä ļīĆņĪ░ĻĄ░ ņŚ░ĻĄ¼Ļ░Ć ļ░£Ēæ£ļÉśņŚłņ£╝ļ®░, ļ©╝ņĀĆ 2) REMoxTB ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļīĆņĪ░ĻĄ░ Ēæ£ņżĆņ▓śļ░®ņŚÉņä£ EMBĻ░Ć MFXļĪ£ ļīĆņ▓┤ļÉ£ INHĻĄ░Ļ│╝ INHĻ░Ć MFXļĪ£ ļīĆņ▓┤ļÉ£ EMBĻĄ░ņ£╝ļĪ£ ļéśļłäņ¢┤ ņ┤Ø 17ņŻ╝Ļ░ä ņ╣śļŻīĒĢśņŚ¼ ļīĆņĪ░ĻĄ░(2HREZ/4HR), INHĻĄ░(2HRMZ/2HRM), EMBĻĄ░(2MREZ/2MR)ņØś ņäĖ ĻĄ░ņØä ļ╣äĻĄÉĒĢśņśĆļŗż. ņ╣śļŻī ņóģļŻī 12Ļ░£ņøö Ēøä ņ╣śļŻī ņŗżĒī© ļ░Å ņ×¼ļ░£ņØä ĒżĒĢ©ĒĢ£ 1ņ░© ĒÅēĻ░Ćļ│ĆņłśļŖö 4Ļ░£ņøö ļŗ©ņČĢ ņ╣śļŻīĻ░Ć 6Ļ░£ņøö Ēæ£ņżĆ ņ╣śļŻīņŚÉ ļīĆĒĢ£ ļ╣äņŚ┤ļō▒ņä▒ņØä ņ×ģņ”ØĒĢśņ¦Ć ļ¬╗ĒĢśņśĆņ£╝ļéś Ļ░Øļŗ┤ ņĢĪņ▓┤ ļ░Å Ļ│Āņ▓┤ļ░░ņ¦Ć ļ░░ņ¢æņŚÉņä£ ļ¬©ļæÉ ļŹö ļ╣ĀļźĖ ņØīņĀäņØä ļ│┤ņŚ¼ņŻ╝ņŚłļŗż. ņäĖ ĻĘĖļŻ╣ņŚÉņä£ 3, 4ļŗ©Ļ│ä ļČĆņ×æņÜ® ļ░£ņāØļźĀņØś ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļŖö ņŚåņŚłļŗż[28]. 3) OFLOTUB ņŚ░ĻĄ¼ļŖö ļīĆņĪ░ĻĄ░ Ēæ£ņżĆņ▓śļ░®(2HREZ/4HR)ņŚÉņä£ EMB ļīĆņŗĀ GFX 400 mg (2HRGZ/2HRG)ņ£╝ļĪ£ ļīĆņ▓┤ĒĢśĻ│Ā ņ┤Ø 4Ļ░£ņøöĻ░ä ņ╣śļŻīĒĢ£ ļÆż ļīĆņĪ░ĻĄ░Ļ│╝ ļ╣äĻĄÉĒĢśņśĆļŗż. ņ╣śļŻī ņóģļŻī 24Ļ░£ņøö Ēøä 1ņ░© ĒÅēĻ░Ćļ│ĆņłśļŖö ņ╣śļŻī ņŗżĒī©, ņ×¼ļ░£, ņé¼ļ¦Ø, ņżæļÅäĒāłļØĮņØä ĒżĒĢ©ĒĢśņśĆņ£╝ļ®░ ļ│Ė ņŚ░ĻĄ¼ ņŚŁņŗ£ ļīĆņĪ░ĻĄ░ņŚÉ ļ╣äĒĢ┤ ļ╣äņŚ┤ļō▒ņä▒ņØä ņ×ģņ”ØĒĢśņ¦Ć ļ¬╗ĒĢśņśĆļŗż[29]. 4) RIFAQUIN ņŚ░ĻĄ¼ļŖö ļīĆņĪ░ĻĄ░ Ēæ£ņżĆņ▓śļ░®(2HREZ/4HR)ņŚÉņä£ INH ļīĆņŗĀ MFXļĪ£ ļīĆņ▓┤ĒĢśņŚ¼ 2Ļ░£ņøö ņ¦æņżæ ņ╣śļŻīĻ░Ć ļüØļé£ ļÆż 4Ļ░£ņøöĻĄ░ņŚÉņä£ļŖö ņ£Āņ¦Ć ņ╣śļŻīĻĖ░ļź╝ RPT 900 mgĻ│╝ MFXļź╝ ņŻ╝ 2ĒÜīļĪ£ 2ļŗ¼Ļ░ä ņ£Āņ¦ĆĒĢśņŚ¼ ņ┤Ø 4Ļ░£ņøöĻ░ä ņ╣śļŻīĒĢśņśĆĻ│Ā 6Ļ░£ņøöĻĄ░ņŚÉņä£ļŖö ņ£Āņ¦Ć ņ╣śļŻīĻĖ░ļź╝ RPT 1,200 mgĻ│╝ MFXļź╝ ņŻ╝ 1ĒÜīļĪ£ 4Ļ░£ņøöĻ░ä ņ£Āņ¦ĆĒĢśņŚ¼ ņ┤Ø 6Ļ░£ņøöĻ░ä ņ╣śļŻīĒĢśņŚ¼ ļīĆņĪ░ĻĄ░(2HREZ/4HR), 4Ļ░£ņøöĻĄ░(2MREZ/2MPtwice weekly), 6Ļ░£ņøöĻĄ░(2MREZ/4MPonce weekly)ņØś ņäĖ ĻĄ░ņØä ļ╣äĻĄÉĒĢśņśĆļŗż. ņ╣śļŻī ņóģļŻī 12Ļ░£ņøö Ēøä 1ņ░© ĒÅēĻ░Ćļ│ĆņłśļŖö ņ╣śļŻī ņŗżĒī©, ņ×¼ļ░£, ņé¼ļ¦Ø, ņżæļÅäĒāłļØĮņØä ĒżĒĢ©ĒĢśņśĆņ£╝ļ®░, ļ│Ė ņŚ░ĻĄ¼ ņŚŁņŗ£ 4Ļ░£ņøöĻĄ░ņØĆ ļīĆņĪ░ĻĄ░ņŚÉ ļ╣äĒĢ┤ ļ╣äņŚ┤ļō▒ņä▒ņØä ņ×ģņ”ØĒĢśņ¦Ć ļ¬╗ĒĢśņśĆļŗż[30]. ĒĢśņ¦Ćļ¦ī Ļ│ĄļÅÖņØ┤ ņŚåļŖö ĒÅÉĻ▓░ĒĢĄ ĒÖśņ×Éļ¦ī ĒĢśņ£ä ĻĘĖļŻ╣ ļČäņäØņØä ņ¦äĒ¢ēĒĢśņśĆņØä ļĢīņØś ņ╣śļŻī ĒÜ©Ļ│╝ļŖö 6Ļ░£ņøö Ēæ£ņżĆ ņ╣śļŻīņŚÉ ļÆżņ¦Ćņ¦Ć ņĢŖņĢśļŗż[35]. ļśÉ ļŗżļźĖ ņŚ░ĻĄ¼ņŚÉņä£ ņ£äņØś ņŚ░ĻĄ¼ļź╝ ļ░öĒāĢņ£╝ļĪ£ patient-level pooled analysisļź╝ ņŗ£Ē¢ēĒĢ£ Ļ▓░Ļ│╝ Ļ░Øļŗ┤ ĒĢŁņé░ĻĘĀ ļÅäļ¦É < 2 + Ēś╣ņØĆ Ļ│ĄļÅÖņØ┤ ņŚåļŖö ļ»ĖņäĖļ│æļ│Ć(minimal disease)ņØä Ļ░Ćņ¦ä ĒÖśņ×ÉņŚÉņä£ļŖö 4Ļ░£ņøö ņ╣śļŻīĻ░Ć 6Ļ░£ņøö Ēæ£ņżĆ ņ╣śļŻīņŚÉ ļÆżņ¦Ćņ¦Ć ņĢŖļŖö Ļ▓āņØä ļ│┤ņŚ¼ņŻ╝ņŚłļŗż[36]. ņĢ×ņäĀ ļäż Ļ░Ćņ¦Ć ņ×äņāüņŗ£ĒŚśņØä ĒåĄĒĢ┤ FQļź╝ ĒżĒĢ©ĒĢ£ 4Ļ░£ņøö ļŗ©ĻĖ░ņÜöļ▓ĢņØĆ 2017ļģä WHO ņ¦äļŻīņ¦Ćņ╣©ņŚÉņä£ ņé¼ņÜ®ĒĢ┤ņä£ļŖö ņĢł ļÉśļŖö ņ╣śļŻīļ▓Ģņ£╝ļĪ£ ĻČīĻ│ĀļÉśņŚłļŗż. ĒĢśņ¦Ćļ¦ī ņĄ£ĻĘ╝ 2021ļģä 5ņøö NEJMņŚÉ ņāłļĪ£ņÜ┤ ļ¼┤ņ×æņ£ä ļīĆņĪ░ĻĄ░ ņŚ░ĻĄ¼Ļ░Ć ļ░£Ēæ£ļÉśņ¢┤ WHO ņ¦äļŻīņ¦Ćņ╣©ņØś ļ│ĆĒÖöļź╝ ņśłĻ│ĀĒĢśņśĆļŗż. Study 31/A5349 ņŚ░ĻĄ¼ļŖö ļīĆņĪ░ĻĄ░ Ēæ£ņżĆņ▓śļ░®(2HREZ/4HR)ņŚÉņä£ RIFļź╝ RPT (1,200 mg, once-daily)ļĪ£ ļīĆņ▓┤ĒĢśņŚ¼ 2Ļ░£ņøö ņ¦æņżæ ņ╣śļŻī Ēøä 2Ļ░£ņøö ņ£Āņ¦Ć ņ╣śļŻīļź╝ ļ¦łņ╣£ RPTĻĄ░(2HPZE/2HP)Ļ│╝ RIFļź╝ RPTļĪ£ ļīĆņ▓┤ĒĢśĻ│Ā EMBļź╝ MFX 400 mgņ£╝ļĪ£ ļīĆņ▓┤ĒĢśņŚ¼ 2Ļ░£ņøö ņ¦æņżæ ņ╣śļŻīņÖĆ 2Ļ░£ņøö ņ£Āņ¦Ć ņ╣śļŻīĻ╣īņ¦Ć MFXļź╝ ņ£Āņ¦ĆĒĢ£ RPT/MFXĻĄ░(2HPZM/2HPM)ņ£╝ļĪ£ ļéśļłäņ¢┤ ņäĖ ĻĄ░ņØä ļ╣äĻĄÉĒĢśņśĆļŗż. ņ╣śļŻī ņóģļŻī 6Ļ░£ņøö Ēøä 1ņ░© ĒÅēĻ░Ćļ│ĆņłśļŖö ņ╣śļŻī ņŗżĒī©, ņ×¼ļ░£, ņé¼ļ¦Ø, ņżæļÅäĒāłļØĮņØä ĒżĒĢ©ĒĢśņśĆņ£╝ļ®░ RPTĻĄ░ņŚÉņä£ļŖö ļ╣äņŚ┤ļō▒ņä▒ņØä ņ×ģņ”ØĒĢśņ¦Ć ļ¬╗ĒĢśņśĆņ£╝ļéś RPT/MFXĻĄ░ņŚÉņä£ļŖö ļ╣äņŚ┤ļō▒ņä▒ņØ┤ ņ×ģņ”ØļÉśņŚłļŗż[37]. ļö░ļØ╝ņä£ ņØ┤ ņŚ░ĻĄ¼ņØś Ļ▓░Ļ│╝ļź╝ ļ░öĒāĢņ£╝ļĪ£ 2021ļģä 6ņøö WHOņŚÉņä£ RPT/MFX 4Ļ░£ņøö ļŗ©ĻĖ░ņÜöļ▓ĢņŚÉ ļīĆĒĢ£ rapid communicationņØä ļ░£Ēæ£ĒĢśņśĆņ£╝ļ®░ ĻĘ╝ņŗ£ņØ╝ ļé┤ņŚÉ RPT/MFX 4Ļ░£ņøö ļŗ©ĻĖ░ņÜöļ▓ĢņØ┤ ĻĖ░ņĪ┤ Ēæ£ņżĆ ņ╣śļŻīņØś ļīĆņĢłņØ┤ ļÉĀ ņłś ņ׳ļŗżļŖö WHO ņ¦äļŻīņ¦Ćņ╣©ņØś Ļ░£ņĀĢņØ┤ Ēśäņ×¼ ņśłĻ│ĀļÉ£ ņāüĒā£ņØ┤ļŗż(Table 2).
RPTļŖö rifamycin Ļ│äĒåĄņØś ņĢĮļ¼╝ļĪ£ RIFņÖĆ ĒĢŁĻ▓░ĒĢĄĒÜ©Ļ│╝ļŖö ņ£Āņé¼ĒĢśļŗżĻ│Ā ņĢīļĀżņĀĖ ņ׳ņ£╝ļéś ļ░śĻ░ÉĻĖ░Ļ░Ć ĻĖĖņ¢┤ ņŻ╝ 1ĒÜī ļ│ĄņÜ®ņØ┤ Ļ░ĆļŖźĒĢ£ ņĢĮņĀ£ņØ┤ļŗż. ņØ┤ļ¤¼ĒĢ£ ņןņĀÉņ£╝ļĪ£ RPTļŖö ņ×Āļ│ĄĻ▓░ĒĢĄ ņ╣śļŻīņŚÉņä£ ĒÜŹĻĖ░ņĀüņ£╝ļĪ£ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŖö ņĢĮņĀ£ļĪ£ņä£ 2011ļģä ļ¦ÉņŚÉ WHOņŚÉņä£ļŖö INH/RPT 3Ļ░£ņøö Ļ░äĒŚÉņÜöļ▓Ģ(ņŻ╝ 1ĒÜī, ņ┤Ø 12ņŻ╝)ņØä ņ×Āļ│ĄĻ▓░ĒĢĄĻ░ÉņŚ╝ ņ╣śļŻīņØś ņāłļĪ£ņÜ┤ ņÜöļ▓Ģņ£╝ļĪ£ ĻČīĻ│ĀĒĢśņśĆĻ│Ā Ēśäņ×¼ ĒĢ┤ņÖĖņŚÉņä£ļŖö ĒÖ£ļ░£Ē׳ ņé¼ņÜ® ņżæņØ┤ļŗż. ĻĄŁļé┤ņŚÉļŖö 2016ļģä ļ¦ÉņŚÉ ĻĖ┤ĻĖē ļÅäņ×ģļÉśņ¢┤ ņĀ£ĒĢ£ļÉ£ ļ│æ┬ĘņØśņøÉ ņØśļŻīņ¦äņØś ņ×Āļ│ĄĻ▓░ĒĢĄĻ░ÉņŚ╝ ņ╣śļŻīņŚÉ ņé¼ņÜ®ļÉśņŚłņ£╝ļéś, ņŚ░ĻĄ¼ Ļ▓░Ļ│╝ ņĢĮļ¼╝ ļ│ĄņÜ®ņÖäļŻīņ£©ņØĆ INH/RPT Ļ░äĒŚÉņÜöļ▓ĢņØ┤ 3Ļ░£ņøö INH/RIF ļ│æĒĢ®ņÜöļ▓Ģ(ļ¦żņØ╝)ņŚÉ ļ╣äĒĢśņŚ¼ ļåÆņĢśņ£╝ļéś(92.9% vs. 86.7%, p=0.036), ļČĆņ×æņÜ®ņØś ļ╣łļÅä(ĒŖ╣Ē׳ ļÅģĻ░Éņ¢æ ņ”ØĒøäĻĄ░ 19.0%, ņĢäļéśĒĢäļØĮņŗ£ņŖż 1.8%)Ļ░Ć INH/RPT Ļ░äĒŚÉņÜöļ▓ĢņŚÉņä£ ĒśäņĀĆĒ׳ ļåÆĻ▓ī ĒÖĢņØĖļÉśņ¢┤(75.2% vs. 56.7%, p<0.001) ņŚ░ĻĄ¼Ļ░Ć ņżæļŗ©ļÉśņŚłļŗż. ļö░ļØ╝ņä£ Ēśäņ×¼ ĻĄŁļé┤ņŚÉņä£ļŖö RPTņØś ņé¼ņÜ®ņØĆ ļČłĻ░ĆļŖźĒĢ£ ņāüĒā£ņØ┤ļŗż[38].
ņ£äņÖĆ Ļ░ÖņØ┤ FQļź╝ ņé¼ņÜ®ĒĢ£ ņŚ░ĻĄ¼ ļ┐Éļ¦ī ņĢäļŗłļØ╝ Ēśäņ×¼ ĻČīĻ│ĀņÜ®ļ¤ēļ│┤ļŗż Ļ│ĀņÜ®ļ¤ēņØś rifamycinņØä ņé¼ņÜ®ĒĢśĻ▒░ļéś ņŗĀņĢĮņØä ņé¼ņÜ®ĒĢśņŚ¼ ņ╣śļŻī ĻĖ░Ļ░äņØä ļŗ©ņČĢņŗ£ĒéżļĀżļŖö ņŚ░ĻĄ¼ ņŚŁņŗ£ ņ¦äĒ¢ēļÉśĻ│Ā ņ׳ļŗż[39]. ĻĘĖņżæ ĒĢśļéśĻ░Ć RIFASHORT ņŚ░ĻĄ¼ļĪ£ RIF 600 mg 6Ļ░£ņøö ņ╣śļŻī(2HREZ/4HR)ņÖĆ RIF 1,200 mg (2HREZ/2HR1,200 mg), RIF 1,800 mg (2HREZ/2HR1,800 mg)ņ£╝ļĪ£ ļīĆņ▓┤ĒĢśņŚ¼ ņ┤Ø 4Ļ░£ņøöĻ░ä ņ╣śļŻīĒĢśņŚ¼ ņäĖĻĄ░ņØä ļ╣äĻĄÉĒĢśļŖö ņŚ░ĻĄ¼ņØ┤ļŗż. ļśÉ ļŗżļźĖ ņŚ░ĻĄ¼ļĪ£ļŖö ņāłļĪ£ņÜ┤ ņŚ░ĻĄ¼ņäżĻ│äļ▓ĢņØĖ multi-arm, multi-stage (MAMS) ņäżĻ│äļ░®ņŗØņØä ļÅäņ×ģĒĢ£ TRUNCATE-TB ņŚ░ĻĄ¼Ļ░Ć ņ׳ļŗż. ņØ┤ ņŚ░ĻĄ¼ļŖö ņĢĮņĀ£ņØś ņłśĻ░Ć ņĀ£ĒĢ£ņĀüņØ┤Ļ│Ā, Ļ▓░ĒĢĄ ĒÖśņ×ÉņØś ņłśĻ░Ć ļ¦ÄņĢśļŹś Ļ│╝Ļ▒░ņŚÉ ļ╣äĒĢ┤ Ēśäņ×¼ņØś ĒĢ£ņĀĢļÉ£ ņ×ÉņøÉņØä ņĄ£ņĀüĒÖöĒĢśņŚ¼ ņ×äņāü ņŚ░ĻĄ¼ ņä▒Ļ│Ą Ļ░ĆļŖźņä▒ņØä ļåÆņØ┤ĻĖ░ ņ£äĒĢ┤ ņāłļĪ£ņÜ┤ ņŚ░ĻĄ¼ ļ░®ļ▓ĢņØä ņé¼ņÜ®ĒĢśņśĆļŗż. TRUNCATE-TB ņŚ░ĻĄ¼ļŖö Arm1ļĪ£ RIF 10 mg/kgņØĖ Ēæ£ņżĆ 6Ļ░£ņøö ņ╣śļŻī(2HREZ/4HR)ņÖĆ Arm2ļĪ£ Ēæ£ņżĆ ņ▓śļ░®ņŚÉ RIF 35 mg/kgņ£╝ļĪ£ ņ”Øļ¤ē + linezolidļź╝ ņČöĻ░Ć(2HR35ZELi), Arm3ļĪ£ Ēæ£ņżĆņ▓śļ░®ņŚÉ RIF 35 mg/kgņ£╝ļĪ£ ņ”Øļ¤ē + clofazimineņØä ņČöĻ░Ć(2HR35ZEC), Arm4ļĪ£ Ēæ£ņżĆņ▓śļ░®ņŚÉ EMB ļīĆņŗĀ linezolidņÖĆ levofloxacinņØä ņČöĻ░Ć(2HPZLiLe), Arm5ļĪ£ Ēæ£ņżĆņ▓śļ░®ņŚÉ RIF ļīĆņŗĀ linezolidņÖĆ bedaquilineņØä ņČöĻ░Ć(2HZELiB)ĒĢśļŖö 5ĻĄ░ņ£╝ļĪ£ ņŚ░ĻĄ¼ļź╝ ņŗ£ņ×æĒĢśņŚ¼ 2Ļ░£ņøö ĻĖ░ņżĆņ£╝ļĪ£ ņżæĻ░ä ļČäņäØņØä ņŗ£Ē¢ē, ņ┤łĻĖ░ ņżæĻ░ä Ļ▓░Ļ│╝ņŚÉņä£ ņČ®ļČäĒĢ£ ĒÜ©Ļ│╝ļź╝ ļ│┤ņØ┤ņ¦Ć ļ¬╗ĒĢ£ ĻĄ░ņØĆ ņł£ņ░©ņĀüņ£╝ļĪ£ ļ¬©ņ¦æņØä ņżæļŗ©ĒĢśĻ│Ā ļīĆņĪ░ĻĄ░Ļ│╝ Ļ░ĆļŖźņä▒ņØ┤ ļ│┤ņØ┤ļŖö ĻĄ░ņØĆ ļüØĻ╣īņ¦Ć ļ¬©ņ¦æņØä ņ£Āņ¦ĆĒĢśļŖö ļ░®ļ▓Ģņ£╝ļĪ£ Ēśäņ×¼ ņŚ░ĻĄ¼Ļ░Ć ņ¦äĒ¢ē ņżæņØ┤ļŗż.
ņĄ£ĻĘ╝ņŚÉļŖö Ļ│╝Ļ▒░ņŚÉ ņĢĮņĀ£Ļ░Éņłśņä▒ Ļ▓░ĒĢĄņØĆ 1ņ░© ņĢĮņĀ£, ņĢĮņĀ£ļé┤ņä▒ Ļ▓░ĒĢĄņØĆ 2ņ░© ņĢĮņĀ£ļĪ£ ņ╣śļŻīĒĢśļŹś ĻĖ░ņĪ┤ ņøÉņ╣ÖņŚÉņä£ ļ▓Śņ¢┤ļéś Ļ░Éņłśņä▒ Ļ▓░ĒĢĄ ļ░Å ņĢĮņĀ£ļé┤ņä▒Ļ▓░ĒĢĄņØä ĻĄ¼ļ│äĒĢśņ¦Ć ņĢŖĻ│Ā ļ¬©ļæÉ ņ╣śļŻīĒĢĀ ņłś ņ׳ļŖö PAN-TB regimenņŚÉ ļīĆĒĢ£ Ļ░£ļ░£ļÅä ĒÖ£ļ░£ĒĢśļŗż. ĻĘĖ ņśłļĪ£ Simplici TB ņŚ░ĻĄ¼ļŖö Arm1ļĪ£ Ēæ£ņżĆ 6Ļ░£ņøö ņ╣śļŻī(2HREZ/4HR)ļź╝ ļīĆņĪ░ĻĄ░ņ£╝ļĪ£ Arm2ļŖö ņĢĮņĀ£Ļ░Éņłśņä▒ Ļ▓░ĒĢĄņØä ļīĆņāüņ£╝ļĪ£ ņ¦æņżæ ņ╣śļŻīĻĖ░ņŚÉļŖö bedaquiline 200 mg, protomanid, MFX, PZA (2B200PaMZ)ļź╝ 2Ļ░£ņøöĻ░ä ņé¼ņÜ®ĒĢśĻ│Ā ņ£Āņ¦Ć ņ╣śļŻīĻĖ░ļŖö Ļ░ÖņØĆ ņĢĮņĀ£ņĪ░ĒĢ®ņ£╝ļĪ£ ĒĢśļÉś bedaquilineņØä 100 mgņ£╝ļĪ£ Ļ░Éļ¤ē(2B100PaMZ)ĒĢśņŚ¼ 2Ļ░£ņøöĻ░ä ņ╣śļŻīĒĢśņŚ¼ ņ┤Ø 4Ļ░£ņøö ņ╣śļŻīĻĄ░ņØ┤ļ®░, Arm3ļŖö ļŗżņĀ£ļé┤ņä▒ Ļ▓░ĒĢĄņØä ļīĆņāüņ£╝ļĪ£ ņ¦æņżæ ņ╣śļŻīĻĖ░ļŖö Arm2ņÖĆ ļÅÖņØ╝(2B200PaMZ)ĒĢśĻ│Ā ņ£Āņ¦Ć ņ╣śļŻīĻĖ░ļź╝ Arm2ņØś 2Ļ░£ņøöņŚÉņä£ 4Ļ░£ņøöļĪ£ ņŚ░ņן(4B100PaMZ)ņŗ£ņ╝£ ņ┤Ø 6Ļ░£ņøö ņ╣śļŻīĻĄ░, ņØ┤ļĀćĻ▓ī ņäĖ ĻĄ░ņ£╝ļĪ£ ļéśļłäņ¢┤ Ēśäņ×¼ ņŚ░ĻĄ¼Ļ░Ć ņ¦äĒ¢ē ņżæņØ┤ļŗż. ĻĘĖ ļ░¢ņŚÉ ņŚ¼ļ¤¼ ņŚ░ĻĄ¼ļōżņØ┤ ņ╣śļŻī ĻĖ░Ļ░ä ļŗ©ņČĢņØä ņ£äĒĢ┤ ņ¦äĒ¢ē ņżæņŚÉ ņ׳ļŗż[39].
ļ╣Āļź┤Ļ▓ī ļ│ĆĒĢśļŖö ļŗżņĀ£ļé┤ņä▒ Ļ▓░ĒĢĄņØś ņ╣śļŻīņŚÉ ļ╣äĒĢ┤ Ļ░Éņłśņä▒ Ļ▓░ĒĢĄņØś ņ╣śļŻīļŖö 35ļģäĻ░ä Ēü░ ļ│ĆĒÖöĻ░Ć ņŚåņØ┤ ņ£Āņ¦ĆļÉśņŚłĻ│Ā, 6Ļ░£ņøöņØ┤ļØ╝ļŖö ĻĖ┤ ņ╣śļŻī ĻĖ░Ļ░äĻ│╝ ņØ┤ļĪ£ ņØĖĒĢ£ ļČĆņ×æņÜ® ņ”ØĻ░Ć ļ░Å ņĢĮņĀ£ņł£ņØæļÅä Ļ░Éņåī ļō▒ņØś ļ¼ĖņĀ£ņÖĆ ņØ┤ļź╝ ĒĢ┤Ļ▓░ĒĢśĻĖ░ ņ£äĒĢ£ ļ¦ÄņØĆ ļģĖļĀźņØ┤ ņ׳ņ¢┤ ņÖöļŗż. Ēśäņ×¼ Ļ░Éņłśņä▒ Ļ▓░ĒĢĄņØś ņ¦äļŻīņ¦Ćņ╣©ņØĆ ĒöäļĪ£ĻĘĖļש ņżæņŗ¼ņĀüņØ┤Ļ│Ā, ļŗ©ņł£ĒĢśļ®░ ļ¬©ļōĀ ĒÖśņ×ÉņŚÉ ņØ╝ļźĀņĀüņØĖ ŌĆśone-size-fits-allŌĆÖ 6Ļ░£ņøö Ēæ£ņżĆ ņ╣śļŻīļĪ£ņŹ© ņØ╝ļČĆņØś ĒÖśņ×ÉņŚÉĻ▓īļŖö ĒĢäņÜöĒĢ£ Ļ▓āļ│┤ļŗż ĻĖ┤ ņ╣śļŻīļØ╝ļŖö Ļ▓āņØĆ ļČäļ¬ģĒĢśļŗż. ĻĖ┤ ņäĖņøö ļÅÖņĢł ņ╣śļŻī ĻĖ░Ļ░äņØä 4Ļ░£ņøöļĪ£ ļŗ©ņČĢņŗ£ņ╝£ļ│┤ļĀżļŖö ņŚ¼ļ¤¼ ņŚ░ĻĄ¼Ļ░Ć ļīĆļČĆļČä ņŗżĒī©ļĪ£ ļÅīņĢäĻ░öņ£╝ļéś ņĄ£ĻĘ╝ņŚÉ ļ░£Ēæ£ļÉ£ Study 31/A5349 ņŚ░ĻĄ¼ Ļ▓░Ļ│╝ RPTņÖĆ MFXļź╝ ņé¼ņÜ®ĒĢ£ 4Ļ░£ņøö ļŗ©ĻĖ░ ņÜöļ▓ĢņØ┤ ĻĖ░ņĪ┤ 4ņĀ£ 6Ļ░£ņøöņÜöļ▓ĢņŚÉ ņŚ┤ļō▒ĒĢśņ¦Ć ņĢŖļŗżļŖö Ļ▓āņØ┤ ĒÖĢņØĖļÉśņ¢┤ ĻĘ╝ņŗ£ņØ╝ ļé┤ņŚÉ RPT/MFX 4Ļ░£ņøö ļŗ©ĻĖ░ņÜöļ▓ĢņØ┤ ĻĖ░ņĪ┤ Ēæ£ņżĆ ņ╣śļŻīņØś ļīĆņĢłņØ┤ ļÉĀ ņłś ņ׳ļŗżļŖö WHO ņ¦äļŻīņ¦Ćņ╣©ņØś Ļ░£ņĀĢņØ┤ Ēśäņ×¼ ņśłĻ│ĀļÉ£ ņāüĒā£ņØ┤ļŗż. ĒĢśņ¦Ćļ¦ī RPTĻ░Ć ļåÆņØĆ ļ╣łļÅäņØś ļČĆņ×æņÜ®ņ£╝ļĪ£ ņØĖĒĢ┤ Ēśäņ×¼ ĻĄŁļé┤ņŚÉņä£ļŖö ņé¼ņÜ®ņØ┤ ņĀ£ĒĢ£ņĀüņØĖ ņāüĒÖ®ņ£╝ļĪ£ ĻĄŁļé┤ņŚÉņä£ RPT/MFX 4Ļ░£ņøö ļŗ©ĻĖ░ņÜöļ▓ĢņØ┤ ļ░öļĪ£ ņĀüņÜ®ļÉśĻĖ░ļŖö ņ¢┤ļĀżņÜĖ Ļ▓āņ£╝ļĪ£ ļ│┤ņØĖļŗż.
REFERENCES
1. Diagnostic standards and classification of tuberculosis in adults and children. This official statement of the American Thoracic Society and the Centers for Disease Control and Prevention was adopted by the ATS Board of Directors, July 1999. This statement was endorsed by the Council of the Infectious Disease Society of America, September 1999. Am J Respir Crit Care Med 2000;161:1376ŌĆō1395.


2. Park YS, Lee CH, Lee SM, et al. Rapid increase of non-tuberculous mycobacterial lung diseases at a tertiary referral hospital in South Korea. Int J Tuberc Lung Dis 2010;14:1069ŌĆō1071.

3. Kanchana MV, Cheke D, Natyshak I, Connor B, Warner A, Martin T. Evaluation of the BACTEC MGIT 960 system for the recovery of mycobacteria. Diagn Microbiol Infect Dis 2000;37:31ŌĆō36.


4. Centers for Disease Control and Prevention (CDC). Updated guidelines for the use of nucleic acid amplification tests in the diagnosis of tuberculosis. MMWR Morb Mortal Wkly Rep 2009;58:7ŌĆō10.


5. MacLean E, Kohli M, Weber SF, et al. Advances in molecular diagnosis of tuberculosis. J Clin Microbiol 2020;58:e01582ŌĆō19.



6. Joint Committee for the Revision of Korean Guidelines for Tuberculosis Korea Centers for Disease Control and Prevention. Korean guidelines for tuberculosis. Seoul: The Korean Academy of Tuberculosis and Respiratory Diseases, 2011.
7. Joint Committee for the Revision of Korean Guidelines for Tuberculosis Korea Centers for Disease Control and Prevention. Korean guidelines for tuberculosis. 3rd ed. Seoul: The Korean Academy of Tuberculosis and Respiratory Diseases, 2017.
8. Boehme CC, Nabeta P, Hillemann D, et al. Rapid molecular detection of tuberculosis and rifampin resistance. N Engl J Med 2010;363:1005ŌĆō1015.



9. Joint Committee for the Revision of Korean Guidelines for Tuberculosis Korea Centers for Disease Control and Prevention. Korean guidelines for tuberculosis. 2nd ed. Seoul: The Korean Academy of Tuberculosis and Respiratory Diseases, 2014.
10. Joint Committee for the Revision of Korean Guidelines for Tuberculosis Korea Centers for Disease Control and Prevention. Korean guidelines for tuberculosis. 4th ed. Seoul: The Korean Academy of Tuberculosis and Respiratory Diseases, 2020.
11. Steingart KR, Schiller I, Horne DJ, Pai M, Boehme CC, Dendukuri N. Xpert® MTB/RIF assay for pulmonary tuberculosis and rifampicin resistance in adults. Cochrane Database Syst Rev 2014;2014:CD009593.


12. Zifodya JS, Kreniske JS, Schiller I, et al. Xpert Ultra versus Xpert MTB/RIF for pulmonary tuberculosis and rifampicin resistance in adults with presumptive pulmonary tuberculosis. Cochrane Database Syst Rev 2021;2:CD009593.


13. Ramaswamy S, Musser JM. Molecular genetic basis of antimicrobial agent resistance in Mycobacterium tuberculosis: 1998 update. Tuber Lung Dis 1998;79:3ŌĆō29.


14. Bai Y, Wang Y, Shao C, Hao Y, Jin Y. GenoType MTBDRplus assay for rapid detection of multidrug resistance in mycobacterium tuberculosis: a meta-analysis. PLoS One 2016;11:e0150321.



15. Mao X, Ke Z, Shi X, et al. Diagnosis of drug resistance to fluoroquinolones, amikacin, capreomycin, kanamycin and ethambutol with genotype MTBDRsl assay: a meta-analysis. Ann Clin Lab Sci 2015;45:533ŌĆō544.

16. Kang SM, Lee JG, Chung JH, et al. Delayed treatment of pulmonary tuberculosis in a university hospital. Tuberc Respir Dis 2006;60:277ŌĆō284.

17. Song JK, Ahn HJ, Kim YA. Critical value report: survey and literature review. J Lab Med Qual Assur 2017;39:31ŌĆō41.

18. Treatment of pulmonary tuberculosis with streptomycin and para-aminosalicylic acid; a Medical Research Council investigation. Br Med J 1950;2:1073ŌĆō1085.



19. Various combinations of isoniazid with streptomycin or with P.A.S. in the treatment of pulmonary tuberculosis; seventh report to the Medical Research Council by their Tuberculosis Chemotherapy Trials Committee. Br Med J 1955;1:435ŌĆō445.


20. Doster B, Murray FJ, Newman R, Woolpert SF. Ethambutol in the initial treatment of pulmonary tuberculosis. U.S. Public Health Service tuberculosis therapy trials. Am Rev Respir Dis 1973;107:177ŌĆō190.

21. Controlled clinical trial of four 6-month regimens of chemotherapy for pulmonary tuberculosis. Second report. Second East African/British Medical Research Council Study. Am Rev Respir Dis 1976;114:471ŌĆō475.

22. Controlled trial of 6-month and 8-month regimens in the treatment of pulmonary tuberculosis: the results up to 24 months. Am Rev Respir Dis 1976;114:471ŌĆō475.

23. Controlled trial of 4 three-times-weekly regimens and a daily regimen all given for 6 months for pulmonary tuberculosis. Second report: the results up to 24 months. Hong Kong Chest Service/British Medical Research Council. Tubercle 1982;63:89ŌĆō98.


24. Long-term follow-up of a clinical trial of six-month and four-month regimens of chemotherapy in the treatment of pulmonary tuberculosis. Singapore Tuberculosis Service/British Medical Research Council. Am Rev Respir Dis 1986;133:779ŌĆō783.

25. Iseman MD. Tuberculosis therapy: past, present and future. Eur Respir J Suppl 2002;36:87sŌĆō94s.


26. World Health Organization. Guidelines for treatment of drug-susceptible tuberculosis and patient care: 2017 update [Internet]. Geneva: WHO, c2017. [cited 2021 Jul 20]. Available from: https://apps.who.int/iris/bitstream/handle/10665/255052/9789241550000-eng.pdf
27. Jawahar MS, Banurekha VV, Paramasivan CN, et al. Randomized clinical trial of thrice-weekly 4-month moxifloxacin or gatifloxacin containing regimens in the treatment of new sputum positive pulmonary tuberculosis patients. PLoS One 2013;8:e67030.



28. Gillespie SH, Crook AM, McHugh TD, et al. Four-month moxifloxacin-based regimens for drug-sensitive tuberculosis. N Engl J Med 2014;371:1577ŌĆō1587.



29. Merle CS, Fielding K, Sow OB, et al. A four-month gatifloxacin-containing regimen for treating tuberculosis. N Engl J Med 2014;371:1588ŌĆō1598.


30. Jindani A, Harrison TS, Nunn AJ, et al. High-dose rifapentine with moxifloxacin for pulmonary tuberculosis. N Engl J Med 2014;371:1599ŌĆō1608.



31. World Health Organization. Treatment of drug-susceptible tuberculosis: rapid communication [Internet]. Geneva: WHO, c2021. [cited 2021 Jul 20]. Available from: https://apps.-who.int/iris/bitstream/handle/10665/341729/9789240028678-eng.pdf?sequence=1
32. Jo KW, Kim M, Kim YJ, et al. Early discontinuation of ethambutol in pulmonary tuberculosis treatment based on results of the GenoType MTBDRplus assay: a prospective, multicenter, non-inferiority randomized trial in South Korea. Antimicrob Agents Chemother 2019;63:e00980ŌĆō19.


33. Jo KW, Yoo JW, Hong Y, et al. Risk factors for 1-year relapse of pulmonary tuberculosis treated with a 6-month daily regimen. Respir Med 2014;108:654ŌĆō659.


34. Johnson JL, Hadad DJ, Dietze R, et al. Shortening treatment in adults with noncavitary tuberculosis and 2-month culture conversion. Am J Respir Crit Care Med 2009;180:558ŌĆō563.



35. Alipanah N, Cattamanchi A, Menzies R, Hopewell PC, Chaisson RE, Nahid P. Treatment of non-cavitary pulmonary tuberculosis with shortened fluoroquinolone-based regimens: a meta-analysis. Int J Tuberc Lung Dis 2016;20:1522ŌĆō1528.


36. Imperial MZ, Nahid P, Phillips PPJ, et al. A patient-level pooled analysis of treatment-shortening regimens for drug-susceptible pulmonary tuberculosis. Nat Med 2018;24:1708ŌĆō1715.



37. Dorman SE, Nahid P, Kurbatova EV, et al. Four-month rifapentine regimens with or without moxifloxacin for tuberculosis. N Engl J Med 2021;384:1705ŌĆō1718.


38. Jo KW, Kim JS, Kwon HS, et al. Adverse event and treatment completion rates of a 12-dose weekly isoniazid and rifapentine course for South Korean healthcare workers. Respir Med 2019;158:42ŌĆō48.


Landmarks in pulmonary tuberculosis therapy. INH, isoniazid; PAS, para-aminosalicylic acid; SM, streptomycin; EMB, ethambutol; RIF, rifampicin; PZA, pyrazinamide; H, isoniazid; R, rifampicin; Z, pyrazinamide; E, ethambutol; P, rifapentine; M, moxifloxacin.
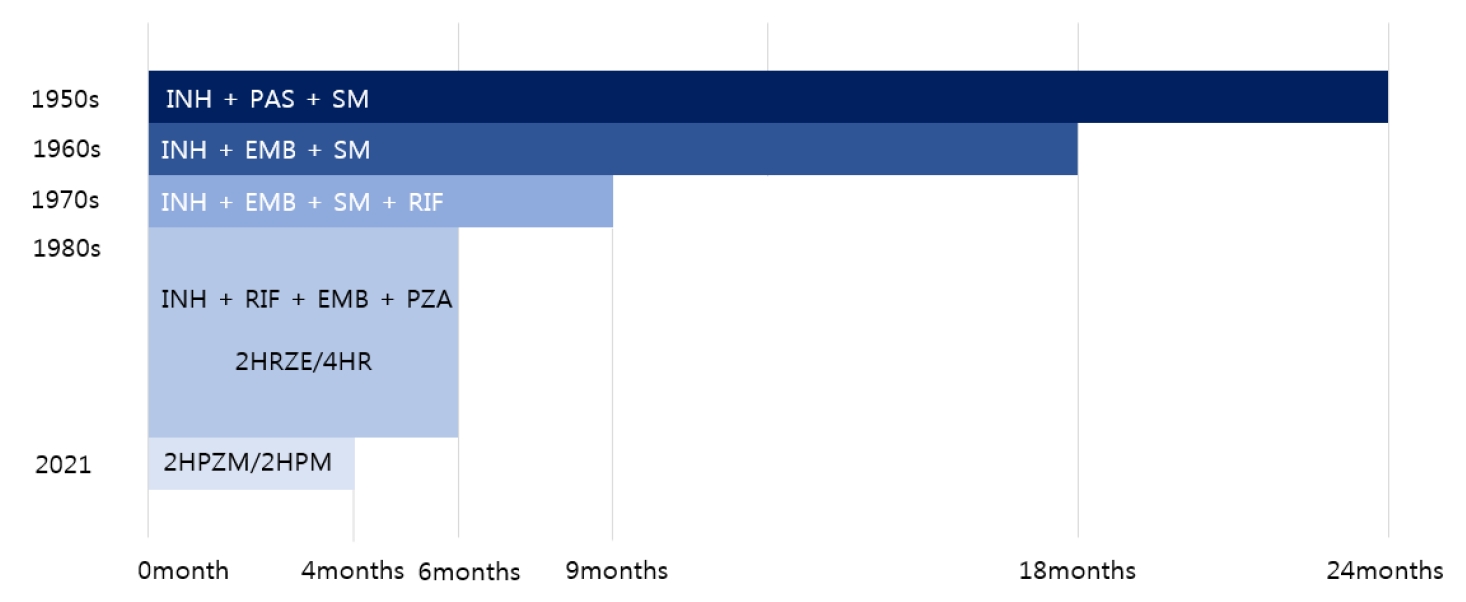
Figure┬Ā1.
Table┬Ā1.
Preferred drug regimens for microbiologically confirmed pulmonary tuberculosis caused by drug-susceptible organisms
Adopted from World Health Organization [26].
INH, isoniazid; RIF, rifampicin; EMB, ethambutol; PZA, pyrazinamide; H, isoniazid; R, rifampicin; Z, pyrazinamide; E, ethambutol; FDC, fixed dose combination.
Table┬Ā2.
Comparisons of current trials which aimed to shorten duration of TB treatment
| Regimen |
Intensive phase |
Continuation phase |
Per-protocol |
Modified ITT |
|||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Drugs | Interval | Drugs | Interval | Favorable (%) | Unfavorable (%) | Differencea | Favorable (%) | Unfavorable (%) | Differencea | ||
| Control |
2 months |
4 months |
|||||||||
| INH, RIF, EMB, PZA | Daily | INH, RIF | Daily | ||||||||
| REMoxTB | Control | 92 | 8 | NA | 84 | 16 | NA | ||||
| 2 months | 2 months | ||||||||||
| INH Group | INH, RIF, MFX, PZA | Daily | INH, RIF, MFX | Daily | 85 | 15 | 6.1 (1.7-10.5) | 77 | 23 | 7.8 (2.7-13.0) | |
| EMB Group | MFX, RIF, EMB, PZA | Daily | MFX, RIF | Daily | 80 | 20 | 11.4 (6.7-16.1) | 76 | 24 | 9(3.8-13.0) | |
| OFLOTUB | Control | 88.7 | 11.3 | NA | 82.8 | 17.2 | NA | ||||
| GFX Group | 2 months | 2 months | 82.3 | 17.7 | 3.5 (-0.7 to 7.7) | 79 | 21 | 3.5 (-0.7 to 7.7) | |||
| INH, RIF, GFX, PZA | Daily | INH, RIF, GFX | Daily | ||||||||
| RIFAQUIN | Control | 95.1 | 4.9 | NA | 85.6 | 14.4 | NA | ||||
| 4M Group | 2 months | 2 months | 81.8 | 18.2 | 13.6 (7.0-20.2) | 73.1 | 26.9 | 13.1 (6.8-19.4) | |||
| MFX, RIF, EMB, PZA | Daily | MFX, RPT | Twice weekly | ||||||||
| 6M Group | 2 months | 4 months | 96.8 | 3.2 | -1.8 (-6.1 to 2.4) | 86.3 | 13.7 | 0.4 (-4.7 to 5.6) | |||
| MFX, RIF, EMB, PZA | Daily | MFX, RPT | Once weekly | ||||||||
| Microbiologically eligible population | Assessable population | ||||||||||
| Study 31/A5349 | Control | 85.4 | 14.6 | NA | 90.4 | 9.6 | NA | ||||
| RJPT Group | 2 months | 2 months | 82.3 | 17.7 | 3.0 (-0.6 to 6.6) | 85.8 | 14.2 | 4.4(1.2-7.7) | |||
| INH, RPT, PZA, EMB | Daily | INH, RPT | Daily | ||||||||
| RPT/MFX Group | INH, RPT, PZA, MFX | Daily | INH, RPT, MFX | Daily | 84.5 | 15.5 | 1.0 (-2.6 to 4.5) | 88.4 | 11.6 | 2.0 (-1.1 to 5.1) | |
Modified from Shin and Kwon [40].
ITT, intention-to-treat; NA, not applicable; INH, isoniazid; RIF, rifampicin; MFX, moxifloxacin; PZA, pyrazinamide; EMB, ethambutol; GFX, gatifloxacin; RPT, rifapentine.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




