м„ң лЎ
к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқм—җм„ң лӮҳнғҖлӮ мҲҳ мһҲлҠ” лҢҖмһҘ мқҙмҷёмқҳ лі‘ліҖмқҖ лӢӨм–‘н•ҳлӢӨ. мў…м–‘ лі‘ліҖмңјлЎңлҠ” к°„лӘЁм„ёнҸ¬мў…, лҚ°мҠӨлӘЁмқҙл“ңмў…м–‘, к°‘мғҒм„ м•”, мӢӯмқҙм§ҖмһҘм—җ л°ңмғқн•ҳлҠ” м„ мў… л°Ҹ м„ м•”, мҶҢмһҘмқҳ мҡ©мў… л°Ҹ м•”, мң„мқҳ мҡ©мў… л°Ҹ м•”, лӢҙлҸ„кі„ л°Ҹ м·ҢмһҘмқҳ м„ мў…, лҮҢмў…м–‘ л“ұмқҙ мһҲлӢӨ. м–‘м„ұ лі‘ліҖмңјлЎңлҠ” кіЁмў…м–‘, н”јм§ҖлӮӯмў…, м№ҳм•„мқҳ мқҙмғҒ, лҲҲм—җ лӮҳнғҖлӮҳлҠ” л§қл§үмғүмҶҢмғҒн”јмқҳ м„ мІңм„ұ 비лҢҖ л“ұмқҙ мһҲлӢӨ[1].
кіјкұ°м—җ 비н•ҙ к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқ нҷҳмһҗм—җм„ң мҳҲл°©м Ғмқё лҢҖмһҘ мҲҳмҲ мқҙ 진н–үлҗҳлҠ” кІҪмҡ°к°Җ лҠҳм–ҙлӮҳл©ҙм„ң лҢҖмһҘ мҷё м§Ҳнҷҳ, нҠ№нһҲ мғҒл¶Җ мң„мһҘкҙҖ м§Ҳнҷҳм—җ мқҳн•ң мӮ¬л§қлҘ мқҙ мҰқк°Җн•ҳкІҢ лҗҳм—ҲлӢӨ[2]. к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқ нҷҳмһҗм—җм„ңмқҳ мӢӯмқҙм§ҖмһҘ м„ мў… л°Ҹ м„ м•”мқҖ м„ңм–‘м—җм„ң м—ӯн•ҷмқҙлӮҳ м№ҳлЈҢ, 추м Ғ лӮҙмӢңкІҪ кё°к°„ л“ұмқҙ м—°кө¬лҗҳм–ҙ мҷ”мңјлӮҳ, лҸҷм–‘м—җм„ң 비көҗм Ғ нқ”н•ҳкІҢ лҸҷл°ҳлҗҳлҠ” мң„мқҳ м„ мў… л°Ҹ м„ м•”м—җ лҢҖн•ҙм„ңлҠ” м—°кө¬к°Җ л¶ҖмЎұн•ҳлӢӨ.
мң„ л°”лӢҘмғҳмў…(fundic gland polyp)мқҙ к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқ нҷҳмһҗмқҳ м•Ҫ 50-60%м—җм„ң лҸҷл°ҳлҗ мҲҳ мһҲкі , м„ мў…(adenoma)лҠ” 6-14%м—җм„ң лҸҷл°ҳлҗңлӢӨ[3]. мқјл°ҳм ҒмңјлЎң мң„л°”лӢҘмғҳмў…мқҖ м•…м„ұмңјлЎң ліҖнҷҳмқҙ кұ°мқҳ м—ҶлӢӨкі м•Ңл Өм ё мһҲмңјлӮҳ мң„л°”лӢҘмғҳмў…м—җм„ң л°ңмғқн•ң мқҙнҳ•м„ұ(dysplasia) л°Ҹ м№ЁмңӨм„ұ м„ м•”мў…мқҙ мҰқлЎҖлЎң ліҙкі лҗҳм—ҲлӢӨ[4].
м Җмһҗл“ӨмқҖ к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқ нҷҳмһҗм—җм„ң л§җлӢЁ нҡҢмһҘл¶ҖмҷҖ лӢҙлӮӯм—җ кҙҖмғҳмў…мқҙ мһҲм—Ҳкі , 1л…„ мқҙлӮҙм—җ лӮҙмӢңкІҪм—җм„ң мӢӯмқҙм§ҖмһҘ мң л‘җл¶Җ м„ м•”мў…кіј мң„мқҳ л°”лӢҘмғҳмў…м—җм„ң л°ңмғқн•ң кІғмңјлЎң мғқк°ҒлҗҳлҠ” мң„ м„ м•”мў…мқҙ л°ңкІ¬лҗң нҷҳмһҗлҘј кІҪн—ҳн•ҳмҳҖкё°м—җ л¬ён—Ңкі м°°кіј н•Ёк»ҳ ліҙкі н•ҳлҠ” л°”мқҙлӢӨ.
мҰқ лЎҖ
63м„ё лӮЁмһҗ нҷҳмһҗк°Җ нҡҢмһҘлЈЁ мЈјмң„м—җ л¶ҲнҺёк°җмқҙ мһҲм–ҙ лӮҙмӣҗн•ҳмҳҖлӢӨ. нҷҳмһҗлҠ” к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқмңјлЎң 14л…„ м „м—җ м „мІҙлҢҖмһҘм Ҳм ңмҲ кіј нҡҢмһҘлЈЁмҲ мқ„ мӢңн–үл°ӣм•ҳкі , Levamisoleкіј FluorouracilлЎң ліҙмЎ°нҷ”н•ҷмҡ”лІ•мқ„ л°ӣм•ҳлӢӨ. нҡҢмһҘлЈЁкөҗм •мҲ мқ„ л°ӣкё° мң„н•ҙ мһ…мӣҗн•ҳм—¬ мӢңн–үн•ң мғҒл¶Җмң„мһҘкҙҖлӮҙмӢңкІҪм—җм„ң мң„мқҳ мғҒл¶Җ мІҙл¶Җл¶Җн„° кё°м Җл¶Җ, 분문л¶Җм—җ лӢӨл°ңм„ұмқҳ мҡ©мў…мқҙ кҙҖм°°лҗҳм–ҙ кё°м Җл¶Җм—җм„ң мЎ°м§ҒкІҖмӮ¬лҘј мӢңн–үн•ҳмҳҖкі , мЎ°м§ҒкІҖмӮ¬ кІ°кіј мң„л°”лӢҘмғҳмў…мқҳ мҶҢкІ¬мқ„ ліҙмҳҖлӢӨ. нҡҢмһҘлЈЁкөҗм •мҲ мӢң нҡҢмһҘ м Ҳм ң л¶Җмң„м—җ мҡ©мў…мқҙ кҙҖм°°лҗҳм—Ҳкі , мЎ°м§ҒкІҖмӮ¬ кІ°кіј кҙҖмғҳмў…(tubular adenoma)мқҳ мҶҢкІ¬мқ„ ліҙмҳҖлӢӨ.
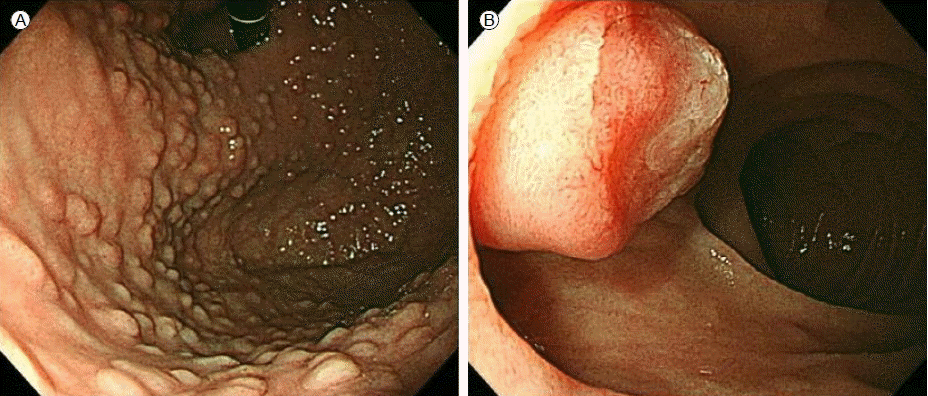
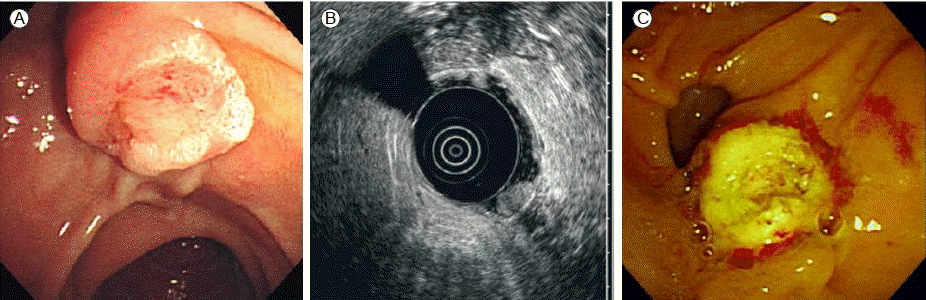
1л…„ л’Ө мғҒл¶Җмң„мһҘкҙҖ лӮҙмӢңкІҪм—җм„ң мң„мқҳ лӢӨл°ңм„ұ мҡ©мў…мқҖ мқҙм „ кІҖмӮ¬мҷҖ 비көҗн–Ҳмқ„ л•Ң ліҖнҷ” м—Ҷм—Ҳкі , мЎ°м§ҒкІҖмӮ¬ кІ°кіјлҸ„ ліҖнҷ” м—Ҷмқҙ мң„л°”лӢҘмғҳмў…мҰқмқҙм—ҲлӢӨ(Fig. 1A). м „м •л¶Җм—җлҠ” мҡ©мў…мқҙ кҙҖм°°лҗҳм§Җ м•Ҡм•ҳмңјлӮҳ, мӢӯмқҙм§ҖмһҘ мң л‘җл¶Җмқҳ м җл§үмқҙ кІ°м ҲмғҒмңјлЎң кҙҖм°°лҗҳм–ҙ(Figs. 1B and 2A) мЎ°м§ҒкІҖмӮ¬н•ҳмҳҖкі , мңөлӘЁмғҳмў…(villous adenoma)мңјлЎң 진лӢЁлҗҳм—ҲлӢӨ. лӮҙмӢңкІҪ м Ҳм ңмҲ к°ҖлҠҘ м—¬л¶ҖлҘј нҢҗлӢЁн•ҳкё° мң„н•ҳм—¬ мӢңн–үн•ң лӮҙмӢңкІҪ мҙҲмқҢнҢҢм—җм„ң мң л‘җл¶ҖлҠ” м•Ҫ 12 mmмқҙкі , м Җм—җмҪ” мҶҢкІ¬мқҳ мң л‘җл¶Җ нҢҪлҢҖмҶҢкІ¬мқҙ м җл§ү, м җл§үн•ҳмёөм—җм„ң ліҙмқҙкі , кі мң к·јмёөкіј мЈјмң„мЎ°м§Ғмқҳ м№ЁлІ”мқҖ кҙҖм°°лҗҳм§Җ м•Ҡм•ҳлӢӨ(Fig. 2B). мқҙлҹ¬н•ң мҶҢкІ¬мңјлЎң лӮҙмӢңкІҪ мң л‘җм Ҳм ңмҲ мқ„ мӢңн–үн•ҳмҳҖмңјл©°(Fig. 2C) мЎ°м§ҒмҶҢкІ¬мқҖ мһҳ 분нҷ”лҗң м„ м•”мў…мңјлЎң 진лӢЁлҗҳм—ҲлӢӨ. мқҙм—җ 추к°Җм Ғмқё кІҪмӢӯмқҙм§ҖмһҘ мң л‘җм Ҳм ңмҲ кіј лӢҙлӮӯм Ҳм ңмҲ мқ„ мӢңн–үн•ҳмҳҖкі , лӢҙлӮӯ лӮҙ мҡ©мў…мқҖ кҙҖмғҳмў…мқҳ мҶҢкІ¬мқ„ лӮҳнғҖлӮҙм—ҲлӢӨ.
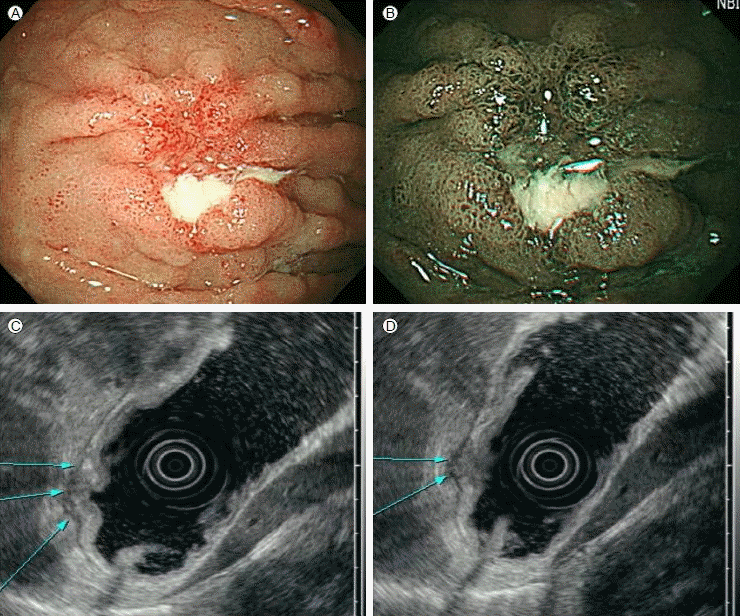
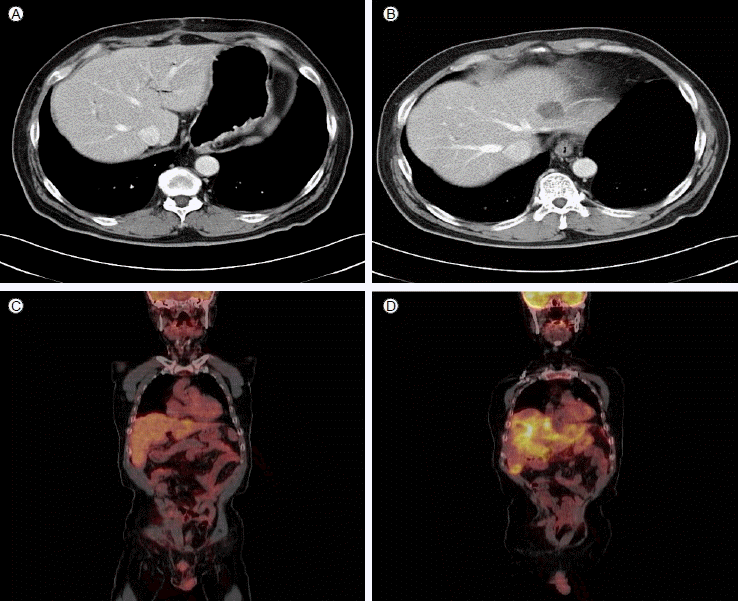
мң л‘җм Ҳм ңмҲ мӢңн–ү 4к°ңмӣ” л’Ө мғҒл¶Җмң„мһҘкҙҖлӮҙмӢңкІҪм—җм„ң мғҒмІҙл¶Җ лҢҖл§Ңм—җ ліҖм—°мқҳ мңөкё°лҘј ліҙмқҙлҠ” кІҪкі„к°Җ л¶Ҳ분лӘ…н•ң к¶Өм–‘мқҙ кҙҖм°°лҗҳм—Ҳкі (Fig. 3A and 3B), мЎ°м§ҒкІҖмӮ¬ кІ°кіј мң„л°”лӢҘмғҳмў…м—җм„ң л°ңмғқн•ң м„ м•”мў…мңјлЎң 진лӢЁлҗҳм—ҲлӢӨ. лӮҙмӢңкІҪ мҙҲмқҢнҢҢм—җм„ң кі мң к·јмёөкіј мһҘл§үмқҳ м№ЁлІ”мқҙ мқҳмӢ¬лҗҳм—ҲлӢӨ(Fig. 3C and 3D). мқҙм—җ м „мң„м Ҳм ңмҲ кі л Өн•ҳмҳҖмңјлӮҳ нҷҳмһҗ кұ°л¶Җн•ҳм—¬ ліөк°•кІҪ мҗҗкё°мң„м Ҳм ңмҲ л§Ңмқ„ мӢңн–үн•ҳмҳҖлӢӨ. мЎ°м§ҒкІҖмӮ¬ кІ°кіј мӨ‘л“ұлҸ„мқҳ 분нҷ”лҸ„лҘј к°Җ진 м„ м•”мў…мңјлЎң 진лӢЁлҗҳм—Ҳмңјл©°, нҷҳмһҗлҠ” 추к°Җм Ғмқё н•ӯм•”м№ҳлЈҢ л°Ҹ л°©мӮ¬м„ м№ҳлЈҢ кұ°м Ҳн•ҳм—¬ л¬ён•©л¶ҖмҷҖ мЈјліҖ л°”лӢҘмғҳмў…м—җ argon plasma coagulationлҘј мӢңн–үн•ҳкі м¶”м ҒкҙҖм°°н•ҳмҳҖлӢӨ.
кі м°°
к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқмқҖ мў…м–‘м–өм ңмң м „мһҗмқё APC мң м „мһҗмқҳ лҸҢм—°ліҖмқҙлЎң мқён•ҙ м„ёнҸ¬ лӮҙ лІ нғҖм№ҙн…ҢлӢҢмқҳ 분н•ҙк°Җ мқҙлЈЁм–ҙм§Җм§Җ м•Ҡм•„ м„ёнҸ¬ лӮҙм—җ м№ҙн…ҢлӢҢмқҙ 축м Ғлҗҳм–ҙ м„ёнҸ¬ лӮҙ мӢ нҳём „лӢ¬кіјм •мқҙ көҗлһҖлҗңлӢӨ. нҷҳмһҗмқҳ 70-80%м—җм„ңлҠ” к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқмқҳ к°ҖмЎұл Ҙмқҙ мһҲм§Җл§Ң м•Ҫ 20-30%м—җм„ңлҠ” к°ҖмЎұл Ҙмқҙ м—Ҷмқҙ лӢ№лҢҖмқҳ лҸҢм—°ліҖмқҙ нҳ•нғңлЎңм„ң лӮҳнғҖлӮңлӢӨ[5].
к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқм—җм„ң мӢӯмқҙм§ҖмһҘ мҡ©мў…мқҖ 50-90%м—җм„ң лҸҷл°ҳлҗңлӢӨкі м•Ңл Өм ё мһҲкі , м№ҳлЈҢн•ҳм§Җ м•Ҡмқ„ кІҪмҡ° м•Ҫ 5%м—җм„ң м•…м„ұмңјлЎң м „нҷҳлҗңлӢӨкі ліҙкі лҗҳм—ҲлӢӨ[6]. мқјл°ҳ мқёкө¬м—җм„ң мӢӯмқҙм§ҖмһҘм•”мқҳ л°ңмғқмңЁмқҙ 0.01-0.04%мқёлҚ° л°ҳн•ҙ к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқ нҷҳмһҗм—җм„ңлҠ” мң„н—ҳлҸ„к°Җ 100-330л°° мҰқк°Җн•ңлӢӨ[1]. мқҙлҹ¬н•ң м җм—җм„ң Spigelman л“ұмқҖ мӢӯмқҙм§ҖмһҘ мҡ©мў…мқҳ к°ңмҲҳ, нҒ¬кё°, нҳ•нғң, 분нҷ”мқҳ м •лҸ„м—җ л”°лқј лі‘кё°лҘј м„Өм •н•ҳмҳҖкі [7], мқҙ лі‘кё°м—җ л”°лқј лӮҙмӢңкІҪ 추м ҒкІҖмӮ¬ к°„кІ©мқ„ 추мІңн•ҳкі мһҲлӢӨ[1].
мӢӯмқҙм§ҖмһҘ м„ мў…мқҖ м„ңм–‘м—җм„ң мң лі‘лҘ мқҙ лҶ’кІҢ ліҙкі лҗҳкі мһҲкі , мң„мқҳ м„ мў…мқҖ м„ңм–‘м—җ 비н•ҙ лҸҷм–‘м—җм„ң лҚ” нқ”н•ң кІғмңјлЎң м•Ңл Өм ё мһҲлӢӨ[3,4]. мң„мқҳ м•…м„ұ мў…м–‘м—җ лҢҖн•ҙм„ңлҠ” м•„мӢңм•„, нҠ№нһҲ н•ңкөӯ(4.2%)кіј мқјліё(2.1%)мқ„ мӨ‘мӢ¬мңјлЎң к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқ нҷҳмһҗм—җм„ң мң„м•”мқҳ л°ңлі‘мқҙ мҰқк°ҖлҗңлӢӨкі ліҙкі лҗҳкі мһҲм§Җл§Ң м„ңм–‘м—җм„ңлҠ” мқјл°ҳ мқёкө¬мҷҖ 비көҗн–Ҳмқ„ л•Ң мң„м•”мқҳ мң лі‘лҘ мқҙ мқҳлҜё мһҲлҠ” м°Ёмқҙк°Җ м—Ҷм—ҲлӢӨ[3,6].
мқјл°ҳм ҒмңјлЎң мң„л°”лӢҘмғҳмў…мқҖ м•…м„ұмңјлЎңмқҳ м „нҷҳмқҙ кұ°мқҳ м—ҶлӢӨкі м•Ңл Өм ё мһҲмңјлӮҳ мң„л°”лӢҘмғҳмў…м—җм„ң л°ңмғқн•ң мқҙнҳ•м„ұ л°Ҹ м№ЁмңӨм„ұ м„ м•”мў…мқҙ мҰқлЎҖлЎң ліҙкі лҗҳм—ҲлӢӨ[4]. лҳҗн•ң лӘҮлӘҮ м—°кө¬м—җм„ң к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқмқҳ мң„л°”лӢҘмғҳмў…м—җм„ң мӢңн–үн•ң мң м „мһҗ 분м„қ кІ°кіј мқјл°ҳ мқёкө¬мқҳ мң„л°”лӢҘмғҳмў…кіјлҠ” лӢ¬лҰ¬ мІҙм„ёнҸ¬(5лІҲ м—јмғүмІҙ мһҘ축)м—җм„ң APC мң м „мһҗмқҳ ліҖмқҙк°Җ м•Ҫ 50%м—җм„ң нҷ•мқёлҗҳм—ҲлӢӨ. мқҙлҘј нҶөн•ҙ мғқмӢқм„ёнҸ¬мқҳ APC мң м „мһҗ ліҖмқҙмҷҖ мІҙм„ёнҸ¬мқҳ APC мң м „мһҗмқҳ ліҖмқҙк°Җ мқјм–ҙлӮҳл©ҙм„ң(second-hit) мқҙнҳ•м„ұ л°Ҹ м•”мў… л°ңмғқмқҙ мқјм–ҙлӮ мҲҳ мһҲлӢӨкі м„ӨлӘ…н•ҳмҳҖлӢӨ[8]. ліё мҰқлЎҖм—җм„ңлҠ” мғҒл¶Җмң„мһҘкҙҖлӮҙмӢңкІҪм—җм„ң м—¬лҹ¬ к°ңмқҳ мң„л°”лӢҘмғҳмў…л§Ң мһҲлҚҳ нҷҳмһҗм—җм„ң 14к°ңмӣ” л’Ө мӢңн–үн•ң лӮҙмӢңкІҪ 추м ҒкІҖмӮ¬м—җм„ң мӢӯмқҙм§ҖмһҘм•”мқҙ л°ңкІ¬лҗҳм—Ҳкі , к·ё нӣ„ 4к°ңмӣ” л§Ңм—җ мң„мқҳ м„ м•”мў…мқҙ л°ңкІ¬лҗҳм—ҲлӢӨ. л”°лқјм„ң к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқ нҷҳмһҗм—җм„ң мғҒл¶Җмң„мһҘкҙҖлӮҙмӢңкІҪмқ„ мӢңн–үн• л•ҢлҠ” мӢӯмқҙм§ҖмһҘ нҢҪлҢҖл¶Җмң„к№Ңм§Җ мһҗм„ёнһҲ кҙҖм°°н•ҳлҠ” кІғкіј мң„ мҡ©мў…м—җ лҢҖн•ҙ м„ мў… к°ҖлҠҘм„ұмқҙ мһҲлҠ”м§Җ л©ҙл°ҖнһҲ кҙҖм°°н•ҳлҠ” кІғмқҙ мӨ‘мҡ”н•ҳлӢӨ. к·ёлҰ¬кі мң„м—җ л°”лӢҘмғҳмў…л§Ң мһҲлӢӨ н•ҳлҚ”лқјлҸ„ мЎ°м§ҒкІҖмӮ¬лҘј мӢңн–үн•ҳм—¬ мқҙнҳ•м„ұ м—¬л¶ҖлҘј нҷ•мқён•ҙм•ј н•ҳкі , мқҙнҳ•м„ұ м—¬л¶Җ л°Ҹ м •лҸ„м—җ л”°лқј 6к°ңмӣ”м—җм„ң 1л…„ к°„кІ©мқҳ мғҒл¶Җмң„мһҘкҙҖлӮҙмӢңкІҪ кІҖмӮ¬ лҳҗлҠ” prophylactic gastrectomyлҘј кі л Өн•ҙм•ј н• кІғмңјлЎң мғқк°Ғн•ңлӢӨ[4]. м•„мӢңм•„мқҳ к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқ нҷҳмһҗм—җм„ң мң„м•”кіј мң„м„ мў…мқҳ л°ңлі‘лҘ мқҙ лҶ’кі , мң„мҡ©мў…м—җ лҢҖн•ң мӨ‘мҰқлҸ„ нҢҗм • л°Ҹ 추м Ғ лӮҙмӢңкІҪ кІҖмӮ¬ к°„кІ©м—җ лҢҖн•ң м—°кө¬ л°Ҹ м§Җм№Ёмқҙ м•„м§Ғ м—Ҷм–ҙ мқҙкІғмқҳ л§Ҳл Ёмқҙ н•„мҡ”н• кІғмңјлЎң мғқк°Ғн•ңлӢӨ.
ліё мҰқлЎҖмқҳ нҷҳмһҗлҠ” мң л‘җнҢҪлҢҖл¶Җ м Ҳм ңмҲ мқ„ мӢңн–үн•ҳл©ҙм„ң лӢҙлӮӯм Ҳм ңмҲ лҸ„ лҸҷмӢңм—җ мӢңн–үн•ҳмҳҖкі , мЎ°м§Ғ мҶҢкІ¬мқҖ м„ мў…мқҙм—ҲлӢӨ. к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқм—җм„ң л°ңмғқн•ң лӢҙлҸ„кі„мқҳ м„ мў…мқҙлӮҳ м„ м•”мў…м—җ лҢҖн•ҙ мҰқлЎҖк°Җ ліҙкі лҗң м ҒмқҖ мһҲм§Җл§Ң[9,10] мқҙм—җ лҢҖн•ң м—ӯн•ҷ мЎ°мӮ¬к°Җ мқҙлЈЁм–ҙм§Җм§Җ м•Ҡм•„ мқјл°ҳ мқёкө¬мҷҖ 비көҗн–Ҳмқ„ л•Ңмқҳ л°ңмғқлҘ мқҙлӮҳ мң„н—ҳлҸ„ л“ұмқ„ м•„м§Ғ м•Ң мҲҳ м—ҶлӢӨ. л”°лқјм„ң мқҙм—җ лҢҖн•ң м—°кө¬к°Җ лҚ” н•„мҡ”н•ҳлӢӨкі мғқк°Ғн•ҳл©°, к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқ нҷҳмһҗм—җм„ң ліөл¶Җ мҙҲмқҢнҢҢлҘј мқҙмҡ©н•ң лӢҙлҸ„кі„ м§Ҳнҷҳ м—¬л¶Җмқҳ мЎ°мӮ¬ л°Ҹ 추м ҒкҙҖм°°мқҙ н•„мҡ”н•ҳлӢӨ.
ліё мҰқлЎҖлҠ” к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқм—җм„ң нҡҢмһҘкіј лӢҙлӮӯм—җ м„ мў…мқҙ мһҲм—Ҳкі , мң„мҷҖ мӢӯмқҙм§ҖмһҘм—җ м„ м•”мў…мқҙ мһҲлҠ” нҷҳмһҗлЎң м§ҖкёҲк№Ңм§Җ лҢҖмһҘ мҷём—җ мқҙл ҮкІҢ лӢӨл°ңм ҒмңјлЎң мў…м–‘мқҙ л°ңмғқн•ң нҷҳмһҗм—җ лҢҖн•ң ліҙкі лҠ” м—Ҷм—ҲлӢӨ. к°ҖмЎұм„ұмғҳмў…нҸҙлҰҪмҰқм—җм„ң лҢҖмһҘ мҷёмқҳ м§Ҳнҷҳм—җ лҢҖн•ҙ кҙҖмӢ¬мқ„ к°Җм§Җкі мЈјкё°м Ғмқё 추м ҒкҙҖм°°мқҙ н•„мҡ”н•ҳлӢӨкі мғқк°Ғлҗҳм–ҙ л¬ён—Ңкі м°°кіј н•Ёк»ҳ ліҙкі н•ҳлҠ” л°”мқҙлӢӨ.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






