 |
 |
| Korean J Med > Volume 82(2); 2012 > Article |
|
Abstract
Reactivation of hepatitis B virus (HBV) has been well documented as a complication in HBV surface antigen (HBsAg) carriers who receive cytotoxic or immunosuppressive therapy. With the recent introduction of newer agents with a high level of immunosuppressive effect, this unfavorable event often occurs in patients with HBsAg-negative and/or occult HBV infection. The first step in HBV reactivation management is the identification of the patients at risk of viral reactivation by testing for HBV serology prior to commencing immunosuppressive treatment or chemotherapy. Multiple publications have consistently indicated the benefit of prophylactic or preemptive antiviral therapy in this setting, and justified such approach before the start of cytotoxic therapy. Unresolved issues concerning such prophylactic approach remain in the situations of HBsAg-negative/anti-HBc-positive or negative status, which presumably consists of a large number of occult HBV infection cases. This topic review will summarize clinical issues related to HBV reactivation, focusing clinical manifestations, risk factors associated with HBV reactivation, and a growing body of evidence supporting preventive antiviral therapy in high-risk patients. (Korean J Med 2012;82:149-158)
BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖżņØś ņ”ØņŗØņä▒, ĒÖ£ļÅÖņä▒ ņāüĒā£ļŖö ņłÖņŻ╝ņÖĆ BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖż Ļ░äņØś ņāüĒśĖņ×æņÜ®ņŚÉ ņØśĒĢ┤ Ļ▓░ņĀĢļÉ£ļŗż. ļ░öņØ┤ļ¤¼ņŖżĻ░Ć ļ╣äņ”ØņŗØņä▒ ņāüĒā£ļØ╝ ĒĢĀņ¦ĆļØ╝ļÅä ĒÖśņ×ÉņØś ļ®┤ņŚŁņØ┤ ņĢĮĒÖöļÉśļŖö ņāüĒÖ®ņŚÉļŖö ļ░öņØ┤ļ¤¼ņŖżņØś ņ”ØņŗØņä▒ņØ┤ ļŗżņŗ£ ĒÜīļ│ĄļÉśņ¢┤ Ļ░äņŚ╝ņØ┤ ļ░£ņāØĒĢśĻ▓ī ļÉ£ļŗż. ņØ┤ļ¤¼ĒĢ£ BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖżņØś ņ×¼ĒÖ£ņä▒ĒÖöļŖö 1975ļģä ĒĢŁņĢöņ╣śļŻīļź╝ ļ░øļŖö ĒśłņĢĪņ¦łĒÖś ĒÖśņ×ÉņŚÉņä£ ņ▓śņØī ļ│┤Ļ│ĀļÉ£ ņØ┤Ēøä ņŚ¼ļ¤¼ ņ×äņāüņé¼ļĪĆļōżņŚÉņä£ ļäÉļ”¼ ņĢīļĀżņĀĖ ņ׳ļŗż[1]. ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝Ļ│╝ Ļ┤ĆļĀ©ļÉ£ ņ┤łĻĖ░ņØś ņŚ░ĻĄ¼ļōżņØĆ ļīĆĻ░£ ņ╣śļŻīļĪ£ ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£ļź╝ ĒżĒĢ©ĒĢ£ Ļ░ĢļĀźĒĢ£ ņäĖĒżļÅģņä▒ņĢĮņĀ£ļź╝ ņé¼ņÜ®ĒĢśļŖö ĒśłņĢĪņ¦łĒÖśņØś ņ×äņāü ņśłĻ░Ć ļīĆļČĆļČäņØ┤ņŚłļŗż. ĻĘ╝ļלņŚÉ ņןĻĖ░ņØ┤ņŗØņØ┤ ĒÖ£ļ░£ĒĢ┤ņ¦ĆĻ│Ā ĒĢŁņĢöņĀ£ ļ░Å ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£ņØś ĒÜ©ļŖźņØ┤ ļ│┤ļŗż Ļ░ĢļĀźĒĢ┤ņ¦ÉņŚÉ ļö░ļØ╝ ĒśłņĢĪņ¦łĒÖśļ┐É ņĢäļŗłļØ╝ ņ£Āļ░®ņĢö, Ļ░äņĢö, ĒÅÉņĢö, ļźśļ¦łĒŗ░ņŖż ņ¦łĒÖś ļō▒ņŚÉņä£ļÅä ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØś ļ╣łļÅäĻ░Ć ļÜ£ļĀĘĒĢśĻ▓ī ņ”ØĻ░ĆĒĢśĻ│Ā ņ׳ļŗż. ņĄ£ĻĘ╝ ļ░£Ēæ£ļÉ£ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ ņŚ░ĻĄ¼ļōżņŚÉ ļö░ļź┤ļ®┤ BĒśĢĻ░äņŚ╝ņØś ņ×¼ĒÖ£ņä▒ņØĆ ļīĆņ▓┤ņĀüņ£╝ļĪ£ ņ╣śļŻīņØś Ļ░ĢļÅäĻ░Ć Ļ░ĢĒĢĀņłśļĪØ ņłÖņŻ╝ņØś ļ®┤ņŚŁņ¢ĄņĀ£ ņĀĢļÅäĻ░Ć ņŗ¼ĒĢĀņłśļĪØ ļŹö ĒØöĒ׳ ļ│┤Ļ│ĀļÉśņ¢┤, ņóģņ¢æņ╣śļŻī ņżæ ļ░£ņāØĒĢśļŖö ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ ņ£äĒŚśļÅäļź╝ ņ¦łĒÖśņŚÉ ļö░ļØ╝ ļČäļźśĒĢ┤ļ│┤ļ®┤ Ēæ£ 1Ļ│╝ Ļ░Öļŗż. ļ¦īņä▒BĒśĢĻ░äņŚ╝ ļ│┤ņ£Āņ×ÉņŚÉņä£ ĒśłņĢĪņ¦łĒÖś ļ░Å ņØ┤ņŗØņŗ£ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØś ļ░£ņāØļźĀņØĆ 40-50% ņØ┤ņāüņ£╝ļĪ£ ļåÆņ£╝ļ®░, Ļ░äņäĖĒżņĢö, ĒÅÉņĢö ļ░Å ļ╣äņØĖļæÉĻ░ĢņĢöņØĆ ņżæĻ░äņ£äĒŚśļÅäļĪ£ 10-30%, ĻĘĖļ”¼Ļ│Ā 5-fluorouracilņØä ĻĖ░ņ┤łļĪ£ ĒĢśļŖö ļīĆņןņĢö ĒÖśņ×ÉņØś ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØĆ 5% ņĀĢļÅäļĪ£ ļé«Ļ▓ī ļéśĒāĆļé£ļŗż[2]. ņĄ£ĻĘ╝ ņ×äņāüņŚÉ ļÅäņ×ģļÉśĻ│Ā ņ׳ļŖö Ēæ£ņĀüņ╣śļŻīņĀ£ļŖö ļĢīļĢīļĪ£ ĒÖśņ×ÉņØś ļ®┤ņŚŁņäĖĒżņØś ņŗ¼ĒĢ£ Ļ▓░ĒĢŹņØä ņ£ĀļÅäĒĢśĻĖ░ļÅä ĒĢśļ»ĆļĪ£ Ļ│╝Ļ▒░ņŚÉ ļ╣äĒĢ┤ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØä ļ╣äļĪ»ĒĢ£ ļŗżņ¢æĒĢ£ Ļ░äņŚ╝ ĒĢ®ļ│æņ”Ø ņ£äĒŚśņØ┤ ņ”ØĻ░ĆĒĢśĻ▓ī ļÉśņŚłļŗż. ĻĘĖļ¤¼ļ»ĆļĪ£ ņóģņ¢æĒÖśņ×ÉļōżņØä ņ¦äļŗ©ĒĢśĻ│Ā ņ╣śļŻīļź╝ ļŗ┤ļŗ╣ĒĢśļŖö ņ×äņāüņØśļŖö ņØ┤ņŚÉ ļīĆĒĢ£ ņČ®ļČäĒĢ£ ņØśļŻīņ¦ĆņŗØņØä ņłÖņ¦ĆĒĢ┤ņĢ╝ ĒĢĀ ĒĢäņÜöĻ░Ć ņ׳ļŗż. ļ│Ė ļģ╝Ļ│ĀņŚÉņä£ļŖö ĒĢŁņĢö-ļ®┤ņŚŁņ¢ĄņĀ£ ņ╣śļŻī ņżæ ļ░£ņāØĒĢśļŖö BĒśĢĻ░äņŚ╝ ņ×¼ĒÖ£ņä▒ņØś ņŚ¼ļ¤¼ ņ×äņāüĻ▓░Ļ│╝ļōżņØä Ļ│Āņ░░ĒĢ┤ļ│┤Ļ│Ā ņØ┤ņŚÉ ļīĆĒĢ£ ņĀüņĀłĒĢ£ ļīĆņ▓śļ░®ņĢłņØä ņÜöņĢĮ ĻĖ░ņłĀĒĢśņśĆļŗż.
ĒĢŁņĢöņ╣śļŻīļź╝ ļ░øĻ│Ā ņ׳ļŖö BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖż Ēæ£ļ®┤ĒĢŁņøÉ(HBsAg) ņ¢æņä▒ņØĖ ņóģņ¢æĒÖśņ×ÉņØś BĒśĢĻ░äņŚ╝ ņ×¼ĒÖ£ņä▒ĒÖö ļ╣äņ£©ņØĆ ĒÅēĻĘĀ 25-40%ļĪ£ ļ│┤Ļ│ĀļÉśļ®░ ņØ┤ ņżæ ņØ╝ļČĆļŖö ĒÖ®ļŗ¼, ļ│Ąņłś ļō▒ Ļ░äļČĆņĀä ņ”ØņäĖļź╝ ļ│┤ņØ┤Ļ│Ā ņŗ¼ĒĢ£ Ļ▓ĮņÜ░ ņé¼ļ¦ØĻ╣īņ¦Ć ņØ┤ļź┤Ļ▓ī ļÉ£ļŗż[2]. ņóģņ¢æņŚÉ ņØ┤ĒÖśļÉ£ ļ░öņØ┤ļ¤¼ņŖż ļ│┤ņ£Āņ×ÉĻ░Ć ņóģņ¢æņ╣śļŻīļź╝ ļ░øļŖö ļÅÖņĢł ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØ┤ ļ░£ņāØĒĢśĻ▓īļÉśļ®┤ Ļ░äĻĖ░ļŖźņØ┤ ĒśĖņĀäļÉĀ ļĢīĻ╣īņ¦Ć ĒŖ╣ņĀĢ ņóģņ¢æ-ļ®┤ņŚŁņ¦łĒÖśņØś ņ╣śļŻīļź╝ ņżæļŗ©ĒĢśĻ▒░ļéś ņŚ░ĻĖ░ĒĢĀ ņłś ļ░¢ņŚÉ ņŚåļŖö Ļ▓ĮņÜ░Ļ░Ć ĒØöĒ׳ ļ░£ņāØĒĢśĻ▓ī ļÉ£ļŗż. ĒĢ£ ņĀäĒ¢źņĀü ņŚ░ĻĄ¼ņŚÉ ņØśĒĢśļ®┤ ņóģņ¢æ ņ╣śļŻīņØś ņ¦ĆņŚ░ ļ░Å ņĪ░ĻĖ░ ņżæļŗ©ņØś ņé¼ļĪĆĻ░Ć BĒśĢĻ░äņŚ╝ ņ×¼ĒÖ£ņä▒ņØ┤ ļ░£ņāØĒĢśņśĆņØä Ļ▓ĮņÜ░Ļ░Ć ĻĘĖļĀćņ¦Ć ņĢŖņØĆ Ļ▓ĮņÜ░ļ│┤ļŗż ņĢĮ 2ļ░░ ņØ┤ņāüņ£╝ļĪ£ ņ£ĀņØśĒĢśĻ▓ī ļ¦ÄņĢśļŗż[3]. ļö░ļØ╝ņä£ BĒśĢĻ░äņŚ╝ ņ×¼ĒÖ£ņä▒ņØ┤ ņżæņÜöĒĢ£ Ļ╣īļŗŁņØĆ BĒśĢĻ░äņŚ╝ ņ×¼ĒÖ£ņä▒ņŚÉ ņØśĒĢ┤ ņ¦üņĀæņĀüņ£╝ļĪ£ ņŗ¼ĒĢ£ Ļ░äņ¦łĒÖśņØ┤ ļ░£ņāØĒĢśļŖö Ļ▓āĻ│╝ ļÅÖņŗ£ņŚÉ ņóģņ¢æņØś ņ╣śļŻīĻ░Ć ņ¦ĆņŚ░ļÉśĻ▒░ļéś ņĪ░ĻĖ░ ņóģļŻīļÉ©ņ£╝ļĪ£ņŹ© ņĀäņ▓┤ ņāØņĪ┤ņ£©ņØś Ļ░Éņåīļź╝ ļČłļ¤¼ņś¼ ņłś ņ׳ļŗżļŖö ņĀÉ ļĢīļ¼ĖņØ┤ļŗż.
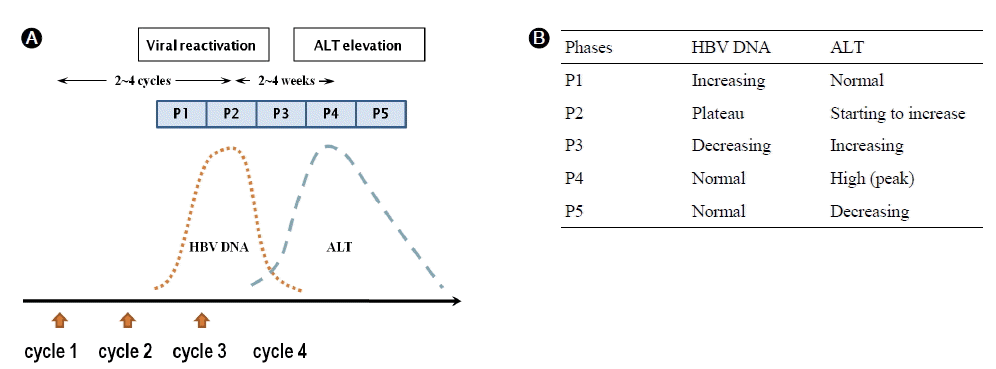
BĒśĢĻ░äņŚ╝ ļ│┤ņ£Āņ×ÉņŚÉņä£ ĒĢŁņĢö-ļ®┤ņŚŁņ¢ĄņĀ£ ņ╣śļŻī ņżæ ļ░£ņāØĒĢśļŖö ņĀäĒśĢņĀüņØĖ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØĆ ņĢĮ 5ļŗ©Ļ│äļĪ£ ļéśļłäņ¢┤ ņäżļ¬ģĒĢĀ ņłś ņ׳ļŗż (Fig. 1). ļ░śļ│ĄņĀüņØĖ ņ╣śļŻīņŻ╝ĻĖ░ ļÅÖņĢł ņ¦äĒ¢ēļÉśļŖö ļ®┤ņŚŁļŖź ņĀĆĒĢśļĪ£ ļ¦Éļ»ĖņĢöņĢä BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖżĻ░Ć ņłÖņŻ╝ņØś ļ®┤ņŚŁĻ░Éņŗ£ļź╝ ļ▓Śņ¢┤ļéśĻ▓ī ļÉśļ®┤ ņŖżņŖżļĪ£ ņ”ØņŗØĒĢĀ ņłś ņ׳ļŖö ĻĖ░ĒÜīļź╝ ņ¢╗Ļ▓īļÉśĻ│Ā(Phase 1), ĒĢŁņĢöņŻ╝ĻĖ░Ļ░Ć ļüØļéśļ®┤ņä£ ņĀÉņ░©ļĪ£ ņłÖņŻ╝ņØś ļ®┤ņŚŁļŖźņØ┤ ļŗżņŗ£ ĒÜīļ│ĄĒĢśĻĖ░ ņŗ£ņ×æĒĢśļ®┤ņä£ ļ░öņØ┤ļ¤¼ņŖż ļåŹļÅä ņ”ØĻ░ĆļŖö ņÖäļ¦īĒĢ┤ņ¦ĆļŗżĻ░Ć(Phase 2), Ļ▓░ĻĄŁ ļ®┤ņŚŁļŖźņØ┤ ļ░öņØ┤ļ¤¼ņŖż ņ”ØņŗØļŖźļ│┤ļŗż ņÜ░ņøöĒĢśĻ▓ī ļÉśļ®┤ ļ░öņØ┤ļ¤¼ņŖżļŖö ļŗżņŗ£ Ļ░ÉņåīĒĢśĻ▓ī ļÉ£ļŗż(Phase 3). ņØ┤ļĢīĻ╣īņ¦Ć ĒŖĖļ×£ņŖżņĢäļ»ĖļéśņĀ£(alanine aminotransferase, ALT) ņłśņ╣śļŖö ņāüņŖ╣ĒĢśņ¦Ć ņĢŖļŗżĻ░Ć ņłÖņŻ╝ņØś ļ®┤ņŚŁļŖźņØ┤ ņÖäņĀäĒ׳ ĒÜīļ│ĄĒĢśĻ│Ā ļéśļ®┤ TņäĖĒż ļ¦żĻ░£-ņäĖĒżņä▒ ļ®┤ņŚŁņŚÉ ņØśĒĢ┤ ļ░öņØ┤ļ¤¼ņŖżņŚÉ Ļ░ÉņŚ╝ļÉ£ Ļ░äņäĖĒżļōżņØ┤ ĒĢ£Ļ║╝ļ▓łņŚÉ Ļ┤æļ▓öņ£äĒĢśĻ▓ī ņé┤ņāüļÉśļ»ĆļĪ£ņŹ© Ļ░äņŚ╝ņØ┤ ļ░£ņāØĒĢśĻ▓ī ļÉ£ļŗż(Phase 4). ņØ┤Ēøä Ļ░ÉņŚ╝ļÉ£ Ļ░äņäĖĒżļōżņØ┤ ĒÜ©Ļ│╝ņĀüņ£╝ļĪ£ ņĀ£Ļ▒░ļÉśĻ│Ā ļéśļ®┤ ļ╣äļĪ£ņåī ALT ņłśņ╣śļÅä Ļ░ÉņåīĒĢśĻ▓ī ļÉ£ļŗż(Phase 5). ĻĘĖļ¤¼ļéś ņØ┤ņÖĆ Ļ░ÖņØĆ ņäżļ¬ģņØĆ ĒĢśļéśņØś Ļ░ĆņäżņØ┤Ļ│Ā, ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒Ļ│╝ Ļ┤ĆļĀ©ļÉ£ ņłÖņŻ╝, ļ░öņØ┤ļ¤¼ņŖż, ĒĢŁņĢöĒÖśĻ▓Į ņé¼ņØ┤ņØś ņāüĒśĖĻĘĀĒśĢņŚÉļŖö ņŗżļĪ£ ļīĆļŗ©Ē׳ ļ¦ÄņØĆ ņÜöņØĖļōżņØ┤ ņ×æņÜ®ĒĢśĻ▓ī ļÉ£ļŗż. ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ ĻĖ░ņĀäņŚÉ ļīĆĒĢśņŚ¼ ĒĢŁņĢöņŻ╝ĻĖ░ ņóģļŻī Ēøä ĒÜīļ│ĄļÉ£ ņäĖĒżņä▒ ļ®┤ņŚŁņŚÉ ņØśĒĢ£ ņäĖĒżņé┤ņāü(cell lysis)ņØś Ļ▓░Ļ│╝ļĪ£ ņäżļ¬ģĒĢśļŖö Ļ▓āņØ┤ ņØ╝ļ░śņĀüņØ┤ņ¦Ćļ¦ī, ĒĢŁņĢö-ļ®┤ņŚŁņ¢ĄņĀ£ ņ╣śļŻīļź╝ ņ¦ĆņåŹĒĢśĻ│Ā ņ׳ļŖö ļÅÖņĢłņŚÉļÅä ļ░£ņāØĒĢśļŖö Ļ▓ĮņÜ░Ļ░Ć ņ׳ņ¢┤ ļ░öņØ┤ļ¤¼ņŖżņŚÉ ņØśĒĢ£ ņ¦üņĀæņĀüņØĖ ņäĖĒżņāüĒĢ┤ ĒÜ©Ļ│╝(direct cytopathic effect)ļÅä ļČĆļČäņĀüņ£╝ļĪ£ļŖö Ļ┤ĆņŚ¼ĒĢĀ Ļ▓āņ£╝ļĪ£ ļ│┤ņØĖļŗż[4,5]. ļö░ļØ╝ņä£ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØĆ ņ¢┤ļŖÉ ĒĢ£ ņÜöņØĖļ│┤ļŗżļŖö ļ░öņØ┤ļ¤¼ņŖż-ņłÖņŻ╝ Ļ░äņØś ļ│Ąņ×ĪĒĢ£ ņāüĒśĖņ×æņÜ®ņŚÉ ņØśĒĢ┤ ļ░£ņāØĒĢśļŖö Ļ▓āņ£╝ļĪ£ ņØ┤ĒĢ┤ĒĢśņŚ¼ņĢ╝ ĒĢ£ļŗż.
Ļ│╝Ļ▒░ ņĢĮ 30ņŚ¼ļģä ņĀä BĒśĢĻ░äņŚ╝ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØ┤ ņ▓śņØī ļ│┤Ļ│ĀļÉśļŹś ņŗ£ņĀłņŚÉļŖö ĒśłņĢĪņŚÉņä£ Ļ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖżļź╝ ņ¦üņĀæ ņĖĪņĀĢĒĢĀ ņłś ņ׳ļŖö Ļ▓Ćņé¼ļ▓ĢņØ┤ ņŚåņ¢┤ņä£ ĒśłņĢĪņŚÉ ņĪ┤ņ×¼ĒĢśļŖö ļ░öņØ┤ļ¤¼ņŖż ĒĢŁņøÉ-ĒĢŁņ▓┤ ļ░śņØæ ņŚŁĻ░Ćņłśņ╣śņŚÉ ņØśņĪ┤ĒĢśņŚ¼ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØä ņČöņĀĢĒĢśļŖö ņłś ļ░¢ņŚÉ ņŚåņŚłļŗż. ņ”ē, ņØ┤ ĒśäņāüņØä ĒĢŁņøÉ ņŚŁĻ░ĆņØś ņ”ØĻ░Ć ļśÉļŖö ĒĢŁņ▓┤ ņŚŁĻ░ĆņØś Ļ░ÉņåīļĪ£ ņ¦äļŗ©ĒĢśņśĆļŗż[1]. ĻĘĖļ¤¼ļéś ņĄ£ĻĘ╝ ļČäņ×ÉņāØļ¼╝ĒĢÖņĀü ĻĖ░ļ▓ĢņØ┤ ļ░£ļŗ¼ĒĢśņŚ¼ ĒśłņĢĪļé┤ņŚÉņä£ ņśłļ»╝ĒĢśĻ▓ī ļ░öņØ┤ļ¤¼ņŖż ļåŹļÅäļź╝ ņ¦üņĀæ ņĖĪņĀĢĒĢĀ ņłś ņ׳Ļ▓ī ļÉśņ¢┤ ņØ┤ņĀ£ļŖö Ēśłņ▓ŁĒĢÖņĀüņØĖ ļ│ĆĒÖö ņØ┤ņÖĖņŚÉļÅä ļ░öņØ┤ļ¤¼ņŖż ļåŹļÅäļ│ĆĒÖöļź╝ ĒåĄĒĢ┤ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØä ņ¦äļŗ©ĒĢ£ļŗż. BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖżņØś ņ×¼ĒÖ£ņä▒ņØś ņ¦äļŗ©ņØĆ BĒśĢĻ░äņŚ╝ Ēæ£ļ®┤ĒĢŁņøÉ(HBsAg) ņ¢æņä▒ņØĖ Ļ▓ĮņÜ░ņÖĆ ņØīņä▒ņØĖ Ļ▓ĮņÜ░ Ļ░üĻ░ü ļŗ¼ļ”¼ ņĀüņÜ®ĒĢ£ļŗż.
HBsAg ĒĢŁņøÉ ņ¢æņä▒ņØĖ Ļ▓ĮņÜ░ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ ņé¼ļĪĆņŚÉņä£ Ēśłņ▓ŁĒĢÖņĀü Ēæ£ņ¦Ćņ×ÉļōżņØś ļ│ĆĒÖöļŖö ņé¼ņŗżņāü Ļ▒░ņØś ņŚåĻĖ░ ļĢīļ¼ĖņŚÉ ļ░öņØ┤ļ¤¼ņŖż ļåŹļÅäļ│ĆĒÖöļź╝ Ļ░Ćņ¦ĆĻ│Ā ĒīÉļŗ©ĒĢśļŖö Ļ▓āņØ┤ ņĀüņĀłĒĢśļŗż. ņØ╝ļ░śņĀüņ£╝ļĪ£ BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒ņØĆ ņóģņ¢æ-ļ®┤ņŚŁ ņ╣śļŻī ņĀäņŚÉ ļ╣äĒĢ┤ BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖż ļåŹļÅä(HBV DNA)Ļ░Ć 10ļ░░ ņØ┤ņāü ņāüņŖ╣ļÉ£ Ļ▓ĮņÜ░ļĪ£ ņ¦äļŗ©ĒĢĀ ņłś ņ׳ļŗż[2,6]. ļ░öņØ┤ļ¤¼ņŖżĻ░Ć ņ×¼ĒÖ£ņä▒ ļÉśņŚłļŗżĻ│Ā ĒĢ┤ņä£ ļ¬©ļōĀ Ļ▓ĮņÜ░ņŚÉ Ļ░äņŚ╝ņØ┤ ļ░£ņāØĒĢśļŖö Ļ▓āņØĆ ņĢäļŗłĻ│Ā ALTĻ░Ć ņĀĢņāüņØĖ Ļ▓ĮņÜ░ļÅä ļéśĒāĆļé£ļŗż. ņ╣śļŻīņØś ĒśĢĒā£, ĻĖ░ņĀĆ ļ░öņØ┤ļ¤¼ņŖż ņ”ØņŗØ ņāüĒā£ņŚÉ ļö░ļØ╝ ļŗżņ¢æĒĢśņ¦Ćļ¦ī ļīĆĻ░£ ņ╣śļŻīņØś Ļ░ĢļÅäĻ░Ć Ļ░ĢĒĢĀņłśļĪØ ņłÖņŻ╝ņØś ļ®┤ņŚŁņ¢ĄņĀ£ ņĀĢļÅäĻ░Ć ņŗ¼ĒĢĀņłśļĪØ ALT ņłśņ╣śĻ░Ć ļŹö ņāüņŖ╣ĒĢśņŚ¼ Ļ░äņŚ╝ļÅä ņŗ¼ĒĢśĻ▓ī ļéśĒāĆļé£ļŗż. ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ ņ¦äļŗ©ņŚÉņä£ ļ¼ĖņĀ£ņĀÉņØĆ ņØ┤ļĀćĻ▓ī ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒ņŚÉ ļö░ļźĖ Ļ░äņåÉņāü ņĀĢļÅäĻ░Ć ļŗżņ¢æĒĢśņŚ¼ ŌĆśĻ░äņŚ╝ŌĆÖņØś ņĀĢņØśĻ░Ć ļ¬©ĒśĖĒĢśļŗżļŖö ņĀÉņØ┤ļŗż. ņøÉņ╣ÖņĀüņ£╝ļĪ£ BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒ ņāüĒā£ņŚÉņä£ Ļ░äņŚ╝ņØ┤ ļ░£ņāØĒĢśņśĆļŖöĻ░Ć ņŚ¼ļČĆļŖö ņĪ░ņ¦üĻ▓Ćņé¼ļź╝ ĒåĄĒĢ┤ ņ¦äļŗ©ĒĢśļŖö Ļ▓āņØ┤ ĒÖĢņŗżĒĢ£ ļ░®ļ▓ĢņØ┤Ļ▓Āņ£╝ļéś, ņØ┤ļ¤░ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņāüĒā£ņŚÉņä£ļŖö ļĢīļĪ£ ĻĖēĻ▓®ĒĢ£ ņĢģĒÖöļĪ£ ļ¦Éļ»ĖņĢöņĢä ņŗ¼Ļ░üĒĢ£ Ļ░äļČĆņĀäņØä ņ┤łļלĒĢśļ»ĆļĪ£ ņĪ░ņ¦üĻ▓Ćņé¼ļź╝ ņØ╝ļźĀņĀüņ£╝ļĪ£ ņŗ£Ē¢ēĒĢśļŖö Ļ▓āņØĆ ĒśäņŗżņĀüņ£╝ļĪ£ ņ¢┤ļĀĄļŗż. ļö░ļØ╝ņä£ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØś ņ£Āļ¼┤ļŖö ALT ņāüņŖ╣ņØś ņĀĢļÅäļĪ£ ĒÅēĻ░ĆĒĢśļŖö Ļ▓āņØ┤ ņĀ£ņĢłļÉśņŚłļŖöļŹ░ ļīĆĻ░£ ņ╣śļŻī ņĀäņŚÉ ļ╣äĒĢ┤ ALT ņłśņ╣śĻ░Ć 3ļ░░ņØ┤ņāü ņāüņŖ╣ĒĢśņśĆņØä ļĢīļĪ£ ņĀĢņØśĒĢśļŖö Ļ▓āņØ┤ ņÜ░ņäĖĒĢśļŗż[7-9]. ĻĘĖļ¤¼ļéś ĻĖ░ņĀĆ Ļ░äņ¦łĒÖśņØś ņāüĒā£ņŚÉ ļö░ļØ╝ ALT ņāüņŖ╣ņĀĢļÅäĻ░Ć ļŗżņ¢æĒĢśļ»ĆļĪ£ ALT ņāüņŖ╣ņØś cut-offņ╣śņØś Ļ▓░ņĀĢņŚÉ ļīĆĒĢ┤ņä£ļŖö ļŹö ļ¦ÄņØĆ ņŚ░ĻĄ¼ņ×ÉļŻīĻ░Ć ĒĢäņÜöĒĢśļŗż.
HBsAg ņØīņä▒ņØś Ļ▓ĮņÜ░ļŖö ņØ┤ņĀäņŚÉ BĒśĢĻ░äņŚ╝ņØä ņĢōĻ│Ā ĒÜīļ│ĄļÉ£ Ēøä ļśÉļŖö ņ×Āņ×¼Ļ░ÉņŚ╝ņØś ņāüĒā£ļĪ£ ņ׳ļŗżĻ░Ć ņóģņ¢æņ╣śļŻīņŚÉ ņØśĒĢ┤ ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒ņØ┤ ļéśĒāĆļéśļŖö Ļ▓ĮņÜ░Ļ░Ć ĒØöĒĢśļŗż. ļö░ļØ╝ņä£ ņØ┤ Ļ▓ĮņÜ░ ļ░öņØ┤ļ¤¼ņŖż ļåŹļÅäņ”ØĻ░Ćļ│┤ļŗż ļīĆņ▓┤ļĪ£ Ēśłņ▓ŁĒĢÖņĀü ļ│ĆĒÖöĻ░Ć ļ©╝ņĀĆ ļéśĒāĆļéśĻ▓ī ļÉ£ļŗż. ļö░ļØ╝ņä£ HBsAg ņØīņä▒ņØĖ ĒÖśņ×ÉņØś ņ×¼ĒÖ£ņä▒ņØĆ ņ╣śļŻī ņżæ ĒśłņĢĪļé┤ HBsAgņØ┤ ņ×¼ņČ£ĒśäĒĢśĻ▒░ļéś, ņśłļ»╝ĒĢ£ Ļ▓Ćņé¼ļ▓Ģņ£╝ļĪ£ HBV DNAĻ░Ć ņ×¼Ļ▓ĆņČ£ļÉśļŖö Ļ▓ĮņÜ░ļĪ£ ņĀĢņØśĒĢ£ļŗż[10].
ļ░öņØ┤ļ¤¼ņŖżĻ░Ć ņ×¼ĒÖ£ņä▒ļÉ£ ĒÖśņ×ÉļōżņØś Ļ░äņŚ╝ņłśņ╣śļŖö ņĀĢņāüņØĖ Ļ▓ĮņÜ░ļČĆĒä░ ņŗ¼ĒĢ£ Ļ░äņŚ╝, Ļ░äļČĆņĀäĻ╣īņ¦Ć ļ¦żņÜ░ ļŗżņ¢æĒĢśĻ▓ī ļéśĒāĆļéśĻ▓ī ļÉśļŖöļŹ░ ņØ┤ņŚÉļŖö ņé¼ņÜ®ļÉ£ ņĢĮņĀ£, ļ░öņØ┤ļ¤¼ņŖż, ĒÖśņ×ÉņØś ĒŖ╣ņä▒, ĻĖ░ņĀĆ Ļ░äņ¦łĒÖśņØś ņāüĒā£ ļō▒ņØ┤ Ļ┤ĆņŚ¼ļÉ£ļŗż. BĒśĢĻ░äņŚ╝ ņ×¼ĒÖ£ņä▒ņØĆ ĒĢŁņĢöņ╣śļŻī ņżæ ņ▓½ ļ▓łņ¦Ė ņŻ╝ĻĖ░ņŚÉņä£ ļ░£ņāØĒĢśļŖö Ļ▓ĮņÜ░ļ│┤ļŗż 2-4ĒÜī ņŻ╝ĻĖ░ņŚÉņä£ ļ░£ņāØĒĢśļŖö Ļ▓ĮņÜ░Ļ░Ć ļ│┤ļŗż ņØ╝ļ░śņĀüņØ┤ļŗż[2,8,11]. BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖż ļ│┤ņ£Āņ×ÉņŚÉņä£ ļ░£ņāØĒĢśļŖö ņĀäĒśĢņĀüņØĖ ĒśĢĒā£ņØś ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØś ņłśņ╣ś ļ│ĆĒÖöļź╝ ļ│┤ļ®┤ 2-4ņŻ╝ĻĖ░ ņ╣śļŻī Ēøä ļ░öņØ┤ļ¤¼ņŖż ņ”ØĻ░ĆĻ░Ć ļ©╝ņĀĆ ļéśĒāĆļéśĻ▓ī ļÉśĻ│Ā, ļÆżņØ┤ņ¢┤ ņĢĮ 2-4ņŻ╝ Ēøä ALTĻ░Ć ņāüņŖ╣ĒĢśĻ▓ī ļÉ£ļŗż(Fig. 1). ĻĘĖļ¤¼ļéś ņØ┤ ļĢī ļ░£ņāØĒĢ£ Ļ░äņŚ╝ņØś ņ×äņāüĻ▓ĮĻ│╝ļŖö ĒÖśņ×ÉņØś ĻĖ░ņĀĆ Ļ░äņ¦łĒÖś ņĀĢļÅä, ņé¼ņÜ®ļÉ£ ņ╣śļŻīļ▓ĢņØś Ļ░ĢļÅä, ĒÖśņ×ÉņØś ļ®┤ņŚŁņ¢ĄņĀ£ ņĀĢļÅä ļō▒ņŚÉ ļö░ļØ╝ ņŗ¼Ļ░üĒĢ£ ĒĢ®ļ│æņ”ØņØä ļéśĒāĆļé┤ĻĖ░ļÅä ĒĢ£ļŗż.
HBsAg ņ¢æņä▒ņØĖ Ļ▓ĮņÜ░ ņóģņ¢æ-ļ®┤ņŚŁņ╣śļŻī ņżæ ļ░£ņāØĒĢśļŖö ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØĆ ņĢĮ 25-40%ļĪ£ ļ│┤Ļ│ĀļÉśļ®░, ņØ┤ ņżæ 5-30%ļŖö ĒÖ®ļŗ¼, ļ│Ąņłś, ņ£äņןĻ┤Ć ņČ£Ēśł ļō▒ņØś Ļ░äļČĆņĀä ņ”ØņäĖļź╝ ļ│┤ņØ┤Ļ│Ā ņŗ¼ĒĢ£ Ļ▓ĮņÜ░ ņé¼ļ¦ØĻ╣īņ¦Ć ņØ┤ļź┤Ļ▓ī ļÉ£ļŗż[2]. ņØ╝ļ░śņĀüņ£╝ļĪ£ HBsAg ņ¢æņä▒ņØĖ Ļ▓ĮņÜ░Ļ░Ć HBsAg ņØīņä▒ņØĖ Ļ▓ĮņÜ░ļ│┤ļŗż ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØś ļ╣łļÅäĻ░Ć ļåÆņ¦Ćļ¦ī, ņĀäĻ▓®ņä▒ Ļ░äņŚ╝ņØś ļ╣łļÅäļŖö HBsAgņØīņä▒ņØĖ ĒÖśņ×ÉņØś ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņŚÉņä£ ļŹö ļ¦Äļŗż[12].
ņóģņ¢æ ļśÉļŖö ļ®┤ņŚŁĻ│ä ņ¦łĒÖśņØś ņ╣śļŻī ņĢĮņĀ£ļōżņØĆ ņ¦ü-Ļ░äņĀæņĀüņ£╝ļĪ£ BĒśĢĻ░äņŚ╝ņØś ņ”ØņŗØņä▒ņŚÉ ņśüĒ¢źņØä ņżä ņłś ņ׳ļŗż. ņØ┤ ņżæ ņŖżĒģīļĪ£ņØ┤ļō£ ņĀ£ņĀ£ļŖö BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖż ļé┤ņŚÉ ņ׳ļŖö glucocorticoid responsive element (GRE)ļź╝ ņ×ÉĻĘ╣ĒĢśĻ│Ā, ļÅÖņŗ£ņŚÉ ļ░öņØ┤ļ¤¼ņŖż ņ£ĀņĀäņ×Éļé┤ enhancer I ļČĆņ£äņØś ņ×æņÜ®ņØä Ļ░ĢĒÖöņŗ£Ēé┤ņ£╝ļĪ£ņŹ© ļ░öņØ┤ļ¤¼ņŖż ņ”ØņŗØņØä ņ¦üņĀæņĀüņ£╝ļĪ£ ņ£ĀļÅäĒĢĀ ņłś ņ׳ļŗż[13]. ņ£Āļ░®ņĢö, Ļ░äņäĖĒżņĢöņóģ ļō▒ ņŚ¼ļ¤¼ Ļ│ĀĒśĢņĢöņŚÉ ņé¼ņÜ®ļÉśļŖö anthracycline ņĀ£ņĀ£ļŖö Ļ░äņĢöņäĖĒżņŻ╝ņŚÉņä£ ļåŹļÅäņŚÉ ļ╣äļĪĆĒĢśņŚ¼ HBsAgĻ│╝ HBV DNA ļČäļ╣äļź╝ ņ”ØĻ░Ćņŗ£ĒéżļŖö ņ×æņÜ®ņØä ĒĢśņśĆļŗż[14]. ļ░®ņé¼ņäĀ ņ╣śļŻīĻ┤ĆļĀ© ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØś Ļ▓ĮņÜ░ ļ░®ņé¼ņäĀņØ┤ ņĪ░ņé¼ļÉ£ ņśüņŚŁņØś ĒśłĻ┤Ćļé┤Ēö╝ņäĖĒżņŚÉņä£ interleukin (IL)-6 ļō▒ņØś ņŗĖņØ┤ĒåĀņ╣┤ņØĖņØś ļČäļ╣äĻ░Ć ņ”ØĻ░ĆļÉśĻ│Ā ņØ┤Ļ▓āņØ┤ Ļ░äņäĖĒżļé┤ BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖżņØś ņ”ØņŗØņØä ņ£ĀļÅäĒĢ£ļŗż[15]. ļśÉĒĢ£ ņłśņłĀņĀü ņĀłņĀ£ ņØ┤Ēøä ĒśłņĢĪļé┤ ĻĖēĻ▓®ĒĢśĻ▓ī ņ”ØĻ░ĆĒĢśļŖö ņĮöĒŗ░ņĪĖ, IL-6, tumor necrosis factor (TNF)-╬▒ ļō▒ņØś ņŗĖņØ┤ĒåĀņ╣┤ņØĖ, ņä▒ņןņØĖņ×É ļō▒ņØś ĻĖēņä▒ ņŖżĒŖĖļĀłņŖż ļ░śņØæļ¼╝ņ¦łņØĆ ļ░öņØ┤ļ¤¼ņŖżņØś ņ”ØņŗØ ļ░Å ņ×¼ĒÖ£ņä▒ņØä ņ£ĀļÅäĒĢĀ ņłś ņ׳ļŗż[16].
ĻĘĖļ¤¼ļéś ņ╣śļŻīĻ┤ĆļĀ© ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØä Ļ▓░ņĀĢĒĢśļŖö Ļ░Ćņן ņżæņÜöĒĢ£ ņøÉņØĖņØĆ ņĢĮļ¼╝ ļ░Å ņ╣śļŻīņŚÉ ņØśĒĢ┤ ņ£ĀļÅäļÉ£ ņłÖņŻ╝ņØś ļ®┤ņŚŁļŖź ņĀĆĒĢśņØ┤ļŗż. ņØ┤ļĪĀņĀüņ£╝ļĪ£ ņ¢┤ļ¢ż ĒĢŁņĢöņĀ£ņØ┤ļōĀ ņĀĢļÅäņØś ņ░©ņØ┤ļŖö ņ׳ņ¢┤ļÅä ņ¢┤ļŖÉņĀĢļÅä ļ®┤ņŚŁņ¢ĄņĀ£ĻĖ░ļŖźņØä Ļ░Ćņ¦ĆĻ│Ā ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ ļ░öņØ┤ļ¤¼ņŖżņØś ņ×¼ĒÖ£ņä▒ņØä ņ£Āļ░£ĒĢĀ ņłś ņ׳Ļ│Ā, ĒÖśņ×ÉņŚÉĻ▓ī ņäĖĒżļÅģņä▒ ņ╣śļŻī ņŗ£ ņ£ĀļÅäļÉśļŖö ļ®┤ņŚŁņ¢ĄņĀ£ ņĀĢļÅäņŚÉ ļö░ļØ╝ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØś ņØ┤ĒÖśņ£©ņØ┤ ļŗżļź┤Ļ▓ī ļéśĒāĆļéĀ ņłś ņ׳ļŗż. ņŗżņĀ£ļĪ£ ņĪ░Ēśłļ¬©ņäĖĒżņØ┤ņŗØ ņŗ£ ņĀäņ▓śņ╣śļĪ£ ņé¼ņÜ®ļÉśļŖö ļ¦żņÜ░ Ļ░ĢļĀźĒĢ£ ņäĖĒżļÅģņä▒ņ╣śļŻīļéś ņ×äĒīīņóģņŚÉ ņé¼ņÜ®ļÉśļŖö ĒĢŁņĢöņĀ£ļōżņØĆ ļ¬©ļæÉ ļŗżļźĖ Ļ▓ĮņÜ░ņØś ĒĢŁņĢöņ╣śļŻīļ│┤ļŗż Ļ░ĢļĀźĒĢśĻ▓ī ņłÖņŻ╝ņØś ļ®┤ņŚŁņØä Ļ░Éņåīņŗ£ĒéżļŖö Ļ▓āņ£╝ļĪ£ ļåÆņØĆ ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒ļźĀ(Ōēź 50%)ņØä ļ│┤ņØĖļŗż[2,17]. Ļ░ÖņØĆ ļ¦źļØĮņŚÉņä£ ļ░®ņé¼ņäĀ ņ╣śļŻīļÅä ņŗ¼ĒĢśĻ▓ī ĒÖśņ×ÉļōżņØś ļ®┤ņŚŁņØä Ļ░Éņåīņŗ£Ēé¼ ņłś ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ ļ░£ņāØņØ┤ ļåÆņØĆ Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[18,19].
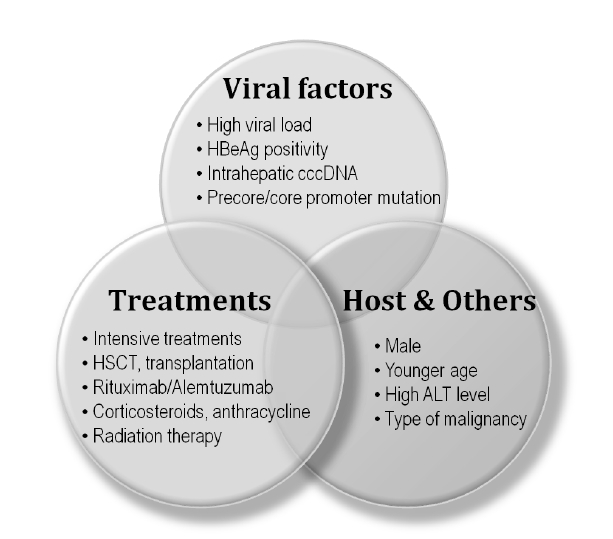
ĒØźļ»ĖļĪ£ņÜ┤ ņé¼ņŗżņØĆ ņĀäņŗĀņĀü ĒÜ©Ļ│╝Ļ░Ć ņĀüņØä Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉśļŖö ĻĄŁņåī-ĻĄ¼ņŚŁ ņ╣śļŻī(ņśłņ╗©ļīĆ Ļ░äļÅÖļ¦ź ĒÖöĒĢÖņāēņĀäņłĀ) ņŗ£ņŚÉļÅä BĒśĢĻ░äņŚ╝ ņ×¼ĒÖ£ņä▒ĒÖöĻ░Ć ņĀüņ¦Ć ņĢŖĻ▓ī ļéśĒāĆļé¼ņ£╝ļ»ĆļĪ£[20,21], ņ×¼ĒÖ£ņä▒ĒÖöņÖĆ Ļ┤ĆļĀ©ļÉ£ ņóģņ¢æņ¦łĒÖś ņ×Éņ▓┤ņØś Ļ░Éņłśņä▒ļÅä Ļ│ĀļĀżĒĢ┤ņĢ╝ĒĢĀ ļīĆņāüņØ┤ļŗż. ļśÉ Ļ░äņäĖĒżņĢöņóģņØś Ļ▓ĮņÜ░ņ▓śļ¤╝ Ļ░ÖņØĆ ņóģņ¢æņØ┤ļØ╝ ĒĢśļŹöļØ╝ļÅä ņłÖņŻ╝ņØś ļ®┤ņŚŁņ¢ĄņĀ£ļź╝ ļŹö Ļ░ĢĒĢśĻ▓ī ņ£ĀļÅäĒĢśļŖö ņĀäņŗĀĒĢŁņĢöņ╣śļŻīļŖö ĻĄŁņåīņ╣śļŻīļ│┤ļŗż ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒ņØ┤ ļŹö ĒØöĒĢ£ Ļ▓āņ£╝ļĪ£ ļéśĒāĆļé¼ļŗż[11,20,22]. ņĄ£ĻĘ╝ ļ░£Ēæ£ļÉ£ Ļ░äņäĖĒżņĢöņóģ ĒÖśņ×ÉļōżņØś ņ×äņāüņŚ░ĻĄ¼ļź╝ ļ│┤ļ®┤ ņ╣śļŻīņŚÉ ļö░ļźĖ ļ®┤ņŚŁņ¢ĄņĀ£ ņĀĢļÅäņÖĆ ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒ ņ£äĒŚśļÅäļŖö ļ╣äļĪĆĒĢśņśĆļŗż[19]. ņÜöņĢĮĒĢśļ®┤ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņŚÉņä£ Ļ░£ļ│äņĀüņØĖ ņ╣śļŻīņØĖņ×Éļź╝ Ļ│ĀļĀżĒĢśĻĖ░ļ│┤ļŗżļŖö ņäĖĒżļÅģņä▒ņ╣śļŻīņŚÉ ņØśĒĢ┤ ņ£ĀļÅäļÉ£ ņĀäļ░śņĀüņØĖ ņłÖņŻ╝ņØś ļ®┤ņŚŁņ¢ĄņĀ£ņāüĒā£ņØś ņĀĢļÅäņŚÉ ļö░ļØ╝ ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒ņØ┤ ļ░£ņāØĒĢĀ ņłś ņ׳ļŖö Ļ▓āņ£╝ļĪ£ ņØ┤ĒĢ┤ļÉśņ¢┤ņĢ╝ ĒĢ£ļŗż. ļīĆĒæ£ņĀüņØĖ ņśłļĪ£ Ļ░äņäĖĒżņĢöņóģņØä ļōż ņłś ņ׳ļŖöļŹ░ ņ╣śļŻīļĪ£ ņé¼ņÜ®ļÉśļŖö ņĢĮļ¼╝ņØś ņóģļźś, ņÜ®ļ¤ē, ĒĢŁņĢöņŻ╝ĻĖ░, ņĢĮļ¼╝ņŻ╝ņ×ģĻ▓ĮļĪ£, ļ│æĒĢ®ņ╣śļŻīņØś ņ£Āļ¼┤ ļō▒ņŚÉ ņØśĒĢ┤ ļŗżņ¢æĒĢ£ ļ╣äņ£©ļĪ£ ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒ņØ┤ ļéśĒāĆļé£ļŗż[8,11,18,20-24] (Table 2).
ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ ņŚ░ĻĄ¼Ļ▓░Ļ│╝ļōżņØä ļ│┤ļ®┤ ņóģņ¢æņ╣śļŻī ņżæ ļéśĒāĆļéśļŖö ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒ņØĆ ņ╣śļŻī ņĀä ļ░öņØ┤ļ¤¼ņŖżņØś ņ”ØņŗØņāüĒā£ņÖĆ ļ░ĆņĀæĒĢśĻ▓ī Ļ┤ĆļĀ©ļÉśņ¢┤ ņ׳ņØīņØä ņĢī ņłś ņ׳ļŗż. ņ”ē, ņ╣śļŻī ņĀä ļ░öņØ┤ļ¤¼ņŖżĻ░Ć ĒÖ£ļÅÖņä▒ ņāüĒā£ņŚÉ ņ׳ļŖö Ļ▓ĮņÜ░Ļ░Ć ļ╣äĒÖ£ļÅÖņä▒ ņāüĒā£ļ│┤ļŗż ņ×¼ĒÖ£ņä▒ņØś ļ╣łļÅäĻ░Ć Ēø©ņö¼ ļ¦ÄņĢśļŗż. ņĀ£ņŗ£ļÉ£ ļ░öņØ┤ļ¤¼ņŖż ņØĖņ×ÉļĪ£ļŖö HBeAg ņ¢æņä▒ņØĖ Ļ▓ĮņÜ░, HBV DNA 20,000 IU/mL ļśÉļŖö 2,000 IU/mL ņØ┤ņāüņØĖ Ļ▓ĮņÜ░ņŚÉņä£ ĻĘĖļĀćņ¦Ć ņĢŖņØĆ Ļ▓ĮņÜ░ļ│┤ļŗż ņ×¼ĒÖ£ņä▒ņØś ļ╣łļÅäĻ░Ć ļåÆņĢśļŗż[8,25,26]. ļśÉĒĢ£ BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖż ņ£ĀņĀäņ×Éļ│ĆņØ┤ ņ”ē, basal core promoter ļśÉļŖö precore ņśüņŚŁņØś ļ│ĆņØ┤Ļ░Ć ņ׳ņØä ļĢī ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØś ņĀĢļÅäĻ░Ć ļŹö ļåÆĻ│Ā ņŗ¼ĒĢśļŗżļŖö ļ│┤Ļ│ĀļÅä ņ׳ļŗż[27,28]. ņ£ĀņĀäņ×ÉĒśĢņ£╝ļĪ£ļŖö ļ╣äAĒśĢņØ╝ ļĢī ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØ┤ ĒśĖļ░£ĒĢśņśĆļŗż[29].
ņĄ£ĻĘ╝ Ļ░üņóģ ņןĻĖ░ņØ┤ņŗØņØ┤ ņĀÉņ░© ļ│┤ĒÄĖĒÖöļÉ©ņŚÉ ļö░ļØ╝ BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒ņØś ļ╣łļÅä ļśÉĒĢ£ ļŖśņ¢┤ļéśĻ│Ā ņ׳ļŖöļŹ░ ņØ┤ļŖö Ļ▒░ļČĆļ░śņØæņØä ņ¢ĄņĀ£ĒĢśĻĖ░ ņ£äĒĢ┤ Ēł¼ņŚ¼ĒĢśļŖö ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£ņØś ņé¼ņÜ®Ļ│╝ Ļ┤ĆļĀ©ļÉ£ļŗż. ņØ┤ņŗØ ņŗ£ ņé¼ņÜ®ĒĢśļŖö corticosteroid, calcineurin ņ¢ĄņĀ£ņĀ£, ĒĢŁļīĆņé¼ņĀ£, mTOR ņ¢ĄņĀ£ņĀ£ļōżņØĆ ļŗżņ¢æĒĢ£ ĻĖ░ņĀäņ£╝ļĪ£ ņłÖņŻ╝ņØś ļ®┤ņŚŁņäĖĒżņØś ĻĖ░ļŖźņØä ņ¢ĄņĀ£ņŗ£Ēé┤ņ£╝ļĪ£ņŹ© ļ░öņØ┤ļ¤¼ņŖż ņ”ØņŗØņØä ņ£ĀļÅäĒĢĀ ņłś ņ׳ļŗż. Ēśäņ×¼ ņ×äņāüņŚÉņä£ ņŗ£Ē¢ēļÉśĻ│Ā ņ׳ļŖö ņŚ¼ļ¤¼ ņןĻĖ░ņØ┤ņŗØ ņżæ ņĪ░Ēśłļ¬©ņäĖĒż ņØ┤ņŗØņØĆ BĒśĢĻ░äņŚ╝ ņ×¼ĒÖ£ņä▒ļźĀņØ┤ Ļ░Ćņן ļåÆņØĆ Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[2,12].
ņóģņ¢æ-ļ®┤ņŚŁņ¦łĒÖśņØś ņóģļźśļÅä ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒Ļ│╝ ņŚ░Ļ┤ĆļÉśņ¢┤ ņ׳ļŖöļŹ░, ņØ┤ ņżæ ĒśłņĢĪņĢöņØś Ļ▓ĮņÜ░ ņ×¼ĒÖ£ņä▒ņØś ļ╣łļÅäĻ░Ć ļåÆĻ│Ā, ĒŖ╣Ē׳ ļ”╝ĒöäņóģņØś Ļ▓ĮņÜ░ļŖö ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØś ļ╣łļÅä ļ░Å ņżæņ”ØļÅäĻ░Ć Ļ░Ćņן ņŗ¼ĒĢśļŗż. ņØ┤ļŖö ļ”╝Ēöäņóģ ĒÖśņ×ÉņØś Ļ▓ĮņÜ░ ņ╣śļŻīņĢĮņĀ£ņŚÉ ņØśĒĢ£ ņ×¼ĒÖ£ņä▒ ņ£ĀļÅäĻ░Ć ļåÆņØä ļ┐É ņĢäļŗłļØ╝ ņ¦łĒÖśņØś ĒŖ╣ņä▒ņāü Ļ│©ņłśĻĖ░ļŖź ļ░Å ļ®┤ņŚŁņäĖĒżņÖĆ Ļ┤ĆļĀ©ļÉśņ¢┤ ĒÖśņ×ÉņØś ļ®┤ņŚŁļŖźņØ┤ ņ¢┤ļŖÉņĀĢļÅä ņĀĆĒĢś ņāüĒā£ņŚÉ ņ׳ņ£╝ļ®░, HBsAg ļ│┤ņ£Āņ£©ņØ┤ ņĀĢņāüņØĖļ│┤ļŗż ļåÆļŗżļŖö ņĀÉ ļĢīļ¼ĖņØ┤ļŗż[2,17]. Ļ│ĀĒśĢņĢöņóģ ņżæņŚÉļŖö ņ£Āļ░®ņĢöņŚÉņä£ ņ×¼ĒÖ£ņä▒ ļ╣łļÅäĻ░Ć ļåÆņĢśļŖöļŹ░ ņ╣śļŻīļĪ£ ņé¼ņÜ®ļÉśļŖö ņĢĮņĀ£Ļ░Ć ļ╣äĻĄÉņĀü Ļ│ĀņÜ®ļ¤ēņØ┤ļØ╝ļŖö ņĀÉņØ┤ ņøÉņØĖņØ╝ ņłś ņ׳ļŗż[2,3].
ņĄ£ĻĘ╝ BņäĖĒż ņ×äĒīīņóģ, ļźśļ¦łĒŗ░ņŖż ņ¦łĒÖś ļō▒ņŚÉ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŖö Ēæ£ņĀüņ╣śļŻīņĀ£ļōżņØĆ ĒÖśņ×ÉņØś ņäĖĒżņä▒ ļ®┤ņŚŁņŚÉ ņ¦üņĀæņĀüņ£╝ļĪ£ ņ×æņÜ®ĒĢśņŚ¼ ņŗ¼Ļ░üĒĢ£ ņłśņżĆĻ╣īņ¦Ć ļ®┤ņŚŁļŖźņØä ļ¢©ņ¢┤ļ£©ļ”¼ļ»ĆļĪ£ ņ×äņāüņŚÉņä£ ņØ┤ Ļ░ÖņØĆ ņĢĮņĀ£ļź╝ ņé¼ņÜ®ĒĢśļŖö Ļ▓ĮņÜ░ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØ┤ ĒØöĒ׳ ļ░£ņāØĒĢĀ ņłś ņ׳ļŗżļŖö ņĀÉņØä ņŚ╝ļæÉņŚÉ ļæÉņ¢┤ņĢ╝ ĒĢ£ļŗż[30-32]. ņØ┤ ņżæ rituximabņØĆ B cell ļ¦łņ╗żņØĖ CD20ņŚÉ ļīĆĒĢ£ anti-CD20 monoclonal antibodyļĪ£ mature B cellņØä Ļ▒░ņØś ņÖäņĀäĒĢ£ ņłśņżĆņ£╝ļĪ£ Ļ▓░ĒĢŹņŗ£Ēé┤ņ£╝ļĪ£ņŹ© ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒ņØä ņ£ĀļÅäĒĢ£ļŗż[10]. ņØ┤ļŖö ĒŖ╣Ē׳ Ļ│╝Ļ▒░ BĒśĢĻ░äņŚ╝ņ£╝ļĪ£ ĒÜīļ│ĄļÉ£ HBsAg ņØīņä▒ņØĖ ĒÖśņ×ÉņŚÉņä£ļÅä ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØä ļ╣äĻĄÉņĀü ĒØöĒ׳ ņ£Āļ░£ĒĢśĻ│Ā ļĢīļĪ£ ņŗ¼Ļ░üĒĢ£ Ļ░äņåÉņāüņØä ņĢ╝ĻĖ░ĒĢśņŚ¼ ņé¼ļ¦ØņŚÉ ņØ┤ļź┤Ļ▓īĻ╣īņ¦Ć ĒĢśļŖö ņĢĮņĀ£ļĪ£ ņ×äņāüņĀüņ£╝ļĪ£ļŖö ņØ┤ņŚÉ ļīĆĒĢ£ ļīĆņ▒ģņØ┤ ņĀłņŗżĒ׳ ĒĢäņÜöĒĢśļŗż[31]. ņØ┤ ļ░¢ņŚÉļÅä TNF-╬▒ ņ¢ĄņĀ£ņĀ£ ļō▒ļÅä ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØä ņØ╝ņ£╝Ēé¼ ņłś ņ׳ļŗż[33].
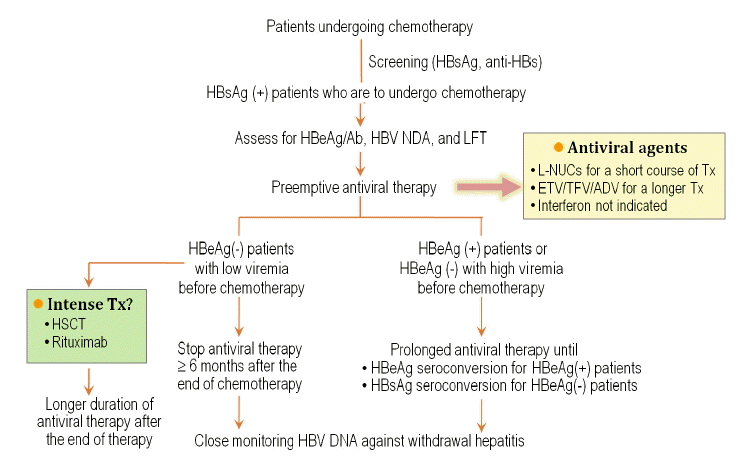
ļ®┤ņŚŁņ¢ĄņĀ£ ņ╣śļŻī ļśÉļŖö ĒĢŁņĢöņ╣śļŻī ņżæ ļ░£ņāØĒĢśļŖö ņ×¼ĒÖ£ņä▒ BĒśĢĻ░äņŚ╝ņØĆ Ļ▓░ĻĄŁ ļ░öņØ┤ļ¤¼ņŖż ņ”ØņŗØņŚÉņä£ ļ╣äļĪ»ļÉśļ»ĆļĪ£ ņ╣śļŻīņĀäļץ ņłśļ”ĮļÅä ĻČüĻĘ╣ņĀüņ£╝ļĪ£ ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ļź╝ ņĀüņĀłĒ׳ Ēł¼ņŚ¼ĒĢśļŖö Ļ▓āņØ┤ļŗż. BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖż ļ│┤ņ£Āņ×ÉņŚÉņä£ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØä ņśłļ░®ĒĢśļŖö ĒĢŁļ░öņØ┤ļ¤¼ņŖż ņ╣śļŻīņĀü ņĀæĻĘ╝ņØĆ ņĪ░ĻĖ░ņäĀņĀ£ņ╣śļŻī(early preemptive therapy)ņÖĆ ņ¦ĆņŚ░ņäĀņĀ£ņ╣śļŻī(deferred preemptive therapy) ļæÉ Ļ░Ćņ¦Ć ļ░®ļ▓Ģņ£╝ļĪ£ ļéśļłäņ¢┤ ļ│╝ ņłś ņ׳ļŗż. ņĪ░ĻĖ░ņäĀņĀ£ņ╣śļŻīļ▓ĢņØĆ BĒśĢĻ░äņŚ╝ ļ│┤ņ£Āņ×ÉņŚÉĻ▓ī ļ░öņØ┤ļ¤¼ņŖż ļåŹļÅäņŚÉ ņāüĻ┤ĆņŚåņØ┤ ĒĢŁņĢöņ╣śļŻī ņĀäļČĆĒä░ ĒĢŁļ░öņØ┤ļ¤¼ņŖż ņ╣śļŻīļź╝ ņŗ£ņ×æĒĢśļŖö Ļ▓āņØ┤Ļ│Ā, ņ¦ĆņŚ░ņäĀņĀ£ņ╣śļŻīļ▓ĢņØĆ ņ╣śļŻī ņĀäļČĆĒä░ ĒĢŁņĢöņ╣śļŻīņŻ╝ĻĖ░ ļÅÖņĢł ļ░öņØ┤ļ¤¼ņŖżļåŹļÅä Ļ▓Ćņé¼ļź╝ ņ¦ĆņåŹņĀüņ£╝ļĪ£ ļ®┤ļ░ĆĒĢśĻ▓ī ņŗ£Ē¢ēĒĢśņŚ¼ ņĢäņ¦ü Ļ░äņŚ╝ņØ┤ ļ░£ņāØĒĢśĻĖ░ ņĀä ļ░öņØ┤ļ¤¼ņŖż ņ”ØņŗØņāüĒā£ņŚÉņä£ ņĀüņŗ£ņŚÉ ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ļź╝ Ēł¼ņŚ¼ĒĢśņŚ¼ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØä ņ¢ĄņĀ£ĒĢśļĀżļŖö ņĀäļץņØ┤ļŗż.
ņØ┤ ļæÉ Ļ░Ćņ¦Ć ņżæ ņ¦ĆņŚ░ņäĀņĀ£ņ╣śļŻīļ▓ĢņØ┤ ļ│┤ļŗż ĒĢ®ļ”¼ņĀüņØ┤Ļ│Ā Ļ│╝ĒĢÖņĀüņØ╝ ņłś ņ׳ļŖö ņĀäļץņØ┤ņ¦Ćļ¦ī ņ×äĒīīņóģņØä ļīĆņāüņ£╝ļĪ£ ĒĢ£ ļ¼┤ņ×æņ£ä ļīĆņĪ░ ņŚ░ĻĄ¼ņØś Ļ▓░Ļ│╝ļź╝ ļ│┤ļ®┤ ņĪ░ĻĖ░ņäĀņĀ£ ņ╣śļŻīņĀäļץņØ┤ ņ¦ĆņŚ░ņäĀņĀ£ ņ╣śļŻīņĀäļץļ│┤ļŗż ņ£ĀņØśĒĢśĻ▓ī ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØä ņ¢ĄņĀ£ĒĢśņśĆļŗż[7]. ņØ┤ļŖö ņ¦ĆņŚ░ ņäĀņĀ£ ņ╣śļŻīņØś Ļ▓ĮņÜ░ ņĄ£ņ┤ł ļ░öņØ┤ļ¤¼ņŖż ņ”ØņŗØņŗ£ĻĖ░ļČĆĒä░ Ļ░äņŚ╝ļ░£ņāØĻ╣īņ¦ĆņØś ņŗ£Ļ░äņĀü ņ░©ņØ┤Ļ░Ć 2-4ņŻ╝ļĪ£ ņ¦¦ņĢä ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ļź╝ Ēł¼ņŚ¼ĒĢ┤ņä£ ņĢĮļ¼╝ņØ┤ ņ×æņÜ®ĒĢśļŖö ļŹ░ Ļ▒Ėļ”¼ļŖö ņŗ£Ļ░äņ░©ņŚÉ ņØśĒĢ┤ Ļ░äņŚ╝ņØ┤ ļ░£ņāØĒĢĀ ņłś ņ׳ĻĖ░ ļĢīļ¼ĖņØĖļŹ░, ņØ┤ļĢī Ļ▓ĮņÜ░ņŚÉ ļö░ļØ╝ņä£ļŖö Ļ░äļČĆņĀä, ņé¼ļ¦ØĻ╣īņ¦Ć ņØ┤ļź╝ ņłś ņ׳Ļ│Ā, ļśÉ ĒĢŁņĢöņ╣śļŻī ļō▒ņØ┤ ņŚ░ĻĖ░ļÉĀ ņłś ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ ĒÖśņ×ÉņØś ņ×äņāüĻ▓ĮĻ│╝ņŚÉ ņŗ¼Ļ░üĒĢ£ ņĢģņśüĒ¢źņØä ļü╝ņ╣Ā ņłś ņ׳ļŗżļŖö ņĀÉņØ┤ ņĢĮņĀÉņ£╝ļĪ£ ņ×æņÜ®ĒĢśĻ│Ā ņ׳ļŗż.
ļö░ļØ╝ņä£ ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØä ņ¢ĄņĀ£ĒĢśĻĖ░ ņ£äĒĢ┤ņä£ļŖö ĒĢŁņĢöņ╣śļŻī ņĀäļČĆĒä░ ņäĀņĀ£ņĀüņ£╝ļĪ£ ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ļź╝ Ēł¼ņŚ¼ĒĢ©ņØä ņøÉņ╣Öņ£╝ļĪ£ ĒĢśĻ│Ā ņ׳ļŗż[34]. ņóģņ¢æ-ļ®┤ņŚŁņ╣śļŻī ņŗ£ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØä ņ¢ĄņĀ£ĒĢśĻĖ░ ņ£äĒĢ£ ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ ņ╣śļŻīņŚÉ Ļ┤ĆĒĢśņŚ¼ ņ¦ĆĻĖłĻ╣īņ¦Ć ļæÉĻ░£ņØś ļ¼┤ņ×æņ£äņŚ░ĻĄ¼ļź╝ ĒżĒĢ©ĒĢ£ ļ¬©ļōĀ ņŚ░ĻĄ¼Ļ▓░Ļ│╝ņŚÉņä£ ņØ┤ļ¤¼ĒĢ£ ņĪ░ĻĖ░ ņäĀņĀ£ņĀü ĒĢŁļ░öņØ┤ļ¤¼ņŖż ņ╣śļŻīļ▓ĢņØĆ ĒÜ©Ļ│╝ņĀüņ£╝ļĪ£ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØä ņ¢ĄņĀ£ĒĢĀ ņłś ņ׳ņØīņØ┤ ļ░ØĒśĆņĪīļŗż[7,8,35-40] (Table 3). ļö░ļØ╝ņä£ Ēśäņ×¼ ņØ┤ņÖĆ Ļ┤ĆļĀ©ļÉ£ ĻĄŁļé┤ņÖĖ ņ×äņāüņ╣śļŻī ņ¦Ćņ╣©ņØĆ ĒĢŁņĢöņ╣śļŻī ļ░Å ļ®┤ņŚŁņ¢ĄņĀ£ņ╣śļŻīļź╝ Ļ│äĒÜŹĒĢśĻ│Ā ņ׳ļŖö ļ¬©ļōĀ ļ¦īņä▒ BĒśĢĻ░äņŚ╝ ļ│┤ņ£Āņ×ÉņŚÉņä£ ņ╣śļŻī ņĀä ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ļź╝ ņäĀņĀ£ņ╣śļŻīĒĢśļÅäļĪØ ĻČīĻ│ĀĒĢśĻ│Ā ņ׳ļŗż[41-43]. ļŗżļ¦ī ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ ņżæ ņØĖĒä░ĒÄśļĪĀ ņĀ£ņĀ£ļŖö ņ×æņÜ®ņŗ£Ļ░ä, ļČĆņ×æņÜ®ņØś ļ░£ņāØ, ļ░śņØæņä▒ņØ┤ļ¢©ņ¢┤ņ¦ĆļŖö ļ¼ĖņĀ£ņĀÉ ļō▒ņ£╝ļĪ£ ĒÜ©ļŖźņØä ĻĖ░ļīĆĒĢĀ ņłś ņŚåņ¢┤ Ļ▓ĮĻĄ¼ņÜ® ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ļź╝ Ēł¼ņŚ¼ĒĢ┤ņĢ╝ ĒĢ£ļŗż. ņśłļ░®ņĀü ļśÉļŖö ņäĀņĀ£ņĀü ĒĢŁļ░öņØ┤ļ¤¼ņŖż ņ╣śļŻīņŚÉ Ļ┤ĆĒĢ£ ļ╣äĻĄÉņ×äņāüņŚ░ĻĄ¼ļŖö Ļ▒░ņØś ļØ╝ļ»ĖļČĆļöśņŚÉ ĻĄŁĒĢ£ļÉśņ¢┤ ņ׳ņ£╝ļ»ĆļĪ£ Ēæ£ 3ņŚÉņä£ļŖö ņØ┤ņŚÉ ļīĆĒĢ£ ņ×ÉļŻīļ¦īņØä ņÜöņĢĮĒĢśņśĆļŗż. ļŗżļźĖ Ļ▓ĮĻĄ¼ņÜ® ņĢĮņĀ£ļōżņØś ļ╣äĻĄÉņ×äņāüņŚ░ĻĄ¼ ņ×ÉļŻīļŖö ļČĆņĪ▒ĒĢśņ¦Ćļ¦ī ņĢĮļ¼╝ņØś ĒÜ©ļŖź, ņ£ĀņĀäņ×É ņןļ▓Į ļō▒ņØä Ļ│ĀļĀżĒĢĀ ļĢī ņŚöĒģīņ╣┤ļ╣äņ¢┤, ĒģīļģĖĒżļ╣äņ¢┤ ļō▒ņØś ņĢĮņĀ£ļōżļÅä ļØ╝ļ»ĖļČĆļöśĻ│╝ ļÅÖļō▒ĒĢśĻ▒░ļéś ĻĘĖ ņØ┤ņāüņØś ņäĀņĀ£ņ╣śļŻīĒÜ©Ļ│╝ļź╝ ļ│┤ņØ╝ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖżņØś ņ×¼ĒÖ£ņä▒ņØä ņ¢ĄņĀ£ĒĢśĻĖ░ ņ£äĒĢ┤ņä£ļŖö ņśłļ░®ņØ┤ ņżæņÜöĒĢśļ»ĆļĪ£ ĒĢŁņĢö-ļ®┤ņŚŁņ¢ĄņĀ£ņ╣śļŻīļź╝ Ļ│äĒÜŹĒĢśĻ│Ā ņ׳ļŖö ļ¬©ļōĀ ĒÖśņ×ÉņŚÉņä£ ņ╣śļŻī ņĀä BĒśĢĻ░äņŚ╝ Ēæ£ņ¦Ćņ×É ņ”ē, HBsAg, anti-HBs, anti-HBcļź╝ Ļ▓Ćņé¼ĒĢ┤ņĢ╝ ĒĢ£ļŗż. ļ¦īņĢĮ HBsAg ņ¢æņä▒ņØĖ ĒÖśņ×ÉņØś Ļ▓ĮņÜ░ ĒĢŁņĢöņ╣śļŻī ņĀüņ¢┤ļÅä 1ņŻ╝ņØ╝ ņĀäņŚÉ ņäĀņĀ£ņĀü ĒĢŁļ░öņØ┤ļ¤¼ņŖż ņ╣śļŻīļź╝ ņŗ£ņ×æĒĢśļŖö Ļ▓āņØ┤ ņĀüņĀłĒĢśļŗż[34] (Fig. 3). ņØ┤ņÖĆ Ļ░ÖņØĆ ņĀäļץņØĆ ņĢäļ¼┤ļ”¼ Ļ░ĢļĀźĒĢ£ ļ®┤ņŚŁņ¢ĄņĀ£ņ╣śļŻīņØś Ļ▓ĮņÜ░ļØ╝ļÅä ņäĀņĀ£ņĀüņ£╝ļĪ£ ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ļź╝ Ēł¼ņŚ¼ĒĢśļ®┤ ĒÜ©Ļ│╝ņĀüņ£╝ļĪ£ Ļ░äņŚ╝ņØä ņ¢ĄņĀ£ĒĢĀ ņłś ņ׳ļŗżļŖö ņŚ░ĻĄ¼Ļ▓░Ļ│╝ļōżņŚÉ ĻĖ░ļ░śĒĢ£ļŗż. ĻĘĖļÅÖņĢł ņäĀņĀ£ņĀü ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ Ēł¼ņŚ¼ņŚÉ Ļ┤ĆĒĢ£ ņ×ÉļŻīļōżņØĆ Ļ▒░ņØś ļØ╝ļ»ĖļČĆļöśņŚÉ ĻĄŁĒĢ£ļÉśņ¢┤ ņ׳ļŖöļŹ░ ņןĻĖ░ Ēł¼ņŚ¼Ļ░Ć ĒĢäņÜöĒĢĀ Ļ▓ĮņÜ░ ļØ╝ļ»ĖļČĆļöśņØĆ ļé┤ņä▒ņØ┤ ļ¼ĖņĀ£Ļ░Ć ļÉśļ»ĆļĪ£ ļé┤ņä▒ ņ£äĒŚśļÅäĻ░Ć ņĀüņØĆ ņŚöĒģīņ╣┤ļ╣äņ¢┤, ĒģīļģĖĒżļ╣äņ¢┤ ļō▒ņØ┤ ņĀüņĀłĒĢ£ ņäĀĒāØņØ┤ ļÉĀ Ļ▓āņØ┤ļŗż. ĻĘĖļĀćņ¦Ćļ¦ī ĒĢŁņĢö-ļ®┤ņŚŁņ¢ĄņĀ£ ņ╣śļŻīĻĖ░Ļ░äņØ┤ 1ļģäņØ┤ļé┤ļĪ£ ņ¦¦ņØä Ļ▓ĮņÜ░ļŖö ņŚ¼ņĀäĒ׳ ĒĢĄņé░ņ£ĀļÅäņ▓┤(ļØ╝ļ»ĖļČĆļöś, Ēģöļ╣äļČĆļöś, Ēü┤ļĀłļČĆļöś)ļź╝ ņäĀĒāØĒĢĀ ņłś ņ׳ļŗż[41].
ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØś ņśłļ░®ļ¬®ņĀüņ£╝ļĪ£ Ēł¼ņŚ¼ĒĢ£ ņäĀņĀ£ņĀü ĒĢŁļ░öņØ┤ļ¤¼ņŖż ņ╣śļŻīļź╝ ņ¢ĖņĀ£ ņóģĻ▓░ĒĢ┤ņĢ╝ ĒĢśļŖöĻ░ĆņŚÉ ļīĆĒĢ£ ļ¬ģĒÖĢĒĢ£ ĒĢ®ņØśņĀÉņØĆ ņŚåļŖö ņŗżņĀĢņØ┤ļŗż. ņØ┤ļŖö ĻĘĖ ļÅÖņĢłņØś ņŚ░ĻĄ¼Ļ░Ć ņäĀņĀ£ņĀü ņ╣śļŻīņ£Āļ¼┤ ĻĘĖ ņ×Éņ▓┤ņØś ĒÜ©ļŖźņŚÉ ņ┤łņĀÉņØä ļæÉņŚłĻĖ░ ļĢīļ¼ĖņØ┤Ļ│Ā, ņóģĻ▓░ņŗ£ņĀÉņØä ļČäņäØĒĢ£ ņśłļŖö Ļ▒░ņØś ņŚåņŚłĻĖ░ ļĢīļ¼ĖņØ┤ļŗż. ļīĆļČĆļČäņØś ņ┤łĻĖ░ ņŚ░ĻĄ¼ņØś ņ×ÉļŻīļōżņØĆ ĒĢŁņĢöņ╣śļŻī ņóģĻ▓░ Ēøä 3-6Ļ░£ņøö ņĀĢļÅäļź╝ ņ£Āņ¦ĆĻĖ░Ļ░äņ£╝ļĪ£ ĒĢśņśĆļŖöļŹ░ ņØ┤ļĢī ļ¦ÄņØĆ Ļ▓ĮņÜ░ņŚÉņä£ ņĢĮņĀ£ņżæļŗ© ņØ┤Ēøä ļ░öņØ┤ļ¤¼ņŖżĻ░Ć ļŗżņŗ£ reboundĒĢśļ®░ withdrawal hepatitisĻ░Ć ļ░£ņāØĒĢśĻ▓ī ļÉśņŚłļŗż. ņØ┤ļŖö ņĢäļ¦łļÅä ĒĢŁņĢöņ╣śļŻī ņóģĻ▓░ Ēøä ņĢĮņĀ£ ņ£Āņ¦ĆĻĖ░Ļ░äņØ┤ ņ¦¦ņĢä ņłÖņŻ╝ņØś ļ®┤ņŚŁņØ┤ ņĢäņ¦ü ņČ®ļČäĒ׳ ĒÜīļ│ĄļÉśņ¦Ć ņĢŖņØĆ ņāüĒā£ņŚÉņä£ ņĢĮņĀ£ņżæļŗ© Ēøä ņ¢ĄņĀ£ļÉśņ¦Ć ņĢŖņØĆ ļ░öņØ┤ļ¤¼ņŖżņØś ņ”ØņŗØņä▒ņØ┤ ļŗżņŗ£ ņé┤ņĢäļéśĻĖ░ ļĢīļ¼Ėņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
ņóģņ¢æņ╣śļŻī Ēøä ļ®┤ņŚŁļŖź ņĀĆĒĢśĻ░Ć Ļ│╝ņŚ░ ņ¢╝ļ¦łĻ░ä ņ£Āņ¦ĆļÉśļŖö Ļ░ĆņŚÉ Ļ┤ĆĒĢ£ ņŚ░ĻĄ¼ļŖö ļČĆņĪ▒ĒĢśņ¦Ćļ¦ī ļ¬ćļ¬ć ņŚ░ĻĄ¼ļōżņŚÉ ņØśĒĢśļ®┤ ĒĢŁņĢöņ╣śļŻīņŚÉ ņØśĒĢ┤ TņäĖĒż, BņäĖĒż, plasma cell, natural killer cell ļō▒ ļ®┤ņŚŁĻ┤ĆļĀ©ņäĖĒżļōżņØĆ ņłśļ┐É ņĢäļŗłļØ╝ ĻĖ░ļŖźĻ╣īņ¦ĆļÅä ņåÉņāüļÉśĻ│Ā ņØ┤ļ¤¼ĒĢ£ ļ®┤ņŚŁĻ▓░ĒĢŹĒśäņāüņØĆ ņ╣śļŻī ņóģĻ▓░ Ēøä 6-12Ļ░£ņøöĻ╣īņ¦ĆļÅä ņ¦ĆņåŹļÉ£ļŗż[44,45]. ļśÉĒĢ£ ņ╣śļŻīņØś Ļ░ĢļÅäĻ░Ć Ļ░ĢĒĢĀņłśļĪØ ļ®┤ņŚŁĻĖ░ļŖźņĀĆĒĢśĻ░Ć ļŹö ļÜ£ļĀĘĒĢśĻ▓ī ļÉ£ļŗż[45]. ņØ┤ņĀÉņØä Ļ│ĀļĀżĒĢĀ ļĢī ņäĀņĀ£ņĀü ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ņØś ņĪ░ĻĖ░ņóģļŻīļĪ£ ļ¦Éļ»ĖņĢöņĢä withdrawal hepatitis ļ░£ņāØņØś Ļ░£ņŚ░ņä▒ņØĆ ņČ®ļČäĒ׳ ņĪ┤ņ×¼ĒĢ£ļŗż. ņØ┤ņŚÉ ļīĆĒĢ£ ņÜöņØĖ ņżæ ĒĢśļéśļĪ£ ņ╣śļŻī ņĀä BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖżņØś ņ”ØņŗØņāüĒā£Ļ░Ć Ļ┤ĆļĀ©ņØĖņ×ÉļĪ£ ņĀ£ņŗ£ļÉśņŚłļŗż. ņ”ē, ņ╣śļŻī ņĀä ļ░öņØ┤ļ¤¼ņŖżĻ░Ć ņ”ØņŗØņāüĒā£ņØ╝ ļĢī(HBV DNA > 2,000 IU/mLņØ╝ Ļ▓ĮņÜ░) withdrawal hepatitisĻ░Ć ļŹö ĒØöĒĢśņśĆļŗż[46]. ĻĘĖļ¤¼ļ»ĆļĪ£ ĒĢŁņĢöņ╣śļŻī ņĀä ļ░öņØ┤ļ¤¼ņŖż ĒÅēĻ░ĆņŚÉņä£ HBV DNA > 2,000 IU/mLņØ┤ļ®┤ ņäĀņĀ£ņĀü ĒĢŁļ░öņØ┤ļ¤¼ņŖż ņ╣śļŻīļź╝ ĒĢŁņĢöņ╣śļŻī ņóģĻ▓░ Ēøä ņןĻĖ░Ļ░ä Ēł¼ņŚ¼ĒĢ┤ņĢ╝ ĒĢśļ®░, ļīĆĻ░£ ļ¦īņä▒ BĒśĢĻ░äņŚ╝ ņ╣śļŻīņØś ņØ╝ļ░śņĀü ņóģļŻī ņŗ£ņĀÉņŚÉ ļÅäļŗ¼ĒĢĀ ļĢīĻ╣īņ¦Ć ņ£Āņ¦ĆĒĢśļŖö Ļ▓āņØ┤ ņČöņ▓£ļÉ£ļŗż[41] (Fig. 3). ĻĘĖļĀćņ¦Ćļ¦ī ļ░öņØ┤ļ¤¼ņŖż ņāüĒā£Ļ░Ć ļ®┤ņŚŁĻ┤ĆņÜ®ĻĖ░ņØ╝ Ļ▓ĮņÜ░ ņ╣śļŻīņóģļŻī ņŗ£ņĀÉņØ┤ ļ¦żņÜ░ ņןĻĖ░Ļ░äņØ┤ ļÉĀ ņłśļÅä ņ׳ņ£╝ļ»ĆļĪ£ ĒÖśņ×ÉļōżņØś ņ╣śļŻī ņĀä ļ░öņØ┤ļ¤¼ņŖż ņāüĒā£, ĻĖ░ņĀĆ Ļ░äņ¦łĒÖś ņāüĒā£ ļ░Å BĒśĢĻ░äņŚ╝ņØś ņ×ÉņŚ░Ļ▓ĮĻ│╝ ņŗ£ņĀÉņØä Ļ│ĀļĀżĒĢśņŚ¼ ņóģļŻī ņŗ£ņĀÉņØä ņĀüņĀłĒ׳ ĒīÉļŗ©ĒĢ┤ņĢ╝ ĒĢĀ Ļ▓āņ£╝ļĪ£ ņāØĻ░üĒĢ£ļŗż.
ņĄ£ĻĘ╝ ņ¦łĒÖśņŚÉ ļīĆĒĢ£ ļČäņ×ÉņāØļ¼╝ĒĢÖņĀüņØĖ ĻĖ░ņĀäņØś ņŚ░ĻĄ¼Ļ░Ć Ļ░ĆņåŹĒÖö ļÉśļ®┤ņä£ Ļ░üņóģ ņóģņ¢æ-ļ®┤ņŚŁņ¦łĒÖśņØś Ēæ£ņĀüņ╣śļŻīņĀ£ļĪ£ ĒŖ╣ņĀĢĒĢŁņøÉņŚÉ ļīĆĒĢ£ ļŗ©ņØ╝Ēü┤ļĪĀĒĢŁņ▓┤Ļ░Ć ņ×äņāüņŚÉ ņØæņÜ®ļÉśĻ│Ā ņ׳ļŗż. ņØ┤ļōżņØĆ ņŻ╝ļĪ£ ļ”╝ĒöäĻĄ¼ Ļ┤ĆļĀ© ņ¦łĒÖś, ļźśļ¦łĒŗ░ņŖż ņ¦łĒÖś, ņŚ╝ņ”Øņä▒ņן ņ¦łĒÖś ļō▒ņŚÉņä£ ņØ┤ņÜ®ļÉśļŖö Ļ▓āņ£╝ļĪ£ rituximab, alemtuzumab, anti-TNF-╬▒ inhibitors(infliximab, etanercept, adalimumab) ļō▒ņØ┤ ņ׳ļŗż. ņØ┤ ņżæ rituximabņØĆ Bļ”╝ĒöäĻĄ¼ņØś ĒĢŁņøÉņØĖ CD20ņŚÉ ļīĆĒĢ£ ļŗ©ņØ╝Ēü┤ļĪĀĒĢŁņ▓┤ļĪ£ ņłÖņŻ╝ņØś ļ®┤ņŚŁņäĖĒżņØś ņłś ļ░Å ĻĖ░ļŖźņØä ņāüļŗ╣ĒĢ£ ņłśņżĆņ£╝ļĪ£ Ļ▓░ĒĢŹņŗ£Ēéżļ®░ BĒśĢĻ░äņŚ╝ņØś ņ×¼ĒÖ£ņä▒ņØä ĒØöĒ׳ ņØ╝ņ£╝ĒéżļŖö ļīĆĒæ£ņĀüņØĖ ņĢĮņĀ£ņØ┤ļŗż. RituximabņØä ņĢģņä▒ļ”╝Ēöäņóģ ĒÖśņ×ÉņŚÉĻ▓ī Ēł¼ņŚ¼ ĒĢśņśĆņØä ļĢī HBsAg ņ¢æņä▒ņØĖ ĒÖśņ×ÉņŚÉņä£ 80%, HBsAg ņØīņä▒ņØĖ ĒÖśņ×ÉņŚÉņä£ 12.2-23.8%ņØś BĒśĢĻ░äņŚ╝ ņ×¼ĒÖ£ņä▒ņØ┤ ļ│┤Ļ│ĀļÉśņŚłļŗż[30-32]. TNF-╬▒ļŖö ņāØļ¼╝ĒĢÖņĀüņ£╝ļĪ£ BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖżņØś ļ®┤ņŚŁļ│æļ”¼, ļ░öņØ┤ļ¤¼ņŖż ņĀ£Ļ▒░ņŚÉ Ļ┤ĆņŚ¼ĒĢśļŖö ņŗĖņØ┤ĒåĀņ╣┤ņØĖņ£╝ļĪ£ ņØ┤ņŚÉ ļīĆĒĢ£ ļŗ©ņØ╝Ēü┤ļĪĀĒĢŁņ▓┤ ņ╣śļŻī ņŗ£ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØ┤ ļ░£ņāØĒĢĀ ņłś ņ׳ļŗż. TNF-╬▒ ņ¢ĄņĀ£ņĀ£ ņżæ infliximabņŚÉ ļīĆĒĢ£ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ ņé¼ļĪĆĻ░Ć Ļ░Ćņן ļ¦ÄĻ│Ā, etanerceptņÖĆ adalimumabņØĆ infliximab ļ│┤ļŗżļŖö ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØś ļ╣łļÅäĻ░Ć ņĀüļŗżĻ│Ā ļ│┤Ļ│ĀļÉśņŚłļŗż[33]. ĻĘĖļĀćņ¦Ćļ¦ī TNF-╬▒ Ļ┤ĆļĀ© ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØś ļ│┤Ļ│ĀļŖö ņé░ļ░£ņĀüņ£╝ļĪ£ ņØ┤ļŻ©ņ¢┤ņ¦ä ņ”ØļĪĆņ£äņŻ╝ņØś ļ│┤Ļ│ĀĻ░Ć ļ¦ÄņĢä ņäĀņĀ£ņĀü ĒĢŁļ░öņØ┤ļ¤¼ņŖż ņ╣śļŻīņØś ņØ┤ļōØņØä ļÜ£ļĀĘņØ┤ ņ×ģņ”ØĒĢĀļ¦īĒĢ£ ņŗĀļó░ņä▒ ņ׳ļŖö ļīĆĻĘ£ļ¬© ņ×ÉļŻīņØś Ļ▓░Ļ│╝Ļ░Ć ĒĢäņÜöĒĢśļŗż.
ĒĢŁņĢöņ╣śļŻī ņĀä ļ░öņØ┤ļ¤¼ņŖż Ēæ£ņ¦Ćņ×É Ļ▓Ćņé¼ņŚÉņä£ HBsAgņØīņä▒ (+/- anti-HBs), anti-HBc ņ¢æņä▒ņØĖ Ļ▓ĮņÜ░ļŖö ņ×Āņ×¼ Ļ░ÉņŚ╝ ļśÉļŖö Ļ│╝Ļ▒░ Ļ░ÉņŚ╝ņ£╝ļĪ£ļČĆĒä░ ĒÜīļ│ĄļÉ£ Ļ▓ĮņÜ░ļź╝ ņØśļ»ĖĒĢ£ļŗż. ņĄ£ĻĘ╝ ņØ╝ļĀ©ņØś ļ│┤Ļ│ĀļōżņŚÉ ņØśĒĢśļ®┤ ņØ┤ļ¤¼ĒĢ£ HBsAg ņØīņä▒ ĒÖśņ×ÉņŚÉņä£ļÅä ņāüļīĆņĀüņ£╝ļĪ£ ņĀüņØĆ ļ╣łļÅäņØ┤ņ¦Ćļ¦ī BĒśĢĻ░äņŚ╝ņØś ņ×¼ĒÖ£ņä▒ņØ┤ ļ░£ņāØĒĢśļ®░(3-4%) [9,30], HBsAg ņØīņä▒ņØś ņ×¼ĒÖ£ņä▒Ļ░äņŚ╝ņØĆ ņśżĒ׳ļĀż HBsAg ņ¢æņä▒ņØĖ Ļ▓ĮņÜ░ļ│┤ļŗż Ļ░äļČĆņĀä, ņé¼ļ¦Ø ļō▒ņØ┤ ļŹö ĒØöĒĢ£ Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳ļŗż[12]. ļö░ļØ╝ņä£ ņØ┤ ĒÜīļ│ĄļÉ£ Ļ░äņŚ╝ ĒÖśņ×ÉĻĄ░ ļśÉļŖö ņ×Āņ×¼Ļ░ÉņŚ╝ ĒÖśņ×ÉĻĄ░ņŚÉņä£ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØä ņ¢ĄņĀ£ĒĢĀ ļīĆņ▒ģņØ┤ ņÜöĻĄ¼ļÉ£ļŗż.
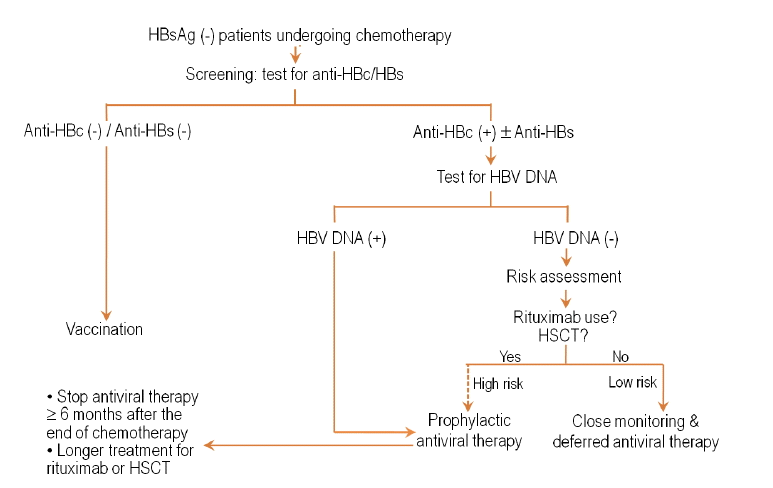
HBsAg ņØīņä▒ ĒÖśņ×ÉņŚÉņä£ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØ┤ ļ░£ņāØĒĢśļŖö ĒØöĒĢ£ ņÜöņØĖņ£╝ļĪ£ļŖö ļīĆĻ░£ anti-HBc (+)/anti-HBs (-)ņØĖ Ļ▓ĮņÜ░, ņ╣śļŻīņĢĮņĀ£ļĪ£ rituximabņØä ņé¼ņÜ®ĒĢ£ Ļ▓ĮņÜ░, ņĪ░Ēśłļ¬©ņäĖĒż ņØ┤ņŗØņØś Ļ▓ĮņÜ░ņ▓śļ¤╝ Ļ░ĢļĀźĒĢ£ ņäĖĒżļÅģņä▒ņ╣śļŻīļź╝ ļ░øļŖö Ļ▓ĮņÜ░ļōżļĪ£, ņĄ£ĻĘ╝ ļ│┤Ļ│ĀņŚÉ ņØśĒĢśļ®┤ rituximabņØä ĒżĒĢ©ĒĢ£ R-CHOP (rituximab, cyclophosphamide, doxorubicin, vincristine, prednisolone)ņ£╝ļĪ£ ņ╣śļŻīļ░øļŖö B cell lymphomaņØś Ļ▓ĮņÜ░ HBsAg ņØīņä▒ ĒÖśņ×ÉņØś 12.2-23.8%ņŚÉņä£ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØ┤ ļ░£ņāØĒĢśņśĆļŗż[30,31]. ļö░ļØ╝ņä£ HBsAg ņØīņä▒ņØ┤ļØ╝ ĒĢĀņ¦ĆļØ╝ļÅä ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒ņØś Ļ│Āņ£äĒŚśĻĄ░ņØ╝ Ļ▓ĮņÜ░[ņĪ░Ēśłļ¬©ņäĖĒż ņØ┤ņŗØ, rituximab, anti-HBc (+)/anti-HBs (-) ļō▒]ļŖö ņśłļ░®ņĀü ĒĢŁļ░öņØ┤ļ¤¼ņŖż ņ╣śļŻīļź╝ Ļ│ĀļĀżĒĢ┤ ļ│╝ ņłś ņ׳ļŗż(Fig. 4). ļŗżļ¦ī HBsAg ņØīņä▒ ĒÖśņ×ÉņØś Ļ▓ĮņÜ░ HBsAg ņ¢æņä▒ ĒÖśņ×ÉņŚÉ ļ╣äĒĢ┤ ĒĢŁņĢöņ╣śļŻī ņŗ£ņ×æņŗ£ņĀÉļČĆĒä░ ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒Ļ╣īņ¦Ć Ļ▒Ėļ”¼ļŖö ņŗ£Ļ░äĻ│╝ ļ░öņØ┤ļ¤¼ņŖż ņ×¼ĒÖ£ņä▒ļČĆĒä░ Ļ░äņŚ╝ņØś ļ░£ņāØņŗ£ņĀÉĻ╣īņ¦Ć ņŗ£Ļ░äņŻ╝ĻĖ░Ļ░Ć ĻĖĖĻ▓īļŖö ņłśĻ░£ņøöļĪ£ ļ╣äĻĄÉņĀü ĻĖĖņ¢┤ ĒĢŁņĢöņ╣śļŻī ņżæ ļ░öņØ┤ļ¤¼ņŖż ņāüĒā£ļź╝ ļ®┤ļ░ĆĒ׳ Ļ▓Ćņé¼ĒĢśļ®┤ņä£ ļ░öņØ┤ļ¤¼ņŖż ņ”ØĻ░ĆĻ░Ć ļéśĒāĆļéśĻ│Ā ņĢäņ¦ü Ļ░äņŚ╝ņØ┤ ļ░£ņāØĒĢśņ¦Ć ņĢŖņØĆ ņŗ£ĻĖ░ņŚÉ ņ”ēņŗ£ ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ļź╝ Ēł¼ņŚ¼ĒĢśļŖö ņ¦ĆņŚ░ņ╣śļŻī(deferred therapy) ņĀäļץļÅä Ļ│ĀļĀżĒĢ┤ ļ│╝ ņłś ņ׳ņ£╝ļéś ļ╣äņÜ®-ļīĆļ╣äĒÜ©Ļ│╝, Ļ░äņŚ╝ņØ┤ ņŗżņĀ£ļĪ£ ļ░£ņāØĒ¢łņØä Ļ▓ĮņÜ░ ņé¼ņĢłņØś ņżæļīĆņä▒ ļō▒ņØä ĒĢ©Ļ╗ś Ļ│ĀļĀżĒĢ┤ņä£ Ļ▓░ņĀĢĒĢ┤ņĢ╝ ĒĢ£ļŗż.
Ļ┤ĆļĀ©ņ×ÉļŻīļōżņŚÉ ņØśĒĢśļ®┤ rituximabņØä ņé¼ņÜ®Ē¢łņØä ļĢī ņłÖņŻ╝ņØś ļ®┤ņŚŁļŖź ĒÜīļ│ĄĻ╣īņ¦ĆņØś ņŗ£Ļ░äņØĆ Ļ│ĀņŗØņĀü ĒĢŁņĢöņ╣śļŻīļ│┤ļŗż ĻĖĖļ®░ ļīĆĻ░£ 6-12Ļ░£ņøöņØ┤ ņåīņÜöļÉśļ®░, ņĪ░Ēśłļ¬©ņäĖĒżņØ┤ņŗØņØĆ ņØ┤ļ│┤ļŗż ļŹö ļŖ”Ļ▓ī ĒÜīļ│ĄĒĢśņŚ¼ ņØ┤ņŗØ Ēøä 1-3ļģäņ¦Ė Ēæ£ļ®┤ĒĢŁņ▓┤ņØś ņŚŁĻ░ĆĻ░Ć Ļ░ÉņåīĒĢśĻĖ░ ņŗ£ņ×æĒĢśļ®┤ņä£ ņ×¼ĒÖ£ņä▒ņØ┤ ņØ╝ņ¢┤ļéśļŖö ņØ┤ļźĖļ░ö ņ¦ĆņŚ░ ņ×¼ĒÖ£ņä▒(late-onset reactivation)ņØ┤ ņØ╝ņ¢┤ļéśĻĖ░ļÅä ĒĢ£ļŗż[10,33]. ĻĘĖļ¤¼ļ»ĆļĪ£ rituximab, ņĪ░Ēśłļ¬©ņäĖĒżņØ┤ņŗØĻ│╝ Ļ░ÖņØ┤ ļ®┤ņŚŁņ¢ĄņĀ£ļź╝ Ļ░ĢļĀźĒ׳ ņ£ĀļÅäĒĢśļŖö ņ╣śļŻīņŗ£ņŚÉļŖö ņśłļ░®ņĀü ĒĢŁļ░öņØ┤ļ¤¼ņŖż ņ╣śļŻīņØś ĻĖ░Ļ░äņØä ņóĆ ļŹö ĻĖĖĻ▓ī ņ×ĪņØä ĒĢäņÜöĻ░Ć ņ׳ļŗż.
ņØśĒĢÖĻĖ░ņłĀņØś ļ░£ļŗ¼ļĪ£ ņןĻĖ░ņØ┤ņŗØņØ┤ ĒÖ£ļ░£ĒĢ┤ņ¦ĆĻ│Ā, ĒĢŁņĢöņĀ£ ļ░Å ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£ņØś ĒÜ©ļŖźņØĆ ņĀÉņ░© Ļ░ĢļĀźĒĢ┤ņ¦ĆĻ│Ā ņ׳ņ¦Ćļ¦ī ņØ┤ņŚÉ ļö░ļØ╝ ņ╣śļŻīņÖĆ Ļ┤ĆļĀ©ļÉ£ ĒĢ®ļ│æņ”Øņ£╝ļĪ£ BĒśĢĻ░äņŚ╝ņØś ņ×¼ĒÖ£ņä▒ņØ┤ ļ¼ĖņĀ£ņĀÉņ£╝ļĪ£ ļéśĒāĆļéśĻ▓ī ļÉśņŚłļŗż. ņØ┤ļŖö ļīĆĒæ£ņĀüņØĖ ņóģņ¢æ-ļ®┤ņŚŁņ╣śļŻīĻ┤ĆļĀ© ļČĆņ×æņÜ®ņ£╝ļĪ£ ĻĘĖ ņ×äņāüĻ▓ĮĻ│╝ļŖö ĒÖśņ×ÉļōżņØś ĻĖ░ņĀĆ Ļ░äņ¦łĒÖś ļō▒ņŚÉ ļö░ļØ╝ ļŗżņ¢æĒĢśĻ▓ī ļéśĒāĆļéśņ¦Ćļ¦ī, ņĀüņ¦Ć ņĢŖņØĆ ĒÖśņ×ÉļōżņŚÉņä£ ĒĢŁņĢöņ╣śļŻīņØś ņŚ░ĻĖ░ ļ░Å ņĪ░ĻĖ░ņżæļŗ©ņØä Ļ░ĆņĀĖņś¼ ņłś ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ ņ╣śļŻī ņĀä ņśłļ░®(ņäĀņĀ£ņĀü ĒĢŁļ░öņØ┤ļ¤¼ņŖżņ╣śļŻī)ņØ┤ ņżæņÜöĒĢśļŗż. ņØ┤ļź╝ ņ£äĒĢ┤ Ēśä ņ×äņāüņŚÉņä£ ļ¼┤ņŚćļ│┤ļŗż ĒĢäņÜöĒĢ£ Ļ▓āņØĆ ĒĢŁņĢöņ╣śļŻīļź╝ ļŗ┤ļŗ╣ĒĢśĻ│Ā ņ׳ļŖö ĒĢŁņĢöĻ┤ĆļĀ© ņ×äņāüņØśĻ░Ć ņ╣śļŻī ņżæ ļ░£ņāØĒĢĀ ņłś ņ׳ļŖö BĒśĢĻ░äņŚ╝ļ░öņØ┤ļ¤¼ņŖżņØś ņ×¼ĒÖ£ņä▒ņØä ņČ®ļČäĒ׳ ņØĖņ¦ĆĒĢśĻ│Ā ņĀüņĀłĒ׳ ļīĆņ▓śĒĢśļŖö Ļ▓āņØ┤ļŗż. ņØ┤ņÖĆ ĒĢ©Ļ╗ś BĒśĢ Ļ░äņŚ╝ ņ×¼ĒÖ£ņä▒ ņśłļ░®ņØä ņ£äĒĢ£ ņĀüņĀłĒĢ£ ĒĢŁļ░öņØ┤ļ¤¼ņŖż ņ╣śļŻīļīĆņ▒ģņŚÉ Ļ┤ĆĒĢ┤ Ļ░ü ņ×äņāüĻ│╝Ļ░ä Ēśæņ¦äņ▓┤Ļ│äļź╝ ĻĖ┤ļ░ĆĒ׳ ņ£Āņ¦ĆĒĢśļŖö Ļ▓āļÅä ņżæņÜöĒĢ£ ņÜöņåīņØ┤ļŗż. ĒĢŁņĢöņ╣śļŻī ņżæ ļ░£ņāØĒĢśļŖö ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņØĆ ĒÖĢņŗżĒĢ£ ņśłļ░®ļ▓ĢņØ┤ ņ׳ņ£╝ļ»ĆļĪ£ ņØ┤ļź╝ ņĀüņĀłĒ׳ ĒÖ£ņÜ®ĒĢ£ļŗżļ®┤ ņ×¼ĒÖ£ņä▒ Ļ░äņŚ╝ņŚÉ ņØśĒĢ£ ĒÖśņ×ÉļōżņØś ņĀäņ▓┤ņĀüņØĖ ņ×äņāüĻ▓ĮĻ│╝ ņĢģĒÖöļź╝ ņśłļ░®ĒĢĀ ņłś ņ׳ņØä Ļ▓āņØ┤ļŗż.
REFERENCES
1. Wands JR, Chura CM, Roll FJ, Maddrey WC. Serial studies of hepatitis-associated antigen and antibody in patients receiving antitumor chemotherapy for myeloproliferative and lymphoproliferative disorders. Gastroenterology 1975;68:105ŌĆō112.


2. Yeo W, Johnson PJ. Diagnosis, prevention and management of hepatitis B virus reactivation during anticancer therapy. Hepatology 2006;43:209ŌĆō220.


3. Yeo W, Chan PK, Hui P, et al. Hepatitis B virus reactivation in breast cancer patients receiving cytotoxic chemotherapy: a prospective study. J Med Virol 2003;70:553ŌĆō561.


4. Mindikoglu AL, Regev A, Schiff ER. Hepatitis B virus reactivation after cytotoxic chemotherapy: the disease and its prevention. Clin Gastroenterol Hepatol 2006;4:1076ŌĆō1081.


5. Rossi G. Prophylaxis with lamivudine of hepatitis B virus reactivation in chronic HbsAg carriers with hematooncological neoplasias treated with chemotherapy. Leuk Lymphoma 2003;44:759ŌĆō766.


6. Lau GK. Hepatitis B reactivation after chemotherapy: two decades of clinical research. Hepatol Int 2008;2:152ŌĆō162.



7. Lau GK, Yiu HH, Fong DY, et al. Early is superior to deferred preemptive lamivudine therapy for hepatitis B patients undergoing chemotherapy. Gastroenterology 2003;125:1742ŌĆō1749.


8. Jang JW, Choi JY, Bae SH, et al. A randomized controlled study of preemptive lamivudine in patients receiving transarterial chemo-lipiodolization. Hepatology 2006;43:233ŌĆō240.


9. Lok AS, Liang RH, Chiu EK, Wong KL, Chan TK, Todd D. Reactivation of hepatitis B virus replication in patients receiving cytotoxic therapy. Report of a prospective study. Gastroenterology 1991;100:182ŌĆō188.


10. Kusumoto S, Tanaka Y, Ueda R, Mizokami M. Reactivation of hepatitis B virus following rituximab-plus-steroid combination chemotherapy. J Gastroenterol 2011;46:9ŌĆō16.


11. Park JW, Park KW, Cho SH, et al. Risk of hepatitis B exacerbation is low after transcatheter arterial chemoembolization therapy for patients with HBV-related hepatocellular carcinoma: report of a prospective study. Am J Gastroenterol 2005;100:2194ŌĆō2200.


12. Kusumoto S, Tanaka Y, Mizokami M, Ueda R. Reactivation of hepatitis B virus following systemic chemotherapy for malignant lymphoma. Int J Hematol 2009;90:13ŌĆō23.


13. Tur-Kaspa R, Burk RD, Shaul Y, Shafritz DA. Hepatitis B virus DNA contains a glucocorticoid-responsive element. Proc Natl Acad Sci U S A 1986;83:1627ŌĆō1631.



14. Hsu CH, Hsu HC, Chen HL, et al. Doxorubicin activates hepatitis B virus (HBV) replication in HBV-harboring hepatoblastoma cells: a possible novel mechanism of HBV reactivation in HBV carriers receiving systemic chemotherapy. Anticancer Res 2004;24:3035ŌĆō3040.

15. Chou CH, Chen PJ, Lee PH, Cheng AL, Hsu HC, Cheng JC. Radiation-induced hepatitis B virus reactivation in liver mediated by the bystander effect from irradiated endothelial cells. Clin Cancer Res 2007;13:851ŌĆō857.


16. Burpee SE, Kurian M, Murakame Y, Benevides S, Gagner M. The metabolic and immune response to laparoscopic versus open liver resection. Surg Endosc 2002;16:899ŌĆō904.


17. Lubel JS, Angus PW. Hepatitis B reactivation in patients receiving cytotoxic chemotherapy: diagnosis and management. J Gastroenterol Hepatol 2010;25:864ŌĆō871.


18. Kim JH, Park JW, Kim TH, Koh DW, Lee WJ, Kim CM. Hepatitis B virus reactivation after three-dimensional conformal radiotherapy in patients with hepatitis B virus-related hepatocellular carcinoma. Int J Radiat Oncol Biol Phys 2007;69:813ŌĆō819.


19. Jang JW, Kwon JH, You CR, et al. Risk of HBV reactivation according to viral status and treatment intensity in patients with hepatocellular carcinoma. Antivir Ther 2011;16:969ŌĆō977.


20. Jang JW, Choi JY, Bae SH, et al. Transarterial chemo-lipiodolization can reactivate hepatitis B virus replication in patients with hepatocellular carcinoma. J Hepatol 2004;41:427ŌĆō435.


21. Nagamatsu H, Itano S, Nagaoka S, et al. Prophylactic lamivudine administration prevents exacerbation of liver damage in HBe antigen positive patients with hepatocellular carcinoma undergoing transhepatic arterial infusion chemotherapy. Am J Gastroenterol 2004;99:2369ŌĆō2375.


22. Yeo W, Lam KC, Zee B, et al. Hepatitis B reactivation in patients with hepatocellular carcinoma undergoing systemic chemotherapy. Ann Oncol 2004;15:1661ŌĆō1666.


23. Nagamatsu H, Kumashiro R, Itano S, Matsugaki S, Sata M. Investigation of associating factors in exacerbation of liver damage after chemotherapy in patients with HBV-related HCC. Hepatol Res 2003;26:293ŌĆō301.


24. Lao XM, Wang D, Shi M, et al. Changes in hepatitis B virus DNA levels and liver function after transcatheter arterial chemoembolization of hepatocellular carcinoma. Hepatol Res 2011;41:553ŌĆō563.


25. Zhong S, Yeo W, Schroder C, et al. High hepatitis B virus (HBV) DNA viral load is an important risk factor for HBV reactivation in breast cancer patients undergoing cytotoxic chemotherapy. J Viral Hepat 2004;11:55ŌĆō59.


26. Lau GK, Leung YH, Fong DY, et al. High hepatitis B virus (HBV) DNA viral load as the most important risk factor for HBV reactivation in patients positive for HBV surface antigen undergoing autologous hematopoietic cell transplantation. Blood 2002;99:2324ŌĆō2330.


27. Sugauchi F, Tanaka Y, Kusumoto S, et al. Virological and clinical characteristics on reactivation of occult hepatitis B in patients with hematological malignancy. J Med Virol 2011;83:412ŌĆō418.


28. Alexopoulou A, Theodorou M, Dourakis SP, et al. Hepatitis B virus reactivation in patients receiving chemotherapy for malignancies: role of precore stop-codon and basic core promoter mutations. J Viral Hepat 2006;13:591ŌĆō596.


29. Borentain P, Colson P, Coso D, et al. Clinical and virological factors associated with hepatitis B virus reactivation in HBsAg-negative and anti-HBc antibodies-positive patients undergoing chemotherapy and/or autologous stem cell transplantation for cancer. J Viral Hepat 2010;17:807ŌĆō815.

30. Hui CK, Cheung WW, Zhang HY, et al. Kinetics and risk of de novo hepatitis B infection in HBsAg-negative patients undergoing cytotoxic chemotherapy. Gastroenterology 2006;131:59ŌĆō68.


31. Yeo W, Chan TC, Leung NW, et al. Hepatitis B virus reactivation in lymphoma patients with prior resolved hepatitis B undergoing anticancer therapy with or without rituximab. J Clin Oncol 2009;27:605ŌĆō611.


32. Pei SN, Chen CH, Lee CM, et al. Reactivation of hepatitis B virus following rituximab-based regimens: a serious complication in both HBsAg-positive and HBsAg-negative patients. Ann Hematol 2010;89:255ŌĆō262.


33. Manzano-Alonso ML, Castellano-Tortajada G. Reactivation of hepatitis B virus infection after cytotoxic chemotherapy or immunosuppressive therapy. World J Gastroenterol 2011;17:1531ŌĆō1537.



34. Loomba R, Rowley A, Wesley R, et al. Systematic review: the effect of preventive lamivudine on hepatitis B reactivation during chemotherapy. Ann Intern Med 2008;148:519ŌĆō528.



35. Yeo W, Hui EP, Chan AT, et al. Prevention of hepatitis B virus reactivation in patients with nasopharyngeal carcinoma with lamivudine. Am J Clin Oncol 2005;28:379ŌĆō384.


36. Idilman R, Arat M, Soydan E, et al. Lamivudine prophylaxis for prevention of chemotherapy-induced hepatitis B virus reactivation in hepatitis B virus carriers with malignancies. J Viral Hepat 2004;11:141ŌĆō147.


37. Shibolet O, Ilan Y, Gillis S, Hubert A, Shouval D, Safadi R. Lamivudine therapy for prevention of immunosuppressiveinduced hepatitis B virus reactivation in hepatitis B surface antigen carriers. Blood 2002;100:391ŌĆō396.


38. Dai MS, Wu PF, Shyu RY, Lu JJ, Chao TY. Hepatitis B virus reactivation in breast cancer patients undergoing cytotoxic chemotherapy and the role of preemptive lamivudine administration. Liver Int 2004;24:540ŌĆō546.


39. Yeo W, Chan PK, Ho WM, et al. Lamivudine for the prevention of hepatitis B virus reactivation in hepatitis B s-antigen seropositive cancer patients undergoing cytotoxic chemotherapy. J Clin Oncol 2004;22:927ŌĆō934.


40. Hsu C, Sur IJ, Hwang WS, et al. A prospective comparative study of prophylactic or therapeutic use of lamivudine for chemotherapy-associated hepatitis B (HBV) reactivation in non-Hodgkin's lymphoma patients [Abstract]. Hepatology 2006;131:S297.
42. European Association For The Study Of The Liver. EASL Clinical Practice Guidelines: management of chronic hepatitis B. J Hepatol 2009;50:227ŌĆō242.

43. Liaw YF, Leung N, Guan R, et al. Asian-Pacific consensus statement on the management of chronic hepatitis B: a 2005 update. Liver Int 2005;25:472ŌĆō489.


44. Pollard AJ, Perrett KP, Beverley PC. Maintaining protection against invasive bacteria with protein-polysaccharide conjugate vaccines. Nat Rev Immunol 2009;9:213ŌĆō220.


(A) Serum HBV DNA and ALT profiles in a typical case of HBV reactivation during chemotherapy. The increase in HBV DNA levels precedes an increase in ALT levels by several weeks. (B) Dynamic changes (phase 1 to 5) in HBV DNA and ALT levels during HBV reactivation. ALT, alanine aminotransferase.
Figure┬Ā1.
Risk factors of HBV reactivation during chemotherapy. ALT, alanine aminotransferase; HSCT, hematopoietic stem cell transplantation.
Figure┬Ā2.
Algorithm for prevention of HBV reactivation in HBsAg-positive patients who are to receive chemotherapy. L-NUCs includes lamivudine, telbivudine, and clevudine. ETV, entecavir; TFV, tenofovir; ADV, adefovir; LFT, liver function test; HSCT, hematopoietic stem cell transplantation.
Figure┬Ā3.
Algorithm for prevention of HBV reactivation in HBsAg-negative patients who are to receive chemotherapy.
HSCT, hematopoietic stem cell transplantation.
Figure┬Ā4.
Table┬Ā1.
Risk of HBV reactivation according to the type of malignancy Risk
Table┬Ā2.
Results of HBV reactivation in patients with HCC
| References | No. of patients | Chemotherapy | No. of sessions |
HBV reactivation, % (Hepatitis, %) |
Outcome |
|---|---|---|---|---|---|
| Nagamatsu, et al. [23] | 33 | TAI | Weekly infusion | 24 | 3 died |
| Jang, et al. [20] | 146 | TACL | 5 (2-14) | 33.7 (21.7) | 25 resolved, 3 died |
| Nagamatsu, et al. [21] | 17 | TAI | Bi-weekly infusion | 67 | 3 died of HBV reactivation |
| Yeo, et al. [22] | 102 | Systemic Tx | 3-weekly intervals | 36 | Twelve (30%) died of HBV reactivation |
| Park, et al. [11] | 89 | TACE | 1 | 4.3 | 3 resolved, 1 had tumor-related hepatic failure |
| Jang, et al. [8] | 73 | TACL | 1-monthly intervals | 40.5 (29.7) | One died of HBV reactivation |
| Kim, et al. [18] | 91 | TACE + RT | NA |
21.8 (a rebound of HBV DNA to > 100 ├Ś baseline) |
4 (12.5%) developed CHB exacerbation |
| Lao, et al. [24] | 172 | TACE | 1.3/person | 14.5 |
12.1% in the reactivation group had CHB exacerbation |
Table┬Ā3.
Clinical trials of preemptive lamivudine for HBV reactivation in HBsAg carriers
| Study | Country | No. (LAM vs. Control): M/F | Disease | Steroid | Relative risk |
|---|---|---|---|---|---|
| Randomized, controlled trials | |||||
| ŌĆāLau et al. [7] | Hongkong | 8/7 vs. 9/6 | NHL, HL | No | 0.00 |
| ŌĆāJang et al. [8] | Korea | 30/6 vs. 31/6 | HCC | No | 0.07 |
| Prospective cohort studies with control groups | |||||
| ŌĆāIdilman et al. [36] | Turkey | 5/3 vs. 4/6 | Hematologic, breast cancer | Yes | 0.00 |
| ŌĆāShibolet et al. [37] | Israel | 10/3 vs. 5/0 | Lymphoma, colon ca, histiocytosis | Yes | 0.00 |
| Prospective cohort studies with historical control groups | |||||
| ŌĆāDai et al. [38] | Taiwan | 0/11 vs. 0/9 | Breast cancer | No | 0.00 |
| ŌĆāYeo et al. [39] | Hongkong | 34/31 vs. 82/111 | Various cancers | Yes | 0.19 |
| ŌĆāYeo et al. [35] | Hongkong | 14/2 vs. 15/6 | Nasopharyngeal carcinoma | Yes | 0.00 |
| ŌĆāHsu et al. [40] | Taiwan | NA | NHL | NA | 0.21 |
The data are modified from the study by Loomba et al. [34].
-
METRICS

-
- 1 Crossref
- 0 Scopus
- 11,432 View
- 157 Download



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



